丁香酸葡萄糖苷在制备抑制pd1和pd-l1蛋白之间相互作用药物中的应用
技术领域
1.本发明属于医药领域,具体涉及丁香酸葡萄糖苷在制备抑制pd1和pd-l1蛋白之间相互作用药物中的应用。
背景技术:
2.新型癌症免疫治疗是最有前途的癌症治疗策略,主要包括嵌合抗原受体t细胞、双特异性抗体和免疫检查点抑制剂。程序性细胞死亡蛋白1/程序性细胞死亡配体1 (pd-1/ pd-l1)轴是一个重要的免疫检查点信号通路,可以下调炎症反应的幅度,维持机体的免疫稳态。这些通路涉及免疫稳态或采用使肿瘤细胞主动逃避免疫细胞消除的特征。它们是t细胞增殖和功能的抑制剂。已有研究表明,以免疫检查点抑制剂为靶点,通过阻断pd-1与其配体的相互作用,从而通过增强抗肿瘤免疫反应来克服免疫监视的内在抗性,从而刺激t细胞的反应。同时这也会导致改善的结果和增加病人的存活率。
3.最近的实验证明临床成功的癌症免疫治疗包括监管批准的t细胞检查点抑制抗体ipilimumab、pembrolizumab和nivolumab。ipilimumab是人源igg1k单克隆抗体,与人源ctla-4的胞外区域结合并具有高亲和力,是该复合体功能的抑制剂。ipilimumab能引起t细胞的激活和增殖,淋巴细胞的浸润,从而导致肿瘤细胞的死亡。效应t细胞功能的增强、cd4 treg细胞和cd8 抑制细胞受到抑制,是ipilimumab发挥其治疗效果的关键。pembrolizumab和nivolumab是人源化的单克隆抗体,它们阻止配体的参与,从而干扰t细胞信号传递和细胞死亡。所有这些单克隆抗体都显示出作为单一药物对黑色素瘤的显著临床益处,并继续作为单一药物和联合药物在临床试验中进行测试。这些成功的免疫肿瘤药物利用了与癌症生长和治疗相关的独特的免疫机制,从早期肿瘤相关抗原反应到t细胞激活和肿瘤免疫抑制的缓解。
4.小分子化合物相对于重组蛋白药物设计具有以下明显的优势:1)对其临床应用和发展有详细的认识和历史先例,具有较高的可行性;2)口服生物利用度;3)暴露于肿瘤微环境或跨越生理屏障(如血脑屏障);4)获得蛋白治疗药物难以控制的胞内疾病靶点;和5)多样和充分了解的配方和剂量选择,以减轻药动学和/或药效学的挑战,并使滴定的药物暴露。小分子药物的另一个引人注目的优势是,与生物免疫疗法相比,患者更容易获得这些类型的药物。小分子药物的成本通常较低,这是由于药物本身、与输注(或注射)相比,递送药片的成本降低了,而且供应链更简单,不需要冷藏。为了使免疫疗法在改变癌症治疗方面发挥其全部潜力,必须降低费用,使所有可能受益的人都能获得治疗。即使成本不是获取的障碍,口服药物相对于输注的便利性是与目前正在发展的免疫肿瘤治疗的一个强大的不同点。
技术实现要素:
5.本发明目的在于克服单克隆抗体的缺陷,提供一种小分子化合物丁香酸葡萄糖苷
在制备抑制pd1和pd-l1蛋白之间相互作用药物中的应用。丁香酸葡萄糖苷是一种小分子化合物,分子式: c
15
h
20
o
10
,分子量:360.3,cas no. 33228-65-8。
6.本发明提供了一种小分子化合物丁香酸葡萄糖苷在制备抑制pd1/pd-l1蛋白之间相互作用药物中的应用。
7.具体的,本发明发现了丁香酸葡萄糖苷在制备抑制pd1/pd-l1信号通路药物中的应用,即其对pd1/pd-l1信号通路具有抑制作用。
8.进一步,pd1浓度为10μg/ml,pd-l1浓度为10μg/ml,丁香酸葡萄糖苷在浓度为2-80 μm时能够抑制pd1与pd-l1的体外结合,能够抑制pd1/pd-l1蛋白之间的体外相互作用。
9.本发明发现:丁香酸葡萄糖苷在制备抑制pd1/pd-l1信号通路药物中的应用,也就是发现了丁香酸葡萄糖苷对pd1/pd-l1信号通路的抑制作用,丁香酸葡萄糖苷对其产生抑制作用的适宜浓度为:2-80 μm。
10.丁香酸葡萄糖苷在制备肺癌免疫治疗药剂中的应用,本技术发现了丁香酸葡萄糖苷在体外结合h1975细胞裂解液(富含pd-l1)以及人pd1(cat: 10377-h03h, human, recombinant, sino biological)和人pd-l1(cat: 10084-h02h, human, recombinant, sino biological)纯蛋白的能力。
11.本发明经研究发现:丁香酸葡萄糖苷可以作为pd1/pd-l1蛋白相互作用的抑制剂。pd1/pd-l1信号通路与免疫应答、肿瘤免疫逃逸密切相关,抑制pd1/pd-l1信号通路的异常激活能够起到预防及治疗肿瘤的作用。本发明的丁香酸葡萄糖苷能够抑制pd1/pd-l1蛋白质之间相互作用。
附图说明
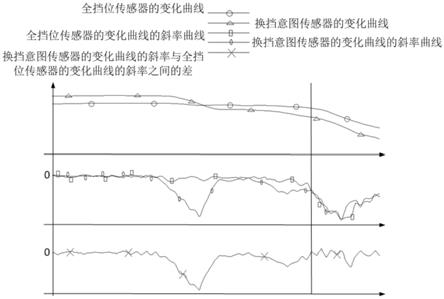
12.图1为测试了不同浓度梯度下丁香酸葡萄糖苷体外结合人pd1和人pd-l1的能力;其中,丁香酸葡萄糖苷在能够结合人pd-1以及人pd-l1,kd值分别为5.631*10-5 m和3.06*10-5
m。
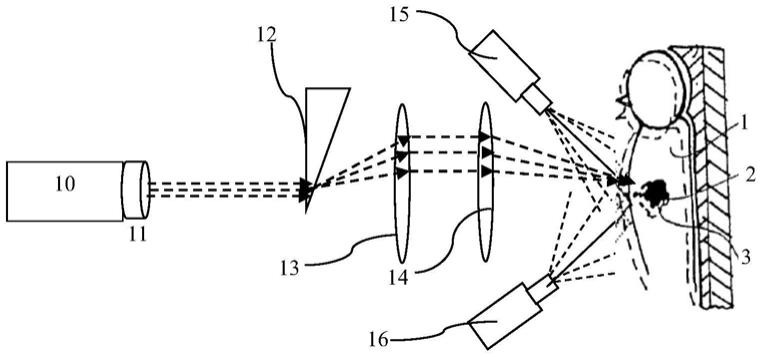
13.图2为丁香酸葡萄糖苷在体外结合h1975细胞裂解液(富含pd-l1)以及人pd1和pd-l1纯蛋白的能力。
具体实施方式
14.以下结合实施例对本发明的技术方案作进一步地详细介绍,但本发明的保护范围并不局限于此。
15.应用试验材料与方法试剂glucosyringic acid(丁香酸葡萄糖苷)购自chem faces公司,纯度为98%。
16.仪器与器材:海尔医用低温保存箱(青岛海尔特种电器有限公司);酶联免疫检测仪(thermo公司):biacore t200(ge healthcare life sciences);电子天平(梅特勒-托利多仪器上海有限公司);细胞培养箱(thermo公司);thermo 超净工作台:氨基偶联试剂盒(amine coupling kit,ge healthcare life sciences)。
17.丁香酸葡萄糖苷在体外结合人pd1和pd-l1的能力人重组pd1蛋白(组蛋白标签),人重组pd-l1蛋白(组蛋白标签),购买自北京义翘神州科技有限公司。具体实验流程如下,首先利用10mm的醋酸盐缓冲液(ph4.5)将蛋白稀释至10μg/ml。借助biacore t200仪器,将人重组pd1蛋白及人重组pd-l1蛋白通过氨基偶联的方式分别交联在series s sensor chip cm5芯片上,偶联量为5000单位。重组蛋白完成交联之后,通过动力学分析,检测化合物丁香酸葡萄糖苷与人重组pd1蛋白(组蛋白标签),人重组pd-l1蛋白(组蛋白标签)的体外物理结合能力。终浓度为2μm,10μm,20μm,40μm,80μm的丁香酸葡萄糖苷溶液分别以30ul/min的流速与cm5芯片上的pd1蛋白及pd-l1蛋白通道反应,其反应过程如图1所示。利用biacore分析软件计算丁香酸葡萄糖苷与人重组pd1蛋白及人重组pd-l1蛋白的体外结合能力,k
d
值如表1所示。通过表1和图1可以得出,丁香酸葡萄糖苷能够在体外与人pd-1和pd-l1重组蛋白发生明显的物理结合。
18.表1表1中: hpd-1代表人重组pd1蛋白,hpd-l1代表人重组pd-l1蛋白。
19.丁香酸葡萄糖苷体外结合h1975细胞裂解液以及人pd1和pd-l1纯蛋白的能力具体实验流程如下,h1975肺癌细胞系使用rpmi-1640培养基((hyclone, usa)),含10%胎牛血清(bi 公司)。用0.25%胰蛋白酶将h1975细胞从培养皿上消化下来,1000rpm离心3分钟后,弃培养基。用1
×
细胞裂解缓冲液(cat#r0020, solarbio, beijing, china)和蛋白酶抑制剂直接裂解制备全细胞提取物。所有蛋白质样品变性采用5
×
sds缓冲区在95
º
c加热5分钟,然后通过sds
ꢀ–ꢀ
page进行蛋白电泳分析。蛋白质上样量采用bca定量试剂盒(cat#pc0020, solarbio, beijing, china)测定蛋白浓度。
20.将h1975细胞裂解液(3.33mg/ml、20μl)、人pd-1重组蛋白(0.25mg/ml、2μl)、pd-l1重组蛋白(0.25mg/ml、2μl)、以及丁香酸葡萄糖苷-琼脂糖凝胶4b混合物(混合物中琼脂糖凝胶4b用量为0.3g,丁香酸葡萄糖苷用量为2mg)分别加入到相应的孔中,电泳电压控制在80伏,100分钟。然后湿法转膜90分钟。用5%脱脂奶粉在1
ꢀ×ꢀ
pbs-t(含0.05%吐温-20的磷酸盐缓冲盐水)中封闭1小时,然后与抗pd1或pd-l1抗体孵育过夜。第2天,在1
×
pbs-t缓冲液中洗涤3次,每次15分钟,然后与抗体对应的辣根过氧化物酶标记的二抗孵育。使用增效化学发光(ecl)检测试剂和amersham imager 600 (ge healthcare life science,匹兹堡,pa, usa)观察特异性蛋白条带。使用image j free software (nih, version 1.47, rrid: scr_ 003070)进行量化,结果见图2。通过图2可以得出丁香酸葡萄糖苷既可以与hpd1结合,又可以与hpd-l1结合。
21.综上可以看出:本发明经研究发现丁香酸葡萄糖苷通过与pd1和pd-l1的结合,进而抑制pd1/pd-l1蛋白之间的体外相互作用。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。