C型肝炎病毒的免疫原性组合物及其用途的制作方法
- 国知局
- 2024-06-20 11:27:13
本发明提供一种包含经α2-3,6,8,9神经氨酸酶a处理的c型肝炎病毒(hcv)假颗粒的免疫原性组合物。此外,本发明进一步提供一种免疫原性组合物在制备hcv疫苗中的用途,其中所述免疫原性组合物包含经α2-3,6,8,9神经氨酸酶a处理的hcv假颗粒。
背景技术:
1、c型肝炎病毒(hcv)是慢性肝病的主要病原体,其影响全世界约1.7亿人口。大多数(约85%)感染hcv的个体会变成慢性感染,且有发展为肝硬化和肝细胞癌的风险。hcv为黄病毒科的其中一员,其是一种含有正链基因体rna的套膜病毒。基于基因组序列的相似性,hcv可分为六种主要基因型和众多亚型。hcv rna基因组包含一个开放阅读框架,其位于非翻译区(utr)的5’和3’端两端。正链基因体rna编码出一条约3010个氨基酸的多蛋白,且该多蛋白经过宿主和病毒蛋白酶共同翻译和翻译后成结构性蛋白(c、e1、e2和p7)和非结构性蛋白(ns2、ns3、ns4a、ns4b、ns5a和ns5b)。
2、病毒附着和进入,其代表病毒与宿主细胞的第一次相互作用,是适应性体液反应的主要目标。负责细胞附着和hcv进入的病毒蛋白为糖蛋白e1和e2。病毒蛋白被宿主的免疫系统识别为异物并诱导抗体的产生。这些抗体中有一小部分在体外表现出抗病毒活性,并被定义为病毒中和抗体。中和抗体反应通常通过限制病毒传播来提供抵抗感染的第一线适应性防御。因此,这些糖蛋白的表达在疫苗发现和药物靶标方面具有重要应用。因此,了解病毒糖蛋白特性的基因型和准种变异(quasispecies variation)对于理解蛋白质的结构-功能关系相当重要。
3、套膜糖蛋白e1和e2为中和抗体的天然靶标。e2是体液和细胞介导的免疫反应的优选靶标。不意外的,大部分hcv序列变异集中在e2的高度变异区。已知这些区域表现出高度的变异性,其可用于区分同一亚型的hcv分离株和准种确认(在同一患者中有不同序列的共存)。
4、与病毒套膜相关的聚糖(glycans)在掩蔽中和表位(epitopes)和调节病毒颗粒的整体免疫原性中具有主要作用。病毒蛋白通常通过三种不同机制的其中之一来进行糖基化。这些过程不仅在所涉及的细胞酶有所不同外,而且还产生了不同类型的聚糖结构。所产生的聚糖被称为n连接、o连接或糖基磷脂酰肌醇(glycosylphosphatidylinositol,gpi)锚定的。在n连接糖基化过程中,聚糖链通过天冬酰胺(asparagine)残基添加到病毒蛋白中。n连接糖基化发生在蛋白质中存在共有氨基酸序列asn-x-ser/thr的位点上。这是到现在为止最常见的病毒蛋白糖基化方式,它们进行n连接糖基化的过程与细胞糖蛋白上发生的过程相似。
5、hcv套膜糖蛋白上的大多数糖基化位点是保守的,并且与这些蛋白质相关的某些聚糖已显示在蛋白质折叠和hcv进入中具有重要作用。这样高度表达的糖基化暗示这些聚糖可以限制hcv套膜蛋白的免疫原性,并限制某些抗体与在病毒粒子表面上的其表位的结合,正如在人类免疫缺陷病毒(hiv)gp120所观察到的那样。根据报导,e2上的至少三个聚糖(e2n1、e2n6和e2n11)降低了hcvpp对抗体中和的敏感性,并且这些聚糖也减少了cd81对其e2结合位点的接入。相对的,没有证据显示e1的n连接聚糖有助于掩蔽中和表位。这些数据暗示聚糖e2n1、e2n6和e2n11能接近cd81的结合位点,并调节cd81和中和抗体与e2的结合。简而言之,这项工作指出该区域为中和抗体的主要靶标,并且hcv聚糖有助于hcv逃避体液免疫反应。
6、由于细胞培养复制系统的缺乏,使抗hcv化合物的发现和hcv疫苗的发展受到严重阻碍。自1990年代后期以来,模拟导致hcv基因体复制的细胞内反应的亚基因组复制子的出现使人们能够发现hcv蛋白酶和聚合酶抑制剂,但无法研究hcv进入或进入抑制剂。最近,已经使用基于反转录病毒的假颗粒(pseudoparticle,pp)测定法研究了hcv e1e2在细胞附着和进入中的功能(它概括了整个hcv复制周期),其中反转录病毒颗粒的感染性由hcv e1e2套膜蛋白所赋予。这些新的实验系统使有关hcv糖蛋白e1和e2如何介导受体结合和病毒进入的认知取得了快速进展。这些系统促进了一系列病毒受体的发现。这种hcvpp测定特别用在对于衍生自感染不同基因型和病毒亚型的患者的hcv e1e2的功能分析、剖析关键e2受体cd81和sr-b1在病毒进入中的作用、以及测量抗体和患者血清对hcvpp所靶标细胞的中和感染的能力。
7、最近,通过表达反转录病毒核心颗粒上未修饰的hcv套膜糖蛋白所组装出感染性假颗粒已经可以成功地制造。hcv假颗粒(hcv pseudoparticles,hcvpp)是通过用分别编码e1e2多蛋白、反转录病毒核心蛋白和具有标记基因的可包装反转录病毒衍生基因体的三种表达载体转染到293t细胞来制造。令人惊讶的是,在没有对hcv套膜糖蛋白进行任何修饰的情况下,还是可以制造出感染性假颗粒。在这些假颗粒上所累积的数据强烈暗示它们可以模拟hcv感染的早期步骤。事实上,它们表现出对肝细胞的优先趋性(tropism),并且它们可以被抗e2单株抗体以及hcv感染患者的血清特异性中和。因此,hcvpp代表了目前可用于研究功能性hcv套膜糖蛋白的最佳工具,并提供研究hcv细胞进入的模型系统。hcvpp的开发提供了与确认的hcv套膜糖蛋白序列的hcv中和研究的可能性,并且hcvpp在中和研究中的使用已得到验证。上述说明已经显示相对强的中和反应的逐渐出现与病毒血症的减少相关。
技术实现思路
1、本发明提供一种制备免疫原性组合物的方法,其包含用α2-3,6,8,9神经氨酸酶a处理hcv假颗粒以产生免疫原性组合物。本发明还提供包含经α2-3,6,8,9神经氨酸酶a处理的hcv假颗粒的免疫原性组合物。此外,本发明进一步提供一种免疫原性组合物在制备hcv疫苗中的用途,其中所述免疫原性组合物包含经α2-3,6,8,9神经氨酸酶a处理的hcv假颗粒。
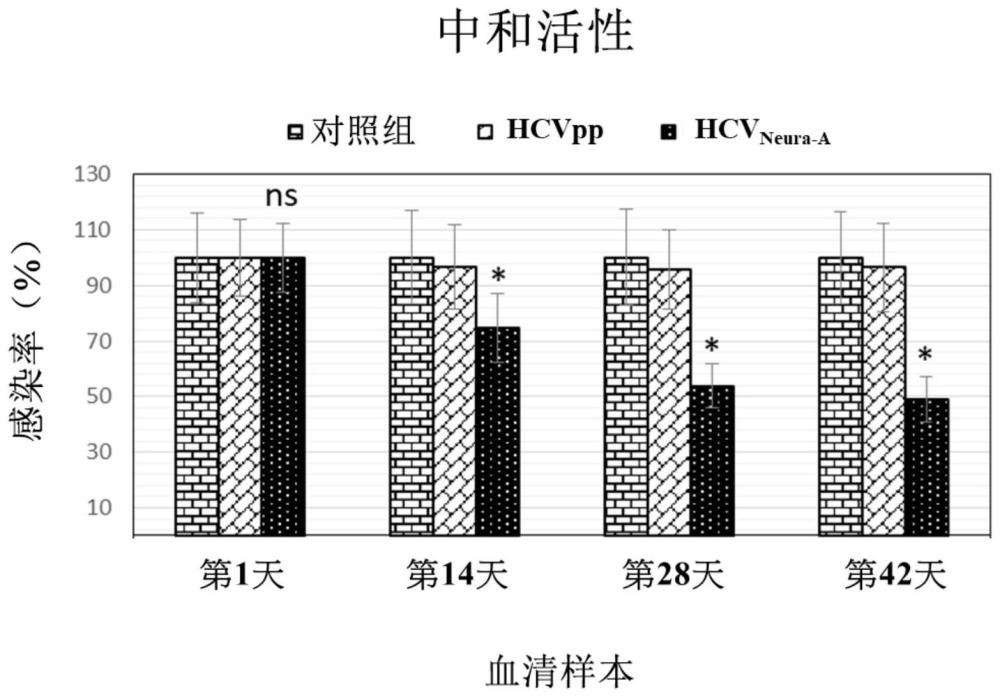
2、病毒附着和进入,代表病毒与宿主细胞的第一次相互作用,是适应性体液反应的主要目标。负责细胞附着和进入hcv的病毒蛋白为糖蛋白e1和e2。本发明提出通过糖苷酶(glycosidase),例如α2-3,6,8,9神经氨酸酶a(一种广泛的特异性糖苷酶,其可以从糖蛋白、糖肽(glycopeptides)和寡糖(oligosaccharides)上切除线性和分支的非还原末端的唾液酸(sialic acid)残基),对e1和e2进行去糖基化,其不仅可以提高检测中和抗体活性的灵敏度,还可以引发识别更高滴度的e1和e2变异体的免疫反应。为了研究用α2-3,6,8,9神经氨酸酶a处理的hcv假颗粒的免疫原性和保护能力,使用小鼠模型。在本发明中,测试hcvneura-a免疫小鼠的抗血清对于抑制hcvpp进入huh7.5细胞的能力(以hcvpp对huh7.5细胞的感染率的抑制情况为代表)。本发明显示,与对照组相比,用hcvneura-a免疫可以诱发具有中和活性的有效系统性体液反应,从而有效抑制hcvpp对huh7.5细胞的感染率。本发明指出hcvneura-a免疫小鼠的抗血清可以有效中和hcvpp,从而抑制hcvpp(携带亲源完整且未修饰的套膜糖蛋白)进入细胞,进而抑制huh7.5细胞的感染。因此,基于从上述中和研究所获得的结果,可以使用hcvpp的去糖基化来设计针对hcv感染的有效疫苗。
3、本发明的策略(通过α2-3,6,8,9神经氨酸酶a水解hcvpp上糖蛋白的唾液酸残基)为疫苗设计开辟了新方向,并且可以与其他不同的疫苗策略一起,来促进抗hcv疫苗的开发。
4、本文中的术语“一”或“一个/一种”用于描述本发明的元件和组件。该术语仅用于描述方便并给出本发明的基本想法。该描述应理解为包含一个或至少一个,并且除非清楚地另有说明,否则单数也包括复数。当与权利要求中的“包含”一词结合使用时,术语“一”可以表示一个或多个。
5、如在权利要求中使用的术语“或”意指“和/或”,除非明确指出仅表示其他选项,或者除非其他选项是互斥的。
6、本发明提供一种制备包含c型肝炎病毒(hcv)的病毒抗原的免疫原性组合物的方法,其包含:(a)提供hcv假颗粒(hcv pseudoparticles,hcvpp);(b)用α2-3,6,8,9神经氨酸酶a处理所述hcv假颗粒以去除所述hcv假颗粒的表面上的唾液酸;以及(c)分离步骤(b)中产生的hcv假颗粒以产生所述免疫原性组合物。
7、在本发明中,所述hcv假颗粒的制备方法包含:(1)递送表达构建体至细胞中,其中所述表达构建体包含用于编码hcv糖蛋白e1和e2、反转录病毒核心蛋白和反转录病毒衍生基因体的序列;以及(2)分离所述细胞产生的hcv假颗粒。
8、在一个实施方案中,所述用于编码hcv糖蛋白e1和e2的序列包含如seq id no:1所示的序列。
9、在所述hcv假颗粒的制备方法中,可以设计三个独立的表达构建体,其包含用于编码反转录病毒核心、基因体以及肝炎病毒糖蛋白的三个核酸序列;或者,也可以设计一个表达包含不同核酸序列的构建体。这样的表达构建体被递送到细胞中,从而诱导进一步的复制的肝炎病毒假颗粒的产生。在这种情况下,反转录病毒的基因体被修饰以表达肝炎病毒糖蛋白e1和e2来取代反转录病毒env基因(编码反转录病毒糖蛋白)。不过编码反转录病毒核心蛋白的基因保持不变。更进一步,例如,编码标记基因或免疫调节剂的附加基因也可以从该基因体中表达出来。
10、在一个实施方案中,所述细胞为体外细胞。在一个优选的实施方案中,所述细胞包含哺乳动物细胞。在一个更优选的实施方案中,所述细胞包含人类胚肾细胞(humanembryonic kidney cells)。
11、在本发明中,所述表达构建体的递送方式可以通过本领域技术人员熟知的任何标准方法来进行,例如转染、电穿孔、显微注射、转导、细胞融合、deae葡萄糖聚糖、磷酸钙沉淀或使用基因枪。
12、在一个实施方案中,所述表达构建体进一步包含用于编码标记基因的序列。在一个优选的实施方案中,所述标记基因为绿色荧光蛋白(gfp)基因。所述标记基因的目的是用于筛选成功转染的细胞。
13、如本文所用,术语“c型肝炎病毒”(也称为丙型肝炎病毒,hepatitis c virus,hcv)是指c型肝炎病毒的多种不同基因型和分离株中的任何一种。因此,“hcv”涵盖hcv的多种基因型、亚型或准种中的任何一种,其包括例如基因型1、2、3、4、6、7等和亚型(例如,1a、1b、2a 、2b、3a、4a、4c等)和准种。代表性的hcv基因型和分离株包括:“chiron”分离株hcv-1、h77、j6、con1、分离株1、bk、ec1、ec10、hc-j2、hc-j5;hc-j6、hc-j7、hc-j8、hc-jt、hct18、hct27、hcv-476、hcv-kf、“湖南”、“日本”、“中国台湾”、th、1型、1a型、h77 1b型、1c型、1d型、1e型、1f型、10型、2型、2a型、2b 型、2c型、2d型、2f型、3型、3a型、3b型、3g型、4型、4a型、4c型、4d型、4f型、4h型、4k型、5型、5a型、6型和6a型。
14、hcv基因体编码两种膜相关套膜糖蛋白(e1和e2),且它们会相互作用形成非共价异二聚体复合物。hcv糖蛋白e1和e2被n连接糖基化严重修饰。e1蛋白是由192个氨基酸所组成,并包含5到6个n-糖基化位点,其取决于hcv基因型。e2蛋白是由363到370个氨基酸所组成,并包含9-11个n-糖基化位点,其取决于hcv基因型。
15、在一个实施方案中,所述hcv的病毒抗原包含hcv的糖蛋白e1和e2。所述hcv的糖蛋白e1和e2表达在该hcv假颗粒的表面上。在一个优选的实施方案中,所述hcv假颗粒具有hcv的糖蛋白e1和e2。
16、如本文所用,α2-3,6,8,9神经氨酸酶a是广泛特异性的唾液酸酶,其会从糖蛋白、糖肽和寡糖上切除线性和分支的非还原末端唾液酸残基。因此,本发明通过α2-3,6,8,9神经氨酸酶a将hcv假颗粒的糖蛋白e1和e2上的唾液酸切除,从而诱发hcv假颗粒的免疫原性。
17、在另一个实施方案中,在步骤(b)中,所述hcv假颗粒用所述α2-3,6,8,9神经氨酸酶a处理0.5至4小时。在一个优选的实施方案中,在步骤(b)中,所述hcv假颗粒用α2-3,6,8,9神经氨酸酶a处理0.5至3小时。在一个更优选的实施方案中,在步骤(b)中,所述hcv假颗粒用所述α2-3,6,8,9神经氨酸酶a处理1至2小时。
18、在一个实施方案中,所述方法进一步包含步骤(d),其包含将步骤(c)的所述hcv假颗粒与医药学上可接受的载体混合以产生免疫原性组合物。更进一步,所述步骤(c)的hcv假颗粒可以与所述医药学上可接受的载体结合来产生hcv疫苗。
19、本发明还提供一种用于诱发对c型肝炎病毒(hcv)的免疫反应的免疫原性组合物,其中所述免疫原性组合物包含经α2-3,6,8,9神经氨酸酶a处理的hcv假颗粒。
20、此外,所述免疫原性组合物可任选合适的医药学上可接受的载体来结合以提高hcv疫苗的保护作用。在一个实施方案中,所述hcv疫苗包含所述免疫原性组合物和医药学上可接受的载体。
21、本发明进一步提供一种在对象内诱发对c型肝炎病毒(hcv)的免疫反应的方法,其包含向所述对象施用有效剂量的hcv疫苗,其中所述hcv疫苗包含免疫原性组合物,并且所述免疫原性组合物包含经α2-,6,8,9神经氨酸酶a处理的hcv假颗粒。
22、在一个实施方案中,所述对象为动物,优选的为哺乳动物,更优选的为人。
23、本发明还提供一种免疫原性组合物在制备hcv疫苗中的用途,其中所述免疫原性组合物包含经α2-3、6、8、9神经氨酸酶a处理的hcv假颗粒。
24、本发明的疫苗可以与本领域技术人员在阅读本发明后可确认的额外的活性剂、载体、媒剂、佐剂、赋形剂或辅助剂一起包入到医药或营养组合物或制剂中。
25、适合包含在本公开的组合物中的佐剂包括本领域熟知的那些,例如不用于人类的弗氏完全佐剂(complete freund's adjuvant,cfa)、弗氏不完全佐剂(incompletefreund's adjuvant,ifa)、角鲨烯(squalene)、角鲨烷(squalane)、明矾和各种油,所有这些都是本领域众所周知的,并且可从多种供货商购获得,例如诺华(例如,mf59佐剂)。
26、在另一个实施方案中,所述疫苗包含医药学上可接受的载体。因此,本发明的免疫原性组合物或疫苗进一步包含医药学上可接受的载体。
27、如本文所用,术语“医药学上可接受的载体”包括可与药物施用相容的溶剂、分散介质、涂层、抗菌剂和抗真菌剂、等张剂和吸收延迟剂等。补充的活性化合物也可以加入疫苗中。该疫苗被配制为与其预期的给药途径兼容。给药途径的实施例包括肠胃外,例如静脉内、皮内、皮下、口服(例如吸入)、经皮(局部)、经黏膜和直肠给药。用于肠胃外、皮内或皮下应用的溶液或悬浮液可以包括以下成分:无菌稀释剂,例如注射用水、食盐水溶液、固定油、聚乙二醇、甘油、丙二醇或其他合成溶剂;抗菌剂,例如苯甲醇或对羟基苯甲酸甲酯;抗氧化剂,例如抗坏血酸或亚硫酸氢钠;螯合剂,例如乙二氨四乙酸;缓冲剂,例如醋酸盐、柠檬酸盐或磷酸盐,以及用于调节张力的试剂,例如氯化钠或葡萄糖。ph值可以用酸或碱调节,例如盐酸或氢氧化钠。肠胃外制剂可以封装在安瓿、一次性注射器或用玻璃或塑料制成的多剂量小瓶中。
28、对于肠胃外给药,本发明的免疫原性组合物或其疫苗可以通过静脉内、皮下、肌肉内、腹膜内或皮内注射,单独给药或在进一步包含到医药学上可接受的载体的组合物中给药。对于注射给药,优选在无菌水性媒剂的溶液中使用所述免疫原性组合物,所述溶液还可以含有其他溶质,例如缓冲剂或防腐剂以及足量的医药学上可接受的盐或葡萄糖以使溶液等张性。本发明的免疫原性组合物可以用本领域熟知的治疗上可接受的盐的形式获得。
29、所述疫苗也可以口服给药。口服组合物通常包括惰性稀释剂或可食用载体。为了口服治疗给药的目的,活性化合物可以与赋形剂结合并以片剂、锭剂或胶囊的形式使用,例如明胶胶囊。口腔组合物也可以使用流体载体制备,用作漱口水。药学相容的黏合剂或佐剂材料可以作为组合物的一部分包括在内。片剂、丸剂、胶囊、锭剂等可以含有任何以下成分或类似性质的化合物:黏合剂,例如微晶纤维素、黄蓍胶或明胶;赋形剂,例如淀粉或乳糖;崩解剂,例如海藻酸、primogel或玉米淀粉;润滑剂,例如硬脂酸镁或sterotes;助流剂,例如胶体二氧化硅;甜味剂,例如蔗糖或糖精;或者调味剂,例如薄荷、水杨酸甲酯或橘子调味剂。
30、全身给药也可以是经黏膜或经皮给药。对于经黏膜或经皮给药,制剂中使用适合待渗透屏障的渗透剂。此类渗透剂在本领域中通常是已知的,并且包括例如用于经黏膜给药的去污剂、胆盐和梭链孢酸衍生物。经黏膜给药可以通过使用鼻喷雾剂或栓剂来完成。对于经皮给药,将活性化合物配制成本领域公知的软膏、油膏、凝胶或乳膏。化合物还可以制成栓剂形式(例如,与常规栓剂基质如可可脂和其他甘油酯)或用于直肠递送的保留灌肠剂。
31、将口服或非肠道的组合物配制成剂量单位形式是有利的,以便于给药和剂量的一致性。如本文所用的剂量单位形式是指适合作为待治疗对象的单位剂量的物理离散单位;每个单位含有预定量的活性化合物,其经计算可以产生所需的治疗效果,并与所需的医药载体有关。
32、将进一步理解,可以用于治疗或预防hcv的本发明的免疫原性组合物或疫苗的量会依据给药途径、所治疗病症的性质以及对象的年龄和状况而有所变化,最终将由主治医师自行决定。
33、包含在疫苗中的免疫原浓度是能诱发免疫反应且没有显著的不利副作用的量。所述量会根据所使用的免疫原以及疫苗中所含佐剂的类型和量而有所变化。通常,疫苗将包含约0.1至约1000 μg/ml,优选约0.2至约100 μg/ml,更优选约0.5 μg至约10 μg/ml的量的免疫原。在最初的疫苗接种之后,被接种的对象可以在其后适当间隔地接受一次或数次加强免疫。
34、本领域技术人员将理解,本文涉及从治疗延伸至预防已确定的感染或症状的治疗。本发明的免疫原性组合物和疫苗可以作为治疗性或预防性施用。治疗优选在感染之前或感染时或在哺乳动物暴露于hcv感染时开始,并持续到病毒不再存在。然而,治疗也可以在感染后、哺乳动物暴露于hcv感染后或出现既定感染症状后开始。
35、因此,当将本发明的免疫原性组合物施用于有需要的对象时,会在所述对象体内诱发针对一种或多种hcv基因型的免疫反应(例如,细胞免疫反应)。
本文地址:https://www.jishuxx.com/zhuanli/20240619/1544.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表