一种盐酸达泊西汀的工艺改进方法与流程
- 国知局
- 2024-11-21 12:22:32
本发明涉及有机合成领域,具体涉及一种盐酸达泊西汀的工艺改进方法。
背景技术:
1、达泊西汀( dapoxetine) 化学名为(+) -( s) -n,n-二甲基-3-(萘基-1-氧基) -苯丙氨基盐酸盐,cas 登记号为119356-77-3,mp. 175~178 ℃。它是一个选择性5-羟色胺再摄取抑制剂( ssris),其结构类似于氟西汀,同样具有抗抑郁作用,临床上使用的是其盐酸盐。该药早期用于治疗抑郁症和相关的情感障碍疾病,后来被用于治疗男性早泄。研究显示,该药可以快速地抑制血液中复合胺类的再摄取,对神经元受体没有直接作用并且半衰期短,可以有效地控制多发于年轻男性的早泄症状。达泊西汀与其他ssris相比,作用更迅速、半衰期更短、不良反应发生率更低。
2、有关达泊西汀的合成已有大量文献报道,主要归纳为两类:第一类为外消旋体拆分法;第二类为不对称合成法。外消旋体拆分法,以手性拆分试剂对外消旋的中间体或最终产物进行拆分反应,得到需要的非对映异构体,再分离拆分剂和单一异构体,最终制得拥有较高光学纯度的目标手性化合物。不对称合成,即是将潜在手性单元转化为手性单元,让其生成不等量的立体异构体产物。该方法最大的优点就是在于无需进行拆分反应,就可以直接合成具有光学纯度的目标产物,这样既降低原料损耗,也符合原子经济学以及绿色化学的要求。
3、wheeler 等(journal of labelled compounds and radiopharmaceuticals,1992, 31(4): 305-315)研究发现,把二甲胺和肉桂酸甲酯作为起始反应原料,首先进行michael加成反应生成中间体3-n, n-二甲基铵-3-苯基丙酸甲酯,接着用还原剂 lialh4对其进行还原反应生成中间体 3-n, n-二甲基铵-3-苯基丙醇,然后再用 1-氟萘与其进行醚化反应生成达泊西汀消旋体化合物,最后使用手性拆分试剂 l-(+)-酒石酸对其进行拆分反应,最终得到目标产物 s-达泊西汀,反应式如下所示:
4、。
5、陈芳军等(cn20121026520.5)把苯乙酮作为起始反应原料和乙腈进行缩合反应,在羧基化反应之后生成中间体 3-苯甲酰丙酸,再先后对其进行酯化反应,羟亚胺化反应,还原反应生成中间体 3-氨基-3-苯基丙醇,接着使用 boc 来保护中间体 3-氨基-3-苯基丙醇上的氨基,再接着进行醚化反应,胺甲基化反应,最终使用拆分剂酒石酸进行拆分反应制得目标产物s-达泊西汀,反应式如下所示:
6、。
7、尹玲丽(中国药物化学志, 2011, 1(1): 37-39)等以3-苯基-1-丙醇作为起始反应原料,首先与1-氟萘进行williamson反应生成中间体3-苯基-1-(萘氧基)-丙烷,接着使用nbs对中间体 3-苯基-1-(萘氧基)-丙烷苯环苄位上的氢进行取代,即溴代制成中间体3-苯基-3-溴-1-(萘氧基)-丙烷,然后再使用中间体 3-苯基-3-溴-1-(萘氧基)-丙烷和二甲胺反应生成达泊西汀的消旋体,最后使用手性拆分试剂 l-(+)-酒石酸对达泊西汀的消旋体进行拆分反应,最终得到目标产物 s-达泊西汀,反应式如下所示:
8、。
9、张德荣等(生物加工过程, 2010, 8(2): 13-17)通过固定化青霉素g酰化酶(pga)对 (±)-n-苯乙酰基-3-氨基-3-苯基丙酸进行酶法拆分,得到合成达泊西汀的中间体(s)-3-氨基-3-苯基丙酸,(s)-3-氨基-3-苯基丙酸经过还原、甲基化、缩合等多步化学合成得到最终产物达泊西汀,其反应式如下:
10、。
11、使用手性试剂拆分外消旋体能得到较高ee值的目标化合物,但是这种拆分过程通常需要多次重结晶,而且在反应的最后阶段进行拆分,会浪费大量的原料。使用不对称合成法的方法有效避免了拆分,能够有效提高ee值,但是合成手性中间体的路线相对繁琐复杂,在合手成过程中使用昂贵的手性催化剂以及有毒或者易爆的试剂。因此,开发一种适合于工业化的盐酸达泊西汀的工艺具有重要的经济价值。
技术实现思路
1、为了解决现有技术中存在的上述技术问题,本发明提供一种盐酸达泊西汀的工艺改进方法。本发明的方法反应步骤简单,无需使用昂贵的手性催化剂,且可以减少原料损失,更适合工业化生产。
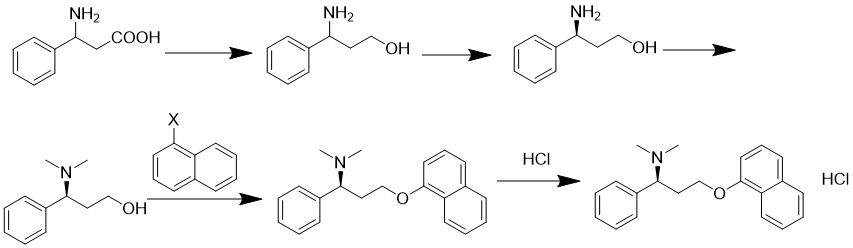
2、本发明提供了一种盐酸达泊西汀的工艺改进方法,包括如下步骤:
3、1)将3-氨基-3-苯基丙酸经还原反应,得到3-氨基-3-苯基丙醇;
4、2)将3-氨基-3-苯基丙醇经结晶诱导不对称转换反应,得到(s)-3-氨基-3-苯基丙醇;
5、3)将(s)-3-氨基-3-苯基丙醇进行胺甲基化反应,得到(s)-3-二甲胺基-3-苯基丙醇;
6、4)将(s)-3-二甲胺基-3-苯基丙醇与1-卤代萘成醚,得到达泊西汀;
7、5)将s-达泊西汀与hcl发生成盐反应,制得盐酸达泊西汀;
8、其反应路线如下:
9、;
10、其中:x为卤素;
11、步骤2)的结晶诱导不对称转换反应在消旋化催化剂、手性有机酸助剂和溶剂存在下进行,所述消旋化催化剂为3-硝基-5-三氟甲基水杨醛。
12、优选地,步骤1)的还原反应的还原剂选自nabh4-i2,kbh4-i2,lialh4或bh3。
13、优选地,步骤2)的手性有机酸助剂为光学纯的形式,选自:酒石酸、扁桃酸、二苯甲酰酒石酸、对甲基二苯甲酰酒石酸和樟脑磺酸中的一种或多种,更优选为d-(-)-酒石酸。
14、优选地,步骤2)的溶剂选自异丙醇,甲醇,乙醇,异丁醇。
15、优选地,步骤2)中手性有机酸助剂与3-氨基-3-苯基丙醇的摩尔比为(1-2):1。
16、优选地,步骤2)的反应温度为40℃~80℃,更优选为70℃~75℃。
17、优选地,步骤3)的胺甲基化反应在甲醛和甲酸存在下进行。
18、优选地,步骤4)的1-卤代萘为1-氟萘。
19、优选地,步骤4)在碱性条件下进行,所述碱选自有机碱或无机碱。
20、优选地,步骤5)的成盐反应在溶剂存在下进行。
21、优选地,步骤5)的反应溶剂选自甲醇、乙醇、丙醇或丁醇。
22、通过结晶作用进行旋光拆分是一个分离对映异构体的经典方法,它简便而且行之有效, 广泛地应用于实验室和工业生产。现有技术中合成盐酸达泊西汀,通常是在成盐反应之前,通过酒石酸等拆分试剂,对外消旋体进行拆分。然而简单地对异构体进行拆分, 理论上能达到的最大收率仅50%, 造成了巨大的浪费。结晶诱导不对称转化(crystallization-induced asymmetric transformation,ciat) 的应用恰恰克服了这一缺陷。ciat 是原位外消旋作用(或者差向异构化作用)和选择性结晶的耦合。成功的ciat过程需要满足下面几点要求: (1)找到使外消旋作用(或者差向异构化作用)顺利进行的环境; (2)找到在消旋过程中稳定而且高效的拆分方法(加入手性催化剂、手性助剂或者酶),使得异构体smr和sms之间的转化速率vri≠ vsi, 而转化速率常数kri与ksi可以相等; (3)过程中至少要有一种异构体结晶出来; (4)在不会被分解或者降解的环境下分离和操作, 而且对映异构体smr和sms之间不能发生共结晶的现象。通常情况下第二点是最关键而且最困难的部分。
23、通过亚胺形式进行的外消旋作用(差向异构化作用)用于氨基酸的手性拆分已有较多的报道,其原理如下:
24、。
25、然而将氨基醇通过亚胺形式的外消旋作用,进而实现手性拆分尚未见文献报道。本发明人在经过大量的创造性劳动,筛选出本发明的外消旋催化剂3-硝基-5-三氟甲基水杨醛,发现其能够以较高收率实现(s)-3-氨基-3-苯基丙醇的结晶诱导不对称转化,且产物ee值也较高。
26、与现有技术相比,本发明具有如下优点:
27、1)本发明的合成工艺以3-硝基-5-三氟甲基水杨醛作为消旋化催化剂,能够实现结晶诱导不对称转化,相对于现有技术采用简单地对异构体进行拆分(理论上能达到的最大收率仅50%),产物纯度高,收率高,节约成本。
28、2)本发明的合成工艺,操作简单,易于实现工业化。
本文地址:https://www.jishuxx.com/zhuanli/20241120/335269.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表