通过ph调控实现巯基化合物和尿酸的荧光检测方法
技术领域
1.本发明属于分析检测领域,具体涉及一种通过ph调控实现巯基化合物和尿酸的荧光检测方法。
背景技术:
2.荧光分析法具有灵敏度高、选择性优异及响应时间迅速等优点,在无机离子、有机化合物、生物小分子检测方面应用广泛。根据荧光探针与分析物作用后,荧光强度的变化,荧光探针可分为强度变化型荧光探针和比率荧光探针两大类。强度变化型荧光探针主要利用探针与目标分析物作用后,荧光增强或减弱,来实现分析物检测。比率荧光探针本身也发荧光,与目标分析物作用后,探针的发射波长改变,通过两个波长下荧光强度的比值变化,实现分析物检测。尽管比率型荧光探针可消除部分环境因素的干扰,实现自我校正,但往往结构复杂,且需要精细的结构设计。
3.目前强度变化型荧光探针的研究主要集中在如何提高检测的灵敏度和选择性。在两种或多种目标分析物检测方面,强度变化型荧光探针主要通过先后加入不同分析物,荧光探针发生“关-开”或“开-关”转化来实现。当两种或多种目标分析物同时存在于样本中时,由于分析物间的相互干扰,强度变化型荧光探针无法检测。
技术实现要素:
4.针对背景技术中的技术问题,本发明利用弱碱性条件下,巯基化合物使siqds/cu
2-β-cd荧光增强;强碱性条件下,尿酸使siqds/cu
2-β-cd荧光减弱,实现对巯基化合物和尿酸的荧光检测。由于两种分析物在不同ph下,对siqds/cu
2-β-cd荧光强度的响应完全不同,可实现在一种分析物存在的条件下,对另一种分析物的检测。
5.本发明提供的通过ph调控实现巯基化合物和尿酸的荧光检测方法,包括以下步骤:
6.(1)将siqds/cu
2-β-cd溶于去离子水中,配制成siqds/cu
2-β-cd溶液;将siqds/cu
2-β-cd溶液与不同浓度的巯基化合物(或尿酸)标准溶液等体积混合,用1mol/l naoh溶液调节混合溶液ph值至规定值,室温下孵育60-120min,测定溶液的荧光发射光谱,建立溶液的荧光强度变化与巯基化合物、尿酸浓度之间的标准曲线;
7.(2)将样品溶液代替标准溶液,进行上述实验,将样品溶液的荧光信号强度带入标准曲线,可得到样品溶液中巯基化合物和尿酸的含量。
8.其中,siqds/cu
2-β-cd溶液浓度为0.4-0.7mg/ml。
9.测定巯基化合物时,混合溶液ph为8.0;测定尿酸时,混合溶液ph为13.0。
10.巯基化合物为半胱氨酸、谷胱甘肽或高半胱氨酸。
11.荧光测试条件为,用于荧光测量的仪器为f-280荧光分光光度计,激发和发射狭缝宽度均为10nm,激发波长为360nm,发射波长为440nm,样品池为10mm标准石英比色皿。
12.巯基化合物和尿酸标准溶液的浓度分别为:0,13.33,26.66,39.99,53.32,66.65,
79.98,93.31,106.64,119.97,133.33,159.96,186.62,213.28,239.94μmol/l和0,0.025,0.05,0.075,0.1,0.125,0.15mmol/l。
13.样品溶液为巯基化合物与尿酸混合溶液;
14.巯基化合物测定时,巯基化合物的浓度为300-600μmol/l,尿酸与其摩尔比为1:1-2:1;尿酸测定时,尿酸浓度为0.15-0.5mmol/l,巯基化合物与尿酸摩尔比为1:1-2:1。
15.本发明利用弱碱性条件下,巯基化合物上巯基与β-环糊精铜的强配位作用,使siqds/cu
2-β-cd荧光簇部分解体,体系中游离的siqds数量增加,荧光增强,来实现对巯基化合物的检测,在此条件下,尿酸对体系荧光强度无影响;在强碱性条件下,尿酸会缓慢分解,形成尿囊素和尿囊酸,cu
2-β-cd对尿囊素的包合作用,会提高cu
2-β-cd上铜的活性,从而可与更多的游离siqds结合,体系中游离的siqds数量减少,荧光强度减弱,而巯基化合物对体系荧光强度无影响。利用不同ph下,巯基化合物和尿酸对siqds/cu
2-β-cd荧光强度响应的显著差异,可在一种分析物存在的条件下,实现对另一种分析物的检测。
16.本发明的优点在于:灵敏度高,操作简单,其他干扰物种对被测物质的干扰小,通过ph调控可实现在巯基化合物和尿酸共存条件下,对单一目标物的检测。
附图说明:
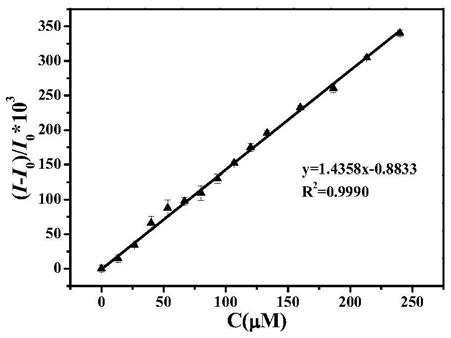
17.图1谷胱甘肽浓度与荧光强度变化率之间的线性关系图(即标准曲线);
18.图2尿酸浓度与荧光强度变化率之间的线性关系图(即标准曲线);
19.图3 ph=8时,尿酸存在对l-半胱氨酸检测的影响;
20.图4 ph=13时,l-半胱氨酸存在对尿酸检测的影响;
21.图5不同ph下,siqds/cu
2-β-cd荧光簇对l-半胱氨酸与尿酸的响应。
具体实施方式
22.下述实施例是对本发明内容的进一步详细地描述。应理解,这些实施例只是为了举例说明本发明,而非以任何方式限制本发明的范围。
23.实施例1
24.(1)将1.5ml不同浓度的谷胱甘肽标准溶液分别与浓度为0.4mg/ml的siqds/cu
2-β-cd荧光簇溶液等体积混合,用1mol/l naoh溶液调节混合溶液ph值至8,室温下孵育60min,测定溶液的荧光发射光谱,建立溶液的荧光强度变化与谷胱甘肽浓度之间关系曲线,以谷胱甘肽浓度为横坐标,荧光强度变化率为纵坐标,绘制标准曲线(如图1);
25.siqds/cu
2-β-cd荧光簇的制备:将浓度为1.0mg/ml的siqds稀释液与浓度为1.0mmol/l的cu
2-β-cd溶液(制备方法见cn111187614实施例3),按照体积比1:1混合,混合溶液总体积为1.5ml,室温静置15min,得到siqds/cu
2-β-cd荧光簇,加入5ml无水乙醇,混合均匀后,15000r/min高速离心15min,收集所得固体,40℃烘干,即可;
26.siqds稀释液的制备方法为:在4ml去离子水中加入1ml硅烷偶联剂kh-550溶液,磁力搅拌器搅拌30min后,加入浓度为0.1mol/l的抗坏血酸溶液1.25ml继续搅拌10min,溶液变为透亮微黄色,转移到25ml聚四氟乙烯的水热反应釜中,放入180℃的马弗炉中保温11h,待反应结束并冷却到室温,即得siqds原液,将其用去离子水稀释至规定浓度即为siqds稀释液。
27.(2)将待测谷胱甘肽与尿酸混合溶液代替标准溶液,进行上述实验,谷胱甘肽的浓度为300μmol/l,尿酸与其摩尔比为1:1,将样品溶液的荧光信号强度带入标准曲线,可得到样品溶液中谷胱甘肽的含量。
28.实施例2
29.(1)将1.5ml不同浓度的尿酸标准溶液分别与浓度为0.7mg/ml的siqds/cu
2-β-cd荧光簇溶液等体积混合,用1mol/l naoh溶液调节混合溶液ph值至13,室温下孵育120min,测定溶液的荧光发射光谱,建立溶液的荧光强度变化与尿酸浓度之间的关系曲线,以尿酸浓度为横坐标,荧光强度变化率为纵坐标,绘制标准曲线(如图2);
30.(2)将尿酸与半胱氨酸混合样品溶液代替标准溶液,尿酸浓度为0.5mmol/l,半胱氨酸与尿酸摩尔比为1:1,进行上述实验,将样品溶液的荧光信号强度带入标准曲线,可得到样品溶液中尿酸的含量。
31.实施例3
32.(1)将1.5ml不同浓度的高半胱氨酸标准溶液分别与浓度为0.5mg/ml的siqds/cu
2-β-cd荧光簇溶液等体积混合,用1mol/l naoh溶液调节混合溶液ph值至8,室温下孵育70min,测定溶液的荧光发射光谱,建立溶液的荧光强度变化与高半胱氨酸浓度之间的关系曲线,以高半胱氨酸浓度为横坐标,荧光强度变化率为纵坐标,绘制标准曲线;
33.(2)将尿酸与高半胱氨酸混合样品溶液代替标准溶液,高半胱氨酸浓度为600μmol/l,尿酸与其摩尔比为1.5:1,进行上述实验,将样品溶液的荧光信号强度带入标准曲线,可得到样品溶液中高半胱氨酸的含量。
34.实施例4
35.(1)将1.5ml l-半胱氨酸(l-cys)与1.5ml浓度为0.4mg/ml的siqds/cu
2-β-cd荧光簇溶液混合,混合溶液中l-半胱氨酸的浓度为300μmol/l,用1mol/l naoh溶液调节混合溶液ph值至8,室温下孵育60min,测定溶液的荧光发射光谱;
36.(2)将1.5ml l-半胱氨酸(l-cys)与尿酸(ua)的混合溶液与1.5ml浓度为0.4mg/ml的siqds/cu
2-β-cd荧光簇溶液混合,混合溶液中l-半胱氨酸与尿酸的浓度分别为300μmol/l和600μmol/l,用1mol/l naoh溶液调节混合溶液ph值至8,室温下孵育60min,测定溶液的荧光发射光谱;将上述荧光发射光谱作图(如图3),从图3可知,ph=8,尿酸存在或不存在时,l-半胱氨酸对siqds/cu
2-β-cd荧光簇荧光强度的影响情况完全一样,表明即使在尿酸存在条件下,也不影响siqds/cu
2-β-cd荧光探针对l-半胱氨酸的检测。
37.实施例5
38.(1)将1.5ml尿酸(ua)与1.5ml浓度为0.7mg/ml的siqds/cu
2-β-cd荧光簇溶液混合,混合溶液中尿酸的浓度为0.15mmol/l,用1mol/l naoh溶液调节混合溶液ph值至13,室温下孵育120min,测定溶液的荧光发射光谱;
39.(2)将1.5ml l-半胱氨酸(l-cys)与尿酸(ua)的混合溶液与1.5ml浓度为0.7mg/ml的siqds/cu
2-β-cd荧光簇溶液混合,混合溶液中l-半胱氨酸与尿酸的浓度分别为0.3mmol/l和0.15mmol/l,用1mol/l naoh溶液调节混合溶液ph值至13,室温下孵育120min,测定溶液的荧光发射光谱;将上述荧光发射光谱作图(如图4),从图4可知,ph=13,l-半胱氨酸存在或不存在时,尿酸对siqds/cu
2-β-cd荧光簇荧光强度的影响情况完全一样,表明即使在l-半胱氨酸存在条件下,也不影响siqds/cu
2-β-cd荧光探针对尿酸的检测。
40.实施例6
41.配制两份1.5ml浓度为0.6mg/ml的siqds/cu
2-β-cd荧光簇溶液,在一份siqds/cu
2-β-cd荧光簇溶液中加入1.5ml尿酸(ua)或半胱氨酸溶液,尿酸或半胱氨酸在荧光簇溶液中的浓度分别为0.5mmol/l和600μmol/l,在另一份siqds/cu
2-β-cd荧光簇溶液中加入1.5ml去离子水,将其作为空白溶液,两份溶液分别用1mol/l naoh溶液调节混合溶液ph值至8或10或13,室温下孵育120min,测定两份溶液的荧光发射光谱;以空白溶液作为基准,计算荧光强度变化,结果如图5。
42.从图5可知,ph 8时,半胱氨酸使siqds/cu
2-β-cd溶液荧光增加35%,尿酸对siqds/cu
2-β-cd溶液荧光强度影响可忽略;ph 13时,尿酸使siqds/cu
2-β-cd溶液荧光降低30%,而半胱氨酸对siqds/cu
2-β-cd溶液荧光强度影响可忽略;因此,在ph 8时,可实现在尿酸存在下对半胱氨酸的检测;在ph 13时,可实现在半胱氨酸存在下对尿酸的检测。ph 10时,半胱氨酸使siqds/cu
2-β-cd溶液荧光增加17%,尿酸使siqds/cu
2-β-cd溶液荧光降低52%,在此ph下,半胱氨酸和尿酸间存在相互干扰,不可在一种分析物存在下对另一分析物检测。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
