1.本发明属于电解水技术领域,具体涉及一种基于单电解槽双电极两步法分步电解水制氢的方法及装置。
背景技术:
2.能源是现在人类社会运转的重要保障。自第二次工业革命以来,煤、石油以及天然气等化石能源的广泛使用,极大的推动了社会发展和提高了人们的生活质量,但也带来了温室效应、空气海洋土地污染等一系列问题。同时中国作为石油天然气进口国,发展受能源输出国的制约。在碳中和以及国家高速发展的背景下,寻找来源广泛且可靠的低碳能源成为一项重要课题。
3.目前水电容量趋向于饱和,人们将目光转向了风电和光电等清洁可再生能源。然而这两种能源获取受环境制约,发电不稳定,直接并网使用容易损坏电网。电解水制氢是解决这一问题的重要手段。氢气密度小、比能量大,且燃烧过程仅生成水,不会对环境造成任何污染,是储能的良好介质。且电解水的原料来源十分广泛,几乎可以随时随地进行。因此电解水制备氢气日益受到人们重视。
4.碱性电解水技术发展最早,工业化较为成熟,应用最为广泛。然而电解过程中氢气和氧气同时同地产生,容易发生混合,难以直接获得较高纯度的氢气,往往需要额外成本提纯。随后发展出基于质子交换膜的酸性电解水,膜的存在可以隔绝阴阳极。然后电化学析氢析氧本身动力学有所差异,使得膜两侧存在压差,易对膜造成损坏,从而减少装置的使用寿命。同时目前性能良好的质子交换膜(如nafion膜)价格较高,提高了电解水的成本。质子交换膜的存在也增大了电解槽内阻,使得电解水能耗增加,能效下降。
5.针对上述问题,我们(王永刚;夏永姚;谌龙)已经发明了一种基于三电极体系的两步法电解水制氢的方法及装置(专利申请号:201510799110.3)以及一种三电极体系双电解槽两步法电解水制氢的装置及方法(专利申请号:201610164054.0),实现了产氢与产氧步骤在时间上的分离,在不需要隔膜的情况下实现了碱性电解水制取纯氢和纯氧。然而这两种方法均基于三电极体系,在产氢和产氧步骤间需要切换外电路连接的电极,这增加了电解操作的复杂度,降低了可行性。同时频繁的电极切换不利于电解槽的串并联集成化,不利于纯氢的大规模工业化制备。
技术实现要素:
6.本发明目的在于克服电解水的难点,提出一种制氢纯度高、成本低且易于串并联集成化的基于单电解槽双电极两步法分步电解水制氢的方法及装置。
7.本发明所提供的基于单电解槽双电极两步法分步电解水制氢的装置,包含一个电解槽,以及放置在电解槽中的一个析氢析氧双功能电极和氢氧化镍电极。
8.本发明中,析氢析氧双功能电极既能催化电解水生成氢气,也能催化电解水,该具
有催化作用的电极材料可以是一种析氢析氧双功能材料,也可以是析氢电极材料和析氧电极材料的复合材料。
9.本发明中,所述析氢析氧双功能材料对电解水生成氢气和氧气均有催化作用。具体的,该具有催化作用的电极材料为:pt电极;或基于cu-co-mo-o的化合物;或基于ni-co-mo-s的化合物;或基于ni-p的化合物;或基于co-p的化合物;或基于ni-mo-co的金属化合物;或fep化合物;或n、p、o、s掺杂的碳材料。
10.本发明中,所述析氢电极材料对电解水生成氢气有催化作用,该具有催化作用的电极材料为:基于金属铂以及其与碳的复合物;或基于ni、co或fe过渡金属的单质或化合物;或基于cu的化合物;或基于w的化合物;或基于mo的化合物;或c3n4化合物。
11.本发明中,所述析氢电极材料对电解水生成氧气有催化作用,该具有催化作用的电极材料为:基于ru或ir贵金属的化合物;或基于ni、co、fe或mn过渡金属的单质或化合物;或n、s、p掺杂的碳;或漆酶等生物电化学催化剂。
12.本发明中,所述氢氧化镍电极为由ni(oh)2活性物质和其他添加成分组成,所述添加成分为银粉、co(oh)2、碳粉及粘结剂中的一种或者几种。
13.本发明中,所述ni(oh)2活性物质和添加成分通过混合成膜或者成浆料的方式,压制或者涂覆在金属集流体上构成ni(oh)2电极;所述金属集流体包括:镍网、泡沫镍、不锈钢网或钛网。
14.本发明中,所述电解水的技术的电解液是碱性水溶液,碱性水溶液溶质为氢氧化钾或氢氧化钠。
15.本发明中,所述装置作为一个电解水单元,多个单元间可以通过不同单元的ni(oh)2电极和析氢析氧双功能电极相连的方式进行串联,也可以通过不同单元的ni(oh)2电极之间以及析氢析氧双功能电极之间相连的方式进行并联。
16.本发明进一步提供基于上述装置的基于单电解槽双电极两步法分步电解水制氢方法,具体步骤包括:(一)电解制氢:
在电解槽中,h2o在作为阴极的析氢析氧双功能电极的表面被电化学还原为h2,即2h2o 2e-→ꢀ
h2↑
oh-;同时作为阳极的ni(oh)2电极被电化学氧化为niooh电极,即ni(oh)
2 oh-ꢀ‑ꢀ
e-→
niooh h2o;此过程中电子由ni(oh)2电极经由外电路流向析氢析氧双功能电极;(二)电解制氧:在电解罐中,作为阴极的niooh电极被电化学还原为ni(oh)2电极,即niooh h2o e-→ꢀ
ni(oh)
2 oh-;同时oh-在作为阳极的析氢析氧双功能电极的表面被电化学氧化为o2, 即4oh-‑ꢀ
4e-→
2h2o o2↑
;此过程中电子由析氢析氧双功能电极经由外电路流向niooh电极。
17.所述步骤(一)和步骤(二)交替进行,实现纯氢的制取。
18.和现有技术相比,本发明的有益效果在于:本发明设计的基于单电解槽双电极两步法分步电解水制氢最显著的特点是利用ni(oh)
2-niooh作为氧化还原媒介,将电解水分解成两步,实现制氢和制氧在时间上的分离,不需要隔膜即可得到纯氢。此外通过使用析氢析氧双功能电极,使得分步电解可以在两个电极上实现,制氢和制氧之间无需切换电极,可以减少操作复杂度。并且电解槽之间可以方便的串并联集成化,以实现工业化大规模分步电解水制氢。
19.与传统的酸性电解水制氢相比,本发明不涉及氢气和氧气的同时产生,不需要离子交换膜来分隔两极,直接生成高纯氢气,大幅降低电解成本。同时单电解槽的结构便于操作及其在实际生产中串并联,易于扩大规模,提高生产效率。
附图说明
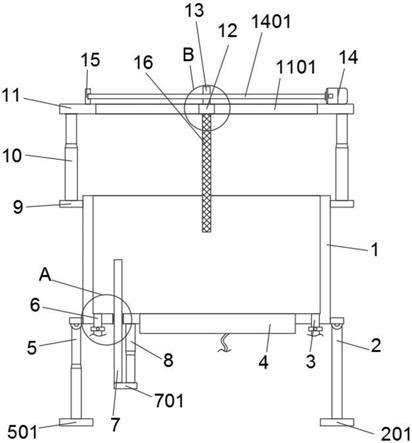
20.图1为基于单电解槽双电极两步法分步电解水制氢的装置及方法示意图。
21.图2为基于单电解槽双电极两步法分步电解水制氢的电解曲线。
22.图3为三个电解槽串联示意图。
具体实施方式
23.为进一步清楚地说明本发明的技术方案和优点,本发明用以下具体实施例进行说明,但是本发明并不局限于这些例子。
24.实施例1析氢析氧双功能电极采用cop@n掺杂石墨烯电极,氢氧化镍电极采用市场购买的商业化氢氧化镍电极。所有电极均为20平方厘米。电解液采用500毫升1摩尔/升的氢氧化钾溶液,采用200毫安恒电流,使用2a量程的蓝电电池测试装置进行恒流电解。首先阴极连接析氢析氧双功能电极,阳极连接氢氧化镍(ni(oh)2)电极,施加200毫安电流,持续600秒,平均电压为1.58v。此时析氢析氧双功能电极上生成氢气并收集,ni(oh)2电极氧化为羟基氧化镍(niooh)电极。随后阴极连接niooh电极,阳极连接析氢析氧双功能电极,施加200毫安电流,持续600秒,结束时电压上升至1.0v,平均电压为0.52v。此时析氢析氧双功能电极上生成氧气并收集,niooh电极被还原为ni(oh)2电极。收集两种气体的过程中分别使用气相质谱鉴定,证实氢气和氧气没有发生混合。(图2)(见表1)。
25.实施例2
析氢析氧双功能电极采用co3o4@石墨烯,氢氧化镍电极采用市场购买的商业化氢氧化镍电极。所有电极均为20平方厘米。电解液采用500毫升1摩尔/升的氢氧化钾溶液,采用200毫安恒电流,使用2a量程的蓝电电池测试装置进行恒流电解。首先阴极连接析氢析氧双功能电极,阳极连接氢氧化镍(ni(oh)2)电极,施加200毫安电流,持续600秒,平均电压为1.65v。此时析氢析氧双功能电极上生成氢气并收集,ni(oh)2电极氧化为羟基氧化镍(niooh)电极。随后阴极连接niooh电极,阳极连接析氢析氧双功能电极,施加200毫安电流,持续600秒,结束时电压上升至1.0v,平均电压为0.67v。此时析氢析氧双功能电极上生成氧气并收集,niooh电极被还原为ni(oh)2电极。收集两种气体的过程中分别使用气相质谱鉴定,证实氢气和氧气没有发生混合。(见表1)。
26.实施例3析氢析氧双功能电极采用mos2@ni3s2,氢氧化镍电极采用市场购买的商业化氢氧化镍电极。所有电极均为20平方厘米。电解液采用500毫升1摩尔/升的氢氧化钾溶液,采用200毫安恒电流,使用2a量程的蓝电电池测试装置进行恒流电解。首先阴极连接析氢析氧双功能电极,阳极连接氢氧化镍(ni(oh)2)电极,施加200毫安电流,持续600秒,平均电压为1.55v。此时析氢析氧双功能电极上生成氢气并收集,ni(oh)2电极氧化为羟基氧化镍(niooh)电极。随后阴极连接niooh电极,阳极连接析氢析氧双功能电极,施加200毫安电流,持续600秒,结束时电压上升至1.0v,平均电压为0.51v。此时析氢析氧双功能电极上生成氧气并收集,niooh电极被还原为ni(oh)2电极。收集两种气体的过程中分别使用气相质谱鉴定,证实氢气和氧气没有发生混合。(见表1)。
27.实施例4析氢析氧双功能电极采用cu-co-mo-o 复合物,氢氧化镍电极采用市场购买的商业化氢氧化镍电极。所有电极均为20平方厘米。电解液采用500毫升1摩尔/升的氢氧化钾溶液,采用200毫安恒电流,使用2a量程的蓝电电池测试装置进行恒流电解。首先阴极连接析氢析氧双功能电极,阳极连接氢氧化镍(ni(oh)2)电极,施加200毫安电流,持续600秒,平均电压为1.60v。此时析氢析氧双功能电极上生成氢气并收集,ni(oh)2电极氧化为羟基氧化镍(niooh)电极。随后阴极连接niooh电极,阳极连接析氢析氧双功能电极,施加200毫安电流,持续600秒,结束时电压上升至1.0v,平均电压为0.54v。此时析氢析氧双功能电极上生成氧气并收集,niooh电极被还原为ni(oh)2电极。收集两种气体的过程中分别使用气相质谱鉴定,证实氢气和氧气没有发生混合。(见表1)。
28.实施例5析氢析氧双功能电极采用fep@石墨烯,氢氧化镍电极采用市场购买的ni(oh)2@碳纳米管。所有电极均为20平方厘米。电解液采用500毫升1摩尔/升的氢氧化钾溶液,采用200毫安恒电流,使用2a量程的蓝电电池测试装置进行恒流电解。首先阴极连接析氢析氧双功能电极,阳极连接氢氧化镍(ni(oh)2)电极,施加200毫安电流,持续600秒,平均电压为1.63v。此时析氢析氧双功能电极上生成氢气并收集,ni(oh)2电极氧化为羟基氧化镍(niooh)电极。随后阴极连接niooh电极,阳极连接析氢析氧双功能电极,施加200毫安电流,持续600秒,结束时电压上升至1.0v,平均电压为0.58v。此时析氢析氧双功能电极上生成氧气并收集,niooh电极被还原为ni(oh)2电极。收集两种气体的过程中分别使用气相质谱鉴定,证实氢气和氧气没有发生混合。(见表1)。
29.实施例6析氢析氧双功能电极采用c3n4@石墨烯复合iro2,氢氧化镍电极采用市场购买的商业化氢氧化镍电极。所有电极均为20平方厘米。电解液采用500毫升1摩尔/升的氢氧化钾溶液,采用200毫安恒电流,使用2a量程的蓝电电池测试装置进行恒流电解。首先阴极连接析氢析氧双功能电极,阳极连接氢氧化镍(ni(oh)2)电极,施加200毫安电流,持续600秒,平均电压为1.59v。此时析氢析氧双功能电极上生成氢气并收集,ni(oh)2电极氧化为羟基氧化镍(niooh)电极。随后阴极连接niooh电极,阳极连接析氢析氧双功能电极,施加200毫安电流,持续600秒,结束时电压上升至1.0v,平均电压为0.53v。此时析氢析氧双功能电极上生成氧气并收集,niooh电极被还原为ni(oh)2电极。收集两种气体的过程中分别使用气相质谱鉴定,证实氢气和氧气没有发生混合。(见表1)。
30.实施例7析氢析氧双功能电极采用mos2@石墨烯复合iro2,氢氧化镍电极采用市场购买的商业化氢氧化镍电极。所有电极均为20平方厘米。电解液采用500毫升1摩尔/升的氢氧化钾溶液,采用200毫安恒电流,使用2a量程的蓝电电池测试装置进行恒流电解。首先阴极连接析氢析氧双功能电极,阳极连接氢氧化镍(ni(oh)2)电极,施加200毫安电流,持续600秒,平均电压为1.60v。此时析氢析氧双功能电极上生成氢气并收集,ni(oh)2电极氧化为羟基氧化镍(niooh)电极。随后阴极连接niooh电极,阳极连接析氢析氧双功能电极,施加200毫安电流,持续600秒,结束时电压上升至1.0v,平均电压为0.51v。此时析氢析氧双功能电极上生成氧气并收集,niooh电极被还原为ni(oh)2电极。收集两种气体的过程中分别使用气相质谱鉴定,证实氢气和氧气没有发生混合。(见表1)。
31.实施例8析氢析氧双功能电极采用mos2@ni3s2,氢氧化镍电极采用市场购买的商业化氢氧化镍电极。所有电极均为20平方厘米。将3个电解槽根据图3的方式进行三串联集成,电解液均采用500毫升1摩尔/升的氢氧化钾溶液,采用200毫安恒电流,使用2a量程的蓝电电池测试装置进行恒流电解。首先阴极连接析氢析氧双功能电极,阳极连接氢氧化镍(ni(oh)2)电极,施加200毫安电流,持续600秒,平均电压为4.70v。此时析氢析氧双功能电极上生成氢气并收集,ni(oh)2电极氧化为羟基氧化镍(niooh)电极。随后阴极连接niooh电极,阳极连接析氢析氧双功能电极,施加200毫安电流,持续600秒,结束时电压上升至3.0v,平均电压为1.60v。此时析氢析氧双功能电极上生成氧气并收集,niooh电极被还原为ni(oh)2电极。收集两种气体的过程中分别使用气相质谱鉴定,证实氢气和氧气没有发生混合。(见表1)。
32.表1采用不同电极组装以及连接方式的电解槽200毫安恒电流电解水性能比较
。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。