KDM7A作为靶点在防治骨质疏松和肿瘤骨转移中的应用
- 国知局
- 2024-07-12 10:19:55
本发明属于生物医药,涉及kdm7a作为靶点在治疗骨质疏松及肿瘤骨转移的潜在应用。
背景技术:
1、骨质疏松症一种以骨密度和骨质量低下、骨组织超微结构退变为特征的,导致骨脆性及骨折风险增加的全身代谢性骨病。
2、目前临床上治疗骨质疏松症的药物主要机制包括促进骨形成和抑制骨吸收两种:促进骨形成的药物种类少,而抑制骨吸收类药物会带来各种不良反应。因此,迫切需要开发新的骨质疏松症治疗方法。
3、组蛋白赖氨酸去甲基化酶7a(histone lysine demethylase 7a,kdm7a)使组蛋白h3的赖氨酸9或赖氨酸27(h3k9me2,h3k27me2)去甲基化,属于包含jumonji c(jmjc)结构域的组蛋白去甲基化酶家族。kdm7a具有多种生物学功能,包括调节神经元分化和发育、前后轴发育及参与肿瘤发生。
4、目前现有技术中尚未有记载kdm7a具有调控骨量和骨稳态的研究报道。
技术实现思路
1、针对现有技术的不足和实际需求,本发明提出组蛋白赖氨酸去甲基化酶7a(histone lysine demethylase 7a,kdm7a)在制备治疗骨质疏松药物中的应用,该药物可通过靶向kdm7a来治疗骨质疏松。
2、kdm7a基因位于人类7号染色体和小鼠6号染色体上,其成熟多肽是含有941个(人)/940个(小鼠)氨基酸蛋白,多肽氨基酸序列如seq no id.1(人)或seq no id.2(鼠)所示,现有报道显示,kdm7a具有多种生物学功能,包括调节神经元分化和发育、前后轴发育及参与肿瘤发生。
3、seq no id.1:
4、
5、
6、seq no id.2:
7、
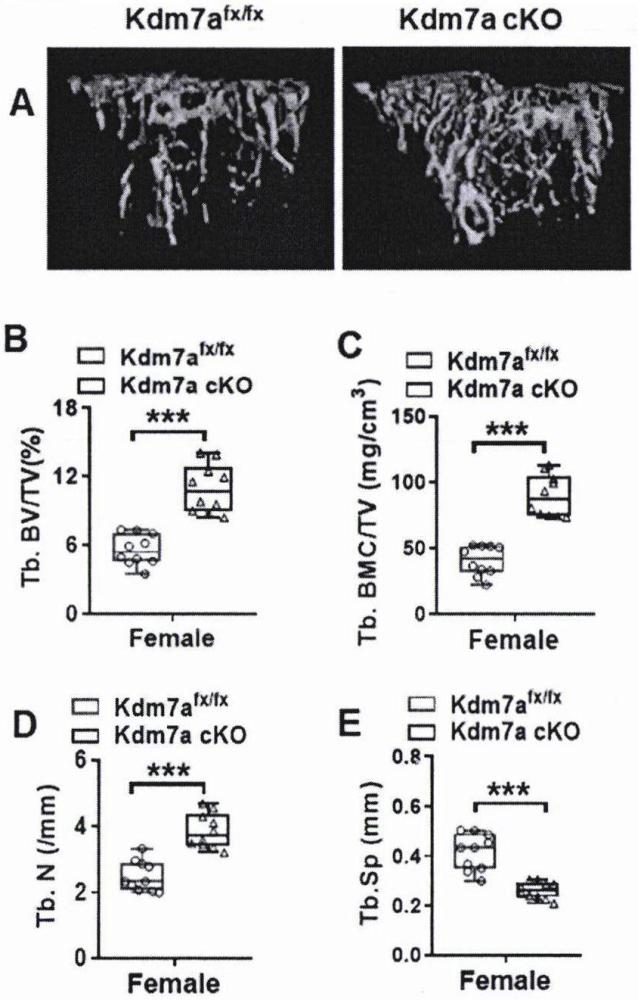
8、本发明kdm7a能够调控骨量和骨稳态。在小鼠成骨祖细胞中敲除kdm7a编码基因(表示为kdm7a)能够增加成骨细胞,减少破骨细胞,增加骨量;成骨祖细胞中敲除kdm7a编码基因能抵抗卵巢切除(ovx)引起的骨量丢失。kdm7a能够移除fap和rankl启动子区的h3k9和h3k27的二甲基化标记,促进fap和rankl表达。下调kdm7a有利于促进骨形成和抑制骨吸收,增加骨量,具有治疗骨质疏松症等骨骼代谢性疾病的潜力。
9、本发明还提出kdm7a在制备骨质疏松的检测试剂中的应用。
10、本发明还提出kdm7a在制备防治肿瘤骨转移药物中的应用。
11、kdm7a基因位于人类7号染色体和小鼠6号染色体上,主要通过去除组蛋白h3的赖氨酸9或赖氨酸27(h3k9me2,h3k27me2)二甲基化,进而对基因转录发挥调控作用。现有报道显示,kdm7a蛋白主要在神经分化、肿瘤发生发展等过程中发挥重要调节作用。发明人经研究发现,特异性敲除小鼠成骨细胞谱系中的kdm7a基因,可以使小鼠骨量增加,从而可以治疗骨质疏松。
12、根据本发明的第一个方面,本发明提供一种骨质疏松的潜在治疗药物,所述治疗药物靶向作用于kdm7a编码基因或其蛋白,特异性地调控与骨质疏松相关的基因或蛋白表达,达到精准治疗骨质疏松的目的。该药物特异性强,副作用小,不会增加骨折的风险或诱发其他病症。
13、本发明提出了kdm7a在制备治疗骨质疏松药物中的应用,所述药物包括下述(1)-(4)中的任一种:
14、(1)靶向成骨谱系中的kdm7a编码基因或其蛋白的药物;
15、(2)用于增加成骨细胞、或减少破骨细胞数目和活性,促进骨量增加的药物;
16、(3)用于下调或抑制成纤维细胞激活蛋白α(fibroblast activation proteinα,fap)的药物;
17、(4)用于下调或抑制核因子-κb受体活化因子配体(receptor activator ofnuclear factor-κb ligand,rankl)的药物。
18、在本发明的一些实施方式中,所述药物为kdm7a下调剂或抑制剂,用于促进成骨细胞分化,增加骨形成及骨量,进而治疗所述骨质疏松。
19、在本发明的一些实施方式中,所述药物为kdm7a下调剂或抑制剂,用于抑制破骨细胞分化,抑制骨吸收,增加骨量,进而治疗所述骨质疏松。
20、在本发明的一些实施方式中,所述药物为kdm7a下调剂或抑制剂,用于下调或抑制成纤维细胞激活蛋白α(fibroblast activation proteinα,fap)的药物,以治疗所述骨质疏松。
21、在本发明的一些实施方式中,所述药物为kdm7a下调剂或抑制剂,用于下调或抑制核因子-κb受体活化因子配体(receptor activator of nuclear factor-κb ligand,rankl)的药物,以治疗所述骨质疏松。
22、在本发明的一些实施方式中,所述药物为kdm7a下调剂或抑制剂,通过下调或抑制kdm7a蛋白,下调或抑制所述成骨谱系中的fap蛋白,进而增加成骨细胞分化、增加血清中i型前胶原氨基端原肽(pinp)水平,及增加骨矿化沉积率(mar)、矿化表面(ms/bs)和骨形成率(bfr/bs)等,最终促进骨量增加,以治疗所述骨质疏松。
23、在本发明的一些实施方式中,所述药物为kdm7a下调剂或抑制剂,通过下调或抑制kdm7a蛋白,下调或抑制所述成骨谱系中的rankl蛋白,进而减少破骨细胞分化、降低血清中i型胶原c端肽(ctx-1)水平,减少骨吸收,最终促进骨量增加,以治疗所述骨质疏松。
24、在本发明的一些实施方式中,所述药物包括针对所述kdm7a编码基因的敲低药物、敲除药物或针对kdm7a蛋白的抑制药物中的至少一种。
25、在本发明的一些实施方式中,针对所述kdm7a编码基因的敲低药物包括靶向所述kdm7a编码基因的shrna、sirna或crispr/cas药物中的任一种。
26、在本发明的一些实施方式中,针对所述kdm7a编码基因的敲除药物为包括cre/loxp系统的药物,用于特异性敲除所述成骨细胞谱系中的所述kdm7a编码基因。
27、在本发明的一些实施方式中,所述针对kdm7a蛋白的抑制药物包括小分子化合物或多肽中的任一种。
28、所述抑制药物通过与所述成骨细胞谱系中的所述kdm7a蛋白特异性结合,以阻断所述kdm7a蛋白发挥相应的作用。
29、根据本发明的第二个方面,提出了kdm7a在制备骨质疏松的检测试剂中的应用,所述检测试剂以所述kdm7a作为骨质疏松的生物标记物。
30、根据本发明的第三个方面,提出了kdm7a在制备防治肿瘤骨转移药物中的应用,所述药物包括下述1)~4)中的任一种:
31、(1)靶向成骨谱系中的kdm7a编码基因或其蛋白的药物;
32、(2)用于增加成骨细胞、或减少破骨细胞数目和活性,促进骨量增加的药物;
33、(3)用于下调或抑制fap蛋白的药物;
34、(4)用于下调或抑制rankl蛋白的药物。
35、在本发明的一些实施方式中,所述药物为kdm7a下调剂或抑制剂,用于促进成骨细胞分化,增加骨形成及骨量,进而防治所述肿瘤骨转移。
36、在本发明的一些实施方式中,所述药物为kdm7a下调剂或抑制剂,用于抑制破骨细胞分化,抑制骨吸收,增加骨量,进而防治所述肿瘤骨转移。
37、在本发明的一些实施方式中,所述药物为kdm7a下调剂或抑制剂,用于下调或抑制fap蛋白的药物,增加骨形成和骨量,以防治所述肿瘤骨转移。
38、在本发明的一些实施方式中,所述药物为kdm7a下调剂或抑制剂,用于下调或抑制rankl蛋白的药物,抑制骨吸收,促进骨量增加,以防治所述肿瘤骨转移。
39、所述药物通过下调kdm7a,最终促进骨形成和抑制骨吸收,使所述骨量的增加,骨细胞占位增加,进而可以防治肿瘤的骨转移症状,促进肿瘤患者预后。
40、优选地,所述骨质疏松的潜在治疗药物还包括药学上可接受的辅料。
41、优选地,所述辅料包括赋形剂、稀释剂、载体或助溶剂中的任意一种或至少两种的组合。
42、与现有技术相比,本发明具有以下有益效果:
43、本发明首次发现kdm7a能够调控骨量和骨稳态。在小鼠成骨祖细胞中敲除kdm7a基因能够增加成骨细胞,减少破骨细胞,增加骨量;成骨祖细胞中敲除kdm7a基因能抵抗卵巢切除(ovx)引起的骨量丢失。kdm7a能够移除fap和rankl启动子区的h3k9和h3k27的二甲基化标记,促进fap和rankl表达。下调kdm7a有利于促进骨形成和抑制骨吸收,增加骨量,具有治疗骨质疏松症等骨骼代谢性疾病的潜力。
本文地址:https://www.jishuxx.com/zhuanli/20240615/86258.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表