1.本发明属于生物医药技术领域,具体涉及一种钙超载型小分子药物自组装纳米粒子及其在制备免疫佐剂中的应用。
背景技术:
2.恶性肿瘤是当前严重威胁人类生命健康的重大疾病之一。近年来,利用离子干扰疗法特别是钙离子进行肿瘤治疗逐渐成为研究人员关心的热点。钙离子是人体的一种常量元素,在人体内部的平衡稳态与细胞代谢和增殖密切相关。目前已有研究指出,钙离子ca2 作为细胞信号传导的第二信使,参与了细胞凋亡信号等过程的传导。若体内钙离子平衡稳态被打破,钙离子充分进入胞质,便会导致细胞钙超载(calcium overload)。当前,学术界对于钙超载这一新型的诱导肿瘤细胞凋亡形式的关注逐年提高。
3.目前在临床研究上,主要通过钙电穿孔的方式诱导细胞钙超载进行治疗。钙电穿孔作为一种治疗恶性肿瘤的手段,其突出的优点是相比于传统的手术切除,其针对皮下转移瘤的治疗更加容易,无需进行手术即可基本消除肿瘤。但是其仍存在许多问题和缺点,其一,此种方法需要额外的电脉冲仪器,使用成本高;其二,此种方法治疗范围窄,目前在临床研究中仅适用于皮下转移瘤;其三,此方法首先需要在患处注射大量氯化钙,对于心脏功能不全者可能不适用。
4.2020年,诺贝尔奖聚焦于辣椒素受体(trpv1),这种受体在受到药物刺激后能够打开,使得细胞间质液中高浓度的ca
2
进入细胞内部,因此可以用来作为钙超载的诱导手段。姜黄素(curcumin)作为经典的抗癌药物,能够促进细胞内质网钙离子储库释放出钙并抑制钙的外排。因此,将二者结合,可以“内外兼修”的促进细胞内部钙离子水平的提高且不会增加心脏负担。目前未见有将trpv1激动剂和姜黄素联合用来诱导钙超载的应用。
技术实现要素:
5.本发明的目的是提供一种钙超载型小分子药物自组装纳米粒子,通过采用trpv1激动剂和姜黄素联合的纳米粒子取代成本较高且繁琐的电穿孔技术,能够实现对于肿瘤的钙超载和免疫治疗的效果。
6.为了实现上述目的,本发明采用以下技术方案:一种钙超载型小分子药物自组装纳米粒子,由姜黄素、trpv1激动剂和稳定剂制成;所述trpv1激动剂选自辣椒素、树脂毒素、维生素d、胡椒碱、吴茱萸碱、花椒麻素、辣椒素酯、6-姜烯酚、姜辣素、姜油酮、姜酮酚或水蓼二醛;所述稳定剂选自吐温80、维生素e聚乙二醇琥珀酸酯、聚氧乙烯吡咯烷酮、聚乙烯醇、dspe-peg2000或泊洛沙姆。
7.进一步地,所述trpv1激动剂为辣椒素或树脂毒素。
8.进一步地,所述稳定剂为聚氧乙烯吡咯烷酮或dspe-peg
2000
。
9.上述钙超载型小分子药物自组装纳米粒子的制备方法,包括以下步骤:步骤1,将姜黄素溶解于有机溶剂中,浓度为1~50 mg/ml,优选为10~20 mg/ml;步骤2,将trpv1激动剂溶解于有机溶剂中,浓度为1~50 mg/ml,优选为10~20 mg/ml;步骤3,将稳定剂溶解于水中,浓度为1~100 % w/w,优选为1%~10% w/w;步骤4,将步骤1的姜黄素溶液和步骤2的trpv1激动剂溶液混合,然后加至步骤3的稳定剂溶液中混合;步骤5,将步骤4得到的混合溶液加到水中,于10~80℃下100-1000 rpm搅拌0.1~4 h后,停止搅拌,静置24 h除去有机溶剂,即得到钙超载型小分子自组装纳米粒子。
10.进一步地,所述有机溶剂为乙醇、二氯甲烷、三氯甲烷、二甲基亚砜、丙酮、乙腈或四氢呋喃。优选乙醇、四氢呋喃或丙酮。
11.进一步地,将步骤4得到的混合溶液加到水中,于10~50℃下200-800 rpm搅拌0.1~2 h后,停止搅拌,静置24 h除去有机溶剂。优选地,于20~30℃下200-400 rpm搅拌0.1~5h。
12.上述钙超载型小分子药物自组装纳米粒子在制备免疫佐剂中的应用。
13.上述钙超载型小分子药物自组装纳米粒子在制备肿瘤治疗药物中的应用。
14.本发明利用姜黄素在水中能够自组装形成纳米粒子以及其和trpv1激动剂能够依赖疏水作用力形成纳米粒子的能力制备得到小分子药物自组装纳米粒子。该纳米粒子使得姜黄素和trpv1激动剂发挥协同作用,促进细胞内部钙离子水平的提高且不会增加心脏负担。由于钙超载能够促进细胞免疫原死亡过程中的危险信号模式分子的释放(damps),因此还可以将其应用拓展并作为免疫佐剂和化疗药物联用。
附图说明
15.图1为小分子药物自组装纳米粒子的外观和结构示意图。
16.图2为小分子药物自组装纳米粒子的粒径分布和外观图。
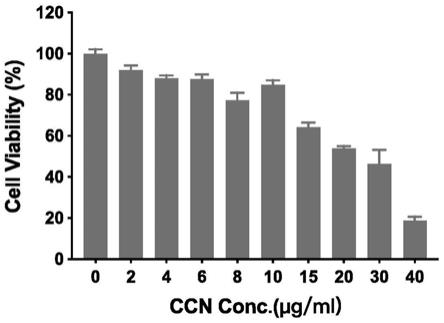
17.图3为小分子药物自组装纳米粒子对于4t1肿瘤细胞杀伤结果。
18.图4为小分子药物自组装纳米粒子促进树突状细胞成熟的结果。
19.图5为小分子药物自组装纳米粒子诱导线粒体膜电位去极化结果。
20.图6为小分子药物自组装纳米粒子和化疗药物联合后对于4t1乳腺癌细胞杀伤结果。
21.图7为小分子药物自组装纳米粒子促进4t1乳腺癌细胞表面crt暴露结果。
22.图8为小分子药物自组装纳米粒子处理4t1乳腺癌细胞后促进树突状细胞成熟结果。
23.图9为小分子药物自组装纳米粒子促进小鼠淋巴结树突状细胞成熟结果。
24.图10为小分子药物自组装纳米粒子促进小鼠肿瘤cd8
t细胞浸润结果。
25.图11为小分子药物自组装纳米粒子抑制4t1乳腺癌生长结果。
具体实施方式
26.下面结合附图和具体实施例对本发明作进一步详细说明,但不应理解为对本发明的限制。在不背离本发明精神和实质的情况下,对本发明方法、步骤或条件所作的修改或替
换,均属于本发明的范围。实施例中未注明具体条件的实验方法及未说明配方的试剂均为按照本领域常规条件。
27.实施例1步骤1,取2 mg和姜黄素和2 mg辣椒素分别加入装有0.1 ml四氢呋喃和0.1 ml无水乙醇的1.5 ml离心管中,分别得到姜黄素溶液和辣椒素溶液。
28.步骤2,取100 mg 聚氧乙烯吡咯烷酮加入到装有1 ml水的1.5 ml离心管中,得到10 %(w/w)浓度的聚氧乙烯吡咯烷酮溶液。
29.步骤3,将步骤(1)获得的姜黄素溶液和辣椒素溶液缓慢加入到步骤(2)获得的聚氧乙烯吡咯烷酮溶液中。
30.步骤4,将步骤(3)获得的混合溶液快速加入到装有20 ml水的烧瓶中,在26℃,400 rpm搅拌0.5 h后静置12 h后除去有机溶剂。
31.步骤5,将步骤(4)获得的纳米粒子通过3000 kda超滤管除去未包载的游离药物后得到钙超载型小分子自组装纳米粒子。
32.图1为小分子药物自组装纳米粒子的外观和示意图。由图(a)看出纳米粒子丁达尔效应明显,且无明显沉淀;图(b)为纳米粒子的示意图。
33.图2为小分子药物自组装纳米粒子的粒径分布(a)和透射电镜图(b)。由图可知制备得到的纳米粒子平均粒径diameter 约为220 nm,多分散系数pdi为0.212
±
0.032的球形粒子。通过透射电镜可以观察到形成了符合上述描述的粒径均一的类球形结构。
34.图3为小分子药物自组装纳米粒子对于4t1肿瘤细胞杀伤示意图。通过mtt法评价了纳米粒子对于4t1细胞的细胞毒性。药物处理后加入噻唑蓝(浓度为0.5 mg/ml)4 h后加入二甲基亚砜(dmso)后测定其在490 nm处的吸光度值。随后计算得到其ic
50
值约为24.14 μg/ml。
35.图4为小分子药物自组装纳米粒子促进树突状细胞成熟的流式图。通过流式细胞仪检测,经过不同药物处理后的树突状细胞表面标志物的表达情况。本实验利用cd80和cd86两种抗体作为评价dc细胞成熟的标志物。由图中可以看出,和对照组相比,游离的辣椒素和姜黄素相比促进dc细胞成熟的能力较弱,而所述纳米粒子能够有效促进dc细胞成熟,百分比约为85.9%,说明纳米粒子能够作为优良的免疫佐剂。
36.图5为小分子药物自组装纳米粒子诱导线粒体膜电位去极化示意图。通过流式细胞仪检测,经过不同药物处理后的4t1细胞线粒体膜电位的变化情况。钙超载会导致细胞氧化应激,进一步诱导线粒体膜电位去极化。利用jc-1探针可以检测膜电位的变化情况,当膜电位下降时,jc-1会以单体形式存在并在激光照射下发出绿色荧光,表现为fitc信号通道上升;反之细胞在正常状态下, jc-1以多聚体形式存在,在激光照射下发出红色荧光,表现为pe通道信号上升。从图中结果可以看出,纳米粒子处理24 h后细胞内具有最高的绿色荧光比例,说明促进线粒体膜电位去极化能力最强。
37.图6为小分子药物自组装纳米粒子和化疗药物联合后对于4t1乳腺癌细胞杀伤示意图。通过mtt法评价了和化疗药物阿霉素联合给药24 h后,不同浓度纳米粒子对于4t1肿瘤细胞的杀伤能力。由图可以看出,随着纳米粒子浓度的提高,联合杀伤能力显著增强。在20 μg/ml时,和对照组仅给予阿霉素相比,细胞毒性从82%降低至21%。
38.图7为小分子药物自组装纳米粒子促进4t1乳腺癌细胞表面crt暴露示意图。crt的
暴露程度变化反映了细胞免疫原性死亡(icd)的程度。通过流式细胞仪检测,经过不同药物处理24 h后4t1细胞表面钙网蛋白crt暴露变化情况。定量结果可以看出,纳米粒子可以有效增强化疗药物诱导细胞暴露出最多的crt,同时说明纳米粒子诱导的细胞死亡具有最强的免疫原性。
39.图8为小分子药物自组装纳米粒子处理4t1乳腺癌细胞后促进树突状细胞成熟示意图。在4t1细胞经过不同处理12h后,将其与dc细胞进行共孵育。共孵育后,dc成熟度的变化,反映了肿瘤死亡后引起免疫反应的程度。通过流式细胞仪检测dc细胞的成熟情况。由图中可以看出,纳米药物和化疗药物联合后能够有效促进dc细胞成熟,百分比为53.9%。
40.图9为小分子药物自组装纳米粒子促进小鼠淋巴结树突状细胞成熟示意图。由图中可以看出,纳米药物和化疗药物联合后能够有效促进小鼠体内淋巴结dc细胞的成熟,成熟度约为69.1%,说明纳米粒子能够作为优良的免疫佐剂。
41.图10为小分子药物自组装纳米粒子促进小鼠肿瘤cd8
t细胞浸润示意图。cd8
t细胞在肿瘤部位的提高说明小鼠对于肿瘤免疫能力的提高。由图中结果可以看出,纳米药物和化疗药物联合给药后,小鼠肿瘤部位cd8
t细胞比例显著上升,相比对照上升3倍,说明纳米粒子能够提高化疗药物诱导的免疫效应,是有效的免疫佐剂。
42.图11为小分子药物自组装纳米粒子抑制4t1乳腺癌生长示意图。由图可以看出,纳米粒子和化疗药物联合给药后,肿瘤生长显著抑制,定量结果显示,和对照相比,肿瘤最终重量约为其1/10,和化疗药物阿霉素组相比,约为其1/4。说明纳米粒子能够有效增强化疗药物对于肿瘤的治疗效果。
43.实施例2步骤1,取2 mg和姜黄素和2 mg树脂毒素分别加入装有0.1 ml四氢呋喃和0.1 ml无水乙醇的1.5 ml离心管中,分别得到姜黄素溶液和树脂毒素溶液。
44.步骤2,取100 mg 聚氧乙烯吡咯烷酮加入到装有1 ml水的1.5 ml离心管中,得到10 %(w/w)浓度的聚氧乙烯吡咯烷酮溶液。
45.步骤3,将步骤(1)获得的姜黄素溶液和树脂毒素溶液缓慢加入到步骤(2)获得的聚氧乙烯吡咯烷酮溶液中。
46.步骤4,将步骤(3)获得的混合溶液快速加入到装有20 ml水的烧瓶中,在26℃,400 rpm搅拌0.5 h后静置12 h后除去有机溶剂。
47.步骤5,将步骤(4)获得的纳米粒子通过3000 kda超滤管除去未包载的游离药物后得到钙超载型小分子自组装纳米粒子。
48.实施例3步骤1,取2 mg和姜黄素和2 mg维生素d分别加入装有0.1 ml四氢呋喃和0.1 ml无水乙醇的1.5 ml离心管中,分别得到姜黄素溶液和维生素d溶液。
49.步骤2,取100 mg 聚氧乙烯吡咯烷酮加入到装有1 ml水的1.5 ml离心管中,得到10 %(w/w)浓度的聚氧乙烯吡咯烷酮溶液。
50.步骤3,将步骤(1)获得的姜黄素溶液和维生素d溶液缓慢加入到步骤(2)获得的聚氧乙烯吡咯烷酮溶液中。
51.步骤4,将步骤(3)获得的混合溶液快速加入到装有20 ml水的烧瓶中,在26℃,400 rpm搅拌0.5 h后静置12 h后除去有机溶剂。
52.步骤5,将步骤(4)获得的纳米粒子通过3000 kda超滤管除去未包载的游离药物后得到钙超载型小分子自组装纳米粒子。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
