1.本发明涉及查尔酮类衍生物技术领域,尤其是一种一价碘试剂催化查尔酮制备的化合物及其制备方法和应用。
背景技术:
2.3,3-二甲氧基-1,2-二苯基丙酮类化合物是新药设计研发的重要前体之一,也是重要的有机合成中间体。从简单的3,3-二甲氧基-1,2-二苯基丙酮类化合物骨架出发,通过一系列官能团转化可以高效地合成含有多种官能团的复杂多环骨架结构。例如,可以制备广泛存在于天然产物、药物以及生物活性分子中的二芳基吡唑,二芳基异噁唑,2,4,6-三苯基嘧啶,6-羟基大黄酮,3-酰基吲哚等化合物(j.nat.prod.2008,71,275-277;org.biomol.chem.,2017,15,6702-6705;med.chem.lett.2008,18,4092
–
4094;mendeleev commun.,2019,29,163
–
165;acs comb.sci.2018,20,700-721.)。其中,二芳基吡唑和二芳基异噁唑已被鉴定为可与苯并磺酰胺类化合物(combretastatin a4)相媲美的有效抗有丝分裂药物,可用于治疗恶性肿瘤。6-羟基大黄酮(6a-hydroxypterocarpans)是一种植物抗毒素,具有显著的抗氧化,抗癌活性和抗真菌活性,可用于治疗神经退行性疾病。3-酰基吲哚(3-acylindoles)是一种天然化合物,具有抗肿瘤、抗病毒和抗炎活性,也是潜在的抗癌药物。鉴于一价碘试剂催化查尔酮制备的化合物在合成化学、生物医药等领域的重要作用,
3.自其报道以来,有机化学家们一直致力于其合成方法的研究。目前,合成一价碘试剂催化查尔酮制备的化合物主要有三种策略,一是通过硝酸铊(iii)催化查尔酮类似物发生氧化重排制备此类化合物。但是硝酸铊(iii)的使用会导致在药物研发的过程中存在金属残留的问题。二是通过电化学或微波法制备一价碘试剂催化查尔酮制备的化合物。第三种方法是通过加入当量的三价碘试剂促进查尔酮类似物发生氧化重排制备一价碘试剂催化查尔酮制备的化合物。与硝酸铊(iii)相比,有机高价碘试剂作为一类非金属氧化剂已引起了化学家们的广泛关注。究其原因主要归于以下几个方面:(1)有机高价碘试剂是一种绿色的氧化剂。有机高价碘试剂具有与hg(ii),tl(iii),pb(iv)等重金属氧化剂相似的化学性质和反应性,然而没有这些重金属所带来的毒性、危险性和环保问题;(2)有机高价碘试剂蕴含着丰富的反应性,其中一些反应性与过渡金属配合物相似,如配体交换,还原消除等。而且在许多天然产物的全合成中也发挥了很大的作用;(3)一些重要的有机高价碘试剂如phi(oac)2,pifa,dmp已经商品化,某些试剂亦可根据相关文献通过简便的方法制得。虽然有机高价碘试剂在无金属条件下制备一价碘试剂催化查尔酮制备的化合物已有报道,但是这些报道大部分都是采用当量的有机高价碘试剂(int j mod phys b.2003,17(8n9),1482-1486;carbohydr res.2006,341(9),1091-1095.j of carbohy chem,2016,35:7,387-395),不符合绿色、可持续发展化学的要求。
4.因此我们想发展一种使用催化量的有机碘试剂在无金属条件下制备一价碘试剂催化查尔酮制备的化合物的方法。
技术实现要素:
5.本发明的第一个目的是针对以上所述现有技术的不足,提供一种具有通式(a)或通式(b)的一价碘试剂催化查尔酮制备的化合物,其中,通式(a)如下:
[0006][0007]
通式(b)如下:
[0008][0009]
其中,r1选自氢、卤素、羟基、氨基、氰基、硝基、未取代或至少一个如下基团取代的烷基、烷氧基、环烷基、芳基、杂环基、杂芳基、烷硫基、烷基磺酰基、烷基羰基或烷氧基羰基,如下基团为卤素、羟基、氨基、氰基或硝基;m选自1-5;
[0010]
r2选自氢、卤素、羟基、氨基、氰基、硝基、未取代或至少一个如下基团取代的烷基、烷氧基、环烷基、芳基、杂环基、杂芳基、烷硫基、烷基磺酰基、烷基羰基或烷氧基羰基,如下基团为卤素、羟基、氨基、氰基或硝基;n选自1-5。
[0011]
具有通式(a)或通式(b)中的查尔酮是新药设计研发的重要前体之一,也是重要的有机合成中间体。从简单的通式(b),即一价碘试剂催化查尔酮制备的化合物骨架出发,通过一系列官能团转化可以高效地合成含有多种官能团的复杂多环骨架结构。
[0012]
例如可以制备广泛存在于天然产物、药物以及生物活性分子中的二芳基吡唑,二芳基异噁唑,2,4,6-三苯基嘧啶,6-羟基大黄酮,3-酰基吲哚等化合物(j.nat.prod.2008,71,275-277;org.biomol.chem.,2017,15,6702-6705;med.chem.lett.2008,18,4092
–
4094;mendeleev commun.,2019,29,163
–
165;acs comb.sci.2018,20,700-721.)。
[0013]
二芳基吡唑和二芳基异噁唑已被鉴定为可与苯并磺酰胺类化合物(combretastatin a4)相媲美的有效抗有丝分裂药物,可用于治疗恶性肿瘤。6-羟基大黄酮(6a-hydroxypterocarpans)是一种植物抗毒素,具有显著的抗氧化,抗癌活性和抗真菌活性,可用于治疗神经退行性疾病。3-酰基吲哚(3-acylindoles)是一种天然化合物,具有抗肿瘤、抗病毒和抗炎活性,也是潜在的抗癌药物。
[0014]
本发明第二个目的在于提供具有通式(a)或通式(b)的一价碘试剂催化查尔酮制备的化合物的制备方法,以一价碘试剂在无金属条件下催化制备的方法。
[0015]
一价碘试剂催化查尔酮制备的化合物的制备方法包括的步骤如下:
[0016]
以具有通式(1)或具有通式(2)的查尔酮类化合物为原料,在有机溶剂中,以碘试
剂作为催化剂,将原料与碘试剂、mcpba(间氯过氧苯甲酸,)和酸均匀混合,室温条件下搅拌反应12-72小时,经柱层析纯化可得到具有通式(a)或具有通式(b)的化合物;
[0017]
通式(1)如下:
[0018][0019]
通式(2)如下:
[0020][0021][0022]
其中,r1选自氢、卤素、羟基、氨基、氰基、硝基、未取代或至少一个如下基团取代的烷基、烷氧基、环烷基、芳基、杂环基、杂芳基、烷硫基、烷基磺酰基、烷基羰基或烷氧基羰基,如下基团为卤素、羟基、氨基、氰基或硝基;m选自1-5;
[0023]
r2选自氢、卤素、羟基、氨基、氰基、硝基、未取代或至少一个如下基团取代的烷基、烷氧基、环烷基、芳基、杂环基、杂芳基、烷硫基、烷基磺酰基、烷基羰基或烷氧基羰基,如下基团为卤素、羟基、氨基、氰基或硝基;n选自1-5。
[0024]
其中,通式(1)制备通式(a)的化合物的过程如下式所示:
[0025][0026]
通式(2)制备通式(b)的化合物的过程如下式所示:
[0027][0028]
所述有机溶剂选自甲醇、三氟乙醇、二氯甲烷、1,4-二氧六环或三氯甲烷。
[0029]
所述碘试剂选自4-碘苯甲醚、2-碘三氟甲基苯、4-碘甲苯、间氟碘苯、3-碘苯腈、1-碘-2-硝基苯或4-碘硝基苯。
[0030]
所述酸选自三氟乙酸、3-吡啶硼酸、3,4-二氟苯硼酸、3,4,5-二氟苯硼酸、对氯苯硼酸、氟硼酸、2-氨基苯硼酸、苯基硼酸、硼酸、甲基硼酸或磷酸等。
[0031]
所述原料与碘试剂的摩尔比为0-0.5。
[0032]
所述原料与mcpba的摩尔比为1-5。
[0033]
所述原料与tfa(三氟乙酸)的摩尔比为1-20。
[0034]
所述原料在反应液中的浓度为0.25-1m。
[0035]
本发明技术方案的有益效果是:具有区域选择性好、底物范围广、条件温和、操作简单、实验步骤可放大等优点;而且反应是在无金属的条件下进行,这样在药物研发的过程中不会存在金属残留的问题;此外,本制备方法使用了催化量的一价碘试剂,使整个实验过程会更加绿色。
附图说明
[0036]
图1a是具有式(b-1)的化合物的氢-1核磁共振图谱;
[0037]
图1b是具有式(b-1)的化合物的碳-13核磁共振图谱;
[0038]
图2a是具有式(b-2)的化合物的氢-1核磁共振图谱;
[0039]
图2b是具有式(b-2)的化合物的碳-13核磁共振图谱;
[0040]
图3a是具有式(b-3)的化合物的氢-1核磁共振图谱;
[0041]
图3b是具有式(b-3)的化合物的碳-13核磁共振图谱;
[0042]
图4a是具有式(b-4)的化合物的氢-1核磁共振图谱;
[0043]
图4b是具有式(b-4)的化合物的碳-13核磁共振图谱;
[0044]
图4c是具有式(b-4)的化合物的氟-19核磁共振图谱;
[0045]
图5a是具有式(b-5)的化合物的氢-1核磁共振图谱;
[0046]
图5b是具有式(b-5)的化合物的碳-13核磁共振图谱;
[0047]
图6a是具有式(b-6)的化合物的氢-1核磁共振图谱;
[0048]
图6b是具有式(b-6)的化合物的碳-13核磁共振图谱;
[0049]
图7a是具有式(b-7)的化合物的氢-1核磁共振图谱;
[0050]
图7b是具有式(b-7)的化合物的碳-13核磁共振图谱;
[0051]
图8a是具有式(b-8)的化合物的氢-1核磁共振图谱;
[0052]
图8b是具有式(b-8)的化合物的碳-13核磁共振图谱;
[0053]
图9a是具有式(b-9)的化合物的氢-1核磁共振图谱;
[0054]
图9b是具有式(b-9)的化合物的碳-13核磁共振图谱;
[0055]
图10a是具有式(b-10)的化合物的氢-1核磁共振图谱;
[0056]
图10b是具有式(b-10)的化合物的碳-13核磁共振图谱;
[0057]
图11a是具有式(b-11)的化合物的氢-1核磁共振图谱;
[0058]
图11b是具有式(b-11)的化合物的碳-13核磁共振图谱;
[0059]
图12a是具有式(b-12)的化合物的氢-1核磁共振图谱;
[0060]
图12b是具有式(b-12)的化合物的碳-13核磁共振图谱;
[0061]
图13a是具有式(a-1)的化合物的氢-1核磁共振图谱;
[0062]
图13b是具有式(a-1)的化合物的碳-13核磁共振图谱;
[0063]
图14a是具有式(a-2)的化合物的氢-1核磁共振图谱;
[0064]
图14b是具有式(a-2)的化合物的碳-13核磁共振图谱;
[0065]
图15是本技术由通式(2)的化合物制备通式(b)的化合物过程图。
具体实施方式
[0066]
以下结合附图与具体实施例对本发明进行详细的说明。下述实例中所涉及的具体制备方法和设备如无特殊说明,均为常规方法或按照制造厂商说明书建议的条件实施;所涉及作为原料、添加剂、催化剂和溶剂等的试剂均可通过市售方式获得。
[0067]
实施例1
[0068]
如具有式(b-1)的化合物的制备,具体步骤和条件如下:
[0069][0070]
在室温条件下,以(45.2mg,0.2mmol)的具有式(2-1)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-1)的化合物,为黄色固体,产率为83%。
[0071]
式(b-1)的化合物的氢-1核磁共振图谱如图1a所示,核磁数据如下:
[0072]1h nmr(400mhz,cdcl3)δ8.10
–
8.04(m,2h),7.49(t,j=7.3hz,1h),7.43
–
7.36(m,3h),7.27
–
7.17(m,1h),6.95
–
6.86(m,2h),5.55(d,j=8.7hz,1h),5.22(d,j=8.7hz,1h),3.92(s,3h),3.44(s,3h),3.22(s,3h);
[0073]
式(b-1)的化合物的碳-13核磁共振图谱如图1b所示,核磁数据如下:
[0074]
13
c nmr(101mhz,cdcl3)δ198.3,156.6,136.8,132.9,128.8,128.6(d,j=6.0hz),128.3,123.5,121.0,111.2,106.4,77.3,77.0,76.7,55.8(d,j=14.8hz),53.1。
[0075]
实施例2
[0076]
如具有式(b-2)的化合物的制备,具体步骤和条件如下:
[0077][0078]
在室温条件下,以(57mg,0.2mmol)的具有式(2-2)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-2)的化合物,为白色固体,产率为93%。
[0079]
式(b-2)的化合物的氢-1核磁共振图谱如图2a所示,核磁数据如下:
[0080]1h nmr(400mhz,cdcl3)δ8.52(s,1h),8.03(dd,j=8.7,1.7hz,1h),7.94(d,j=7.9hz,1h),7.83(t,j=8.1hz,2h),7.60
–
7.48(m,2h),7.43
–
7.38(m,2h),7.26(s,1h),6.89
–
6.83(m,2h),5.16(d,j=8.4hz,1h),5.03(d,j=8.5hz,1h),3.78
–
3.72(m,3h),3.47(s,3h),3.27(s,3h);
[0081]
式(b-2)的化合物的碳-13核磁共振图谱如图2b所示,核磁数据如下:
[0082]
13
c nmr(101mhz,cdcl3)δ197.9,159.0,135.5,134.3,132.4,130.4,130.0,129.6,128.4(d,j=7.6hz),127.6,127.0,126.5,124.3,114.2,106.9,77.3,77.0,76.7,56.14(d,j=5.3hz),55.1,54.5。
[0083]
实施例3
[0084]
如具有式(b-3)的化合物的制备,具体步骤和条件如下:
[0085][0086]
在室温条件下,以(45.2mg,0.2mmol)的具有式(2-3)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-3)的化合物,为黄色固体,产率为95%。
[0087]
式(b-3)的化合物的氢-1核磁共振图谱如图3a所示,核磁数据如下:
[0088]1h nmr(400mhz,cdcl3)δ7.96(t,j=6.0hz,1h),7.59
–
7.45(m,1h),7.39(dd,j=15.8,8.1hz,1h),7.32(s,1h),6.83(s,1h),5.23
–
5.01(m,1h),4.92
–
4.80(m,1h),3.75(d,j=3.6hz,1h),3.51
–
3.39(m,1h),3.22(d,j=3.6hz,1h);
[0089]
式(b-3)的化合物的碳-13核磁共振图谱如图3b所示,核磁数据如下:
[0090]
13
c nmr(101mhz,cdcl3)δ198.0,133.0,130.0,128.6(d,j=10.5hz),126.8,114.2,106.7,77.0,76.7,54.4。
[0091]
实施例4
[0092]
如具有式(b-4)的化合物的制备,具体步骤和条件如下:
[0093][0094]
在室温条件下,以(57.6mg,0.2mmol)的具有式(2-4)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-4)的化合物.
[0095]
式(b-4)的化合物的氢-1核磁共振图谱如图4a所示,核磁数据如下:
[0096]1h nmr(400mhz,cdcl3)δ8.01
–
7.90(m,2h),7.58
–
7.47(m,1h),7.41(ddd,j=11.9,6.6,1.8hz,4h),7.07
–
6.95(m,2h),5.08(d,j=8.4hz,1h),4.90(d,j=8.4hz,1h),3.44(s,3h),3.23(s,3h);
[0097]
式(b-4)的化合物的碳-13核磁共振图谱如图4b所示,核磁数据如下:
[0098]
13
c nmr(101mhz,cdcl3)δ197.7,162.0,136.7,133.2,130.5(dd,j=9.0,3.1hz),128.6,115.8,115.6,106.7,77.3,77.0,76.7,56.2,56.0,54.5;
[0099]
式(b-4)的化合物的氟-19核磁共振图谱如图4c所示,核磁数据如下:
[0100]
19
f nmr(376mhz,cdcl3)δ-114.8(d,j=5.5hz)。
[0101]
实施例5
[0102]
如具有式(b-5)的化合物的制备,具体步骤和条件如下:
[0103][0104]
在室温条件下,以(56.9mg,0.2mmol)的具有式(2-5)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-5)的化合物。
[0105]
式(b-5)的化合物的氢-1核磁共振图谱如图5a所示,核磁数据如下:
[0106]1h nmr(400mhz,cdcl3)δ8.09
–
7.89(m,2h),7.52(ddd,j=8.9,4.7,1.7hz,1h),7.42(dd,j=10.5,4.8hz,2h),7.33(d,j=7.8hz,2h),7.14(d,j=7.7hz,2h),5.14(d,j=8.5hz,1h),4.89(d,j=8.5hz,1h),3.46(s,3h),3.25(s,3h),2.31(s,3h);
[0107]
式(b-5)的化合物的碳-13核磁共振图谱如图5b所示,核磁数据如下:
[0108]
13
c nmr(101mhz,cdcl3)δ197.8,137.2,136.9,133.0,131.7,129.5,128.9
–
128.4(m),106.7,77.4,77.0,76.7,56.5,56.1,54.3,29.7,21.1。
[0109]
实施例6
[0110]
如具有式(b-6)的化合物的制备,具体步骤和条件如下:
[0111][0112]
在室温条件下,以(69.2mg,0.2mmol)的具有式(2-6)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-6)的化合物。
[0113]
式(b-6)的化合物的氢-1核磁共振图谱如图6a所示,核磁数据如下:
[0114]1h nmr(400mhz,cdcl3)δ8.10
–
7.96(m,2h),7.59
–
7.47(m,7h),7.43(td,j=8.0,6.4hz,4h),7.34(d,j=7.3hz,1h),5.19(d,j=8.5hz,1h),4.98(d,j=8.5hz,1h),3.48(s,3h),3.28(s,3h);
[0115]
式(b-6)的化合物的碳-13核磁共振图谱如图6b所示,核磁数据如下:
[0116]
13
c nmr(101mhz,cdcl3)δ197.7,140.42(d,j=13.8hz),136.8,133.7,133.2,129.3,128.8
–
128.5(m),127.4(d,j=18.9hz),127.0(s),106.8(s),77.3,77.0,76.7,56.5,56.2,54.3。
[0117]
实施例7
[0118]
如具有式(b-7)的化合物的制备,具体步骤和条件如下:
[0119][0120]
在室温条件下,以(60.9mg,0.2mmol)的具有式(2-7)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-7)的化合物。
[0121]
式(b-7)的化合物的氢-1核磁共振图谱如图7a所示,核磁数据如下:
[0122]1h nmr(400mhz,cdcl3)δ8.01
–
7.89(m,2h),7.56
–
7.49(m,1h),7.45
–
7.39(m,2h),7.39
–
7.33(m,2h),7.28(dt,j=6.8,3.6hz,2h),5.08(d,j=8.4hz,1h),4.88(d,j=8.4hz,1h),3.44(s,3h),3.23(s,3h);
[0123]
式(b-7)的化合物的碳-13核磁共振图谱如图7b所示,核磁数据如下:
[0124]
13
c nmr(101mhz,cdcl3)δ197.5,133.5,133.3,130.3,129.0,128.6(d,j=2.2hz),106.6,77.3,77.0,76.7,56.2(d,j=12.3hz),54.6.
[0125]
实施例8
[0126]
如具有式(b-8)的化合物的制备,具体步骤和条件如下:
[0127][0128]
在室温条件下,以(60.0mg,0.2mmol)的具有式(2-8)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-8)的化合物。
[0129]
式(b-8)的化合物的氢-1核磁共振图谱如图8a所示,核磁数据如下:
[0130]1h nmr(400mhz,cdcl3)δ8.00
–
7.94(m,2h),7.45
–
7.38(m,2h),7.33
–
7.19(m,4h),6.92
–
6.85(m,2h),5.13(d,j=8.5hz,1h),4.85(d,j=8.5hz,1h),3.82(s,3h),3.44(s,3h),3.21(s,3h);
[0131]
式(b-8)的化合物的碳-13核磁共振图谱如图8b所示,核磁数据如下:
[0132]
13
c nmr(101mhz,cdcl3)δ196.2,163.5,135.2,131.0,129.8,128.9,128.7,127.4,113.7,106.8,77.3,77.0,76.7,56.6,56.1,55.4,54.5。
[0133]
实施例9
[0134]
如具有式(b-9)的化合物的制备,具体步骤和条件如下:
[0135][0136]
在室温条件下,以(72.0mg,0.2mmol)的具有式(2-9)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-9)的化合物。
[0137]
式(b-9)的化合物的氢-1核磁共振图谱如图9a所示,核磁数据如下:
[0138]1h nmr(400mhz,cdcl3)δ7.97(d,j=7.4hz,2h),7.53(t,j=7.4hz,1h),7.43(t,j=7.6hz,2h),6.63(s,2h),5.06(t,j=7.8hz,1h),4.79(d,j=8.5hz,1h),3.89
–
3.82(m,6h),3.79(d,j=7.4hz,3h),3.43(d,j=5.3hz,3h),3.24(d,j=8.2hz,3h)。
[0139]
式(b-9)的化合物的碳-13核磁共振图谱如图9b所示,核磁数据如下:
[0140]
13
c nmr(101mhz,cdcl3)δ142.0,138.4,132.5,129.1
–
127.9(m),127.7,127.5,126.8,126.4,125.7,77.3,77.0,76.7,65.2,63.6,39.1。
[0141]
实施例10
[0142]
如具有式(b-10)的化合物的制备,具体步骤和条件如下:
[0143][0144]
在室温条件下,以(66.1mg,0.2mmol)的具有式(2-10)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-10)的化合物。
[0145]
式(b-10)的化合物的氢-1核磁共振图谱如图10a所示,核磁数据如下:
[0146]1h nmr(400mhz,cdcl3)δ8.01
–
7.92(m,2h),7.37
–
7.30(m,2h),6.92
–
6.80(m,4h),5.08(d,j=8.5hz,1h),4.79(d,j=8.5hz,1h),3.82(s,3h),3.75(s,3h),3.43(s,3h),3.21(s,3h)。
[0147]
式(b-10)的化合物的碳-13核磁共振图谱如图10b所示,核磁数据如下:
[0148]
13
c nmr(101mhz,cdcl3)δ196.4,163.5,158.9,131.0,129.9,127.2,114.2,113.7,106.8,77.3,77.0,76.7,56.1,55.4,55.2,54.5。
[0149]
实施例11
[0150]
如具有式(b-11)的化合物的制备,具体步骤和条件如下:
[0151][0152]
在室温条件下,以(64.1mg,0.2mmol)的具有式(2-11)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-11)的化合物,经柱层析纯化即可得到式(b-3)的化合物,为黄色固体,产率为95%。
[0153]
式(b-11)的化合物的氢-1核磁共振图谱如图11a所示,核磁数据如下:
[0154]1h nmr(400mhz,cdcl3)δ8.03
–
7.98(m,2h),7.86(s,1h),7.80(td,j=8.1,3.9hz,3h),7.59(dd,j=8.5,1.7hz,1h),7.52
–
7.37(m,6h),5.24(d,j=8.5hz,1h),5.07(d,j=8.5hz,1h),3.49(s,3h),3.21(s,3h)。
[0155]
式(b-11)的化合物的碳-13核磁共振图谱如图11b所示,核磁数据如下:
[0156]
13
c nmr(101mhz,cdcl3)δ197.7,133.4,133.1,132.7,132.3,128.8
–
128.3(m),127.9(d,j=7.6hz),127.6,126.9,126.1(d,j=12.5hz),106.9,77.3,77.0,76.7,57.1,56.2,54.7。
[0157]
实施例12
[0158]
如具有式(b-12)的化合物的制备,具体步骤和条件如下:
[0159][0160]
在室温条件下,以(54.0mg,0.2mmol)的具有式(2-12)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(b-12)的化合物。
[0161]
式(b-12)的化合物的氢-1核磁共振图谱如图12a所示,核磁数据如下:
[0162]1h nmr(400mhz,cdcl3)δ8.05
–
7.96(m,2h),7.52(s,1h),7.48
–
7.40(m,4h),7.32(d,j=7.7hz,2h),7.28(s,1h),5.16(d,j=8.5hz,1h),4.93(d,j=8.5hz,1h),3.46(s,3h),3.23(s,3h)。
[0163]
式(b-12)的化合物的碳-13核磁共振图谱如图12b所示,核磁数据如下:
[0164]
13
c nmr(101mhz,cdcl3)δ197.7,133.06,129.0,128.9
–
128.4(m),127.5,106.8,77.3,77.0,76.7,56.9,56.1,54.5。
[0165]
实施例13
[0166]
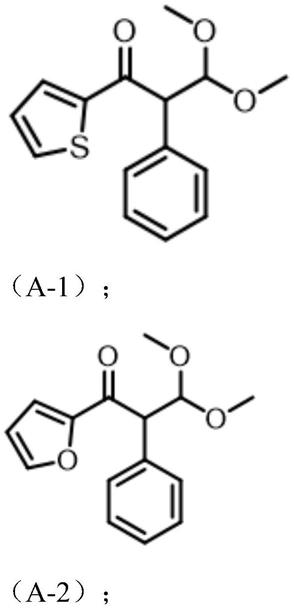
如具有式(a-1)的化合物的制备,具体步骤和条件如下:
[0167][0168]
在室温条件下,以(55.2mg,0.2mmol)的具有式(1-1)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(a-1)的化合物。
[0169]
式(a-1)的化合物的氢-1核磁共振图谱如图13a所示,核磁数据如下:
[0170]1h nmr(400mhz,cdcl3)δ7.78(dd,j=3.8,0.9hz,1h),7.60(dd,j=4.9,0.9hz,1h),7.47
–
7.42(m,2h),7.32(dd,j=10.0,4.7hz,2h),7.28
–
7.23(m,1h),7.08(dd,j=4.8,3.9hz,1h),5.12(d,j=8.5hz,1h),4.70(d,j=8.5hz,1h),3.46(s,3h),3.21(s,3h)。
[0171]
式(a-1)的化合物的碳-13核磁共振图谱如图13b所示,核磁数据如下:
[0172]
13
c nmr(101mhz,cdcl3)δ190.3,144.1,134.8,134.3,132.7,128.8(d,j=11.2hz),128.2,127.6,106.3,77.3,77.0,76.7,58.6,56.2,54.4,50.8。
[0173]
实施例14
[0174]
如具有式(a-2)的化合物的制备,具体步骤和条件如下:
[0175][0176]
在室温条件下,以(52.1mg,0.2mmol)的具有式(1-2)的化合物为原料,在ch3oh(0.5ml)中,与对碘苯甲醚(4.7mg)、(115mg)的mcpba和tfa(225ul)均匀混合,搅拌反应(48)小时,经柱层析纯化即可得到式(a-2)的化合物。
[0177]
式(a-2)的化合物的氢-1核磁共振图谱如图14a所示,核磁数据如下:
[0178]1h nmr(400mhz,cdcl3)δ7.59(d,j=1.0hz,1h),7.50
–
7.43(m,2h),7.34(dd,j=10.0,4.7hz,2h),7.29(dt,j=6.3,2.0hz,1h),7.26
–
7.24(m,1h),6.55
–
6.48(m,1h),5.18(d,j=8.8hz,1h),4.75(d,j=8.8hz,1h),3.47(s,3h),3.23(s,3h)。
[0179]
式(a-2)的化合物的碳-13核磁共振图谱如图14b所示,核磁数据如下:
[0180]
13
c nmr(101mhz,cdcl3)δ186.3,152.3,146.8,134.6,129.0,128.8,127.6,118.3,112.5,105.9,77.3,77.0,76.7,57.2,56.1,53.9。
[0181]
以上所述者,仅为本发明的较佳实施例而已,当不能以此限定本发明实施的范围,即大凡依本发明申请专利范围及发明说明内容所作的简单等效变化与修饰,皆仍属本发明专利涵盖的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。