1.本发明涉及能够进行抗体依赖性细胞毒性的免疫细胞,其包括编码抗原结合分子的核酸序列。本发明还涉及产生免疫细胞的方法和免疫细胞的医学用途。
背景技术:
2.表达嵌合抗原受体(car)的αβ(ab)t细胞形成免疫治疗工具包的重要部分。通过在abt细胞中表达car,可以改变abt细胞的抗原特异性。以这种方式,受试者的适应性免疫系统可以被重编程以靶向受试者中特别感兴趣的抗原,如肿瘤抗原。
3.最近,已经开发了改善car abt细胞的治疗潜力的策略。特别地,已经产生了“装甲的”car abt细胞。装甲的car abt细胞被赋予分泌功能增强分子的能力。carabt细胞可以,例如,分泌增强其治疗效果的细胞因子。carabt细胞可以分泌抑制蛋白激酶a的肽(newick etal.,cancer immunol res,june 2016,4(6):541
–
551).car abt细胞还可以分泌克服免疫检查点的分子。例如,rafiq et al.(nature biotechnology,13aug 2018,36(9):847
–
856)为car abt细胞配备了分泌抗pdl1抗体的能力,以及li et al.(clinical cancer research,november 2017,23(22):6982
–
6992)改造carabt细胞以在效应细胞表面分泌针对pd-1特异性的scfv。
4.与abt细胞相反,γδ(gd)t细胞是相对被忽视的先天样免疫细胞亚群。与abt细胞不同,gdt细胞(特别是vδ2 gdt细胞)能够对抗体标记的肿瘤细胞产生有效的抗体依赖性细胞毒性(adcc)。因此,gdt细胞浸润到肿瘤中与有利的临床结果相关,并且gdt细胞在癌症免疫疗法中具有潜力。骨髓细胞也能够adcc,并可用于癌症免疫治疗。为了优化它们的治疗潜力,需要改造gdt细胞和骨髓细胞以分泌增强它们抗癌作用的分子。
技术实现要素:
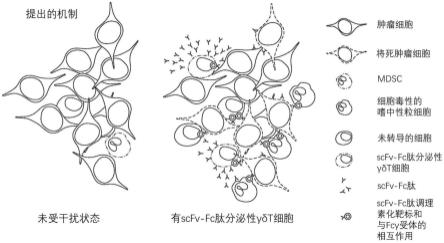
5.本发明人已经证明,能够adcc的免疫细胞可被工程化以分泌靶向在肿瘤微环境中表达的抗原的抗原结合分子(例如抗体或抗体样蛋白,诸如scfv-fc)。抗原结合分子的分泌可以增强免疫细胞的抗癌效果。例如,分泌的抗原结合分子可以增加靶细胞杀伤,例如通过adcc。该示例性机制示于图1中,其中由工程化免疫细胞(例如gdt细胞)分泌的scfv-fc标记表达adcc的同源抗原的靶细胞。这允许工程化免疫细胞通过adcc杀伤靶细胞。旁观者的非工程化免疫细胞也可对靶细胞施加adcc。以这种方式,工程化的和旁观者免疫细胞的抗原特异性细胞毒性得到改善。因此,向受试者施用工程化的免疫细胞提供了改善的抗癌疗法。
6.因此,本发明提供:
7.–
能够adcc的免疫细胞,所述免疫细胞包括编码抗原结合分子的核酸序列,所述抗原结合分子包括抗原结合区;
8.–
产生本发明的免疫细胞的方法,其包括将编码抗原结合分子的核酸序列引入免疫细胞;
9.治疗个体中的疾病的方法,所述方法包括向所述个体施用治疗有效数量的本发明
的免疫细胞;以及
10.–
本发明的免疫细胞,其用于治疗个体中的疾病的方法中,所述方法包括向所述个体施用治疗有效数量的所述免疫细胞。
附图说明
11.图1——提出的机制的实施例,其中在肿瘤微环境中由γδt细胞分泌的scfv-fcs接合adcc感受态细胞上的fc受体。
12.图2——使用流式细胞术检测scfv-fc与表达靶抗原的细胞的结合。cea
capan-1或cea-hela细胞与来自分泌抗ceascfv-fc融合蛋白的vδ2细胞或jurkat细胞的上清液一起孵育。使用抗人fc检测scfv-fc融合蛋白的结合。纯化的scfv融合蛋白用作阳性对照。使用gd2
/-supt1细胞和来自分泌抗gd2 scfv-fc融合蛋白的vδ2细胞的上清液进行类似的实验。在这种情况下,使用临床级达妥昔单抗(抗gd2)作为阳性对照。
13.图3——显示细胞毒性测定中所用条件的实验设置,以测试scfv-fc融合蛋白表达的直接和间接细胞毒性益处。
14.图4——细胞接触依赖性和非依赖性设置中的细胞毒性。
15.所有细胞毒性实验在效应子∶靶标比例为1∶1进行,使用18小时共培养。用celltrace violet
tm
标记靶细胞,并通过用ghostred可固定活力染料染色检测靶细胞的死亡。靶细胞的死亡以从所有值中减去背景死亡(无效应子存在)来显示。
16.a)分泌抗ceascfv-fc的vδ2细胞或未转导的vδ2细胞杀伤cea
capan-1或cea-hela细胞。
17.b)在存在或不存在来自分泌抗cea-scfv-fc的vδ2细胞的上清液的情况下,未转导的vδ2细胞杀伤cea
capan-1或cea-hela细胞。
18.c)未转导的vδ2细胞杀伤cea
capan-1或cea-hela细胞,其中将分泌抗cea scfv-fc的vδ2细胞或未转导的对照隔离在半透膜之后。
19.d)分泌抗gd2 scfv-fc的或未转导的vδ2细胞杀伤gd2
supt1或gd2-野生型supt1细胞。
20.e)在存在或不存在来自分泌抗gd2-scfv-fc的vδ2细胞的上清液的情况下,未转导的vδ2细胞杀伤gd2
supt1或gd2-野生型supt1细胞。
21.f)未转导的vδ2细胞杀伤gd2
supt1或gd2-野生型supt1细胞,其中将分泌抗gd2 scfv-fc的vδ2细胞或未转导的对照隔离在半透膜之后。
22.图5——cea
capan-1或cea-hela细胞与未转导的vδ2细胞共培养18小时后上清液中ifnγ的浓度,其中将分泌抗ceascfv-fc的vδ2细胞或未转导的对照隔离在半透膜之后。
23.图6——通过流式细胞术检测的293t细胞产生的抗gd2抗体(seq id no:17)与gd2
/-靶细胞的结合。用减少体积的编码完整抗gd2抗体14g2a的慢病毒处理293t细胞。将等基因supt1_wt(gd2-)或supt1_gd2(gd2
)与来自转导的293t细胞的上清液一起孵育。使用与pe缀合的抗人fc抗体检测抗体结合。纯的抗gd2抗体(达妥昔单抗,ch14.18,克隆14g2a)用作阳性对照。在转导的293t细胞的上清液中检测到抗体,其水平取决于所用的病毒剂量。
24.图7——由γδt细胞产生的抗体与表达靶抗原的细胞的结合。将等基因supt1_wt(gd2-)或supt1_gd2(gd2
)与来自转导以表达完整抗gd2抗体的vδ2的上清液(克隆14g2a)一
fc”包含两个或更多个这样的scfv-fc,提及“t细胞”包含两个或更多个这样的t细胞,等等。
52.本文引用的所有出版物、专利和专利申请,无论是上文还是下文,均通过引用整体并入本文。
53.免疫细胞
54.本发明提供了能够adcc的免疫细胞,并且其包括编码抗原结合分子的核酸序列。免疫细胞可以是能够adcc的任何免疫细胞。能够adcc的免疫细胞是本领域已知的。
55.adcc是公知的获得性细胞介导的免疫机制。在adcc过程中,免疫效应细胞主动裂解表面抗原已被特异性抗体结合的靶细胞。具体地,抗体结合靶细胞表面上的其同源抗原。存在于免疫效应细胞表面的fc受体识别结合抗体的fc区。fc受体的交联触发免疫效应细胞和靶细胞之间的裂解突触的形成,免疫效应细胞将裂解颗粒脱颗粒到其中。因此,引发靶细胞的凋亡。已知能够adcc的免疫效应细胞包含自然杀伤(nk)细胞、巨噬细胞、嗜中性粒细胞和嗜酸性粒细胞。gdt细胞也能够adcc。
56.免疫细胞可以来自任何物种,例如人、狗、猫、小鼠、大鼠、猪、绵羊、牛、山羊或马。免疫细胞通常是人免疫细胞。免疫细胞可以是犬、猫、鼠、猪、绵羊、山羊、牛或马免疫细胞。
57.优选地,免疫细胞不是abt细胞。abt细胞是拥有包括α链和β链的t细胞受体(tcr)的t细胞。它们通常以mhc依赖性方式被激活。对于abt细胞,adcc尚未被报道。abt细胞通常被认为是“常规”t细胞。
58.免疫细胞可以是gdt细胞。gdt细胞是在其表面具有gd t细胞受体(tcr)的t细胞。也就是说,gdt细胞拥有包括γ链和δ链的tcr。因此,gdt细胞在结构上不同于abt细胞。gdt细胞也与abt细胞功能不同。具体地,gdt细胞能够adcc。gdt细胞通常以mhc非依赖性方式被激活。gdt细胞通常被认为是“非常规”t细胞。
59.存在gdt的几个子集。例如,gdt细胞可以是vδ2 gdt细胞、vδ1 gdt细胞或vδ1-/vδ2-gdt细胞。优选地,gdt细胞是vδ2 gdt细胞。vδ2 gdt细胞、vδ1 gdt细胞和vδ1-/vδ2-t细胞都具有优良的adcc能力并显示良好的抗肿瘤毒性。
60.用于扩增gdt细胞的方法是本领域已知的。例如,gdt细胞可通过在il-2和唑来膦酸存在下培养来扩增(fisher j et al.effective combination treatment using anti-gd2 ch14.18/cho antibody with vδ2 γδt cells in ewing sarcoma and neuroblastoma.oncoimmunology 2015apr 27;5(1):e1025194.)。gdt细胞因此可容易地用于本发明。
61.免疫细胞可以是骨髓细胞。骨髓细胞是源自普通骨髓祖细胞的细胞,例如血小板、红细胞、肥大细胞、巨噬细胞、嗜碱性粒细胞、嗜中性粒细胞、和嗜酸性粒细胞。已经报道了巨噬细胞、嗜碱性粒细胞、嗜中性粒细胞、和嗜酸性粒细胞,的adcc。因此,优选地,骨髓细胞是巨噬细胞、嗜碱性粒细胞、中性粒细胞或嗜酸性粒细胞。分离和扩增髓样细胞的方法是本领域已知的。
62.自然杀伤(nk)细胞也能够adcc。免疫细胞可以是nk细胞。nk细胞是一类先天淋巴细胞,在针对多种疾病的免疫中起作用。例如,nk细胞在检测和控制癌症以及杀死病毒感染的细胞中发挥作用。分离和扩增nk细胞的方法是本领域已知的。
63.优选地,免疫细胞不表达嵌合抗原受体(car)。因此,优选地,免疫细胞不是car t细胞。
64.核酸序列
65.本发明的免疫细胞包括编码抗原结合分子的核酸序列。核酸序列可包括dna。核酸序列可包括rna。核酸序列可包括dna和rna。
66.免疫细胞可包括一个或多个核酸序列,每个核酸序列编码抗原结合分子。例如,免疫细胞可包括2个或更多个、3个或更多个、4个或更多个、5个或更多个、6个或更多个、7个或更多个、8个或更多个、9个或更多个、10个或更多个、15个或更多个、或20个或更多个核酸序列,其各自编码为抗原结合分子。如果免疫细胞包括各自编码抗原结合分子的多个核酸序列,则由各核酸序列编码的抗原结合分子可以相同或不同。优选地,每种抗原结合分子是不同的。优选地,每种抗原结合分子对不同的抗原是特异性的。优选地,抗原是肿瘤抗原。抗原可以在癌细胞上表达或由癌细胞表达。抗原可以在肿瘤微环境中的非癌细胞上表达或由非癌细胞表达。抗原可以分泌到肿瘤微环境中。
67.每个核酸序列可编码一个或多个抗原结合分子。例如,核酸序列可编码2个或更多个、3个或更多个、4个或更多个、5个或更多个、6个或更多个、7个或更多个、8个或更多个、9个或更多个、10个或更多个、15个或更多个、或20个或更多个抗原结合分子。如果核酸序列编码多个抗原结合分子,则每个抗原结合分子可以相同或不同。优选地,每种抗原结合分子是不同的。优选地,每种抗原结合分子对不同的抗原是特异性的。优选地,抗原是肿瘤抗原。抗原可以在癌细胞上表达或由癌细胞表达。抗原可以在肿瘤微环境中的非癌细胞上表达或由非癌细胞表达。抗原可以分泌到肿瘤微环境中。
68.核酸序列可包括外源启动子序列,编码抗原结合分子的序列可操作地连接至外源启动子序列。外源启动子可以是诱导型启动子。或者,核酸序列可以缺少外源启动子序列。在这种情况下,核酸序列可以整合到免疫细胞的基因组,使得抗原结合分子的表达由基因组中的内源启动子控制。外源或内源启动子的激活可由诱导型信号通路控制。例如,外源或内源启动子可以在synnotch受体与同源抗原接合之后被激活。
69.核酸序列可以整合到免疫细胞的基因组。或者,核酸序列可以不整合到免疫细胞的基因组中。如果核酸序列未整合到免疫细胞的基因组中,则其可包括在质粒、载体或人工染色体中。载体可以是病毒载体或非病毒载体。人工染色体可以是酵母人工染色体(yac)、细菌人工染色体(bac)或人类人工染色体(hac)。优选地,人工染色体是hac。
70.抗原结合分子
71.本发明的免疫细胞包括编码抗原结合分子的核酸序列。
72.抗原结合分子包括抗原结合区。抗原结合区是抗原结合分子的能够特异性结合一个或多个抗原的区域。例如,抗原结合区可以能够特异性结合2个或更多个、3个或更多个、4个或更多个、5个或更多个、6个或更多个、7个或更多个、8个或更多个、9个或更多个或10个或更多个不同抗原。示例性抗原结合区是本领域已知的,并且至少包含scfv(单链可变片段)、fab、修饰的fab、fab
′
、修饰的fab
′
、f(ab
′
)2、fv、dab、fd、dsfv、ds-scfv、scfv2、双特异性t细胞衔接物、纳米抗体、darpin、抗体模拟物、双抗体、三抗体和四抗体。因此,抗体结合区可包括scfv、fab、修饰的fab、fab
′
、修饰的fab
′
、f(ab
′
)2、fv、dab、fd、dsfv、ds-scfv、scfv2、双特异性t细胞衔接物、纳米抗体、darpin、抗体模拟物、双抗体、三抗体或四抗体,单独或其任意组合。抗原结合分子可包括scfv、fab、修饰的fab、fab
′
、修饰的fab
′
、f(ab
′
)2、fv、dab、fd、dsfv、ds-scfv、scfv2、双特异性t细胞衔接物、纳米抗体、darpin、抗体模拟物、
双抗体、三抗体、四抗体、或针对免疫细胞靶向的细胞表面上表达的受体的多肽配体,单独或其任意组合。
73.优选地,抗原结合分子包括包括scfv的抗原结合区。抗原结合区可包括2个或更多个,例如3个或更多个、4个或更多个、5个或更多个、6个或更多个、7个或更多个、8个或更多个、9个或更多个或10个或更多个scfv。scfv是本领域已知的。scfv是包括与抗体的轻链可变区(vl)连接的重链可变区(vh)的融合蛋白。通常,vh和vl通过接头肽连接。接头肽的长度可以是约5至约30个氨基酸。例如,接头肽的长度可以是约6至约29、约7至约28、约8至约27、约9至约26、约10至约25、约11至约24、约12至约23、约13至约22、约14至约21、约15至约20、约16至约19、约17或约18个氨基酸。
74.抗原结合分子可以能够结合fc受体。例如,抗原结合分子可包括fc(可结晶片段)区。fc区是本领域已知的。fc区是抗体的尾区,其与fc受体和补体系统的一些蛋白质相互作用。这种特性允许抗体激活免疫系统。fc区包括至少两个重链恒定(ch)结构域。具体地,在衍生自igg、iga或igd抗体的fc结构域中,fc区包括抗体的ch2和ch3结构域。在来源于igm或ige抗体的fc区中,fc区包括抗体的ch2、ch3和ch4区。fc区可以是修饰的fc区。例如,fc区可以是已经被修饰以优化其结合fcr的能力的fc区。这种优化是本领域已知的,并且描述于例如(i)e et al.increasing the efficacy of cd20 antibody therapy through the engineering of a new type ii anti-cd20 antibody with enhanced direct and immune effector cell
–
mediated b-cell cytotoxicity.blood.2010;115(22):4393
–
4402;和(ii)wang et al.2018igg fc engineering to modulate antibody effector functions.protein cell.2018jan;9(1):63
–
73.doi:10.1007/s13238-017-0473-8(及其中的参考文献)。
75.抗原结合分子可以能够经由除fc区以外的区域结合fc受体。即,抗原结合分子不需要为了能够结合fc受体而包括fc区。例如,抗原结合分子可以含有能够结合fc受体的抗原结合区(例如scfv、fab、修饰的fab、fab
′
、修饰的fab
′
、f(ab
′
)2、fv、dab、fd、dsfv、ds-scfv、scfv2、双特异性t细胞衔接物、纳米抗体、darpin、抗体模拟物、双抗体、三抗体、四抗体、或针对免疫细胞靶向的细胞表面上表达的受体的多肽配体)。抗原结合分子可包括能够结合fc受体的抗原结合区,和能够结合不同抗原,例如在肿瘤微环境中表达的抗原,的抗原结合区。例如,抗原结合分子可包括能够结合fc受体的scfv,和能够结合不同抗原,例如在肿瘤微环境中表达的抗原,的scfv。抗原结合分子可包括双特异性t细胞衔接物,其包括能够结合cd3的scfv,和能够结合不同抗原,例如在肿瘤微环境中表达的抗原,的scfv。
76.抗原结合分子可包括抗原结合区和fc区。抗原结合分子可以是抗体、scfv-fc、dab-fc或重链抗体。示例性重链抗体包含ignar和骆驼科抗体。抗体可以,例如,包括(a)由seq id no:18编码的轻链,(b)由seq id no:20编码的重链,和/或(c)由seq id no:19编码的切割序列。抗体分子可以,例如,包括:(a);(b);(c);(a)和(b);(a)和(c);(b)和(c);或(a)、(b)和(c)。抗体可由seq id no:17编码。由seq id no:18编码的轻链包括由seq id no:5编码的vl。由seq id no:20编码的重链包括由seq id no:4编码的vh。
77.优选地,抗原结合分子是scfv-fc。scfv-fc是包括与fc区融合的scfv的融合蛋白。scfv和fc区的结构是本领域已知的,并且如上所述。根据这些结构,scfv-fc可包括vh和vl(一起形成scfv)以及ch2结构域和ch3结构域(一起形成fc区)。scfv-fc可包括vh和vl(一起
形成scfv),以及ch2结构域、ch3结构域和ch4结构域(一起形成fc区)。在scfv-fc中,scfv与fc区连接。优选地,为了将scfv与fc区连接,scfv中的vl或vh与fc区中的ch2连接。scfv可以直接与fc区连接,即不存在接头。scfv可通过接头与fc区连接。连接子可以是(ser(gly)4)、(ser(gly)4)2、(ser(gly)4)3、(ser(gly)4)4或(ser(gly)4)5。接头可以是氨基酸,或由约2个氨基酸组成的短寡肽。接头可以形成铰链区。scfv-fc可以是二价scfv-fc。二价scfv-fc包括各自与fc区连接的两种不同的scfv。实质上,二价scfv-fc包括两个臂,每个臂包括与fc区连接的scfv。scfv、fc区和连接如上所述。两个臂优选地连接。两个臂之间的连接优选将一个臂中scfv和fc区之间的接头与另一个臂中scfv和fc区之间的接头连接。优选地,在每条臂中,两条臂在scfv和fc区之间的点连接。
78.抗原结合分子可以起增加靶细胞毒性的作用。即,抗原结合分子可以增加对表达抗原结合区的同源抗原的细胞的杀伤。例如,抗原结合分子可以增加对肿瘤细胞、内皮细胞和/或免疫细胞的杀伤。增加的杀伤可由工程化免疫细胞(即,由包括编码抗原结合分子的核酸序列的免疫细胞)介导。增加的杀伤可由非工程化(“旁观者”)免疫细胞(即,由不包括编码抗原结合分子的核酸序列的免疫细胞)介导。增加的杀伤可由工程化免疫细胞和非工程化免疫细胞介导。增加的杀伤可过本领域已知的任何机制。优选地,增加的杀伤是由增加的adcc介导的。增加的杀伤可通过增加ab t细胞的接合来介导。
79.抗原结合分子优选是调理素。调理素是结合抗原以增强其吞噬作用的分子。调理素与抗原的结合可有利于抗原与免疫细胞上的细胞表面受体之间的相互作用,从而增强吞噬作用的动力学。因此,抗原结合分子可以增强吞噬作用。特别地,抗原结合分子可以增强抗原结合区对其具有特异性的抗原的吞噬作用。换句话说,抗原结合分子可以增强由抗原结合区(和因此,抗原结合分子)结合的抗原的吞噬作用。
80.抗原结合区(和抗原结合分子)可以能够结合任何抗原。也就是说,任何抗原都可以被抗原结合区(和抗原结合分子)结合。优选地,抗原结合区(和抗原结合分子)能够结合在肿瘤微环境中的细胞上或由细胞表达的抗原。如果抗原由肿瘤微环境中存在的任何类型的细胞表达,则其在肿瘤微环境中表达。例如,抗原可由肿瘤微环境中的肿瘤细胞、内皮细胞、或免疫细胞表达。因此,抗原结合区(和抗原结合分子)可以能够结合肿瘤抗原、内皮抗原或免疫细胞抗原。免疫细胞可以,例如,是cd4 t细胞、cd8 t细胞、gdt细胞、b细胞、nk细胞、nkt细胞、巨噬细胞、单核细胞、嗜碱性粒细胞、嗜酸性粒细胞或嗜中性粒细胞。
81.抗原结合区(和抗原结合分子)可以能够结合选自由tshr、cd19、cd123、cd22、cd20、cd30、cd171、cs-1、cll-1、cd33、egfrviii、gd2、gd3、bcma、tnag、psma、ror1、flt3、fap、tag72、cd38、cd44v6、cea、epcam、b7-h3、kit、il-13ra2、间皮素、il-llra、psca、prss21、vegfr2、lewisy、cd24、pdgfr-β、ssea-4、cd20、叶酸受体α、erbb2(her2/neu)、muc1、egfr、ncam、前列腺酶、pap、elf2m、ephrin b2、igf-i受体、caix、lmp2、gp100、bcr-abl、酪氨酸酶、epha2、岩藻糖基gmi、sle、gm3、tgs5、hmwmaa、o-乙酰基-gd2、叶酸受体β、tem1/cd248、tem7r、cldn6、gprc5d、cxorf61、cd97、cd179a、alk、聚唾液酸、plac1、globoh、ny-br-1、upk2、havcr1、adrb3、panx3、gpr20、ly6k、or51e2、tarp、wt1、ny-eso-1、lage-la、mage-a1、豆荚蛋白、hpv e6、e7、mage al、etv6-aml、精子蛋白17、xage1、tie 2、mad-ct-1、mad-ct-2、fos相关抗原1、p53、p53突变体、前列腺癌相关蛋白(prostein)、存活素和端粒酶、pcta-1/半乳凝素8、melana/mart1、ras突变体、htert、肉瘤易位断点、ml-iap、erg(tmprss2ets融合
基因)、na17、pax3、雄激素受体,周期素bl、mycn、rhoc、trp-2、cyp1b1、boris、sart3、pax5、oytes1、lck、akap-4、ssx2、rage-1、人端粒酶逆转录酶、ru1、ru2、肠羧基酯酶、突变的hsp70-2、cd79a、cd79b、cd72、lair1、fcar、lilra2、cd300lf、clec12a、bst2、emr2、ly75、gpc3、fcrl5、cea、lingo1、cd70、il13rα2、muc-16、psca、ror1、和igll1所组成的组的抗原。
82.抗原结合区(和抗原结合分子)可以能够结合癌胚抗原(cea)。cea可以是cea-cam5。cea可在许多癌中表达,包含结肠和/或直肠、胃、乳腺、胰腺、肺、甲状腺、子宫颈、或卵巢癌,的那些。
83.cea特异性抗原结合区(和抗原结合分子)可包括由seq id no:1编码的vh结构域。cea特异性抗原结合区(和抗原结合分子)可包括由seq id no:2编码的vl结构域。cea特异性抗原结合区(和抗原结合分子)可包括由seq id no:1编码的vh结构域和由seq id no:2编码的vl结构域。cea特异性抗原结合区(和抗原结合分子)可包括由seq id no:1编码的vh结构域和/或由seq id no:2编码的vl结构域的互补决定区(cdr)。
84.即,cea特异性抗原结合区(和抗原结合分子)可包括由seq id no:1编码的vh结构域的重链cdr1、cdr2和/或cdr3。cea特异性抗原结合区(和抗原结合分子)可包括由seq id no:2编码的vl结构域的轻链cdr1、cdr2和/或cdr3。cea特异性抗原结合区(和抗原结合分子)可包括由seq id no:1编码的vh结构域的重链cdr1、cdr2和/或cdr3和由seq id no:2编码的vl结构域的轻链cdr1、cdr2和/或cdr3。cea特异性抗原结合分子可以是由seq id no:3编码的scfv-fc。scfv可以具有seq id no:7的氨基酸序列。
85.抗原结合区(和抗原结合分子)可以能够结合gd2。gd2可由神经外胚层起源的癌症表达,例如成神经细胞瘤和黑素瘤。
86.gd2特异性抗原结合区(和抗原结合分子)可包括由seq id no:4编码的vh结构域。gd2特异性抗原结合区(和抗原结合分子)可包括由seq id no:5编码的vl结构域。gd2特异性scfv-fc抗原结合区(和抗原结合分子)可包括由seq id no:4编码的vh结构域和由seq id no:5编码的vl结构域。
87.gd2特异性抗原结合区(和抗原结合分子)可包括由seq id no:4编码的vh结构域的cdr和/或由seq id no:5编码的vl结构域的cdr。即,gd2抗原结合区(和抗原结合分子)可包括由seq id no:4编码的vh结构域的重链cdr1、cdr2和/或cdr3。gd2特异性抗原结合区(和抗原结合分子)可包括由seq id no:5编码的vl结构域的轻链cdr1、cdr2和/或cdr3。gd2特异性抗原结合区(和抗原结合分子)可包括由seq id no:4编码的vh结构域的重链cdr1、cdr2和/或cdr3和由seq id no:5编码的vl结构域的轻链cdr1、cdr2和/或cdr3。gd2特异性抗原结合分子可以是由seq id no:6编码的scfv-fc。scfv可以具有seq id no:8的氨基酸序列。
88.gd2特异性抗原结合分子可包括(a)由seq id no:18编码的轻链,(b)由seq id no:20编码的重链,和/或(c)切割序列。gd2特异性抗原结合分子可以,例如,包括:(a);(b);(c);(a)和(b);(a)和(c);(b)和(c);或(a)、(b)和(c)。优选地,gd2特异性抗原结合分子以该顺序包括(a)、(b)和(c)。在本文所述的任何方面,切割序列(c)可以,例如,是弗林-v5-sg-p2a。切割序列可以,例如,由seq id no:19编码。其它切割序列也是本领域已知的,并可用作切割序列(c)。例如,切割序列(c)可包括p2a、e2a、f2a或t2a或由其组成。在本文所述的任何方面,ires或ires 2序列都可用于替代切割序列(c)。gd2特异性抗原结合分子可以是
由seq id no:17编码的抗体。
89.抗原结合区(和抗原结合分子)可以能够结合b7-h3。b7-h3可由神经外胚层起源的癌症如成神经细胞瘤和黑素瘤表达。
90.b7-h3特异性抗原结合区(和抗原结合分子)可包括由seq id no:9编码的vh结构域。b7-h3特异性抗原结合区(和抗原结合分子)可包括由seq id no:10编码的vl结构域。b7-h3特异性抗原结合区(和抗原结合分子)可包括由seq id no:9编码的vh结构域和由seq id no:10编码的vl结构域。b7-h3特异性抗原结合区(和抗原结合分子)可包括由seq id no:9编码的vh结构域的cdr和/或由seq id no:10编码的vl结构域的cdr。即,b7-h3特异性抗原结合区(和抗原结合分子)可包括由seq id no:9编码的vh结构域的重链cdr1、cdr2和/或cdr3。b7-h3特异性抗原结合区(和抗原结合分子)可包括由seq id no:10编码的vl结构域的轻链cdr1、cdr2和/或cdr3。b7-h3特异性抗原结合区(和抗原结合分子)可包括由seq id no:9编码的vh结构域的重链cdr1、cdr2和/或cdr3和由seq id no:10编码的vl结构域的轻链cdr1、cdr2和/或cdr3。b7-h3特异性抗原结合分子可以是由seq id no:11编码的scfv-fc。scfv可以具有seq id no:12的氨基酸序列。
91.抗原结合区(和抗原结合分子)可以能够结合cd20。cd20在b细胞发育期间表达,晚期前b细胞阶段通过记忆细胞(尽管不在早期前b细胞或成浆细胞和浆细胞上)。cd20也在b细胞淋巴瘤、毛细胞白血病、b细胞慢性淋巴细胞白血病、和黑素瘤癌症干细胞中表达。
92.cd20特异性抗原结合区(和抗原结合分子)可包括由seq id no:13编码的vh结构域。cd20特异性抗原结合区(和抗原结合分子)可包括由seq id no:14编码的vl结构域。cd20特异性抗原结合区(和抗原结合分子)可包括由seq id no:13编码的vh结构域和由seq id no:14编码的vl结构域。cd20特异性抗原结合区(和抗原结合分子)可包括由seq id no:13编码的vl结构域的cdr和/或由seq id no:14编码的vl结构域的cdr。即,cd20特异性抗原结合区(和抗原结合分子)可包括由seq id no:13编码的vh结构域的重链cdr1、cdr2和/或cdr3。cd20特异性抗原结合区(和抗原结合分子)可包括来自由seq id no:14编码的vl结构域的轻链cdr1、cdr2和/或cdr3。cd20特异性抗原结合区(和抗原结合分子)可以包括来自由seq id no:13编码的vh结构域的重链cdr1、cdr2和/或cdr3和来自由seq id no:14编码的vl结构域的轻链cdr1、cdr2和/或cdr3。cd20特异性抗原结合分子可以是由seq id no:15编码的scfv-fc。scfv可以具有seq id no:16的氨基酸序列。
93.抗原结合分子优选由包括编码抗原结合分子的核酸序列的免疫细胞表达。抗原结合分子的表达可以基于编码抗原结合分子的mrna在免疫细胞中的存在来确定。优选地,抗原结合分子的表达基于抗原结合分子本身在免疫细胞中的存在来确定。测定细胞中mrna或蛋白质存在的方法是本领域公知的。例如,逆转录酶pcr或northern印迹可用于确定细胞中mrna的存在。流式细胞术、免疫荧光成像或western印迹可用于确定细胞中蛋白质的存在。
94.产生免疫细胞的方法
95.本发明提供了一种产生本发明的免疫细胞的方法。所述方法包括将编码抗原结合分子的核酸序列引入免疫细胞。抗原结合分子在上文详细描述。核酸序列可以,例如,通过转导或转染引入免疫细胞。例如,本领域已知的t细胞转导方法可用于转导gdt细胞,可具有所述核酸序列。gdt细胞可在这种转导之前扩增,例如通过在il-2和唑来膦酸存在下培养约5天(如约3天、约4天、约6天、或约7天)的时间。
96.术语“转导”可用于描述病毒介导的核酸转移。病毒载体可用于用核酸序列转导细胞。因此,核酸序列可包括在病毒载体中。病毒载体可以是逆转录病毒、慢病毒、腺病毒、腺相关病毒(aav)或单纯疱疹病毒(hsv)载体。优选地,病毒载体是逆转录病毒载体。用于生产和纯化此类载体的方法是本领域已知的。可以使用本领域已知的任何方法转导免疫细胞。转导可以是体外或离体的。
97.术语“转染”可用于描述非病毒介导的核酸转移。可以使用本领域已知的任何方法转导免疫细胞。转染可以是体外或离体的。可以使用能够转染免疫细胞的任何载体,例如常规质粒dna或rna转染。可以使用人工染色体和/或裸rna和/或sirna用所述核酸序列转染细胞。人类人工染色体描述于例如kazuki et al.,mol.ther.19(9):1591
–
1601(2011),和kouprina et al.,expert opinion on drug delivery 11(4):517
–
535(2014)。可选的非病毒递送系统包含dna质粒、裸核酸、和与递送载体,如脂质体,复合的核酸。核酸的非病毒递送的方法包含脂质转染、显微注射、生物弹(biolistics)、病毒体、脂质体、免疫脂质体、聚阳离子或脂质:核酸缀合物、裸dna、人工病毒体和试剂增强的dna摄取。脂质转染描述于例如美国专利第5,049,386、4,946,787;4,897,355号;而脂质转染试剂是商业销售的(例如transfectam
tm
和lipofectin
tm
)。适于有效受体识别脂质转染多核苷酸的阳离子和中性脂质包含felgner,wo 91/17424;wo 91/16024的那些。脂质:核酸复合物的制备,包含靶向脂质体如免疫脂复合物,是本领域技术人员公知的(参见,例如,crystal,science 270:404
–
410(1995);blaese et al.,cancer gene ther.2:291
–
297(1995);behr et al.,bioconjugate chem.5:382
–
389(1994);remy et al.,bioconjugate chem.5:647
–
654(1994);gao et al.,gene therapy 2:710
–
722(1995);ahmad et al.,cancer res.52:4817
–
4820(1992);美国专利第4,186,183、4,217,344、4,235,871、4,261,975、4,485,054、4,501,728、4,774,085、4,837,028、和4,946,787号)。
98.纳米颗粒递送系统可用于用核酸序列或核酸构建体转染细胞。这样的递送系统包含但不限于基于脂质的系统、脂质体、胶束、微泡和外泌体。关于可以递送rna的纳米颗粒,参见,例如,alabi etal.,proc natl acad sci u s a.2013aug 6;110(32):12881
–
6;zhang etal.,adv mater.2013sep 6;25(33):4641
–
5;jiang etal.,nano lett.2013mar 13;13(3):1059
–
64;karagiannis et al.,acs nano.2012oct 23;6(10):8484
–
7;whitehead et al.,acs nano.2012aug 28;6(8):6922
–
9和lee et al.,nat nanotechnol.2012jun 3;7(6):389
–
93。脂质纳米颗粒、球形核酸30(sna
tm
)构建体、纳米复合物和其它纳米颗粒(特别是金纳米颗粒)也被考虑作为递送根据本发明的构建体或载体的手段。
99.核酸构建体的摄取可通过几种已知的转染技术来增强,例如那些包含使用转染剂的技术。这些试剂的实施例包含阳离子试剂,例如,磷酸钙和deae葡聚糖和脂质转染试剂,例如lipofectamine、fugene和transfectam。
100.免疫细胞可以在合适的条件下转染。免疫细胞和试剂或载体可以,例如,接触五分钟至十天,优选一小时至五天,更优选五小时至两天,甚至更优选十二小时至一天。
101.转导或转染到免疫细胞中的核酸序列引起抗原结合分子在免疫细胞中的表达。核酸序列优选包括与编码抗原结合分子的序列有效连接的启动子。启动子在免疫细胞中可以是组成型活性的。启动子可以是免疫细胞中可诱导的。
102.药物、方法和治疗用途
103.本发明的免疫细胞可用于治疗人或动物体的方法中。因此,本发明提供了治疗个体的疾病的方法,所述方法包括向所述个体施用治疗数量的本发明的免疫细胞。本发明还提供了用于治疗个体的疾病的方法中的本发明的免疫细胞,所述方法包括向所述个体施用治疗量的所述免疫细胞
104.所述个体可以是物种。例如,所述个体可以是人、狗、猫、小鼠、大鼠、猪、绵羊、牛、山羊或马。优选地,所述个体是人。优选地,所述免疫细胞与所述个体属于相同物种。所述免疫细胞相对于所述个体可以是自体的。所述免疫细胞对于所述个体可以是同种异体的。所述个体可以是婴儿、青少年或成人。所述个体可能患有所述疾病、易感所述疾病或处于所述疾病的风险中。
105.本发明涉及向个体施用治疗有效数量的本发明的免疫细胞。治疗有效数量是改善疾病的一种或多种症状的数量。治疗有效数量优选是治疗疾病的数量。可以将任何合适数量的免疫细胞施用给个体。作为指导,待施用的免疫细胞的数目通常为105至109,优选106至108。例如,每kg个体可以施用至少,或约,0.2
×
106、0.25
×
106、0.5
×
106、1.5
×
106、4.0
×
106或5.0
×
106个免疫细胞。例如,可以施用至少,或约,105、106、107、108、或109个免疫细胞。可以施用至少约1
×
106、至少约2
×
106、至少约2.52
×
106、至少约5
×
106、至少约1
×
107、至少约2
×
107、至少约5
×
107、至少约1
×
108或至少约2
×
108个免疫细胞。
106.免疫细胞可以与治疗疾病的其它手段和物质组合使用。例如,免疫细胞可以与一种或多种癌症疗法组合使用。例如,免疫细胞可以与一种或多种化疗剂组合使用。免疫细胞可以与一种或多种表达car的ab t细胞组合使用。免疫细胞可以与放射疗法组合使用。免疫细胞可以与手术,例如切除或去除肿瘤的手术组合使用。
107.免疫细胞可以与一种或多种治疗感染性疾病,例如病毒感染或细菌感染,的疗法组合使用。例如,免疫细胞可以与一种或多种抗病毒药物组合使用。免疫细胞可以与一种或多种抗生素组合使用。
108.免疫细胞可以与支持免疫细胞功能的物质组合使用。例如,免疫细胞可以与氨基二膦酸盐如唑来膦酸联合使用。当,例如,免疫细胞是vδ2 gdt细胞时,免疫细胞可与氨基二膦酸盐联合使用。免疫细胞可以与一种或多种免疫刺激细胞因子如il-2、gm-csf或g-csf联合使用。il-2、gm-csf或g-csf各自均可增强adcc感受态细胞的其它群体。
109.当免疫细胞与一种或多种其它物质组合使用时,免疫细胞可以与其它物质同时、依次或分开施用。免疫细胞可以与现有的用于治疗疾病的治疗方法组合使用,并且可以,例如,简单地与这样的治疗方法混合。因此,免疫细胞可用于增加现有疾病治疗的功效。
110.可以使用任何合适的方法配制免疫细胞用于施用。可以使用药学领域的常规方法进行细胞与标准药学上可接受的载体和/或赋形剂的配制。制剂的确切性质将取决于几个因素,包含待施用的细胞和期望的施用途径。合适类型的制剂在remington’s pharmaceutical sciences,第19版,mack publishing company,eastern pennsylvania,usa中有充分描述。
111.免疫细胞可以用生理学上可接受的载体或稀释剂配制。通常,将这样的制剂制备为细胞的液体悬浮液。细胞可以与药学上可接受的且与活性成分相容的赋形剂混合。合适的赋形剂是,例如,水、盐水、葡萄糖、甘油等及其组合。此外,如果需要,本发明的药物组合
物可以含有少量辅料,例如润湿剂或乳化剂、ph缓冲剂和/或增强有效性的佐剂。
112.免疫细胞可通过任何途径施用。合适的途径包含但不限于静脉内、肌内、腹膜内或其它合适的施用途径。免疫细胞优选静脉内施用。
113.疾病可以是患者可受益于靶向adcc的任何疾病。疾病可以是患者可受益于靶向t细胞应答的任何疾病。例如,疾病可以是其中受试者可受益于杀死不需要的细胞的疾病。不需要的细胞可以,例如,是癌细胞。不需要的细胞可以是被细菌、病毒、真菌、原生动物或寄生虫感染的细胞。不需要的细胞可以是异常免疫细胞,即引起有害免疫应答的免疫细胞。例如,异常免疫细胞可以是自身免疫细胞。因此,疾病可以是感染(例如细菌、病毒、真菌、原生动物或其它寄生虫感染)或自身免疫疾病。优选地,疾病是癌症。癌症可以是造血组织和/或淋巴组织的癌症。优选地,癌症是实体瘤。
114.癌症可以是原发性癌症或继发性癌症。癌症可以是肛门癌、胆管癌(胆管癌)、膀胱癌、血癌、骨癌、肠癌、脑肿瘤、乳腺癌、结肠直肠癌、宫颈癌、内分泌肿瘤、眼癌(例如眼黑色素瘤)、输卵管癌、胆囊癌、头和/或颈癌、卡波西肉瘤、肾癌、喉癌、白血病、肝癌、肺癌、淋巴结癌、淋巴瘤、黑素瘤、间皮瘤、骨髓瘤、神经内分泌肿瘤、卵巢癌、食管癌、胰腺癌、阴茎癌、原发性腹膜癌、前列腺癌、皮肤癌、小肠癌、软组织肉瘤、脊髓肿瘤、胃癌、睾丸癌、胸腺癌、甲状腺癌、气管癌、未知的原发性癌、阴道癌、外阴癌或子宫内膜癌。白血病可以是急性淋巴细胞白血病、急性髓性白血病(aml)、慢性淋巴细胞白血病或慢性髓性白血病。淋巴瘤可以是霍奇金淋巴瘤或非霍奇金淋巴瘤。癌症可以是成神经细胞瘤或黑素瘤。癌症可以是结肠癌、直肠癌、胃癌、乳腺癌、肺癌、甲状腺癌或卵巢癌。癌症可以是癌。优选地,癌症是结肠直肠癌或神经内分泌肿瘤。
115.实施例
116.vδ2
γδt细胞可以被转导以分泌特异性结合靶细胞上的抗原的蛋白质
117.vδ2
γδt细胞被转导以分泌靶向肿瘤相关抗原cea和gd2的scfv融合肽。收获来自转导细胞的上清液,并将其应用于cea
capan-1细胞和cea-hela细胞,或gd2
/-supt1细胞。使用藻红蛋白缀合的抗人fc抗体检测scfv-fc融合蛋白的结合。将在细胞系中产生的纯化的抗cea scfv-fc融合蛋白或纯化的抗gd2抗体用作阳性对照。
118.如图2所示,来自转导的细胞系和转导的vδ2γδt细胞的上清液的成分能够特异性结合抗原阳性细胞,并导致在它们的表面上检测到人fc。
119.细胞毒性实验证明与分泌scfv-fc蛋白的vδ2的直接和间接接触的作用
120.因为工程化的t细胞分泌可能对旁观者非工程化细胞的细胞毒性有影响的蛋白质,所以开发了一系列实验条件来证明这一点。实验设置如图3所示。简单地说,除了比较转导和未转导的vδ2与靶细胞直接共培养时的细胞毒性之外,还加入了两种条件来证明细胞接触的自主作用。首先,将来自转导的vδ2的上清液加入到未转导的vδ2和靶细胞的共培养物中。其次,在转导细胞存在下将未转导细胞与靶标共培养,转导细胞隔离在阻断细胞通过但不阻断分泌分子通过的半透膜后。所有共培养为18小时,在效应子∶靶标比为1∶1进行。为了证明抗cea scfv-fc融合蛋白的作用,使用cea
capan-1和cea-hela细胞。为了证明抗gd2 scfv-fc融合蛋白的作用,使用工程化以表达gd2的supt1或等基因gd2-野生型supt1。
121.与nt vδ2相比,转导以分泌抗ceascfv-fc融合蛋白的vδ2细胞导致cea
靶标的显著更高的死亡(p《0.0001,图4a)。来自转导以表达抗cea scfv-fc融合蛋白的vδ2
细胞的上
清液,通过未转导的vδ2,增强了cea
靶标的杀伤(p《0.0001),并且还导致cea-靶标杀伤的少量增加(p=0.031,图4b)。当分泌抗cea scfv-fc融合蛋白的vδ2被隔离在半透膜后面时,当与隔离未转导的细胞相比时,它们也能够增强未转导的vδ2杀死cea
靶标的能力(p=0.012,图4c)。
122.对于转导以分泌抗gd2 scfv-fc融合蛋白的vδ2,观察到类似的数据。转导的vδ2比未转导的vδ2(p=0.03)更好地杀死gd2
靶标,并且比同基因gd2-对照显示更大的针对gd2
靶标的细胞毒性(p=0.0049,图4d)。当与未转导对照(p=0.0025)或等基因gd2-靶标(p=0.0002,图4e)相比时,来自表达抗gd2 scfv-fc融合蛋白的vδ2的上清液显著增强非转导vδ2杀伤gd2
靶标的能力。当分泌抗gd2 scfv-fc融合蛋白的vδ2被隔离在半透膜后面时,当与隔离未转导的细胞(p=0.0158)或gd2-靶标的杀伤(p=0.0003,图4f)相比时,它们也能够增强未转导的vδ2杀伤gd2
靶标的能力。
123.当在分泌抗cea scfv-fc融合蛋白的vδ2、或隔离在半透膜后面的非转导对照的存在下,将未转导的vδ2与cea
±
靶共培养时,仅当隔离分泌抗cea scfv-fc融合蛋白的细胞被隔离(与隔离的nt vδ2相比,p=0.0014)并使用cea
靶标(与cea-靶相比,p=0.012,图5)时,观察到ifnγ产生的显著增加。
124.vδ2
γδt细胞可以被转导以分泌特异性结合靶细胞上的抗原的完整抗体
125.hek293t和vδ2
γδt细胞被转导以分泌靶向肿瘤相关抗原gd2(seq id no:17)的igg1抗体。收获用减少体积的病毒转导的hek293t细胞的上清液,并应用于gd2
/-supt1细胞。使用藻红蛋白缀合的抗人fc抗体检测scfv-fc融合蛋白的结合(图6)。还收集来自转导的vδ2
γδt细胞的上清液,并将其施加到gd2
/-supt1细胞,并使用alexafluor 647缀合的抗人igg抗体检测抗体结合(图7)。将在细胞系中产生的纯化抗gd2抗体用作阳性对照。
126.如图6和7所示,来自转导细胞系和转导vδ2
γδt细胞的上清液的成分能够特异性结合抗原阳性细胞,并导致在它们的表面上检测到人fc或igg。
127.细胞毒性实验证明与分泌抗体的vδ2的直接和间接接触的作用
128.为了证明细胞接触依赖性和细胞接触自主性效应,使用了两种实验系统(图8a)。简言之,将未转导的vδ2
γδt细胞或转导以表达抗gd2 igg1的vδ2
γδt细胞在效应子∶靶标1∶1下与gd2
/-supt1共培养。在第二个实验中,将来自未转导的vδ2
γδt细胞的上清液或来自转导以表达抗gd2 igg1的vδ2 γδt细胞的上清液加入未转导的vδ2
γδt细胞和gd2
/-supt1的1∶1共培养物中。使用流式细胞术测定靶细胞死亡,图8b和8c显示了三重复的代表性数据。转导以表达抗gd2 igg1的vδ2
γδt细胞具有增强的针对supt1-gd2但不针对supt1-wt的细胞毒性(图8b)。来自转导以表达抗gd2 igg1的vδ2
γδt细胞的上清液增强了未转导的vδ2
γδt细胞针对supt1-gd2但不针对supt1-wt的细胞毒性(图8c)。
129.材料和方法
130.细胞系
131.capan-1、hela和supt1细胞系得自atcc。通过用编码gd2/gd3合酶的载体转导野生型supt1,并分离成功转导的细胞的克隆,产生了supt1-gd2。
132.pbmc的供体选择
133.pbmc从年龄为20
–
36岁的健康供体的血液中分离。在纳入之前,筛选供体的sfp构建体和扩增vδ2细胞之间的交叉反应性。有交叉反应性证据的供体不用于细胞毒性实验。
134.新鲜pbmc的分离和预刺激处理
135.用10ml pbs 500μl 100mm edta稀释20ml全血,并在20ml percoll上分层。将界面pbmc(20分钟,300xg,rt)在pbs中洗涤,并在补充青霉素/链霉素(100iu/ml青霉素、100μg/ml链霉素(sigma-aldrich,missouri,usa))的25ml t细胞培养基(x-vivo 15(lonza biowhittaker,maryland,usa))中重悬,并在使用前培养过夜。
136.vδ2
t细胞扩增
137.对于特定的vδ2
γδt细胞扩增,如上所述分离pbmc。将它们培养在补充了l-谷氨酰胺(2mm,sigma-aldrich)、青霉素/链霉素(100iu/ml青霉素、100μg/ml链霉素(sigma-aldrich))和10%fcs(v/v,(gibco,massachusetts,usa))的rpmi-1640培养基中。vδ2
γδt细胞扩增使用5μm唑来膦酸(actavis,new jersey,usa)和100iu/ml il-2(阿地白介素,novartis,frimley,uk)刺激,在pbmc分离后(第1天)将其加入pbmc悬浮液中。每2
–
3天补充il-2,从孔中除去一半培养基,并用含有200iu/ml il-2的新鲜培养基替换。
138.逆转录病毒构建体的构建
139.用于所有构建体的γ逆转录病毒载体是sfg(riviere etal.,1995),用rd114包膜进行假型化。使用phusion ht ii聚合酶根据制造商的说明(thermo scientific,massachusetts,usa)扩增dna片段。pcr在ptc-200dna engine(mj research,massachusetts,usa)中进行。使用wizard sv gel&pcr clean-up试剂盒(promega,wisconsin,usa)从1%琼脂糖凝胶中提取pcr产物。使用nanodrop nd-1000分光光度计(thermo scientific,massachusetts,usa)测定样品浓度。构建体包含针对,包含与人igg1的fc部分连接的人gd2(克隆14g2a)或人cea(克隆sm3el)的一组靶标,的一系列scfv之一。
140.除了scfv-fc融合蛋白构建体之外,还包含作为携带cd34表位的标志物的rqr8(philip等,2014),其通过可切割的2a肽与scfv-fc融合蛋白分开。这使得表达scfv-fc融合蛋白的细胞可通过流式细胞术使用抗cd34抗体克隆qbend10染色来检测。
141.慢病毒构建体的构建
142.用于完整抗体转导的慢病毒载体是pccl(dull etal.1998),用rdpro包膜假型化(cosset etal.1995)。使用phusion ht ii聚合酶根据制造商的说明(thermo scientific,massachusetts,usa)扩增dna片段。pcr在ptc-200dna engine(mj research,massachusetts,usa)中进行。使用wizard sv gel&pcr clean-up试剂盒(promega,wisconsin,usa)从1%琼脂糖凝胶中提取pcr产物。使用nanodrop nd-1000分光光度计(thermo scientific,massachusetts,usa)测定样品浓度。构建体包括抗gd2 igg1(克隆14g2a)。
143.除了igg1构建体之外,还包含egfp,其通过可切割的2a肽与igg1蛋白分离。这使得表达igg1的细胞可通过流式细胞术检测。
144.通过转染生产病毒颗粒
145.在第1天将1.5
×
106个293t细胞/100mm2培养皿(nucleon delta surface,thermo fisher)铺板于293t培养基(d-mem,10%fcs(v/v))中。按照制造商的说明,使用gene juice transfection reagent(novagen/millipore,massachusetts,usa)在第2天共转染293t细胞,产生γ逆转录病毒或慢病毒颗粒。在第4天收获含有病毒颗粒的上清液;补充培养基,并在第5天收获。将γ逆转录病毒上清液合并,过滤(0.45μm过滤器,millipore)并直接用于转
system.journal ofvirology,nov 1998;72(11):8463
–
71.
160.f.l.cosset,y.takeuchi,j.l.battini,r.a.weiss,m.k.collins.high-titer packaging cells producing recombinantretroviruses resistantto human serum.journal ofvirology,dec 1995;69(12):7430
–
6.
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。