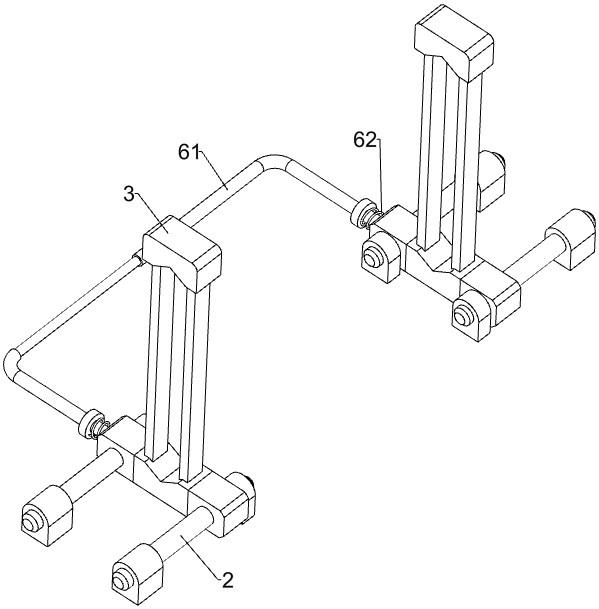
n基因检测引物及探针组、层析试纸条、制备方法、检测试剂盒、检测方法
技术领域
1.本技术涉及一种生物检测技术领域,更具体地说,尤其涉及n基因检测引物及探针组、层析试纸条、制备方法、检测试剂盒、检测方法。
背景技术:
2.新型冠状病毒肺炎(sars-cov-2)引起,新冠的全球传播对各个国家构成了多方面威胁。
3.n基因是新冠病毒核酸检测(sars-cov-2)的靶标基因之一,它是新型冠状病毒基因组中核壳蛋白基因。
4.申请人经过文献调研,发现了以下文献均是基于n基因提出了检测试剂盒:
5.文献1:cn111778356a。
6.文献2:cn114317822a。
7.文献3:cn114277048a。
8.文献4:cn111690772a。
9.文献5:us20220259680a1。
10.文献6:us20220195541a1。
11.文献7:us20220056542a1。
12.文献8:ep3986614a2。
13.文献9:ep3911769a1。
14.申请人在先申请“2022110650049”提出了一种核酸检测装置,其采用层析试纸条来实现核酸检测。所述核酸检测设备将扩增与检测试剂盒两种技术有机结合在一起。但是,上述技术结合在一起,对层析试纸条(即引物、探针)等提出了新的技术挑战:
15.第一,检测装置体型小、加热降温功率慢。因此,pcr扩增在恒温状态下,且温度在40
°
左右是适宜的。而现有技术的检测试剂盒中的扩增程序一般都是在高温状态下进行。
16.第二,现有技术如cn112458210a、cn111500776a等技术均提出了基于rpa技术的引物、探针。上述荧光rpa扩增的程序为:40℃、20min,间隔30s采集一次荧光,计40个循环。但是,上述引物、探针并不适用于“2022110650049”的方案,因为“2022110650049”采用的核酸检测装置没有荧光。
17.第三,现有技术如cn112981008a,在其实施例3公开了一种基于rpa技术的引物、探针,其也能配合层析试纸进行检测。
18.针对n基因的引物、探针、层析试纸也要与申请人研发的“一种引物、探针、组合物、层析试纸及制备方法、试剂盒”均能够搭配在“2022110650049”研发的核酸检测装置。因此,两者的研发目标要相互协调。
19.即针对n基因的引物、探针、层析试纸,也需要满足下述研发目标:
20.1)检测时间要快:恒温扩增温度控制在40℃左右且时间指标控制在10分钟。
21.2)初阳人员能够检测出来:灵敏度控制指标中的扩增体系内的样本在200copies/ml能够检测出来。
22.而通过上述检索分析,目前的现有技术还无法满足上述研发目标。
技术实现要素:
23.本技术的第一目的在于针对上述现有技术的不足,提供一种n基因检测引物及探针组。
24.本技术的第二目的在于提供一种层析试纸条。
25.本技术的第三目的在于提供一种层析试纸条的制备方法。
26.本技术的第四目的在于提供一种检测试剂盒。
27.本技术的第五目的在于提供一种非诊断目的2019-cov-2病毒检测方法。
28.本技术的技术方案是:
29.一种层析试纸,包括pvc底板、样品垫、结合垫、检测垫、吸水垫;沿着层析溶液的流动方向,样品垫、结合垫、检测垫、吸水垫依次布置在pvc底板上;样品垫、结合垫、检测垫、吸水垫相邻的两种结构搭接连接;
30.结合垫中包含:fam抗体-显色颗粒复合物、dnp-显色颗粒复合物,所述fam抗体-显色颗粒复合物经由显色乳胶微球与fam抗体混合反应形成;所述dnp-显色颗粒复合物经由显色乳胶微球与dnp混合反应形成;
31.所述检测垫包括硝酸纤维素膜,在检测垫上设置检测区:其经由抗地高辛抗体加载在硝酸纤维素膜上形成;所述检测抗地高辛抗体是由抗地高辛抗体与磷酸缓冲液组成;
32.在检测垫上设置对照区:其经由对dnp抗体加载在硝酸纤维素膜上形成;dnp抗体由dnp多克隆抗体与磷酸缓冲液组成。
33.进一步,所述的显色颗粒均为红色乳胶微球。
34.进一步,所述乳胶微球粒径为400nm。
35.一种层析试纸的制备方法,其包括如下步骤:
36.s100,制作结合垫:
37.制备显色颗粒溶液,将显色颗粒溶液与fam抗体混合反应形成fam抗体-显色颗粒复合物,将显色颗粒溶液与dnp混合反应形成dnp-显色颗粒复合物,将fam抗体-显色颗粒复合物、dnp-显色颗粒复合物加载到结合垫上。
38.s200,制作检测垫:
39.抗地高辛抗体和dnp抗体分别加载在检测垫上的检测区和对照区。
40.s300,制备试纸大板:
41.样本垫、结合垫、检测垫、吸水垫依次布置在pvc底板上形成试纸大板;其中,结合垫与检测垫两者部分重合,吸水垫与检测垫两者部分重合。
42.s400,制备层析试纸,将步骤三中制备的试纸大板进行裁切,制备成检测试纸。
43.进一步,若有sars-cov-2病毒,其n基因在经过扩增体系后会产生扩增产物;扩增产物首先与样本垫结合,然后经过结合垫,其在经过结合垫时,扩增产物的fitc标签与fam抗体-显色颗粒复合物结合;
44.再经过检测垫:经过检测区时,扩增产物的另一端digoxin标签会和检测区上的抗
地高辛抗体结合使检测区显色;
45.经过对照区,溶液在经过结合垫时,必然会混入dnp-显色颗粒复合物,溶液在层析试纸流动的时候,经过对照区时,dnp-显色颗粒复合物会与dnp抗体结合,对照区显色。
46.2019-cov-2病毒n基因检测引物及探针组,所述的引物的核苷酸序列为:
47.上游引物序列:ccaaa ctgtc actaag aaatc tgctg ctgag
48.下游引物序列:
49.[5
’‑
digoxin]-atcagttccttgtctgattagttcctggtcc
[0050]
探针序列:[5’fam]-ctaagaagcctcggcaaaaacgtactgccac[thf]aaagcatacaatgtaacac-[3’c3spacer]。
[0051]
进一步,所述引物、探针有四个修饰位点:
[0052]
在下游引物5’端标记digoxin;
[0053]
探针5’端标记fam;
[0054]
探针距离5’端约30nt、距离3’端约15nt位置设置一个四氢呋喃修饰位点;
[0055]
探针3’端末端标记阻断探针延伸的阻断基团。
[0056]
进一步,所述阻断基团采用c3-spacer修饰。
[0057]
一种检测试剂盒,其包括前述的引物及探针组、前述的层析试纸。
[0058]
一种非诊断目的2019-cov-2病毒检测方法,包括以下步骤:
[0059]
s1,配置反应体系:
[0060][0061]
所述的引物及探针组为前述的引物及探针组;
[0062]
s2,将s1中配制的体系溶解恒温扩增混合酶冻干微球,酶冻干微球主要成分如下:
[0063][0064]
s3,扩增体系粘稠,配制后需在涡旋仪中涡旋震荡混匀20s后再将体系放置于39-42℃金属浴或其他恒温仪器中,扩增10min;
[0065]
s4,待扩增结束后,使用蒸馏水对扩增产物进行稀释,稀释倍数可根据产物浓度控制在10-120倍不等。
[0066]
s5,产物稀释后,取80μl稀释产物滴加到前述的层析试纸条上,5-10min读取结果。
[0067]
本技术的有益效果在于:
[0068]
第一,本技术的基础构思是设计一种引物、探针,扩增时间仅10min,提高了检测效率;扩增温度低,减少气溶胶产生和核酸污染,同时反应过程无需变温,扩增装置简易;检测产物匹配自制试纸条,无需复杂设备,且检测结果肉眼可鉴。
[0069]
第二,本技术经过灵敏性试验研究,表明:本技术的引物探针组合,最低检测限可低于200copies/ml。对于初阳、无症状人员而言,也能检测出来。
附图说明
[0070]
下面结合附图中的实施例对本技术作进一步的详细说明,但并不构成对本技术的任何限制。
[0071]
图1是本技术的层析试纸的设计图。
[0072]
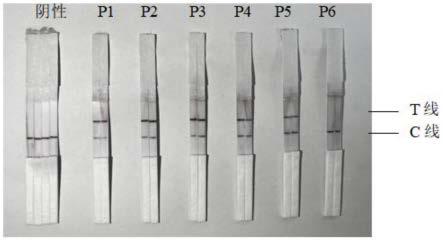
图2是本技术的验证性试验的测试结果。
[0073]
图3是本技术的层析试纸灵敏度验证的测试结果。
[0074]
图4是本技术的特异性扩增试验的测试结果。
[0075]
附图标记:
[0076]
样品垫101、结合垫102、检测垫103、吸水垫104、检测区201、对照区202。
具体实施方式
[0077]
下面结合附图并通过具体实施方式来进一步说明本发明的技术方案,但下述的实例仅仅是本发明的简易例子,并不代表或限制本发明的权利保护范围,本发明的保护范围以权利要求书为准。
[0078]
《研发要求》
[0079]
研发目标(1):检测时间要快:恒温扩增温度控制在40℃左右且时间指标控制在10分钟。
[0080]
研发目标(2)初阳人员能够检测出来:灵敏度控制指标中的扩增体系内的样本在200copies/ml能够检测出来。
[0081]
基于现有知识的分析,本技术的研发重点与难点在于:
[0082]
1)现有的引物、探针、层析试纸还无法满足前述的研发目标(1)。
[0083]
现有技术的恒温扩增,最好的效果就是:温度在40℃扩增20min。恒温扩增技术应用在n基因上,扩增时间缩短到10min,还没有成功经验。
[0084]
2)现有的引物、探针、层析试纸还无法满足前述的研发目标(2)。
[0085]
灵敏度是更具挑战的指标之一。研发团队经过测试:cn112981008a的灵敏度在1000copies/ml;上述设计仍然无法达到本技术的设计目标。
[0086]
而如:cn 112646929 a采用了rna恒温扩增 胶体金层析试纸方案,在其技术效果中认为:在同一管内能够同时扩增新型冠状病毒orf1ab基因、n基因和内参actb基因三种指标,且灵敏度还能达到rna拷贝的最低检测限为100拷贝/ml。
[0087]
本项目在初始设计时,对cn 112646929a的方案进行了大量重复试验,灵敏度事实上无法达到上述效果。事实上,其灵敏度在1000拷贝/ml以上。而从这一现有技术的测试结
果出发,研发团队一度对“恒温扩增 层析试纸”方案能够完成研发目标产生过动摇。
[0088]
《实施例一、研发方案》
[0089]
(1)根据n基因保守序列设计的引物、探针,其核苷酸序列如下:
[0090]
上游引物序列:ccaaa ctgtc actaag aaatc tgctg ctgag。
[0091]
下游引物序列:
[0092]
[5
’‑
digoxin]-atcagttccttgtctgattagttcctggtcc。
[0093]
探针序列:[5’fam]-ctaagaagcctcggcaaaaacgtactgccac[thf]aaagcatacaatgtaacac-[3’c3spacer]。
[0094]
(2)适配的层析试纸
[0095]
硬件设计:如图1所示,一种层析试纸,包括pvc底板、样品垫101、结合垫102、检测垫103、吸水垫104;沿着层析溶液的流动方向,样品垫101、结合垫102、检测垫103、吸水垫104依次布置在pvc底板上;样品垫101、结合垫102、检测垫103、吸水垫104相邻的两种结构的重合长度在1mm。
[0096]
核心设计:
[0097]
(2.1)结合垫102中包含:fam抗体-显色颗粒复合物、dnp-显色颗粒复合物,所述fam抗体-显色颗粒复合物经由显色乳胶微球与fam抗体混合反应形成;所述dnp-显色颗粒复合物经由显色乳胶微球与dnp混合反应形成;所述的显色颗粒均为红色乳胶微球,所述乳胶微球粒径为400nm。
[0098]
(2.2)所述检测垫103包括硝酸纤维素膜。
[0099]
在检测垫上设置检测区201(即t线);检测区201,其经由抗地高辛抗体加载在硝酸纤维素膜上形成(所述检测抗地高辛抗体是由抗地高辛抗体与磷酸缓冲液组成)。
[0100]
在检测垫上设置对照区202(即c线)。对照区202,其经由对dnp抗体加载在硝酸纤维素膜上形成(dnp抗体由dnp多克隆抗体与磷酸缓冲液组成)。
[0101]
作为一种全新的层析试纸,其制备方法是:
[0102]
s100,制作结合垫:
[0103]
制备显色颗粒溶液,将显色颗粒溶液与fam抗体混合反应形成fam抗体-显色颗粒复合物,将显色颗粒溶液与dnp混合反应形成dnp-显色颗粒复合物,将fam抗体-显色颗粒复合物、dnp-显色颗粒复合物加载到结合垫上。
[0104]
s200,制作检测垫:
[0105]
抗地高辛抗体和dnp抗体分别加载在检测垫上的检测区和对照区(或称为质控区)。
[0106]
s300,制备试纸大板:
[0107]
样本垫、结合垫、检测垫、吸水垫依次布置在pvc底板上形成试纸大板;其中,结合垫与检测垫两者部分重合,吸水垫与检测垫两者部分重合。
[0108]
s400,制备层析试纸,将步骤三中制备的试纸大板进行裁切,制备成检测试纸。
[0109]
层析试纸的作用机理为:
[0110]
若有sars-cov-2病毒,其n基因在经过扩增体系后会产生扩增产物;扩增产物首先与样本垫结合,然后经过结合垫,其在经过结合垫时,扩增产物的fitc标签(即fam)与fam抗体-显色颗粒复合物结合。
[0111]
再经过检测垫:经过检测区时,扩增产物的另一端digoxin标签会和检测区上的抗地高辛抗体结合使t线显色(t线显色的要求是:扩增产物的一端与要和fam抗体-显色颗粒复合物连接,另外一端与抗地高辛抗体结合)。
[0112]
经过对照区,溶液在经过结合垫时,必然会混入dnp-显色颗粒复合物,溶液在层析试纸流动的时候,经过对照区时,dnp-显色颗粒复合物会与dnp抗体结合,c线显色。其优点在于c线的显色不受模板浓度的影响,为独立的质控体系,若没采样独立质控体系,当模板浓度较高时,c线会不显色,判定试纸无效。
[0113]
因此,层析试纸会产生如下四种情况:
[0114]
t线显色、c线不显色,表示:无效。
[0115]
t线不显色、c线不显色,表示:无效。
[0116]
t线不显色、c线显色,表示:阴性。
[0117]
t线显色、c线显色,表示:阳性。
[0118]
《验证性试验》
[0119]
制备样本
[0120]
使用申请人自制的核酸提取试剂盒(磁珠法)对新冠n基因假病毒(拷贝数约2
×
108copies/ml)进行核酸提取,提取后n基因核酸分别稀释102、103、104、105、106、107倍后作为阳性模板p1、p2、p3、p4、p5、p6,用以验证引物探针扩增效果。
[0121]
检测体系
[0122]
对新冠n基因核酸进行恒温扩增体系配制,如下表(每组实验均设置1组复孔):
[0123][0124]
检测程序
[0125]
1)将上述配制的体系溶解恒温扩增混合酶冻干微球。
[0126]
2)扩增体系粘稠,配制后需在涡旋仪中涡旋震荡混匀20s后再将体系放置于39-42℃金属浴或其他恒温仪器中,扩增10min。
[0127]
3)待扩增结束后,使用蒸馏水对扩增产物进行稀释,稀释倍数可根据产物浓度控制在10-120倍不等。
[0128]
4)产物稀释后,取80μl稀释产物滴加到研发团队自研的微球法试纸条上,5-10min读取结果。
[0129]
如图2所示,为验证性实验一的测试结果。结果显示:该组引物、探针对n基因核酸
模板的扩增,最低检测限可低于200copies/ml,且未出现非特异性扩增。
[0130]
《层析试纸灵敏度验证》
[0131]
制备样本
[0132]
使用申请人自制的核酸提取试剂盒(磁珠法)对新冠n基因假病毒(拷贝数约2
×
108copies/ml)进行核酸提取,作为阳性模板。
[0133]
检测体系
[0134]
对新冠n基因核酸进行恒温扩增体系配制,如下表(阴性配制4组重复,阳性配制10组重复)。
[0135][0136][0137]
检测程序
[0138]
1)扩增体系粘稠,配制后需在涡旋仪中涡旋震荡混匀20s后再将体系放置于39-42℃金属浴或其他恒温仪器中,扩增10min。
[0139]
2)待扩增结束后,使用蒸馏水对扩增产物进行稀释20倍。
[0140]
3)产物稀释后,取80μl稀释产物滴加到本技术自制的微球法试纸条样品垫上,5-10min读取结果。
[0141]
如图3所示,为验证性实验二的测试结果。结果显示:该组引物、探针对n基因核酸模板的扩增,将200copies/ml的模板重复多次扩增进行检测,均可检出。
[0142]
《特异性扩增试验》
[0143]
模板:
[0144]
1)阴性模板n:dpec-h2o;
[0145]
2)阴性参考品盘模板:
[0146]
编号模板编号模板1阴性拭子样本8冠状病毒oc432乙型流感yamagata9冠状病毒229e3乙型流感victoria10冠状病毒hku14季节性h1n1流感病毒11冠状病毒nl635eb病毒12腺病毒3型
6肺炎支原体13副流感2型7肺炎衣原体14呼吸道合胞病毒
[0147]
3)阳性模板 :n基因假病毒。
[0148]
检测体系
[0149]
检测体系除了模板类型外,其他同“验证性试验”的检测体系。
[0150][0151][0152]
检测程序
[0153]
检测程序同“验证性试验”的检测程序。
[0154]
以上模板使用本技术的引物探针组合物进行恒温扩增;从图4可知显示无非特异性扩增反应。
[0155]
以上所举实施例为本技术的较佳实施方式,仅用来方便说明本技术,并非对本技术作任何形式上的限制,任何所属技术领域中具有通常知识者,若在不脱离本技术所提技术特征的范围内,利用本技术所揭示技术内容所作出局部更动或修饰的等效实施例,并且未脱离本技术的技术特征内容,均仍属于本技术技术特征的范围内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。