pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-oh;
15.其中r2为羧基保护基团。
16.优选的,所述r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2按照以下方法制备:
17.将r
4-pyr-oh与h-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2进行缩合反应,得到r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2。
18.优选的,所述h-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2按照以下方法制备:
19.fmoc-his(r3)-oh与h-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2进行缩合反应后,脱除fmoc保护基,得到h-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2。
20.优选的,所述h-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2按照以下方法制备:
21.将fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh与h-d-leu-leu-or2进行缩合反应后,脱除fmoc保护基,得到h-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2。
22.优选的,所述fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh按照以下方法制备:
23.将fmoc-trp(boc)-ser(tbu)-osu与h-tyr(tbu)-oh进行缩合反应,得到fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh。
24.优选的,所述h-d-leu-leu-or2按照以下方法制备:
25.将r
1-d-leu-oh与h-leu-or2进行缩合反应,脱除r1保护基团,得到h-d-leu-leu-or2;
26.其中r1为氨基保护基团。
27.优选的,所述r1选自fmoc、z或boc;
28.所述r2选自ome或oet;
29.所述r3选自boc、z或trt;
30.所述r4选自fmoc、z或boc。
31.优选的,所述步骤s1)中缩合反应在有机碱与缩合剂存在的条件下进行;所述有机碱选自diea、tea与nmm中的一种或多种;所述缩合剂选自dcc、dic、edc、bop、pybop、aop、tbtu、hbtu与hatu中的一种或多种;
32.所述步骤s1)中缩合反应还在活化剂存在的条件下进行;所述活化剂选自hosu、hobt、hoat与hoobt中的一种或多种;
33.所述步骤s2)中的切割液包括tfa、tis与h2o;所述tfa、tis与h2o的体积比为(94~96):(2~3):(2~3)。
34.本发明提供了一种全液相合成亮丙瑞林的方法,包括:s1)将r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-oh与h-arg(pbf)-pro-nhet进行缩合反应,得到r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-arg(pbf)-pro-nhet;r3与r4为氨基保护基团;s2)将所述r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-arg(pbf)-pro-nhet在切割液中进行反应,得到亮丙瑞林。与现有技术相比,本发明通过全液相合成法,生产工艺绿色、温和,没有使用任何剧毒、易制毒试剂,并且生产的产品纯度高,粗品可达90%以上,成本极大降低,非常适合大规模生产。
附图说明
35.图1为本发明实施例中得到的化合物1的液相色谱图;
36.图2为本发明实施例中得到的化合物2的液相色谱图;
37.图3为本发明实施例中得到的化合物3的液相色谱图;
38.图4为本发明实施例中得到的化合物4的液相色谱图;
39.图5为本发明实施例中得到的化合物5的液相色谱图;
40.图6为本发明实施例中得到的化合物6的液相色谱图;
41.图7为本发明实施例中得到的化合物7的液相色谱图;
42.图8为本发明实施例中得到的化合物8的液相色谱图;
43.图9为本发明实施例中得到的化合物9的液相色谱图;
44.图10为本发明实施例中得到的化合物10的液相色谱图;
45.图11为本发明实施例中得到的化合物11的液相色谱图;
46.图12为本发明实施例中得到的亮丙瑞林粗品的液相色谱图;
47.图13为本发明实施例中得到的亮丙瑞林粗品的质谱图。
具体实施方式
48.下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
49.本发明提供了一种全液相合成亮丙瑞林的方法,包括:
50.s1)将r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-oh与h-arg(pbf)-pro-nhet进行缩合反应,得到r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-arg(pbf)-pro-nhet;r3与r4为氨基保护基团;
51.s2)将所述r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-arg(pbf)-pro-nhet在切割液中进行反应,得到亮丙瑞林。
52.其中,本发明对所有原料的来源并没有特殊的限制,为市售或自制均可。
53.在本发明中,所述h-arg(pbf)-pro-nhet优选按照以下方法制备:将r
5-arg(pbf)-oh与h-pro-nhet
·
hcl进行缩合反应后,脱除r5保护基,得到h-arg(pbf)-pro-nhet;其中r5为氨基保护基团,优选为fmoc、z或boc;所述r
5-arg(pbf)-oh与h-pro-nhet
·
hcl的摩尔比优选为1:(1.05~2),更优选为1:(1.05~1.5);所述缩合反应优选在有机碱与缩合剂存在的条件下进行;所述h-pro-nhet
·
hcl、有机碱与缩合剂的摩尔比优选为1:(1~2.4):(1~1.2),更优选为1:(1~2.1):(1~1.05);进一步还优选在活化剂存在的条件下进行;所述h-pro-nhet
·
hcl与活化剂的摩尔比优选为1:(1~1.2),更优选为1:(1~1.05);所述活化剂为本领域技术人员熟知的多肽合成常用的活化剂即可,并无特殊的限制,本发明中优选为hosu、hobt、hoat与hoobt中的一种或多种;所述有机碱优选为dieatea与nmm中的一种或多种;所述缩合剂为本领域技术人员熟知的多肽合成常用的缩合剂即可,并无特殊的限制,本发明中优选为dcc、dic、edc、bop、pybop、aop、tbtu、hbtu与hatu中的一种或多种;所述缩合反应优选在有机溶剂中进行;所述有机溶剂优选为thf、dcm、dmf、nmp与二氧六环中的一种
d-leu-leu-or2的有机溶剂溶液进行缩合反应;所述缩合反应的时间优选2~3h,更优选为2.5h;缩合反应后,过滤,用酸性溶液沉淀,过滤收集固体洗涤至中性后,得到r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2;所述酸性溶液优选为盐酸溶液;所述酸性溶液的浓度优选为0.3~0.5mol/l。
56.在本发明中,所述h-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2优选按照以下方法制备:fmoc-his(r3)-oh与h-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2进行缩合反应后,脱除fmoc保护基,得到h-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2;所述fmoc-his(r3)-oh与h-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2的摩尔比优选为(1.05~2):1;所述缩合反应优选在活化剂与缩合剂存在的条件下进行;所述fmoc-his(r3)-oh、活化剂与缩合剂的摩尔比优选为1:(1~1.2):(1~1.2):(1~1.2),更优选为1:(1~1.05):(1~1.05):(1~1.05);进一步还优选在有机碱存在的条件下进行;所述fmoc-his(r3)-oh与有机碱的摩尔比优选为1:(1~2),更优选为1:(1~1.05);所述活化剂为本领域技术人员熟知的多肽合成常用的活化剂即可,并无特殊的限制,本发明中优选为hosu、hobt、hoat与hoobt中的一种或多种;所述有机碱优选为dieatea与nmm中的一种或多种;所述缩合剂为本领域技术人员熟知的多肽合成常用的缩合剂即可,并无特殊的限制,本发明中优选为dcc、dic、edc、bop、pybop、aop、tbtu、hbtu与hatu中的一种或多种;所述缩合反应优选在有机溶剂中进行;所述有机溶剂优选为thf、dcm、dmf、nmp与二氧六环中的一种或多种;在本发明中,优选先将fmoc-his(r3)-oh、h-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2与活化剂在有机溶剂中溶解后冷浴,加入缩合剂进行反应,过滤加入乙二胺继续反应;所述冷浴的时间优选为5~15min,更优选为10min;所述反应的时间优选为1.5~3h,更优选为2~2.5h;所述继续反应的时间优选为10~30min,更优选为20min;继续反应后优选加入酸性溶液析出固体,过滤,干燥;所述酸性溶液优选为盐酸溶液;所述酸性溶液的浓度优选为0.3~0.5mol/l;将干燥得到的固体脱除fmoc保护基;所述脱除fmoc保护基的方法为本领域技术人员熟知的方法即可,并无特殊的限制,本发明中优选以二乙胺、哌嗪与哌啶中的一种或多种为脱保护试剂;脱除fmoc保护基后,优选浓缩,加入醚析出固体,过滤,干燥后得到h-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2;所述醚优选为石油醚、异丙醚与乙醚中的一种或多种,更优选为石油醚。
57.在本发明中,所述h-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2优选按照以下方法制备:将fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh与h-d-leu-leu-or2进行缩合反应后,脱除fmoc保护基,得到h-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2;所述fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh与h-d-leu-leu-or2的摩尔比优选为1:(1.05~2);所述缩合反应优选在有机碱与缩合剂存在的条件下进行;所述h-d-leu-leu-or2、有机碱与缩合剂的摩尔比优选为1:(1~1.2):(1~1.2),更优选为1:(1~1.05):(1~1.05);进一步还优选在活化剂存在的条件下进行;所述h-d-leu-leu-or2与活化剂的摩尔比优选为1:(1~1.2),更优选为1:(1~1.05);所述活化剂为本领域技术人员熟知的多肽合成常用的活化剂即可,并无特殊的限制,本发明中优选为hosu、hobt、hoat与hoobt中的一种或多种;所述有机碱优选为dieatea与nmm中的一种或多种;所述缩合剂为本领域技术人员熟知的多肽合成常用的缩合剂即可,并无特殊的限制,本发明中优选为dcc、dic、edc、bop、pybop、aop、tbtu、hbtu与hatu中的一种或多种;所述缩合反应优选在有机溶剂中进行;所述有机溶剂优选为thf、
dcm、dmf、nmp与二氧六环中的一种或多种;在本发明中,优选先将fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh与缩合剂在有机溶剂中溶解后冷浴,加入有机碱,再加入h-d-leu-leu-or2的有机溶剂溶液进行缩合反应;所述冰浴的时间优选为5~15min,更优选为10min;所述缩合反应的时间优选为0.5~2h,更优选为1~1.5h;缩合反应后,优选浓缩,加入酸性溶液沉淀,过滤,干燥;所述酸性溶液优选为盐酸溶液;所述酸性溶液的浓度优选为0.3~0.5mol/l;将干燥后的固体脱除fmoc保护基;所述脱除fmoc保护基的方法为本领域技术人员熟知的方法即可,并无特殊的限制,本发明中优选以二乙胺、哌嗪与哌啶中的一种或多种为脱保护试剂;脱除fmoc保护基后,优选浓缩,加入醚析出固体,过滤,干燥后得到h-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-or2;所述醚优选为石油醚、异丙醚与乙醚中的一种或多种,更优选为石油醚。
58.在本发明中,所述fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh优选按照以下方法制备:将fmoc-trp(boc)-ser(tbu)-osu与h-tyr(tbu)-oh进行缩合反应,得到fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh;所述fmoc-trp(boc)-ser(tbu)-osu与h-tyr(tbu)-oh的摩尔比优选为1:(1.05~2);所述缩合反应优选在有机碱存在的条件进行;所述h-tyr(tbu)-oh与有机碱的摩尔比优选为1:1.2,更优选为1:1.05,再优选为1:1;所述缩合反应优选在有机溶剂中进行;所述有机溶剂选自dmf、thf、甲醇、乙醇与nmp中的一种或多种;在本发明中,此步骤优选先将fmoc-trp(boc)-ser(tbu)-osu溶于有机溶剂后,依次加入h-tyr(tbu)-oh与有机碱进行缩合反应;所述缩合反应的时间优选为40~80min,更优选为50~70min,再优选为60min;缩合反应后,优选加入酸性溶液快速搅拌析出;所述酸性溶液优选为盐酸溶液;所述酸性溶液的浓度优选为0.3~0.6mol/l,更优选为0.5mol/l;然后优选过滤、洗涤至中性,干燥,得到fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh;所述干燥的温度优选为30℃~35℃。
59.在本发明中,所述h-d-leu-leu-or2优选按照以下方法制备:将r
1-d-leu-oh与h-leu-or2进行缩合反应,脱除r1保护基团,得到h-d-leu-leu-or2;其中r1为氨基保护基团,优选为fmoc、z或boc;r
1-d-leu-oh与h-leu-or2的摩尔比优选为1:(1.05~2);所述缩合反应优选在活化剂、有机碱与缩合剂存在的条件下进行;所述h-leu-or2、活化剂、有机碱与缩合剂的摩尔比优选为1:(1~1.2):(1~1.2):(1~1.2),更优选为1:(1~1.05):(1~1.05):(1~1.05);所述活化剂为本领域技术人员熟知的多肽合成常用的活化剂即可,并无特殊的限制,本发明中优选为hosu、hobt、hoat与hoobt中的一种或多种;所述有机碱优选为dieatea与nmm中的一种或多种;所述缩合剂为本领域技术人员熟知的多肽合成常用的缩合剂即可,并无特殊的限制,本发明中优选为dcc、dic、edc、bop、pybop、aop、tbtu、hbtu与hatu中的一种或多种;所述缩合反应优选在有机溶剂中进行;所述有机溶剂优选为thf、dcm、dmf、nmp与二氧六环中的一种或多种;在本发明中,此步骤优选具体为:将r
1-d-leu-oh与活化剂溶于有机溶剂,得到第一溶液;将h-leu-or2溶于有机溶剂后冷浴,加入有机碱,得到第二溶液;将第一溶液与第二溶液混合后继续冷浴,再加入缩合剂进行反应;所述冷浴的时间优选为5~15min,更优选为10min;所述继续冷浴的时间优选为5~10min;所述缩合反应的时间优选为1~2h,更优选为1.5h;缩合反应后,优选过滤,在滤液中加入酸性溶液析出固体,过滤、水洗至中性,干燥;所述酸性溶液优选为盐酸溶液;所述酸性溶液的浓度优选为0.3~0.6mol/l,更优选为0.5mol/l;将干燥后的固体脱除r1保护基团;所述脱除r1保护基的方法为本领域技术人员熟知的方法即可,并无特殊的限制,在本发明中脱除r1保护基所用的试剂优选为
三氟乙酸(tfa)、氯化氢溶液、二乙胺、哌嗪与哌啶中的一种或多种;可根据r1的种类进行选择,当r1为fmoc时,优选以二乙胺为脱保护试剂;当r1为boc时,优选以tfa为脱保护试剂;当r1为z时,可通过接触还原法进行脱保护;脱除r1保护基团可在有机溶剂中进行;所述有机溶剂优选为dmf、甲醇、乙醇、dcm与thf中的一种或多种;脱除r1保护基后,优选浓缩,加入醚析出固体,过滤,干燥后得到h-d-leu-leu-or2;所述醚优选为石油醚、异丙醚与乙醚中的一种或多种,更优选为石油醚。
60.将r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-oh与h-arg(pbf)-pro-nhet进行缩合反应;所述r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-oh与h-arg(pbf)-pro-nhet的摩尔比优选为1:(1.05~2);所述缩合反应优选在有机碱与缩合剂存在的条件下进行;所述h-arg(pbf)-pro-nhet、有机碱与缩合剂的摩尔比优选为1:(1~1.2):(1~1.2):(1~1.2),更优选为1:(1~1.05):(1~1.05):(1~1.05);进一步优选在活化剂存在的条件下进行;所述h-arg(pbf)-pro-nhet与活化剂的摩尔比优选为1:(1~1.2),更优选为1:(1~1.05);所述活化剂为本领域技术人员熟知的多肽合成常用的活化剂即可,并无特殊的限制,本发明中优选为hosu、hobt、hoat与hoobt中的一种或多种;所述有机碱优选为dieatea与nmm中的一种或多种;所述缩合剂为本领域技术人员熟知的多肽合成常用的缩合剂即可,并无特殊的限制,本发明中优选为dcc、dic、edc、bop、pybop、aop、tbtu、hbtu与hatu中的一种或多种;所述缩合反应优选在有机溶剂中进行;所述有机溶剂优选为thf、dcm、dmf、nmp与二氧六环中的一种或多种;在本发明中,此步骤优选具体为:先将r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-oh与缩合剂在有机溶剂中溶解后,冷浴,加入有机碱,再加入h-arg(pbf)-pro-nhet的有机溶剂溶液进行缩合反应;所述冷浴的时间优选为5~15min,更优选为10min;所述缩合反应的时间优选为0.5~2h,更优选为1~1.5h;缩合反应后,优选加入酸性溶液析出固体,过滤、洗涤至中性后,干燥得到r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-arg(pbf)-pro-nhet;所述酸性溶液优选为盐酸溶液;所述酸性溶液的浓度优选为0.3~0.6mol/l,更优选为0.5mol/l。
61.将所述r
4-pyr-his(r3)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-arg(pbf)-pro-nhet在切割液中进行反应;所述切割液优选包括tfa、tis与h2o;所述tfa、tis与h2o的体积比优选为(94~96):(2~3):(2~3),更优选为95:2.5:2.5;所述反应的时间优选为20~40min,更优选为25~35min,再优选为30min;反应后,优选用冷冻乙醚沉淀、过滤,得到亮丙瑞林。
62.本发明通过全液相合成法,生产工艺绿色、温和,没有使用任何剧毒、易制毒试剂,并且生产的产品纯度高,粗品可达90%以上,成本极大降低,非常适合大规模生产。
63.为了进一步说明本发明,以下结合实施例对本发明提供的一种全液相合成亮丙瑞林的方法进行详细描述。
64.以下实施例中所用的试剂均为市售;在本发明中如无特殊说明,所述冷浴均为冰浴。
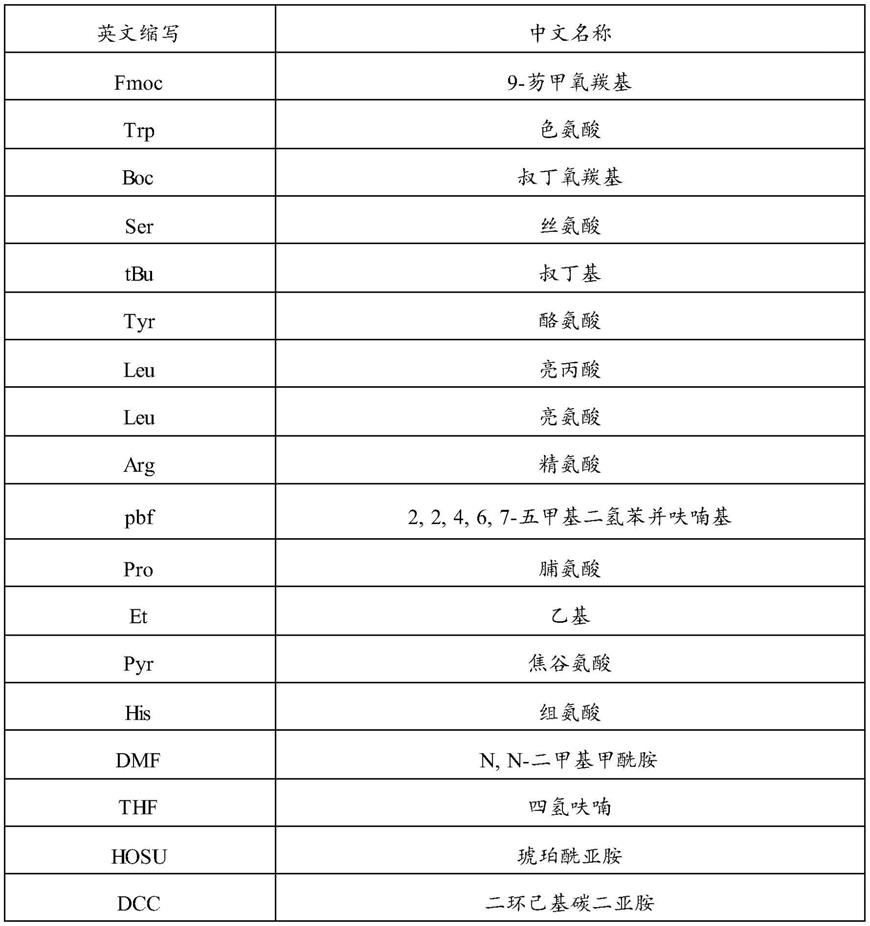
65.本发明权利要求书和说明书中出现物质的英文缩写对应的中文名称见表1。
66.表1中英文对照表
67.[0068][0069]
实施例1
[0070]
1、合成化合物1:fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh
[0071]
1.1投料:
[0072]
按照表2的物料进行投料。
[0073]
表2物料种类及用量
[0074]
[0075][0076]
1.2操作过程
[0077]
将合成fmoc-trp(boc)-ser(tbu)-osu用dmf完全溶解后,再准确称取h-tyr(tbu)-oh加入上述反应瓶,加tea 110mmol开始反应。搅拌反应60min后,hplc检测反应完全。
[0078]
将反应液分两次倒入三角瓶中,再加入0.5m盐酸快速搅拌析出,过滤的固体,然后用纯化水洗至中性,30℃干燥。收集固体装至容器中,称重。
[0079]
利用hplc对得到的化合物1进行分析,得到液相色谱图如图1所示。
[0080]
化合物1的分析方法为:
[0081]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0082]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0083]
梯度:0~30min,70%b~90%b;
[0084]
收率:96.2%;纯度:87.6%。
[0085]
2、合成化合物2:fmoc-d-leu-leu-ome.hcl
[0086]
2.1投料
[0087]
按照表3的物料进行投料。
[0088]
表3物料种类及用量
[0089]
缩写用量fmoc-d-leu-oh150mmolhosu165mmoltea165mmoldcc165mmolh-leu-ome.hcl165mmoldmf500ml0.5m盐酸溶液1l
[0090]
2.2操作过程:
[0091]
准确称取fmoc-d-leu-oh、hosu于反应瓶中,用dmf完全溶解后,再称取h-leu-ome.hcl于三角瓶中,用dmf完全溶解后冷浴10min,加入tea,快速摇匀,加入上述反应瓶中,继续冷浴5min后加入dcc开始反应。
[0092]
反应1.5h后hplc检测反应完全。
[0093]
待完全反应后过滤反应液,用0.5m盐酸水溶液析出,过滤的固体,然后用纯化水洗至中性,30℃干燥。收集固体装至三角瓶中,称重。
[0094]
利用hplc对得到的化合物2进行分析,得到液相色谱图如图2所示。
[0095]
化合物2的分析方法为:
[0096]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0097]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0098]
梯度:0~30min,50%b~90%b;
[0099]
收率:108.1%,纯度:93.4%。
[0100]
3、合成化合物3:h-d-leu-leu-ome
[0101]
3.1按照表4投料。
[0102]
表4物料用量及种类
[0103]
缩写用量fmoc-d-leu-leu-ome.hcl150mmol二乙胺400ml石油醚1l
[0104]
3.2操作过程
[0105]
准确称取fmoc-d-leu-leu-ome.hcl于反应瓶中,加入二乙胺反应20min,浓缩至少量,加入石油醚析出固体,过滤,真空干燥,得到化合物3。
[0106]
利用hplc对得到的化合物3进行分析,得到液相色谱图如图3所示。
[0107]
化合物3的分析方法为:
[0108]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0109]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0110]
梯度:0~30min,3%b~10%b;
[0111]
收率:82.4%,纯度:87.2%。
[0112]
4、合成化合物4:fmoc-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome
[0113]
4.1投料:
[0114]
表5物料用量及种类
[0115]
缩写用量fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh96.2mmolbop105.8mmoldiea105.8mmolh-d-leu-leu-ome105.8mmoldmf200mldcm200ml0.5m盐酸溶液1l
[0116]
4.2操作过程
[0117]
准确称取fmoc-trp(boc)-ser(tbu)-tyr(tbu)-oh、bop于反应瓶中,用dmf完全溶解后冷浴10min后加入diea,再将h-d-leu-leu-ome用dcm溶解后加入反应中开始反应。反应1.0h后hplc检测反应完全,浓缩,用0.5m盐酸沉淀,过滤收集固体,然后用纯化水洗至中性(ph试纸检测),称重,得到化合物4。
[0118]
利用hplc对得到的化合物4进行分析,得到液相色谱图如图4所示。
[0119]
化合物4的分析方法为:
[0120]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0121]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0122]
梯度:0~30min,70%b~90%b;
[0123]
收率:94.1%,纯度:88.6%。
[0124]
5、合成化合物5:h-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome
[0125]
5.1投料
[0126]
按照表6的物料投料。
[0127]
表6物料用量及种类
[0128]
缩写用量fmoc-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome90.5mmol二乙胺500ml石油醚1l
[0129]
5.2操作过程
[0130]
准确称取fmoc-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome于反应瓶中,加入二乙胺反应20min,浓缩至少量,加入石油醚析出固体,过滤,真空干燥。
[0131]
利用hplc对得到的化合物5进行分析,得到液相色谱图如图5所示。
[0132]
化合物5的分析方法为:
[0133]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0134]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0135]
梯度:0~30min,50%b~95%b;
[0136]
收率:93%,纯度:89%。
[0137]
6、合成化合物6:h-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome
[0138]
6.1投料
[0139]
按照表7的物料进行投料。
[0140]
表7物料用量及种类
[0141]
缩写用量fmoc-his(trt)-oh92.5mmolhobt92.5mmoldcc92.5mmolh-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome84.1mmol二乙胺500mldmf400ml0.5m盐酸溶液1l
[0142]
6.2操作过程
[0143]
准确称取fmoc-his(trt)-oh、hobt、h-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome于反应瓶中,用dmf完全溶解后冷浴10min后加入dcc开始反应。
[0144]
反应2h后hplc检测反应完全,过滤反应液,倒入反应瓶中,再加入二乙胺反应20min,浓缩至少量,加入0.5m盐酸溶液析出固体,过滤,烘干。
[0145]
取fmoc-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome于反应瓶中,加入二乙胺反应20min,浓缩至少量,加入石油醚析出固体,过滤,烘干,得到化合物6。收率:82.5%,纯度:88%。
[0146]
利用hplc对得到的化合物6进行分析,得到液相色谱图如图6所示。
[0147]
化合物6的分析方法为:
[0148]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0149]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0150]
梯度:0~30min,70%b~90%b。
[0151]
7.合成化合物7:boc-pyr-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome
[0152]
7.1投料
[0153]
按照表8的物料进行投料。
[0154]
表8物料用量及种类
[0155]
缩写用量boc-pyr-oh76.3mmolbop76.3mmoldiea76.3mmolh-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome69.4mmoldmf350ml0.5m盐酸溶液1l
[0156]
7.2操作过程
[0157]
准确称取boc-pyr-oh、bop于反应瓶中,用dmf完全溶解后加入diea,再将h-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome用dmf溶解后加入反应中开始反应。
[0158]
反应2.5h后hplc检测反应完全,过滤反应液,滤渣用dmf洗涤两次,用0.5m盐酸沉淀,过滤后收集固体,然后用纯化水洗至中性(ph试纸检测),干燥,称重;收率:80%,纯度:85.1%。
[0159]
利用hplc对得到的化合物7进行分析,得到液相色谱图如图7所示。
[0160]
检测方法:
[0161]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0162]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0163]
梯度:0~30min,80%b~95%b。
[0164]
8、合成化合物8:boc-pyr-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-oh
[0165]
8.1投料
[0166]
boc-pyr-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome 55.5mmol;
[0167]
甲醇:1110ml;
[0168]
2m naoh:110ml;
[0169]
0.1m盐酸溶液:2l。
[0170]
8.2操作过程
[0171]
称取boc-pyr-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-ome,置于甲醇中搅拌5min完全溶解后,取2m naoh缓慢加入反应,开始反应。反应3h后hplc检测反应完
全,加入盐酸溶液,沉淀,过滤后收集固体,然后用纯化水洗至中性(ph试纸检测),干燥,称重,得到化合物8;收率:83%,纯度:84%。
[0172]
利用hplc对得到的化合物8进行分析,得到液相色谱图如图8所示。
[0173]
检测方法:
[0174]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0175]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0176]
梯度:0~30min,70%b~90%b。
[0177]
9、合成化合物9:fmoc-arg(pbf)-pro-nhet
[0178]
9.1投料
[0179]
表9物料用量及种类
[0180][0181][0182]
9.2操作过程
[0183]
准确称取fmoc-arg(pbf)-oh、bop于反应瓶中,用dmf完全溶解后,加入diea,撤掉冷浴,反应20min。
[0184]
称取h-pro-nhet.hcl于三角瓶中,用dmf完全溶解后加入tea,快速混匀后加入上反应中开始反应。
[0185]
反应2h后hplc检测反应完全,用0.5m盐酸沉淀,过滤后收集固体,然后用纯化水洗至中性(ph试纸检测),干燥,称重,得到化合物9;收率108.2%,纯度:98%。
[0186]
利用hplc对得到的化合物9进行分析,得到液相色谱图如图9所示。
[0187]
检测方法:
[0188]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0189]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0190]
梯度:0~30min,50%b~90%b。
[0191]
10、合成化合物10:h-arg(pbf)-pro-nhet
[0192]
10.1投料
[0193]
fmoc-arg(pbf)-pro-nhet.hcl:150mmol;
[0194]
二乙胺:500ml。
[0195]
10.2操作过程
[0196]
准确称取fmoc-arg(pbf)-pro-nhet.hcl于反应瓶中,加入二乙胺反应20min,浓缩至少量,加入石油醚析出固体,过滤,真空干燥,得到化合物10。收率94%,纯度95.6%。
[0197]
利用hplc对得到的化合物10进行分析,得到液相色谱图如图10所示。检测方法:
[0198]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0199]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0200]
梯度:0~30min,20%b~50%b。
[0201]
11合成化合物11:boc-pyr-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-arg(pbf)-pro-nhet
[0202]
11.1投料
[0203]
表10物料用量及种类
[0204]
缩写用量boc-pyr-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-oh46.1mmolbop50.7mmoldiea50.7mmolh-arg(pbf)-pro-nhet50.7mmoldmf200ml0.5m盐酸溶液500ml
[0205]
11.2操作过程
[0206]
准确称取boc-pyr-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-oh、bop于反应瓶中,用dmf完全溶解后冷浴10min后加入diea,再将h-arg(pbf)-pro-nhet用dmf溶解后加入反应中开始反应。
[0207]
反应1.0h后hplc检测反应完全,加入0.5m盐酸析出固体,过滤收集固体,然后用纯化水洗至中性(ph试纸检测),干燥,称重,得到化合物11。收率104.2%,纯度:80.5%。
[0208]
利用hplc对得到的化合物11进行分析,得到液相色谱图如图11所示。检测方法:
[0209]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0210]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0211]
梯度:0~30min,70%b~90%b。
[0212]
12、合成亮丙瑞林粗品
[0213]
12.1投料
[0214]
boc-pyr-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-arg(pbf)-pro-nhet:46.1mmol;
[0215]
切割液(tfa:tis:h2o=95:2.5:2.5):300ml。
[0216]
12.2操作过程
[0217]
将boc-pyr-his(trt)-trp(boc)-ser(tbu)-tyr(tbu)-d-leu-leu-arg(pbf)-pro-nhet加入反应瓶中,加入切割液反应30min后用冷冻乙醚沉淀,过滤,收集固体,得到产物粗品,产物用水溶解后hplc检测分析。
[0218]
收率:85.8%,纯度91.2%。
[0219]
利用hplc对得到的粗品进行分析,得到液相色谱图如图12所示。检测方法:
[0220]
流动相a:0.1%tfa/水,流动相b:0.1%tfa/乙腈;
[0221]
检测波长:210nm;流速:1ml/min;固定相:c18色谱柱,5μ,
[0222]
梯度:0~30min,10%b~90%b。
[0223]
利用hplc-ms对得到的粗品进行分析,得到质谱如图13所示。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。