一种基于Au@Ag核壳纳米粒子负载硅纳米线阵列及其制备方法和用途与流程
- 国知局
- 2024-07-27 12:22:07
本发明属于环境生物监测技术领域,具体涉及一种基于au@ag核壳纳米粒子负载硅纳米线阵列及其制备方法和用途。
背景技术:
水源性致病菌及相关疾病已成为公共卫生和人类健康的主要威胁之一,消除及检测水源性致病菌是改善水质和评估微生物污染的关键。随着纳米科技的快速发展,具有特殊形貌和优异表面性能的纳米材料被广泛用于生物技术和生物医学等领域,借助于纳米材料人们已开发出了一些能够选择性去除或捕获细菌的方法,这些方法大多使用抗生素或抗体为作为特异性识别元件对纳米材料进行修饰(参见analyticachimicaacta2017,987,91-97;acsappliedmaterials&interfaces2013,5(21),10874-10881;acsnano2008,2(9),1777-1788;analyticalchemistry1993,65(15),2036-2039),不仅修饰过程复杂成本高,而且可能出现抗生素耐受性增加的风险。因此,细菌的消除或捕获方法仍有改进的余地。
近年来,垂直排列的硅纳米线阵列(sinws)由于其特殊形态及物理化学性质而成为众多研究领域的热点,研究发现细菌不仅可以识别sinws基底的硅纳米线(参见nanoletters2013,13(6),2864-2869),而且sinws基底的纳米级形貌还可以促进硅纳米线与细菌胞外细胞器间的相互作用(参见angewandtechemieinternationaledition2014,53(23),5837-5841)。此外,研究表明sinws基底的硅纳米线直径与一些生物分子尺寸相当,因此可以增强sinws与这些生物分子间的界面作用而提高检测灵敏度(参见analyticalchemistry2007,79(9),3291-3297)。然而,想要获得优异的捕获效率实现低浓度细菌的消除或捕获,sinws基底仍然需要经生物配体或连接分子的修饰,这些繁琐的化学修饰及生物配体的不稳定性限制了sinws的实际使用。
关于细菌粘附在纳米结构表面的研究已经证明,在某些情况下机械因素对细菌粘附的影响比化学作用更大(参见biomaterials2015,73,185-197),而且最近关于纳米粒子修饰多孔电极用于细菌捕获及检测的研究表明,次级纳米结构的多维物理作用可以实现细菌的有效捕获而无需任何生物配体或连接分子(参见biosensorsandbioelectronics2018,101,52-59)。基于此,sinws基底或许可以采用纳米粒子进行简单的修饰后用于细菌捕获。au@ag核壳纳米粒子(au@agnps)具有金纳米均一稳定的特征,同时又具有银纳米优异的光学性质和抗菌活性等特点,在众多领域都引起了广泛的兴趣。目前还没有关于采用au@ag核壳纳米粒子对sinws基底进行修饰以实现水中细菌捕获的相关报道。
尽管传统的检测方法(如平板菌落计数,pcr,elisa等)能够有效的检测细菌,但是耗时的培养过程,繁琐的前处理,以及昂贵的试剂限制了这些方法的广泛使用。激光诱导击穿光谱(laserinducedbreakdownspectroscopy,简称libs)与表面增强拉曼光谱(surface-enhancedramanscattering,简称sers)由于能够实现快速高灵敏度检测而成为化学和生物材料鉴定和检测的有力工具。这两种技术可以分别提供目标物的原子和分子信息,同时sers在定量分析方面的不足还可以通过libs进行弥补,因此libs和sers的联用为开发细菌检测新策略创造了机会(参见analyticachimicaacta,doi:https://doi.org/10.1016/j.aca.2018.06.058)。libs可以直接获取细菌细胞的元素信息而实现定量分析,根据细菌细胞内含有的矿物元素的libs光谱与细菌浓度建立定量关系,从而实现快速定量分析。而基于sers检测细菌则可以分为以下两种,一是借助纳米粒子的热点效应直接获取细菌的指纹光谱,二是通过sers标签(tag)标记后间接检测细菌。采用拉曼信号强的sers标签与目标细菌特异性结合后进行细菌检测,可以避免干扰实现高灵敏度检测。而这种sers标签一般是贵金属纳米粒子表面修饰提供sers信号的报告分子,再修饰与细菌特异性结合的连接分子,通过sers标签可以实现细菌的高灵敏度检测。而目前关于libs与标记sers联用建立细菌检测的方法报道较少。
技术实现要素:
本发明的目的是基于au@ag核壳纳米粒子负载sinws(sinws-au@ag)的制备方法,以及一种适配体修饰的金银双金属sers标签(apt-serstag)的制备方法,并且利用这两种材料以及libs和sers检测技术实现水中细菌的高效捕获及快速检测。
为实现上述目的,本发明通过种子生长法制备单分散的au@ag核壳纳米粒子,并负载到氨基化的sinws表面制备sinws-au@ag基底。sinws-au@ag基底捕获细菌后,可以通过libs进行快速定量检测,或者与apt-serstag结合后通过sers进行特异性识别。
本发明中一种硅纳米线阵列,其为负载au@ag核壳纳米粒子的硅纳米线阵列。
au@ag核壳纳米粒子:以纳米金为核,在其表面包覆一层纳米银为壳,所构成的具有核壳结构的纳米粒子。
硅纳米线阵列:直径长度均匀的硅纳米线在硅衬底上取向一致,排列整齐的阵列结构。
进一步的,所述硅纳米线阵列的纳米线直径200~400nm,间距200~600nm。
进一步的,所述au@ag核壳纳米粒子粒径为25~35nm。
进一步的,所述硅纳米线阵列采用金属辅助化学刻蚀法制备,优选地,按照如下方法制备:
a.将硅片用丙酮、水进行超声清洗,放入浓硫酸与双氧水的混合溶液中进一步清洗,最后用超纯水清洗得到干净的硅片;
优选地,所述硅片为单面抛光方形硅片,大小为0.8cm*0.8cm,p/n型,电阻率为0.01~0.02ω.cm;所述双氧水浓度为30%,浓硫酸与双氧水体积比为3:1;
b.将步骤a清洗干净的硅片注入氢氟酸水溶液中浸泡1~5分钟,在硅片表面形成硅-氢键(si-h);
优选地,所述氢氟酸水溶液浓度为1~10%;
c.将步骤b处理的硅片浸泡至含硝酸银和氢氟酸混合溶液中反应1~5分钟,使硅片表面沉积一层银纳米粒子,然后用超纯水洗去硅片表面残留的银离子;
其中,所述硝酸银与氢氟酸混合溶液中硝酸银浓度为1~10mm,氢氟酸浓度为1~20%;
d.将步骤c表面沉积银纳米粒子的硅片浸入氢氟酸与双氧水混合液中,于室温下避光刻蚀0.5~5h,再将刻蚀后的硅片浸泡至稀硝酸中使银纳米粒子溶解,然后用超纯水洗涤得到硅纳米线阵列;
其中,所述氢氟酸与双氧水混合液中氢氟酸浓度为1~20%,双氧水浓度为0.1~0.9%;所述稀硝酸浓度为5~50%。
金属辅助化学刻蚀,硅片覆盖贵金属膜或纳米粒子后在由hf和氧化剂(一般为双氧水)混合液中刻蚀。
进一步的,所述au@ag核壳纳米粒子按照如下方法制备:
a.取粒径为15~25nm的金纳米种子;优选地,所述金纳米种子采用柠檬酸三钠还原氯金酸制备;其中,所述柠檬酸三钠浓度为0.1~2%;所述氯金酸浓度为0.1~1mm;
b.向步骤a的金纳米种子中加入硝酸银,混匀后加入抗坏血酸和氨水,在碱性条件下,抗坏血酸将硝酸银还原,在金纳米种子表面生成银纳米壳,即得au@ag核壳纳米粒子;
其中,所述硝酸银浓度为0.1~1mm;所述抗坏血酸浓度为0.1~1mm;所述氨水浓度为0.1~1%。
进一步的,所述硅纳米线阵列,其特征在于:它按照如下方法制备
①将硅纳米线阵列氨基化,优选地:将硅纳米线阵列置于浓硫酸与双氧水的混合溶液中,加热至90℃反应25~40分钟,使硅纳米线阵列表面羟基化,经超纯水和无水乙醇洗涤,氮气吹干后置入含3-氨基丙基三甲氧基硅烷的乙醇和乙酸混合液中,反应0.5~3小时得到表面氨基化的硅纳米线阵列;
其中,所述乙醇和乙酸混合液中乙醇和乙酸的体积比为5:2;所述3-氨基丙基三甲氧基硅烷的浓度为0.1~2%;
②将表面氨基化的硅纳米线阵列置于au@ag核壳纳米粒子溶液中,浸泡,优选地:将氨基化的硅纳米线阵列置于置于au@ag核壳纳米粒子溶液中浸泡12小时,使au@agnps通过ag-n键结合至硅纳米线阵列,用超纯水洗涤除去未结合的au@agnps即得到负载au@ag核壳纳米粒子的硅纳米线阵列。
进一步的,本发明硅纳米线阵列的制备方法步骤如下:
①将硅纳米线阵列氨基化,优选地:将硅纳米线阵列置于浓硫酸与双氧水的混合溶液中,加热至90℃反应25~40分钟,使硅纳米线阵列表面羟基化,经超纯水和无水乙醇洗涤,氮气吹干后置入含3-氨基丙基三甲氧基硅烷的乙醇和乙酸混合液中,反应0.5~3小时得到表面氨基化的硅纳米线阵列
其中,所述乙醇和乙酸混合液中乙醇和乙酸的体积比为5:2;所述3-氨基丙基三甲氧基硅烷的浓度为0.1~2%;
②将表面氨基化的硅纳米线阵列置于au@ag核壳纳米粒子溶液中,浸泡,优选地:将氨基化的硅纳米线阵列置于置于au@ag核壳纳米粒子溶液中浸泡12小时,使au@agnps通过ag-n键结合至硅纳米线阵列,用超纯水洗涤除去未结合的au@agnps即得到负载au@ag核壳纳米粒子的硅纳米线阵列。
进一步的,所述硅纳米线阵列作为基底在细菌检测中的应用。
本发明一种细菌的检测方法,是本发明负载au@ag核壳纳米粒子的硅纳米线阵列作为基底,采用libs进行检测,它包括如下步骤:
将负载au@ag核壳纳米粒子的硅纳米线阵列基底置入待检溶液中,于37℃振荡孵育后取出硅纳米线阵基底,并用超纯水淋洗除去未结合牢固的细菌,自然干燥后进行libs检测;
其中,所述待测液的细菌浓度为1×10~1×106cfu/ml;所述超纯水淋洗次数为2~5次。
本发明一种细菌的检测方法,是本发明负载au@ag核壳纳米粒子的硅纳米线阵列作为基底,利用apt-serstag进行sers检测,它包括如下步骤:
将载au@ag核壳纳米粒子的硅纳米线阵列基底置入待检溶液中,于37℃振荡孵育后取出硅纳米线阵基底基底,并用超纯水淋洗除去未结合牢固的细菌,然后将基底置入适配体修饰的金银双金属sers标签(apt-serstag)中,于37℃振荡孵育3小时后,取出基底并用超纯水淋洗为结合牢固的apt-serstag,待自然干燥后进行sers检测;
其中,所述待测液的细菌浓度为1×103~1×106cfu/ml;所述超纯水淋洗次数为2~5次。
进一步的,所述apt-serstag的制备方法包括如下步骤:
ⅰ.向粒径为15~25nm的金纳米种子溶液中加入罗丹明6g溶液,室温下搅拌2小时得到r6g包覆的金纳米粒子(au-r6g);优选地,所述金纳米种子采用柠檬酸三钠还原氯金酸制备;其中,所述柠檬酸三钠浓度为0.1~2%;所述氯金酸浓度为0.1~1mm;
其中,所述罗丹明6g的浓度为10-6~10-4m;
ⅱ.将步骤ⅰ制备的r6g包覆的金纳米粒子离心,洗去多余的r6g并重悬于超纯水中,然后加入硝酸银溶液,混匀后加入抗坏血酸溶液和氨水,涡旋20秒即得到双金属serstag;
其中,所述硝酸银溶液浓度为0.1~1mm;所述抗坏血酸溶液浓度为0.1~1mm;所述氨水浓度为0.1~1%;所述双金属serstag的粒径为20~40nm;
ⅲ.向步骤ⅱ制备的serstag中加入适配体,搅拌反应2小时,然后离心洗去未结合的适配体并重悬于超纯水中得到适配体修饰的serstag(apt-serstag);
其中,所述适配体5’端为巯基修;所述适配体浓度为0.1~2μm。
本发明提供如下具体方案:
本发明第一方面提供一种sinws-au@ag基底的制备方法,具体步骤如下:
(1)采用柠檬酸三钠还原氯金酸制备金纳米种子(auseeds)。
优选的,所述柠檬酸三钠浓度为0.1~2%。
优选的,所述氯金酸浓度为0.1~1mm。
优选的,所述金纳米种子(auseeds)粒径为15-25纳米。
(2)通过种子生长法制备au@ag核壳纳米粒子:向步骤(1)制备的金纳米种子中加入硝酸银,混匀后加入抗坏血酸(aa)和氨水,在碱性条件下抗坏血酸将硝酸银还原,在金纳米种子表面生成银纳米壳。
优选的,所述硝酸银浓度为0.1~1mm。
优选的,所述抗坏血酸浓度为0.1~1mm。
优选的,所述氨水浓度为0.1~1%。
优选的,所述au@ag核壳纳米粒子粒径为25~35nm。
(3)将硅片一次用丙酮、超纯水进行超声清洗,放入浓硫酸与双氧水的混合溶液中进一步清洗,最后用超纯水清洗得到干净的硅片。
优选的,所述硅片为单面抛光方形硅片,大小为0.8cm*0.8cm,p/n型,电阻率为0.01~0.02ω.cm。
优选的,所述双氧水浓度为30%,浓硫酸与双氧水体积比为3:1。
(4)将步骤(3)清洗干净的硅片注入氢氟酸水溶液中浸泡3分钟,在硅片表面形成硅-氢键(si-h)。
优选的,氢氟酸水溶液浓度为1~10%。
(5)将步骤(4)处理的硅片浸泡至含硝酸银和氢氟酸混合溶液中反应1分钟,使硅片表面沉积一层银纳米粒子,然后用超纯水洗去硅片表面残留的银离子。
优选的,所述硝酸银与氢氟酸混合溶液中硝酸银浓度为1~10mm,氢氟酸浓度为1~20%。
(6)将步骤(5)表面沉积银纳米粒子的硅片浸入氢氟酸与双氧水混合液中,于室温下避光刻蚀1h,再将刻蚀后的硅片浸泡至稀硝酸中使银纳米粒子溶解,然后用超纯水洗涤得到sinws。
优选的,所述氢氟酸与双氧水混合液中氢氟酸浓度为1~20%,双氧水浓度为0.1~0.9%。
优选的,所述稀硝酸浓度为5~50%。
优选的,所述sinws基底硅纳米线的直径200~400nm,间距200~600nm,长度为3~6μm。
(7)将步骤(6)制备的sinws置入浓硫酸与双氧水的混合溶液中,加热至90℃反应30分钟使其表面羟基化,经超纯水和无水乙醇洗涤,氮气吹干后置入含3-氨基丙基三甲氧基硅烷(aptms)的乙醇和乙酸混合液中,反应1小时得到表面氨基化的sinws(sinws-nh2)。
优选的,所述乙醇和乙酸混合液中乙醇和乙酸的体积比为5:2。
优选的,所述3-氨基丙基三甲氧基硅烷的浓度为0.1~2%。
(8)将步骤(7)制备的sinws-nh2置入步骤(2)制备的au@ag核壳纳米粒子溶胶中浸泡12小时,使au@agnps通过ag-n键结合至sinws,用超纯水洗涤除去未结合的au@agnps即得到sinws-au@ag。
本发明第二方面提供一种适配体修饰的金银双金属sers标签(apt-serstag)的制备方法,具体步骤如下:
(9)向上述步骤(1)制备的金纳米种子(auseeds)溶液中加入罗丹明6g溶液,室温下搅拌2小时得到r6g包覆的金纳米粒子(au-r6g)。
优选的,所述罗丹明6g的浓度为10-6~10-4m。
(10)将步骤(9)制备的r6g包覆的金纳米粒子离心,洗去多余的r6g并重悬于超纯水中,然后加入硝酸银溶液,混匀后加入抗坏血酸溶液和氨水,涡旋20秒即得到双金属serstag。
优选的,所述硝酸银溶液浓度为0.1~1mm。
优选的,所述抗坏血酸溶液浓度为0.1~1mm。
优选的,所述氨水浓度为0.1~1%。
优选的,所述双金属serstag的粒径为20~40nm。
(11)向步骤(10)制备的serstag中加入适配体,缓慢搅拌反应2小时,然后离心洗去未结合的适配体并重悬于超纯水中得到适配体修饰的serstag(apt-serstag)。
优选的,所述适配体5’端为巯基修饰。
优选的,所述适配体浓度为0.1~2μm。
本发明第三方面提供一种基于sinws-au@ag捕获并通过libs检测饮用水中细菌的方法,具体步骤如下:
(12)将步骤(8)制备的sinws-au@ag基底置入细菌溶液中,于37℃振荡孵育,并通过平板计数测定sinws-au@ag基底加入前后菌液中细菌浓度的变化,并计算捕获效率。
优选的,所述菌液的细菌浓度为4~6×106cfu/ml。
优选的,所述孵育时间为10~90分钟。
优选的,所述捕获效率计算公式为
(13)将步骤(8)制备的sinws-au@ag基底置入添加细菌的饮用水中,于37℃振荡孵育后取出sinws-au@ag基底,并用超纯水淋洗除去未结合牢固的细菌,自然干燥后进行libs检测。
优选的,所述待测液的细菌浓度为1×10~1×106cfu/ml。
优选的,所述超纯水淋洗次数为2~5次。
本发明第四方面提供一种基于sinws-au@ag捕获细菌并利用apt-serstag进行sers检测的方法,具体步骤如下:
(14)将步骤(8)制备的sinws-au@ag基底置入添加细菌的饮用水中,于37℃振荡孵育后取出sinws-au@ag基底,并用超纯水淋洗除去未结合牢固的细菌,然后将基底置入步骤(11)制备的apt-serstag中,于37℃振荡孵育3小时后,取出基底并用超纯水淋洗为结合牢固的apt-serstag,待自然干燥后进行sers检测。
优选的,所述待测液0的浓度为1×103~1×106cfu/ml。
优选的,所述超纯水淋洗次数为2~5次。
本发明第五方面提供一种基于sinws-au@ag杀灭细菌的方法,具体操作如下:
(15)在tsb培养液中接种适量细菌后,加入步骤(8)制备的sinws-au@ag基底,在37℃恒温振荡器中培养12小时,通过测定菌液的od600或平板菌落计数考察基底的抗菌效率。
优选的,所述tsb培养液接入细菌后细菌浓度为1×106cfu/ml。
优选的,所述捕获效率计算公式为:
本发明优点在于:
(1)所制备的sinws-au@ag基底无需复杂的化学修饰即可实现细菌的高效捕获,其对大肠杆菌和金黄色葡萄球菌的捕获容量分别为8.6和5.5×106cells/cm2。
(2)结合sinws-au@ag捕获及libs检测,可实现饮用水中细菌快速定量检测,检测限可低至10cfu/ml。
(3)通过apt-serstag与sinws-au@ag基底捕获的目标细菌间的特异性结合,利用sers特征信号可以特异性识别鼠伤寒沙门氏杆菌。
(4)基于基底硅纳米线间的物理作用和au@ag的抗菌作用,所制备的sinws-au@ag基底对大肠杆菌和金黄色葡萄球菌的抗菌率分别为90%和~100%。
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
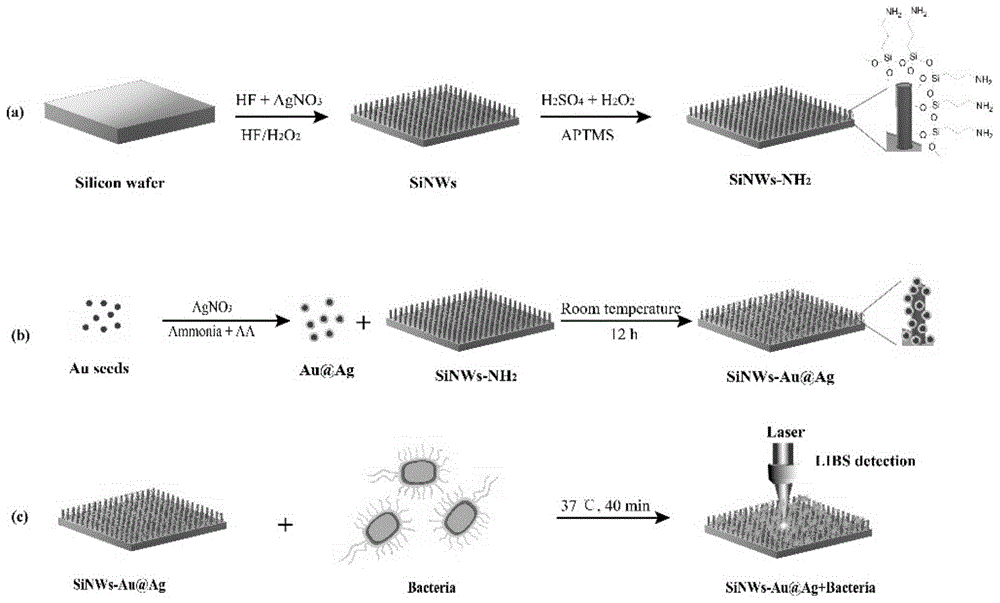
图1为本发明所涉及的sinws-au@ag基底制备、细菌捕获、及libs检测流程图。
图2为本发明所涉及的apt-serstag的制备及sers检测流程图。
图3为本发明制备的au@ag紫外-可见光谱及透射电镜图。
图4为本发明制备的sinws和sinws-au@ag的扫描电镜图。
图5为本发明制备的金银双金属sers标签(apt-serstag)的sers光谱和透射电镜。
图6为本发明制备的sinws-au@ag基底对水中细菌捕获效率随时间的变化。
图7为本发明制备的sinws,sinws-au@ag,及sinws-au@ag捕获细菌后libs光谱。
图8为本发明制备的sinws-au@ag基底捕获不同细菌与apt-serstag结合后的sers光谱。
图9为本发明制备的sinws,sinws-au@ag处理的tsb培养基中细菌生长情况。
具体实施方式
本发明所涉及的sinws-au@ag基底制备、细菌捕获、及libs检测流程图如图1所示。
实施例1、sinws-au@ag基底的制备
通过种子生长法合成au@ag核壳纳米粒子:首先制备金纳米种子(auseeds),取1ml25mm氯金酸水溶液加至50ml超纯水中,磁力搅拌下加热至沸腾,然后快速注入3ml1%柠檬酸三钠水溶液,继续加热反应30分钟至混合液颜色变为酒红色,然后自然冷却至室温即得金纳米种子溶胶。取1ml金纳米种子溶胶至1.5ml离心管中,加入2-14μl0.1m硝酸银溶液,涡旋混匀10秒,然后加入等体积的抗坏血酸(0.1m)及2μl25%氨水,涡旋混匀20秒即得到au@ag核壳纳米粒子溶胶,根据硝酸银加入体积,得到的au@ag核壳纳米粒子标注为au@ag(2)至au@ag(14)。
sinws的制备:通过化学刻蚀法制备,首先硅片经丙酮超声洗涤10分钟,超纯水洗涤2~5次,98%h2so4/30%h2o2(3:1,v/v)混合液浸泡10min,超纯水洗涤2~5次,5%hf浸泡3分钟。然后将清洗干净的硅片浸泡至含4.8mhf和0.005magno3的水溶液中1分钟,使硅片表面沉积银纳米粒子(agnps),用超纯水洗去硅片表面残留的银离子,并将其浸入含4.8mhf和0.15mh2o2的刻蚀液中室温下避光刻蚀1h。最后将刻蚀后的硅片浸泡至稀硝酸(硝酸/水,1:1,v/v)中使agnps溶解,用超纯水洗涤后即得到sinws。
sinws-au@ag的制备:将步骤2)制备的sinws置入98%h2so4/30%h2o2(3:1,v/v)混合液加热至90℃浸泡30min使其表面羟基化,经超纯水和无水乙醇洗涤后,将其浸入1%的3-氨基丙基三甲氧基硅烷(aptms)溶液中(乙醇/乙酸,5:2,v/v),反应1小时得到氨基化的sinws(sinws-nh2),最后将sinws-nh2置入上述加入8μl硝酸银制备的au@agnps溶胶中浸泡12小时,使au@agnps通过ag-n键结合至sinws,用超纯水洗涤除去未结合的au@agnps即得到sinws-au@ag。
实施例2、适配体修饰的金银双金属sers标签(apt-serstag)的制备
取1ml实施例1中制备的金纳米种子溶胶,加入50μl10-5m罗丹明6g(r6g),室温下搅拌2小时得到r6g包覆的金纳米粒子(au-r6g),离心洗去多余的罗丹明6g并重悬于1ml超纯水中,并加入10μl0.1m硝酸银,涡旋10秒后加入等体积的抗坏血酸(0.1m)及2μl25%氨水,涡旋混匀20秒即得到双金属serstag溶胶。最后,向serstag溶胶中加入退火后的适配体,缓慢搅拌反应2小时,离心洗去未结合的适配体,并重悬于1ml超纯水中得到适配体修饰的serstag。
本实施例所用适配体为,鼠伤寒沙门氏杆菌特异性结合适配体,序列为:5’-sh-c6-tatggcggcgtcacccgacggggacttgacattatgacag-3’。
实施例3、基于sinws-au@ag捕获水中细菌
细菌培养:将大肠杆菌,金黄色葡萄球菌和鼠伤寒沙门氏杆菌接种在25ml胰酪胨大豆肉汤培养基(tsb)中,于37℃振荡培养10小时,取5ml培养后的菌液在6000rpm离心5分钟,并用超纯水洗涤三次,最后分散在超纯水中,测定od600并通过平板计数确定细菌浓度。
将实施例1制备的sinws-au@ag基底置入1ml含大肠杆菌或金黄色葡萄球菌的菌液中,于37℃振荡孵育,并在不同时间间隔取10μl菌液通过平板计数测定菌液中细菌浓度的变化,计算sinws-au@ag基底捕获效率。试验结果表明,sinws-au@ag能捕获水中的细菌(如图6所示)。
实施例4、基于sinws-au@ag捕获并结合libs检测饮用水中细菌
将实施例1制备的sinws-au@ag基底置入1ml添加大肠杆菌或金黄色葡萄球菌的饮用水中,于37℃振荡孵育40分钟,然后将sinws-au@ag基底取出,并用超纯水淋洗除去未结合牢固的细菌,自然干燥后进行libs检测。libs检测参数如下:激光脉冲能量30mj,脉宽4-7ns,重复频率10hz,延时1μs,门宽:10μs,采集20*20个位点,每个位点间距为300μm,每个位点累计5发激光得到一个libs光谱。试验结果表明,sinws-au@ag能检测饮用水中细菌(如图7所示)。
实施例5、基于sinws-au@ag捕获细菌并利用apt-serstag进行特异性检测
将实施例1制备的sinws-au@ag基底置入1ml细菌溶液中,于37℃振荡孵育40分钟后取出基底,并用超纯水淋洗除去未结合牢固的细菌,然后将基底置入实施例2制备的apt-serstag中,于37℃振荡孵育3小时后,取出基底并用超纯水淋洗未结合牢固的apt-serstag,待自然干燥后进行sers检测。sers检测参数如下:激光功率10mw,积分时间10秒,随机采集50个位点。试验结果说明,sinws-au@ag能够捕获细菌,并利用apt-serstag可进行特异性检测(如图8所示)。
实施例6、sinws-au@ag抗菌活性的研究
将实施例1制备的sinws-au@ag基底的加入1ml含有细菌的tsb培养液中,细菌浓度为1×106cfu/ml,在37℃恒温振荡器中培养12小时,通过测定未加sinws-au@ag基底和加有基底的tsb菌液的od600或平板菌落计数考察基底的抗菌能力。试验结果说明,sinws-au@ag能够有效抗菌(如图9所示)。
综上,本发明公开了一种基于au@ag核壳纳米粒子负载sinws(sinws-au@ag)的制备方法,以及一种适配体修饰的金银双金属sers标签(apt-serstag)的制备方法,并且利用这两种材料以及libs和sers检测技术实现水中细菌的高效捕获及快速检测。
sequencelisting
<110>四川大学
<120>一种基于au@ag核壳纳米粒子负载硅纳米线阵列及其制备方法和用途
<130>gykh1486-2019p018091ccz
<150>2018111742658
<151>2019-10-09
<160>1
<170>patentinversion3.5
<210>1
<211>40
<212>dna
<213>artificialsequence
<220>
<223>鼠伤寒沙门氏杆菌特异性结合适配体
<400>1
tatggcggcgtcacccgacggggacttgacattatgacag40
本文地址:https://www.jishuxx.com/zhuanli/20240726/121725.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表