疫苗产品中蔗糖含量的检测方法及应用与流程
- 国知局
- 2024-07-30 11:08:47
本技术涉及药物分析及生物检验,尤其是涉及一种采用高效液相色谱法检测疫苗产品中蔗糖含量的方法以及应用。
背景技术:
1、蔗糖是自然界分布最广的非还原性二糖,由一分子葡萄糖和一分子果糖缩合失去一分子水而构成,具有旋光性,但无变旋现象。在酸或蔗糖酶的作用下,蔗糖水解生成等量的d-葡萄糖和d-果糖,其化学结构式为:
2、
3、注射剂的无菌和内有害物质等负荷,企业应考虑对所加入的工艺相关杂质进行有效去除。因此,对蔗糖进行质量控制,对于研究疫苗产品的质量、工艺的稳定性有比较重要的意义。
4、早期实验室对糖进行分析的方法主要为薄层色谱法、纸色谱法和柱层析法等经典方法,这些方法分辨率差、难进行定量测定并且分析时间长无法对大量样品进行测定。
5、目前,疫苗中蔗糖含量的检测方法主要为比旋度法、离子色谱-积分脉冲安培检测法和高效液相色谱-示差折光检测法。比旋度法通过测定溶液中的比旋度来确定蔗糖含量,这种测定方法受制备溶液的影响较大,度数精度较低。离子色谱积分脉冲安培检测时,该方法检测快速准确,灵敏度高。但是其色谱柱价格昂贵,且色谱柱和流动相管路要进行较多的维护不利于实验室日常检测效率的提高。高效液相色谱-示差折光检测法测量蔗糖含量,目前使用较多的是氨基色谱柱,并均以乙腈-水为流动相,然而,这种方法容易导致基线噪音大,平衡时间长。尽管该方法操作简便、精密度较高,相对于早期经典的方法更安全高效,但氨基色谱柱的寿命较短,灵敏度较差,不适用于微量产品的检验。经常更换色谱柱会影响检测的稳定性,并增加蔗糖含量检测的成本。因此对于蔗糖含量的检测,急需开发出一种专属性强、灵敏度高且经济实用的检测方法。
技术实现思路
1、为了解决上述至少一种技术问题,开发一种直接、快速、准确、成本较低的检测疫苗产品中蔗糖含量的检测方法,本技术提供一种采用高效液相色谱法检测疫苗产品中蔗糖含量的方法以及应用。
2、第一方面,本技术提供一种疫苗产品中蔗糖含量的检测方法,所述方法为高效液相色谱法,包括如下色谱条件:
3、色谱柱:采用氢型磺化交联的苯乙烯-二乙烯基苯共聚物为填充剂;
4、色谱柱的柱温为26~30℃;
5、色谱柱的规格为300mm*8.0mm,6μm;
6、流动相:采用硫酸水溶液,所述硫酸水溶液的浓度为0.01~0.03mol/l;流动相的流速为0.5~0.7ml/min;
7、样品的进样量为10~20μl;
8、样品室温度为20~30℃;
9、检测器:采用示差折光检测器为检测器;所述示差折光检测器的检测温度为20~25℃。
10、通过采用上述技术方案,本技术提供的用于检测疫苗中蔗糖含量的高效液相色谱法,采用氢型磺化交联的苯乙烯-二乙烯基苯共聚物作为填充剂的色谱柱,并结合示差折光检测器,能够快速、准确地测定疫苗中蔗糖的含量。使用该方法,样品的前处理相对简单,线性范围广且定量限低而灵敏,而且能够直接测定多种糖类。
11、首先,本技术所选用的氢型磺化交联的苯乙烯-二乙烯基苯共聚物色谱柱对于各种类型的单糖、二糖和多糖的分析具有较好的耐用性和重现性,本技术使用的色谱柱与硅胶基质的氨基柱相比对各种类型的单糖、二糖及多糖的分析具有更好的耐用性和重现性,其色谱柱内添加的磺化剂使色谱柱的强阳离子的交换作用得到明显提升。氢型磺化交联的苯乙烯-二乙烯基苯共聚物色谱柱能够结合尺寸排阻法和离子排斥法分离糖类、有机酸类物质,可实现糖类和有机酸的同时分析。
12、本技术中,需要检验的疫苗样品为流感病毒裂解疫苗中间产品,由于,在检测流感病毒裂解疫苗中蔗糖含量时,需要用到的物料为蔗糖、氯化钠、磷酸氢二钠、磷酸二氢钠等物质,由于氯化钠、磷酸氢二钠、磷酸二氢钠统作为pbs溶液,pbs溶液在示差折光检测下和蔗糖相互干扰,使两种物质的出峰时间基本一致,故不能检测出蔗糖的真实结果,因此,本技术为了解决检测蔗糖含量时出现的,检测精确度较差的问题,在本技术中采用了孔径为6μm的氢型磺化交联的苯乙烯-二乙烯基苯共聚物色谱柱,并且通过控制流动相的流速和浓度,有效的提高了蔗糖含量的检测精确度。
13、本技术还提供了流动相的浓度对于蔗糖与其他干扰物质的分离程度的影响,同时,提供了流动相的流速、样品的进样量和色谱柱的柱温对待测样品保留时间和分离度的影响。本技术提供的流速范围、样品的进样量和色谱柱的柱温,均能够确保高效液相色谱图中目标物的出峰时间适宜、峰形良好、各峰之间的分离度好,从而保证检测结果的真实性和可靠性。
14、本技术提供的方法具有操作简单、重现性好、精密度高、灵敏度高和检测限低等优点。
15、柱温箱是高效液相色谱仪中的一个重要组件,它用于控制色谱柱的温度,以提高分离效果和稳定性。本技术通过设置较低的温度,能够有效地减少背景噪音、增强信号峰、改善分离效果,并延长色谱柱的寿命。
16、另外,本技术使用的色谱柱的耐酸性较强,能够耐受低ph值的流动相。这种优势使得柱子在强酸性条件下仍然能够保持良好的分离性能,而不会发生退化或损坏。对于阳离子交换柱而言,它们相比普通阳离子交换柱具有更强的交换作用。这意味着它们能更有效地吸附和洗脱样品中的阳离子成分,从而实现更好的洗脱效果和更快的出峰时间。这种性能优势大大缩短了检测时间,提高了检测效率。
17、总的来说,柱温箱的使用能够提高高效液相色谱的分离效果和稳定性,而耐酸性强的色谱柱以及具有强交换作用的阳离子交换柱则能够实现更好的洗脱效果和更快的出峰时间,进一步提高分析效率。
18、本技术选用的示差折光检测器与折光仪相比,在对流感病毒裂解疫苗进行蔗糖含量的检测时,示差折光检测器对氯化钠、磷酸氢二钠、磷酸二氢钠等物质干扰程度更小,测出的结果更准确。而折光仪测量的蔗糖浓度(%)最小分度值为0.25,即2500μg/ml,其测量的最小分度值远高于质控标准,因此,会导致测量样品中的值为未检出,进而无法测出其准确数值。因此,本技术采用差折光检测器能够进一步提高检测精确度。
19、此外,在本领域中液相耐受的最低ph值为1.0,而本技术为了保证检测精确度,在本技术中使用浓度相对较高的高浓度硫酸(浓度为0.02mol/l,ph为1.5~1.7)作为流动相,进一步提高了检测精确度。
20、总之,本技术使用浓度为0.02mol/l的硫酸作为流动相,将高浓度硫酸作为流动相,小流速冲洗系统,可有效提高各色谱峰之间的分离度,有利于指导疫苗生产中对蔗糖的日常检测,从而保证产品质量。
21、可选的,所述检测方法还包括供试品溶液的制备,所述供试品溶液的制备包括如下步骤:
22、s1、将疫苗原液稀释,制得稀释后的样品;
23、s2、将稀释后的样品与沉淀剂按体积比1:(2~5)混匀,放置1~4h、离心,离心速度为3000~4000g/min、离心时间为10~15min,取上清液,作为供试品溶液;
24、所述步骤s2中的沉淀剂选自质量百分数为1~2%的磺基水杨酸溶液。
25、通过采用上述技术方案,本技术提供的疫苗样品的制备方法具有简便的优势。本技术通过将样品溶液稀释并去除干扰性絮状沉淀,从而对疫苗中间产品的清液进行检测,使检测结果更为准确。
26、可选的,所述检测方法还包括蔗糖对照品溶液,所述蔗糖对照品溶液的制备方法为如下:称取蔗糖对照品50mg,用超纯水定容至10ml,制得浓度为5mg/ml的蔗糖对照品贮备液;将蔗糖对照品贮备液浓度稀释至1~1000μg/ml,制得所述蔗糖对照品溶液。
27、可选的,所述疫苗样品包括四价流感病毒裂解疫苗、流感病毒裂解疫苗。
28、通过采用上述技术方案,本技术提供的高效液相色谱法检测疫苗制品中蔗糖含量的检测方法能够检测流感疫苗中间产品中的蔗糖含量,且该检测方法具有操作简单、灵敏度高、准确性强、易于标准化操作的优点。
29、本技术中,由于流感病毒裂解疫苗中含有制剂辅料和保护剂等物质,而该类物质对流感疫苗中间产品检测存在一定干扰,因此,对于流感病毒裂解疫苗产品蔗糖含量的检测是在流感病毒裂解疫苗脱糖洗滤液和原液这一步进行的。故本技术中,检测流感病毒裂解疫苗的蔗糖含量即流感病毒裂解疫苗脱糖洗滤液和原液的蔗糖含量。
30、可选的,所述步骤s1中的稀释后的疫苗原液,使用的稀释剂选自pbs缓冲液;所述pbs缓冲液包括重量比为9.8:1:14.4的磷酸氢二钠、磷酸二氢钠以及氯化钠;所述pbs缓冲液中,磷酸根的浓度为0.02mol/l,pbs缓冲液的ph为7.4。
31、可选的,所述色谱柱为dikma carbopac h+色谱柱。
32、可选的,所述色谱柱的柱温为28℃。
33、可选的,所述流动相的流速为0.6ml/min。
34、可选的,所述示差折光检测器的检测温度为25℃。
35、通过采用上述技术方案,本技术通过调整色谱条件,能够使检测的精密度更高,获得的高效液相色谱图的峰面积的rsd值与保留时间的rsd值更小,且高效液相色谱图中的峰形更好、峰高适宜、分离度更佳。
36、可选的,所述样品的进样量为样品的进样量为10~20μl。
37、可选的,所述疫苗原液的稀释浓度为2~1000μg/ml。
38、通过采用上述技术方案,本技术通过将疫苗样品的稀释浓度为调整为2~1000μg/ml,能够保证检测精确度。当样品溶液的浓度过高时,容易导致色谱柱堵塞,损伤检测设备;当样品溶液的浓度过低时,目标检测物的折光效果太弱,易导致检测结果不准确。因此,本技术将疫苗样品溶液的浓度控制在上述范围内,既能保证检测顺利进行,又能使高效液相色谱图中目标检测物的色谱峰高和峰面积适宜,从而可获得更加准确的检测结果。
39、可选的,所述硫酸水溶液的浓度为0.02mol/l。
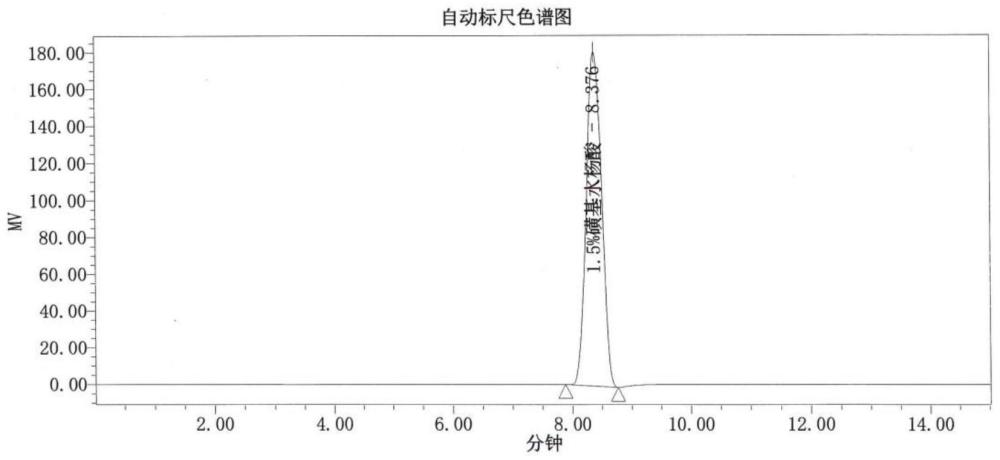
40、可选的,本技术所述疫苗产品中蔗糖含量的检测方法中存在干扰物质a,所述干扰物质a为磺基水杨酸,分子式是c7h6o6s·2h2o;所述干扰物质a的出峰时间在8.3~8.4min之间。
41、可选的,本技术所述疫苗产品中蔗糖含量的检测方法中还存在干扰物质b,所述干扰物质b为pbs溶液,其含有的盐成分为:na2hpo4·12h2o(磷酸氢二钠)nah2po4·2h2o(磷酸二氢钠)和nacl(氯化钠),所述干扰物质b的出峰时间在10.8~11.0之间。
42、综上所述,本发明包括以下至少一种有益技术效果:
43、1.通过采用上述技术方案,本技术提供的一种用于检测疫苗中蔗糖含量的高效液相色谱法,采用氢型磺化交联的苯乙烯-二乙烯基苯共聚物作为填充剂的色谱柱,结合示差折光检测器,能够快速、准确地测定疫苗中蔗糖的含量。使用该方法,样品的前处理相对简单,线性范围广且定量限低而灵敏,而且可以直接测定多种糖类。
44、本技术中,检验的疫苗样品为流感病毒裂解疫苗中间产品,在检测感病毒裂解疫苗中蔗糖含量时,需要用到的物料为蔗糖、氯化钠、磷酸氢二钠、磷酸二氢钠等物质,故采用孔径为6μm的氢型磺化交联的苯乙烯-二乙烯基苯共聚物色谱柱进行蔗糖含量检测。
45、本技术选用的示差折光检测器与折光仪相比,在对流感病毒裂解疫苗进行蔗糖含量的检测时,示差折光检测器对氯化钠、磷酸氢二钠、磷酸二氢钠等物质干扰程度更小,测出的结果更准确。而,折光仪测量的蔗糖浓度(%)最小分度值为0.25,即2500μg/ml,其测量的最小分度值远高于质控标准,因此,会导致测量样品中的值为未检出,进而无法测出其准确数值。
46、此外,本技术中提供了流动相的ph值对于蔗糖与其他干扰物质的分离程度的影响,以及流速、进样量和柱温对待测样品保留时间和分离度的影响。本技术中提供的流速范围、进样量和柱温的调整能够确保高效液相色谱图中目标物的出峰时间适宜、峰形良好、各峰之间的分离度好,从而保证检测结果的真实性和可靠性。本技术提供的方法具有操作简单、重现性好、精密度高、灵敏度高和检测限低等优点。此外,所选用的氢型磺化交联的苯乙烯-二乙烯基苯共聚物色谱柱对于各种类型的单糖、二糖和多糖的分析具有较好的耐用性和重现性。
47、本技术选用的氢型磺化交联的苯乙烯-二乙烯基苯共聚物色谱柱进行检测,该色谱柱与硅胶基质的氨基柱相比对各种类型的单糖、二糖及多糖的分析具有更好的耐用性和重现性,其色谱柱内添加的磺化剂使色谱柱的强阳离子的交换作用得到明显提升。氢型磺化交联的苯乙烯-二乙烯基苯共聚物色谱柱能够结合尺寸排阻法和离子排斥法分离糖类、有机酸类物质,可实现糖类和有机酸的同时分析。
48、柱温箱可设置在较低温度即可得到有效的分析,以保证高效液相色谱仪柱温箱的长久使用;并且该色谱柱耐受的酸度范围很广,可耐受ph极低的流动相,使得阳离子的交换作用比普通阳离子交换柱更强,使得洗脱效果更好、出峰时间更快,大大缩短了检测时间,提高了检测效率。
49、总之,本技术将高浓度硫酸作为流动相,小流速冲洗系统,可有效提高各色谱峰之间的分离度,有利于指导疫苗生产中对蔗糖的日常检测,从而保证产品质量。
50、2.通过采用上述技术方案,本技术提供的高效液相色谱法检测疫苗制品中蔗糖含量的检测方法能够检测流感疫苗中间产品中的蔗糖含量,且该检测方法具有操作简单、灵敏度高、准确性强、易于标准化操作的优点。
51、本技术中,由于流感病毒裂解疫苗中含有制剂辅料和保护剂等物质,而该类物质对流感疫苗中间产品检测存在一定干扰,因此,对于流感病毒裂解疫苗产品蔗糖含量的检测是在流感病毒裂解疫苗脱糖洗滤液和原液这一步进行的。故本技术中,检测流感病毒裂解疫苗的蔗糖含量即流感病毒裂解疫苗脱糖洗滤液和原液的蔗糖含量。
本文地址:https://www.jishuxx.com/zhuanli/20240730/155576.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。