一种基于SAXS分析脂质纳米粒子的方法、装置、存储介质、终端和系统
- 国知局
- 2024-07-30 11:14:40
本发明涉及小角x射线散射saxs理论计算领域,特别是涉及一种基于saxs分析脂质纳米粒子的方法、装置、存储介质、终端和系统。
背景技术:
1、脂质纳米粒子(lipid nanoparticle,lnp)是非病毒基因药物中最先进的基因递送系统,广泛用于小分子和核酸药物的递送。lnps递送的首款sirna(小核酸)药物onpattro于2017年获得fda批准上市。基于lnp技术的复必泰(comirnaty)疫苗在临床试验中表现出较高的有效性。目前已有数十种使用lnp作为药物递送载体的mrna(信使核糖核酸)药物进入临床试验阶段,适应症包括但不限于新兴传染病、肿瘤免疫、自身免疫性疾病、心血管疾病等,在面向生命健康的领域具有重要的商业价值。
2、lnp主要由可电离的阳离子脂质、电中性的辅助脂质、胆固醇以及聚乙二醇(polyethylene glycol, peg)化脂质四种组分构成。细胞转染效率取决于lnp的几何形状、带电分子基团的数量、表面靶向修饰的定向效率以及连接键的性质。其中,peg化脂质延长了核酸药物体内代谢的循环时间,有助于提升药效;辅助脂质可提升递送载体的结构稳定性;阳离子脂质组分可以在低ph环境下与带负电的mrna形成复合体,促进核酸的细胞内吞作用;胆固醇有助于稳定lnp的结构,促进mrna递送体系与宿主细胞膜的融合。
3、lnp通常具有球状的多层膜囊泡结构,脂质和核酸分散在lnp的脂质内核中。lnp微观结构(粒径大小及分布、形貌、包封药物状态、脂质膜壳层分布等)的稳定性和重复性对药物代谢和生物学效应有着重要的影响。其中,脂质膜结构的差异会影响药物的装载率、体内滞留时间以及药物释放速率。通过调控lnp四种组分的类型、比例,结合制备工艺的优化,可以主动调控lnp的组装结构,进而获得理想的生物学效应,是开发新型lnp药物递送纳米载体的关键科学和技术问题。为了建立lnp药物递送系统“工艺-结构-生物学效应”关系,需要精细获取lnp纳米粒子的微观结构,例如脂质双分子层厚度、peg层的分布、多层膜的均匀性等。
4、然而,当前国内外仍欠缺能够有效表征lnp微观结构的实验方法。冷冻透射电子显微镜是当前该领域最常使用的检测技术,可用于确定脂膜层数;由于peg层的衬度太低,而无法被电镜清晰观测。传统的谱学方法(核磁共振、差示扫描量热)只能通过测量peg化脂质层结合水分子的量或peg化脂质层与水分子的相互作用,间接推断脂质膜外层peg修饰的情况。
5、x射线小角散射(saxs)是表征软物质体系纳米尺度微观结构的重要实验方法,可以直接测定脂质膜的层状结构及与其它分子相互作用情况。saxs还具有如下优势:(1)在溶液生理状态下即可进行实验,检测过程不受分子量以及测试体系浓度的限制,可快速进行环境条件变量的测试;(2)实验测试时间相对较短,在第三代同步辐射光源,毫秒量级的曝光时间就可以获得足够信噪比的散射信号;(3)对样品稳定性要求较低,且能够反映溶液中lnps和mrna构象的系综平均;(4)同步辐射saxs技术可以原位快速测量mrna-lnps复合体随时间的演化过程,结合计算机建模和动力学模拟的方法,可进一步获得精细的动力学过程。溶液saxs技术的这些优势可在很大程度上避免常规纳米粒子表/界面化学或生物学实验方法的局限性,是谱学法、成像法和化学表征实验方法的有益补充。然而在lnp微观结构表征领域,仍缺乏适用的saxs数据拟合模型以及通用的saxs检测实验方法。
技术实现思路
1、鉴于以上所述现有技术的缺点,本发明的目的在于提供一种基于saxs分析脂质纳米粒子的方法、装置、存储介质、终端和系统,其为脂质纳米粒子中微结构分析提供较为准确的数据,从而用于解决现有技术中在纳米药物研发以及lnp药物质量评估中存在的表征方法存在的问题。
2、为实现上述目的及其他相关目的,本发明是通过以下技术方案获得的。
3、本发明方面提供一种基于saxs分析脂质纳米粒子的方法,所述方法包括如下步骤:
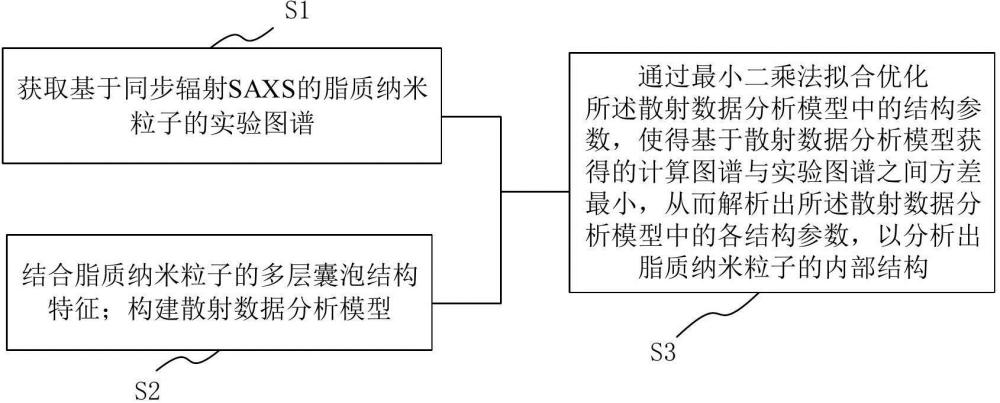
4、获取步骤:获取基于同步辐射saxs的脂质纳米粒子的实验图谱;
5、建模步骤:结合脂质纳米粒子的多层囊泡结构特征,构建散射数据分析模型;
6、解析步骤:调整所述散射数据分析模型中的结构参数,使得基于散射数据模型获得的计算图谱与实验图谱之差总和最小,从而解析出所述散射数据分析模型中的各结构参数,以分析和表征出脂质纳米粒子的内部结构。
7、进一步地,在同等条件下分别测试含脂质纳米粒子的缓冲溶液、不含脂质纳米粒子的缓冲溶液,然后经过预处理获得脂质纳米粒子的实验图谱即脂质纳米粒子的i-q曲线。
8、进一步地,所述预处理步骤至少包括一维数据化步骤。
9、更进一步地,所述预处理步骤还包括:散射强度归一化步骤、散射绝对强度校正步骤、散射背底扣减步骤中的一种或多种。
10、进一步地,所述散射数据分析模型为具有核壳结构的球体模型,其中,所述核壳结构为多壳层。这是结合脂质纳米粒子的多层囊泡结构特征来构建的。
11、进一步地,所述壳层为三壳层,所述三壳层从内到外依次为脂质双分子层尾部疏水部分、脂质双分子层头部亲水部分和peg层。
12、由于在药物递送溶液系统中,lnp浓度较低,它们之间的相互作用可以忽略,因此散射强度等于采样体积内所有lnp散射信号的叠加。
13、进一步地,所述散射数据分析模型为:
14、 式ⅰ;
15、式ⅰ中,n(r)是正态分布函数,用于描述脂质纳米粒子的多分散性和数量密度;
16、p(q)为形状因子,用于描述脂质纳米粒子的多层囊泡结构;
17、其中,n(r)的计算方式如式ⅱ所示:
18、 式ⅱ;
19、式ⅱ中,σ表示脂质纳米粒子的粒径分布的标准差,采用动态光散射实验测试获得;
20、rc为脂质纳米粒子的内核半径;
21、r为脂质纳米粒子的总半径,r=rc+t1+t2+t3;
22、式ⅲ;
23、式ⅲ中,
24、
25、
26、
27、
28、式中,t1为最内层壳厚度,ρ1为最内层壳的散射长度密度;t2为中间壳层的厚度,ρ2为中间壳层的散射长度密度;t3为最外层壳的厚度,ρ3为最外层壳的散射长度密度,ρc为内核的散射长度密度,ρsol为缓冲液的散射长度密度。
29、进一步地,各结构参数值包括rc,t1,t2,t3,ρ1,ρ2、ρ3和ρc。
30、本发明第二方面还公开了一种基于saxs分析脂质纳米粒子的装置,所述装置包括以下模块:
31、获取模块:用于获取基于同步辐射saxs的脂质纳米粒子的实验图谱;
32、建模模块:用于结合脂质纳米粒子的多层囊泡结构特征,构建散射数据分析模型;
33、解析模块:用于通过最小二乘法拟合优化所述散射数据分析模型中的结构参数,使得基于散射数据模型获得的计算图谱与实验图谱之间方差最小,从而解析出所述散射数据分析模型中的各结构参数,以分析出脂质纳米粒子的内部结构。
34、在上述第二方面中,进一步地,还包括预处理模块:用于对所述二维散射数据进行预处理,所述预处理模块包括一维数据转化模块、散射强度归一化模块、散射绝对强度校正模块、散射背底扣减模块中的一种或多种。
35、在上述第二方面中,更进一步地,所述一维数据转化模块用于将各向同性的二维散射数据转化为一维散射曲线(i-q曲线)。
36、在上述第二方面中,更进一步地,所述散射强度归一化模块用于将后电离室计数归一,然后计算散射曲线的欧几里得距离,并建立相似性矩阵,进而评估实验数据的重复性和稳定性,筛选出高质量的i-q曲线。
37、在上述第二方面中,更进一步地,所述散射背底扣减模块用于扣除含脂质纳米粒子的缓冲溶液中缓冲溶液的散射信号。
38、在上述第二方面中,更进一步地,所述散射绝对强度校正模块用于以纯水作为标准样品,计算脂质纳米粒子的绝对散射强度。
39、优选地,在构建散射数据分析模型时,使用sasfit软件构建。
40、本发明第三方面还公开了一种计算机可读存储介质,其上存储有计算机程序,该程序被处理器执行时实现如上述方面任一所述的方法。
41、本发明第四方面还公开了一种终端,所述终端包括:处理器及存储器;所述存储器用于存储计算机程序,所述处理器用于执行所述存储器存储的计算机程序,以使所述终端执行如上述方面任一所述的方法。
42、本发明第五方面还公开了一种基于saxs分析脂质纳米粒子的系统,所述系统包括同步辐射saxs和如上述第四方面所述的终端。
43、本发明中提供的基于saxs分析脂质纳米粒子的方法、装置、存储介质、终端和系统的技术方案包括了分析未负载有核酸的脂质纳米粒子,其具有以下有益效果:
44、本发明根据脂质纳米粒子的结构特性,建立了优化的脂质纳米粒子saxs分析模型与分析方法,可以通过测试样品间的参数的对比分析,评价脂质纳米粒子的多膜层结构,并可监测lnp药物递送样本的产品质量和稳定性;该发明可为lnp药物递送体系的研制提供先进的实验方法和科学依据。
本文地址:https://www.jishuxx.com/zhuanli/20240730/155962.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表