在包括经修剪的N-聚糖的FC区处涉及转谷氨酰胺酶的缀合方法与流程
- 国知局
- 2024-11-06 15:08:11
本公开涉及用于将如药物活性分子等所关注部分与如抗体等靶向分子缀合的方法。
背景技术:
1、已知许多用于将药物活性物连接到抗体和相关分子的方法。例如,已使用马来酰亚胺基团将药物接头连接到免疫球蛋白中的天然或经工程化的半胱氨酸残基。其它方法基于使用n-连接糖基化位点n297,在一些方法中,所述位点被重塑为将聚糖修剪回到核心glcnac部分,并然后使所述部分与udp-糖在存在galt酶的情况下发生反应,所述udp-糖进一步包含反应性叠氮化物部分,所述反应性叠氮化物部分允许随后使用点击化学使药物接头进行加成。另一种方法是将内源性或经工程化的谷氨酰胺残基与微生物转谷氨酰胺酶(microbial transglutaminase,mtgase)一起使用。
技术实现思路
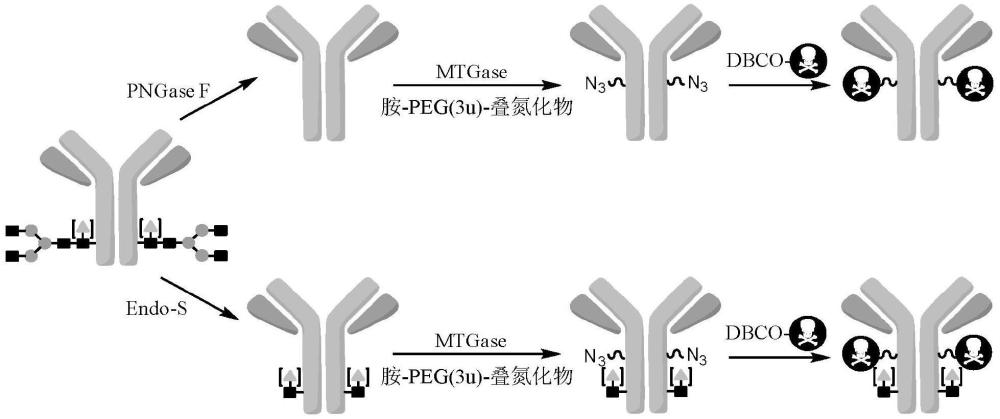
1、使用mtgase以在免疫球蛋白的fc区中的位置q295(kabat eu编号)处的内源性谷氨酰胺残基处连接的现有方法是基于使用pngase f,所述pngase f会去除邻近位置n297处的所有n-连接聚糖,以避免干扰tgase反应。这留下d297处的带负电荷的天冬氨酸残基,并且因此修改的方法涉及使d297发生突变以去除负电荷(并且还需要去除n-聚糖)。现在发现,使用基于endos的对n-聚糖进行的以使核心glcnac部分完整的不同酶促处理允许q295处的高度高效的mtgase反应。进一步地,核心glcnac部分在n297处然后可用于第二缀合,惊讶地发现,即使在邻近的q295处已经存在药物接头,所述第二缀合也是高效的。
2、因此,在第一方面中,本公开涉及一种用于将所关注部分与含fc的多肽(例如,抗体)缀合的方法,所述方法包括:
3、(i)提供含fc的多肽,所述含fc的多肽具有位于存在于所述多肽的fc区中的位点处的n-连接糖基化,所述位点邻近包括谷氨酰胺残基的位点;
4、(ii)用酶(如endos)处理所述多肽,以将位于所述n-连接糖基化位点处的n-连接聚糖修剪回到任选岩藻糖基化的核心n-乙酰葡糖胺(glcnac)部分;以及
5、(iii)(1)在存在转谷氨酰胺酶(tgase)的情况下,使在步骤(ii)中获得的所述多肽与包括受体部分的所关注部分发生反应,使得所述所关注部分通过所述谷氨酰胺残基连接到所述多肽,所述受体部分为所述tgase的底物。
6、在第二相关方面中,本公开还涉及一种用于将所关注部分与含fc的多肽(例如,抗体)缀合的方法,所述方法包括:
7、(i)提供含fc的多肽,所述含fc的多肽具有位于存在于所述多肽的fc区中的位点处的n-连接糖基化,所述位点邻近包括谷氨酰胺残基的位点;
8、(ii)用酶(如endos)处理所述多肽,以将位于所述n-连接糖基化位点处的n-连接聚糖修剪回到任选岩藻糖基化的核心n-乙酰葡糖胺(glcnac)部分;以及
9、(iii)(2)在存在转谷氨酰胺酶(tgase)的情况下,使在步骤(ii)中获得的所述多肽与受体部分发生反应,使得所述受体部分通过所述谷氨酰胺残基连接到所述多肽,所述受体部分为所述tgase的底物,并且所述受体部分进一步包括反应性基团(r),所述r使得所述所关注部分随后能够通过r与连接到所述所关注部分的互补反应性基团(r')之间的反应连接;以及
10、(iv)使在步骤(iii)(2)中形成的多肽缀合物与连接到r'的所述所关注部分在使得r与r'发生反应以形成r-r'的条件下发生反应。
11、在以上方面的一个实施例中,所述受体部分选自胺、氨基氧基、酰肼基、肼基和其芳基衍生物。
12、在一个实施例中,所述受体部分具有式ac-sp-r,在所述式中,ac选自胺、氨基氧基、酰肼基、肼基和其芳基衍生物,sp不存在或为间隔子部分;并且r为反应性基团,例如叠氮化物。
13、在一个实施例中,所述n-连接糖基化位点位于根据kabat编号系统的位置297或等效位置处,和/或所述包括谷氨酰胺残基的位点位于根据kabat编号系统的位置295或等效位置处。
14、在一个实施例中,所述所关注部分包括药物接头。
15、本公开还涉及第二方面,其中在以上所述第一方面的方法中,第二所关注部分与所述含fc的多肽缀合,所述方法进一步包括以下步骤:
16、(v)在存在半乳糖基转移酶(galt)的情况下,使在步骤(iii)(1)、步骤(iii)(2)或步骤(iv)中获得的所述多肽与连接到所述第二所关注部分的糖衍生物发生反应,使得所述糖衍生物通过所述核心n-乙酰葡糖胺(glcnac)部分连接到所述多肽。
17、在一相关方面中,第二所关注部分与所述含fc的多肽缀合,所述方法进一步包括以下步骤:
18、(v)在存在半乳糖基转移酶(galt)的情况下,使在步骤(iii)(1)、步骤(iii)(2)或步骤(iv)中获得的所述多肽与连接到反应性基团(r)的糖衍生物发生反应,使得所述糖衍生物通过所述核心n-乙酰葡糖胺(glcnac)部分连接到所述多肽,所述r使得所述所关注部分随后能够通过r与连接到所述所关注部分的互补反应性基团(r')之间的反应连接;以及
19、(vi)使在步骤(v)中形成的多肽缀合物与连接到r'的所述所关注部分在使得r与r'发生反应以形成r-r'的条件下发生反应。
20、在第三方面中,本公开涉及一种含fc的多肽缀合物,其包括:
21、(i)天冬酰胺残基,所述天冬酰胺残基存在于所述多肽的fc区中,所述fc区具有任选岩藻糖基化的glcnac n-聚糖核,所述核缺乏任何额外的内源性聚糖残基;以及
22、(ii)(q)-nh-l-d或其药学上可接受的盐或溶剂化物;其中q为谷氨酰胺残基,所述谷氨酰胺残基存在于所述多肽的所述fc区中;l为接头,所述接头任选地包括条件可切割部分;并且d为药物部分;
23、其中所述天冬酰胺残基邻近所述谷氨酰胺残基。
24、在一个实施例中,在所述含fc的多肽缀合物中,l包括l1-r-r'-l2;其中l1不存在或为间隔子部分,r-r'是通过使反应性基团r与互补反应性基团r'反应来形成的;并且l2为接头或间隔子部分,d连接到所述接头或间隔子部分,并且所述接头或间隔子部分任选地包括条件可切割部分。
25、在第四方面中,本公开涉及一种含fc的多肽缀合物,其包括:
26、(i)(q)-nh-la-d1或其药学上可接受的盐或溶剂化物;其中q为谷氨酰胺残基,所述谷氨酰胺残基存在于所述多肽的fc区中;la为接头;并且d为药物部分;
27、(ii)(n)-g-s-r2-r2'-lb-d2或其药学上可接受的盐或溶剂化物;其中n为天冬酰胺残基,所述天冬酰胺残基存在于所述多肽的所述fc区中;g为任选岩藻糖基化的glcnac n-聚糖核;s为糖衍生物;r2-r2'是通过使反应性基团r2与互补反应性基团r2'反应来形成的;lb为接头,所述接头任选地包括条件可切割部分;并且d1和d2各自独立地为药物部分;并且
28、其中所述天冬酰胺残基邻近所述谷氨酰胺残基。
29、在一个实施例中,在所述含fc的多肽缀合物中,la包括la1-r1-r1'-la2;其中la1不存在或为间隔子部分,r1-r1'是通过使反应性基团r1与互补反应性基团r1'反应来形成的;并且la2为接头或间隔子部分,d1连接到所述接头或间隔子部分,并且所述接头或间隔子部分任选地包括条件可切割部分。
30、在第三方面或第四方面的一实施例中,所述含fc的多肽缀合物为igg,如与肿瘤抗原特异性结合的igg。
31、在第三方面或第四方面的一实施例中,药物为细胞毒素。
32、在第三方面或第四方面的一实施例中,所述天冬酰胺残基位于根据kabat编号系统的位置297或等效位置处,和/或所述谷氨酰胺残基位于根据kabat编号系统的位置295或等效位置处。
33、本公开还涉及一种含fc的多肽缀合物,其通过上文所描述的第一方面或第二方面的方法获得或可通过上文所描述的第一方面或第二方面的方法获得。
34、在第五方面中,本公开涉及一种药物组合物,其包括如本文所描述的含fc的多肽缀合物以及一种或多种药学上可接受的载体或稀释剂,如缓冲剂、糖和/或洗涤剂。
35、具体实施方式
36、抗体
37、用于在本文所描述的方法中使用的抗体包括n-糖基化的天冬酰胺残基,如免疫球蛋白的重链中的野生型n297或等效位置。n-糖基化位点还可以被工程化到抗体中,例如基于共有序列(序列子)asn-xaa-ser/thr,其中xaa为除脯氨酸之外的任何氨基酸(参见reslan等人,2020,《国际生物大分子杂志(int.j.biol.macromol)》158:189-196;cruz等人,2021《药剂学(pharmaceutics)》13(11):1747;-polo等人,2011,《蛋白质科学(protein sci.)》20(1):179-186)。
38、n-糖基化的天冬酰胺残基侧接有谷氨酰胺残基,所述谷氨酰胺残基为微生物转谷氨酰胺酶的底物。例如,具有n297糖基化位点的免疫球蛋白通常具有位于位置295处的谷氨酰胺残基(即,距n297残基2个残基)。“侧接”意指谷氨酰胺残基位于n-糖基化的天冬酰胺残基的2个、3个或4个氨基酸内,在任一侧(即,在n末端方向或c末端方向上)。在一个实施例中,谷氨酰胺残基距n-糖基化的天冬酰胺残基至少2个氨基酸,如+/-2个氨基酸。
39、谷氨酰胺可以是天然存在的/野生型,如在免疫球蛋白分子中的位置295或其等效形式处的谷氨酰胺残基,或者其可以被工程化到抗体氨基酸序列中。
40、术语抗体包含全长免疫球蛋白(例如igg)以及其包括抗原结合位点的片段。在一个实施例中,抗体包括fc结构域或其包括ch2结构域的片段。
41、在一个实施例中,一个或多个n-糖基化位点和所侧接的谷氨酰胺存在于抗体的恒定区中,如fc结构域或ch2结构域中。
42、用于在本文所描述的方法中使用的抗体以及由此类方法产生的抗体可以与任何所关注抗原结合。在一个实施例中,抗原存在于细胞(如人或动物体内的细胞)的表面上。此类细胞/抗原可以与疾病或病症(例如增殖性疾病)相关。抗原的表达可以在所关注细胞中上调。在一个实施例中,抗原为肿瘤抗原。在另一个实施例中,抗原为存在于免疫细胞(如调节性t细胞)中的细胞表面分子。特异性细胞表面蛋白/肿瘤抗原包含cd19、cd22、cd25、axl、kaag1、dlk-1和psma。
43、抗体重塑
44、在本发明的一个方面中,对抗体进行处理以将n-聚糖(如n297处的n-聚糖)修剪回到核心聚糖,如任选岩藻糖基化的核心n-乙酰葡糖胺(glcnac)部分。这可以通过将抗体与一种或多种可以去除大部分聚糖的酶一起温育来进行。先前,n-聚糖去除使用pngase f进行。然而,这会去除所有聚糖残基,并将天冬酰胺转化为带负电荷的天冬氨酸残基。相反,本公开的方法使用合适的酶以将n-连接糖基化位点处的n-连接聚糖修剪回到任选岩藻糖基化的核心n-乙酰葡糖胺(glcnac)部分。
45、根据聚糖的性质,可以选择合适的内切糖苷酶。内切糖苷酶优选地选自由以下组成的组:endo s酶、endo a酶、efendo18a酶、endo f(例如f1、f2或f3)酶、endo m酶、endo d酶和endo h酶和/或其组合,所述内切糖苷酶的选择取决于聚糖的性质。在进一步优选的实施例中,内切糖苷酶为endo s、endo s49、endo f或其组合。组合的内切糖苷酶公开于us10,858,41中,其包含两种不同的endo s酶作为融合蛋白。使用组合的优点在于,在单个反应中可以识别和修剪更多数量的糖型。
46、endos是从人类病原体酿脓链球菌(streptococcuspyogenes)中分离的内切糖苷酶。已表明,endos的不同形式(如endos(collin等人,2001.《欧洲分子生物学杂志(emboj.)》20:3046–3055)和endos2(等人,2013.《生物化学杂志(biochem j.)》455:107–118))以不同糖型选择性使人免疫球蛋白g的n-连接聚糖水解(等人,2015.《糖生物学(glycobiology)》25(10):1053-1063)。endos和endos2可从吉诺维斯公司(genovis ab,iggzerotm、glycinatortm)获得。
47、将所关注抗体与一种或多种酶在合适的条件下温育,以实现n-聚糖的全部或大部分的去除,以留下核心n-乙酰葡糖胺(glcnac)部分。合适的方法描述于实例中并通过等人,2015,同上描述。
48、具有核心n-乙酰葡糖胺的抗体聚糖在本文中被定义为包括通过任选岩藻糖基化的glcnac的c1(核心glcnac)与抗体键合的聚糖的抗体。
49、使用tgase的所关注部分的加成
50、用于与所关注的含fc的多肽缀合的所关注部分包含药物活性物质/药物、诊断试剂和可检测标记。在一个实施例中,活性部分与接头或间隔子构建体共价键合。
51、在过程的第一步中,在邻近n-糖基化位点的所关注的谷氨酰胺残基处使用转谷氨酰胺酶实现缀合。
52、微生物转谷氨酰胺酶(mtg)催化蛋白质底物上的某些表面暴露的谷氨酰胺(gln)残基与赖氨酸(lys)残基之间的转酰胺化反应,从而使谷氨酰胺残基与赖氨酸残基通过异肽键交联。mtg的催化机制涉及通过酶的活性位点半胱氨酸对靶酰基供体gln进行亲核攻击,以形成硫酯中间体。随后起到酰基受体的作用的胺底物对硫酯的亲核攻击引起经转酰胺化的产物的形成。
53、最常用的mtgase是源自茂原链霉菌(streptomyces mobaraensis)的38-kda的酶。另一种存在于细菌中的转谷氨酰胺酶来自枯草芽孢杆菌(bacillus subtilis)(参见us5,731,183)。已经开发了mtgase的各种变体,如wo2017/059158和wo2017/059160(默克公司(merck))中公开的具有例如选自由以下组成的组的氨基酸取代的mtgase:(a)e300a,(b)i240a和p241a,(c)e249q以及(d)e300a和y302a。
54、因此,经重塑的抗体可以与使用转谷氨酰胺酶(如mtgase)的所关注部分缀合,所述所关注部分包括形成mtgase的底物的酰基受体和位于经重塑的抗体中的提供酰基供体用于转酰胺化反应的所关注的谷氨酰胺残基和/与所述酰基受体和所述谷氨酰胺残基连接。此反应中常用的酰基受体为伯胺。然而,最近的工作已经显示,可以使用包括末端-nh基团的其它酰基受体,即α效应亲核体,如肼、酰肼和烷氧基胺(chio等人,2020.《德国应用化学(angew chem int ed engl)》59(33):13814-13820)。技术人员将理解,术语“α效应”是指由于存在具有孤对电子的相邻(α)原子而增加的原子的亲核性;在此上下文中,酰基受体的末端-nh的氮原子的亲核性增加。在一个实施例中,酰基受体选自胺,如伯胺;肼;酰肼;烷氧基胺或芳氧基胺。在一另外的实施例中,胺、肼、酰肼或氧基胺为芳基衍生物,具体地,任选取代的苯基或任选取代的苄基衍生物,例如,任选取代的苯肼。在一个实施例中,酰基受体为肼或酰肼。在一个实施例中,酰基受体为酰肼或任选取代的芳基肼衍生物。在一另外的实施例中,酰基受体为任选取代的芳基肼衍生物或任选取代的芳基酰肼衍生物。在一又另外的实施例中,酰基受体为任选取代的苯肼或任选取代的苯酰肼衍生物。
55、在一个实施例中,酰基受体包括选自以下的任选取代的部分:
56、
57、具体地
58、
59、*表示连接点。
60、可替代地,酰基受体包括选自以下的任选取代的部分:
61、
62、具体地
63、
64、在一另外的实施例中,酰基受体包括选自以下的任选取代的部分:
65、
66、具体地
67、
68、在一另外的替代性实施例中,酰基受体包括选自以下的部分:
69、
70、具体地
71、
72、在一个实施例中,芳基衍生物可以被多重取代,使得酰基受体通过多个连接点支化。
73、在一个实施例中,酰基受体包括选自以下的任选取代的部分:
74、
75、具体地
76、
77、*表示连接点。
78、可替代地,酰基受体包括选自以下的任选取代的部分:
79、
80、具体地
81、
82、具体实例包含:
83、
84、在一个实施例中,所述酰基受体选自实例1至12,具体地,实例3、4、7、8、11和12。
85、实例1至12中的叠氮化物基团可以被如下文所描述的用于两步反应的其它反应性基团(如bcn和dbco)取代。叠氮化物基团还可以被其它接头组分替代。
86、如本文所使用的,术语“胺”是指其中一个或多个氢原子已被如脂肪族(例如烷基或杂烷基)基团或芳香族(例如芳基或杂芳基)基团等取代基取代的氨的衍生物。伯胺的在氨中的三个氢原子中的仅一个氢原子被取代基取代。
87、如本文所使用的,术语“肼”是指其中氢原子中的一个氢原子已被如脂肪族(例如烷基或杂烷基)基团或芳香族(例如芳基或杂芳基)基团等取代基替代的肼的衍生物(h2n-nh2)。
88、如本文所使用的,术语“酰肼”是指其中氢原子中的一个氢原子已被如酰基、磺酰基或磷酰基(特别是酰基)等取代基替代的无机肼(h2n-nh2)的衍生物。
89、如本文所使用的,术语“烷基”是指具有至多20个碳原子的完全饱和支链或非支链烃部分。除非另有规定,否则烷基是指具有1个至16个碳原子、1个至10个碳原子、1个至7个碳原子或1个至4个碳原子的烃部分。烷基的代表性实例包含但不限于甲基、乙基、正丙基、异丙基、正丁基、仲丁基、异丁基、叔丁基、正戊基、异戊基、新戊基、正己基、3-甲基己基、2,2-二甲基戊基、2,3-二甲基戊基、正庚基、正辛基、正壬基、正癸基等。
90、如本文所使用的,术语“亚烷基”是指如上文所定义的具有1个至20个碳原子的二价烷基。其包括1个至20个碳原子,除非另有规定,否则亚烷基是指具有1个至16个碳原子、1个至10个碳原子、1个至7个碳原子或1个至4个碳原子的部分。亚烷基的代表性实例包含但不限于亚甲基、亚乙基、正亚丙基、异亚丙基、正亚丁基、仲亚丁基、异亚丁基、叔亚丁基、正亚戊基、异亚戊基、新亚戊基、正亚己基、3-甲基亚己基、2,2-二甲基亚戊基、2,3-二甲基亚戊基、正亚庚基、正亚辛基、正亚壬基、正亚癸基等。
91、如本文所使用的,术语“炔基”是指包括一个具有至多20个碳原子的三键的支链或非支链烃部分。除非另有规定,否则炔基是指具有2个至16个碳原子、2个至10个碳原子、2个至7个碳原子或2个至4个碳原子的烃部分。烷基的代表性实例包含但不限于乙炔基、丙炔基、丁炔基、戊炔基、己炔基、庚炔基、辛炔基、壬炔基、癸炔基等。
92、术语“杂烷基”在本领域具有其普通含义并且是指如本文所描述的其中一个或多个碳原子被杂原子(例如,氧、氮、硫)代替的烷基。
93、术语“芳基”是指在环部分中具有6-20个碳原子的芳香族烃基。通常,芳基是具有6-20个碳原子的单环、双环或三环芳基。
94、此外,如本文所使用的,术语“芳基”是指可以是单个芳香族环或多个稠合在一起的芳香族环的芳香族取代基。
95、非限制性实例包含苯基、萘基或四氢萘基,所述基团中的每一者可以任选地被1-4个取代基取代,所述取代基如烷基、三氟甲基、环烷基、卤素、羟基、烷氧基、酰基、烷基-c(o)-o-、芳基-o-、杂芳基-o-、氨基、硫醇、烷基-s-、芳基-s-、硝基、氰基、羧基、烷基-o-c(o)-、氨基甲酰基、烷基-s(o)-、磺酰基、磺酰胺基、苯基和杂环基。
96、如本文所使用的,术语“烷氧基”是指烷基-o-,其中烷基在上文中定义。烷氧基的代表性实例包含但不限于甲氧基、乙氧基、丙氧基、2-丙氧基、丁氧基、叔丁氧基、戊氧基、己氧基、环丙氧基-、环己氧基-等。通常,烷氧基具有约1-7个碳,更优选地,约1-4个碳。
97、如本文所使用的,术语“芳氧基”指--o-芳基和--o-杂芳基,其中芳基和杂芳基在本文中定义。
98、如本文所使用的,术语“杂芳基”是指具有1个至8个选自n、o或s的杂原子的5-14元单环或双环或三环芳香族环体系。通常,杂芳基是5-10元环体系(例如,5-7元单环或者8-10元双环)或5-7元环体系。典型杂芳基包含2-或3-噻吩基、2-或3-呋喃基、2-或3-吡咯基、2-、4-或5-咪唑基、3-、4-或5-吡唑基、2-、4-或5-噻唑基、3-、4-或5-异噻唑基、2-、4-或5-噁唑基、3-、4-或5-异噁唑基、3-或5-1,2,4-三唑基、4-或5-1,2,3-三唑基、四唑基、2-、3-或4-吡啶基、3-或4-哒嗪基、3-、4-或5-吡嗪基、2-吡嗪基和2-、4-或5-嘧啶基。
99、术语“杂芳基”还指杂芳香族环与一个或多个芳基、脂环族或杂环基环稠合的基团,其中自由基或连接点位于杂芳香族环上。非限制性实例包含1-、2-、3-、5-、6-、7-或8-吲哚嗪基、1-、3-、4-、5-、6-或7-异吲哚基、2-、3-、4-、5-、6-或7-吲哚基、2-、3-、4-、5-、6-或7-吲唑基、2-、4-、5-、6-、7-或8-嘌呤基、1-、2-、3-、4-、6-、7-、8-或9-喹嗪基、2-、3-、4-、5-、6-、7-或8-喹啉基、1-、3-、4-、5-、6-、7-或8-异喹啉基、1-、4-、5-、6-、7-或8-酞嗪基、2-、3-、4-、5-或6-萘啶基、2-、3-、5-、6-、7-或8-喹唑啉基、3-、4-、5-、6-、7-或8-噌啉基、2-、4-、6-或7-蝶啶基、1-、2-、3-、4-、5-、6-、7-或8-4ah咔唑基、1-、2-、3-、4-、5-、6-、7-或8-咔唑基、1-、3-、4-、5-、6-、7-、8-或9-咔啉基、1-、2-、3-、4-、6-、7-、8-、9-或10-菲啶基、1-、2-、3-、4-、5-、6-、7-、8-或9-吖啶基、1-、2-、4-、5-、6-、7-、8-或9-咟啶基、2-、3-、4-、5-、6-、8-、9-或10-菲咯啉基、1-、2-、3-、4-、6-、7-、8-或9-吩嗪基、1-、2-、3-、4-、6-、7-、8-、9-或10-吩噻嗪基、1-、2-、3-、4-、6-、7-、8-、9-或10-吩噁嗪基、2-、3-、4-、5-、6-或1-、3-、4-、5-、6-、7-、8-、9-或10-苯并异喹啉基、2-、3-、4-或噻吩并[2,3-b]呋喃基、2-、3-、5-、6-、7-、8-、9-、10-或11-7h-吡嗪并[2,3-c]咔唑基、2-、3-、5-、6-或7-2h-呋喃并[3,2-b]-吡喃基、2-、3-、4-、5-、7-或8-5h-吡啶并[2,3-d]-o-噁嗪基、1-、3-或5-1h-吡唑并[4,3-d]-噁唑基、2-、4-或54h-咪唑并[4,5-d]噻唑基、3-、5-或8-吡嗪并[2,3-d]哒嗪基、2-、3-、5-或6-咪唑并[2,1-b]噻唑基、1-、3-、6-、7-、8-或9-呋喃并[3,4-c]噌啉基、1-、2-、3-、4-、5-、6-、8-、9-、10-或11-4h-吡啶并[2,3-c]咔唑基、2-、3-、6-或7-咪唑并[1,2-b][1,2,4]三嗪基、7-苯并[b]噻吩基、2-、4-、5-、6-或7-苯并噁唑基、2-、4-、5-、6-或7-苯并咪唑基、2-、4-、4-、5-、6-或7-苯并噻唑基、1-、2-、4-、5-、6-、7-、8-或9-苯并噁啉基、2-、4-、5-、6-、7-或8-苯并噁嗪基、1-、2-、3-、5-、6-、7-、8-、9-、10-或11-1h-吡咯并[1,2-b][2]苯并氮杂基。典型稠合的杂芳基包含但不限于2-、3-、4-、5-、6-、7-或8-喹啉基、1-、3-、4-、5-、6-、7-或8-异喹啉基、2-、3-、4-、5-、6-或7-吲哚基、2-、3-、4-、5-、6-或7-苯并[b]噻吩基、2-、4-、5-、6-或7-苯并噁唑基、2-、4-、5-、6-或7-苯并咪唑基和2-、4-、5-、6-或7-苯并噻唑基。
100、杂芳基可以被1个至5个独立地选自由以下组成的组的取代基取代:
101、(a)烷基;
102、(b)羟基(或受保护的羟基);
103、(c)卤代;
104、(d)氧代,即,=o;
105、(e)氨基、烷基氨基或二烷基氨基;
106、(f)烷氧基;
107、(g)环烷基;
108、(h)羧基;
109、(i)杂环氧基,其中杂环氧基表示通过氧桥键合的杂环基;
110、(j)烷基-o-c(o)-;
111、(k)巯基;
112、(l)硝基;
113、(m)氰基;
114、(n)氨磺酰基或磺酰胺基;
115、(o)芳基;
116、(p)烷基-c(o)-o-;
117、(q)芳基-c(o)-o-;
118、(r)芳基-s-;
119、(s)芳氧基;
120、(t)烷基-s-;
121、(u)甲酰基,即,hc(o)-;
122、(v)氨基甲酰基;
123、(w)芳基-烷基-;以及
124、(x)被烷基、环烷基、烷氧基、羟基、氨基、烷基-c(o)-nh-、烷基氨基、二烷基氨基或卤素取代的芳基。
125、如本文所使用的,术语“酰基”是指其中碳原子被如脂肪族(例如烷基或杂烷基)基团或芳香族(例如芳基或杂芳基)基团等取代基取代的经取代的羰基。
126、如本文所使用的,术语“卤素”或“卤代”是指氟、氯、溴和碘。
127、如本文所使用的,除非另有规定,否则术语“任选取代的”是指未经取代的或被一个或多个(典型地,1个、2个、3个或4个)合适的非氢取代基取代的基团,所述非氢取代基中的每一者独立地选自由以下组成的组:
128、(a)烷基;
129、(b)羟基(或受保护的羟基);
130、(c)卤代;
131、(d)氧代,即,=o;
132、(e)氨基、烷基氨基或二烷基氨基;
133、(f)烷氧基;
134、(g)环烷基;
135、(h)羧基;
136、(i)杂环氧基,其中杂环氧基表示通过氧桥键合的杂环基;
137、(j)烷基-o-c(o)-;
138、(k)巯基;
139、(l)硝基;
140、(m)氰基;
141、(n)氨磺酰基或磺酰胺基;
142、(o)芳基;
143、(p)烷基-c(o)-o-;
144、(q)芳基-c(o)-o-;
145、(r)芳基-s-;
146、(s)芳氧基;
147、(t)烷基-s-;
148、(u)甲酰基,即,hc(o)-;
149、(v)氨基甲酰基;
150、(w)芳基-烷基-;以及
151、(x)被烷基、环烷基、烷氧基、羟基、氨基、烷基-c(o)-nh-、烷基氨基、二烷基氨基或卤素取代的芳基。
152、酰基受体可以包括间隔子部分,如聚乙二醇,例如具有1个至50个乙二醇单元(如1个至30个乙二醇单元)的聚乙二醇/可以与所述间隔子部分连接。合适的间隔子部分可以包含但不限于经取代的或未经取代的亚烷基或杂亚烷基链,碳链的长度(n)为例如选自2至20的整数。
153、酰基受体还可以包括药物-接头构建体的其它组分/可以与所述药物接头构建体的其它组分连接。在本领域中,多种接头技术可用于将如细胞毒素等药物与细胞粘合剂连接。接头可以并入各种不同的部分以帮助抗体-药物缀合物稳定并确定药物释放特性。例如,接头可以包含可切割部分,如可被组织蛋白酶b切割的部分(例如缬氨酸-丙氨酸或缬氨酸-瓜氨酸)。另一种策略是使用ph敏感性接头,由此核内体和溶酶体的较低ph分隔接头内的如腙、碳酸酯、甲硅烷基醚或硅烷醇等酸不稳定基团(例如-si(me2)-o-si(me2)-参见wo2016/183359)的水解。可替代地,接头可以是非可切割的,这可以避免或减少脱靶效应并提高循环期间的血浆稳定性。
154、在另一个实施例中,接头可以包含间隔子部分(如聚乙二醇),例如与酰基受体连接或以其它方式连接的间隔子部分,和/或经取代的或未经取代的亚烷基或杂亚烷基链,碳链的长度(n)是选自2至20的整数。间隔子部分还可以是用于增加所产生的缀合物的整体亲水性的亲水性间隔子,如-nh-so2-nh-(考虑到许多所关注药物可能是相当疏水性的)。
155、接头还可以包括与药物部分连接,使得药物可以在没有保留任何接头基团的情况下释放的自焚基团。此类基团的实例为对氨基苯甲醇(paba)和对氨基苄氧基羰基(pabc)。自焚是多组分化合物通过级联的环化或消除反应自发且不可逆地碎片化为小分子。在此上下文下,自焚基团是经历自焚的部分,并起到用于暂时地将可切割的保护基团(指定为“触发器”)与药物部分连接的接头的作用。自焚基团维触发器与药物部分之间的空间,并增强促进完全且无痕的脱保护的熵驱动力。
156、接头包含直链和支链构型。支链接头使多种活性剂能够通过抗体上的一个缀合点连接。各种支链接头描述于wo2016/183359中。支链接头包含支链peg接头,如支链peg叠氮化物和支链peg马来酰亚胺。
157、药物部分(d)可以是期望递送到靶细胞的任何合适的药物活性物质。实例包含细胞毒素,如紫杉烷、蒽环、喜树碱、埃博霉素(epothilone)、丝裂霉素(mytomycin)、康普瑞汀(combretastatin)、长春花生物碱(vinca alkaloid)、氮芥、马坦霉素(maytansinoid)、刺孢霉素(calicheamycin)、多卡霉素(duocarmycin)、微管溶素(tubulysin)、鹅膏蕈碱(amanitin)/鹅膏毒素、多拉司他汀(dolastatin)、澳瑞他汀(auristatin)、烯二炔、吡咯并苯并二氮杂卓、海鞘素(ecteinascidin)和乙烯亚胺。其它实例包含免疫刺激分子,如tlr激动剂(例如tlr7、tlr8和tlr9激动剂)和sting激动剂。在存在两个或更多个药物部分的一个实施例中,至少一个药物部分具有第一作用模式,并且至少一个药物部分具有第二不同的作用模式。例如,至少一个药物部分为免疫刺激分子,并且至少一个药物部分为细胞毒素。
158、药物接头可以在一个或多个步骤中与抗体连接。例如,在一步过程中,具有酰基受体部分的药物接头与具有mtgase的所关注抗体发生反应。
159、在一个实施例中,所产生的分子包括下式:(q)-nh-l-d;其中q为谷氨酰胺残基,所述谷氨酰胺残基存在于多肽的fc区中;nh源自酰基受体;l为接头,并且d为药物部分。
160、在具体实施例中,考虑到酰基受体的相关化学,所产生的分子可以包括下式的任一者:
161、(q)-nh-l-d 胺;
162、(q)-nh-ar-l-d 芳基胺;
163、(q)-nh-o-l-d 氨基氧基;
164、(q)-nh-o-ar-l-d 芳基氨基氧基;
165、(q)-nh-nh-c(o)-l-d 酰肼;
166、(q)-nh-nh-c(o)-ar-l-d 芳基酰肼;
167、(q)-nh-nh-l-d 肼;
168、(q)-nh-nh-ar-l-d 芳基肼;
169、(ar)表示任选取代的芳基,所述任选取代的芳基包含但不限于任选取代的苯基、任选取代的苄基和任选取代的苯甲酰基。
170、在一个实施例中,考虑到酰基受体的相关化学,所产生的分子包括选自以下的任选取代的部分:
171、
172、具体地
173、
174、*表示与接头的连接点。
175、可替代地,酰基受体包括选自以下的任选取代的部分:
176、
177、具体地
178、
179、在一另外的实施例中,酰基受体包括选自以下的任选取代的部分:
180、
181、具体地
182、
183、在一另外的替代性实施例中,酰基受体包括选自以下的部分:
184、
185、具体地
186、
187、在一个实施例中,芳基衍生物可以被多重取代,使得酰基受体通过多个连接点支化。
188、在具体实施例中,考虑到酰基受体的相关化学,所产生的分子可以包括下式的任一者:
189、(q)-nh-ar-(l-d)y 芳基胺;
190、(q)-nh-o-ar-(l-d)y 芳基氨基氧基;
191、(q)-nh-nh-c(o)-ar-(l-d)y芳基酰肼;
192、(q)-nh-nh-ar-(l-d)y芳基肼;
193、其中y为2、3、4或5,具体地,2、3或4,具体地,2或3,最具体地,2。
194、l和d在每次出现时可以是相同的或不同的。
195、可替代地,使用两步程序可能是方便的,由此酰基受体部分包含反应性基团(r),所述反应性基团使得所关注部分的其余部分(如药物接头)能够在第二步骤中基于与反应性基团的进一步反应而进行加成。在此实施例中,所关注部分的其余部分包括可以与r反应的互补反应性基团r'。
196、例如,在一个实施例中,r或r'是包括以下的部分:生物正交反应相容性反应性基团,例如未受保护或受保护的硫醇、环氧化物、马来酰亚胺、卤代乙酰胺、o-磷杂环戊二烯芳香族酯、叠氮化物、雷酸酯、磺酸酯、炔烃、氰化物、氨基-硫醇基、羰基、醛,通常地,能够形成肟和肼的任何基团、1,2,4,5-四嗪、降冰片烯、其它染色的或以其它方式电子激活的烯烃、经取代的或未经取代的环炔烃,通常地,通过生物正交环加成反应形成1,3-或1,5二取代的三唑、可以通过逆电子需求的狄尔斯-阿尔德(inverse electron demand diels-alder,iedda)反应进行反应的任何二烯或应变烯烃亲二烯体、受保护的或未受保护的胺、羧酸、醛、氧基胺的任何反应性基团。
197、例如,r或r'可以被选择以与如药物接头等所关注部分的与其余部分连接的互补反应性基团r'经受硫代-马来酰亚胺(或卤代乙酰胺)加成、施陶丁格连接(staudingerligation)、胡伊斯根1,3-环加成(huisgen 1,3-cycloaddition,点击反应)或狄尔斯–阿尔德环加成(diels-alder cycloaddition)。
198、在一个实施例中,所述反应性基团为卤代乙酰胺(例如溴-乙酰胺、碘-乙酰胺、氯-乙酰胺)。此类反应性基团在体内(和血清中)将比马来酰亚胺基团更稳定。在一个实施例中,反应性基团为能够进行“点击”反应的试剂。例如,1,3-偶极官能化合物可以在环化反应中与炔烃发生反应以形成杂环化合物,优选地在基本上不存在所添加的催化剂(例如,cu(i))的情况下。可以使用具有连接到其的至少一个1,3-偶极基团的各种化合物(具有含有4个在三个原子上离域的电子的三原子π电子体系)以与本文公开的炔烃发生反应。示例性1,3-偶极基团包含但不限于叠氮化物、氧化腈、硝酮、氧化偶氮基和酰基重氮基。
199、实例包含o-磷杂环戊二烯芳香族酯、叠氮化物、雷酸酯、炔烃(包含任何应变环炔烃)、氰化物、蒽、1,2,4,5-四嗪或降冰片烯(或其它应变环烯烃)。
200、在一个实施例中,r或r'为具有末端炔烃或叠氮化物的基团;此类部分描述于例如美国专利第7,763,736号中。
201、在一个实施例中,r或r'为经取代的或未经取代的环炔烃,如经取代的或未经取代的杂环应变炔烃。例如,r或r'可以为dbco(二苄基环辛基)基团或bcn(双环壬炔)基团。
202、如上文所描述的炔烃等炔烃可以在环化反应中与至少一种1,3-偶极官能化合物发生反应以形成杂环化合物,优选地在基本上不存在所添加的催化剂(例如,cu(i))的情况下。可以使用具有连接到其的至少一个1,3-偶极基团的各种各样的化合物(具有含有4个在三个原子上离域的电子的三原子π电子体系)以与本文公开的炔烃反应。示例性1,3-偶极基团包含但不限于叠氮化物、氧化腈、硝酮、氧化偶氮基和酰基重氮基。
203、因此,在一个实施例中,在过程的第一步之后,所产生的分子具有下式:(q)-nh-l1-r;其中q为谷氨酰胺残基,所述谷氨酰胺残基存在于多肽的fc区中;nh源自酰基受体;l1为任选的接头或间隔子部分,并且r为如上文所描述的反应性基团。然后,所述分子可以与包括r'的药剂(如r'-l2-d)发生反应,其中l2为任选的接头或间隔子部分,并且d为药物。因此,在此实施例中,就所所产生的产物而言,-l1-r-r'-l2-共同形成接头l,如上文所描述。因此,所产生的分子具有下式:(q)-nh-l1-r-r'-l2-d;其中q为谷氨酰胺残基,所述谷氨酰胺残基存在于多肽的fc区中;nh源自酰基受体;l1和l2独立地不存在,接头或间隔子部分(l1-r-r'-l2共同形成接头l,如上文所描述)(优选地l1和l2中的至少一者)并非不存在;并且d为药物部分。
204、关于上述单步骤过程,由于可以使用不同的酰基受体,因此具体实施例包含
205、(q)-nh-l1-r-r'-l2-d;
206、(q)-nh-ar-l1-r-r'-l2-d;
207、(q)-nh-o-l1-r-r'-l2-d;
208、(q)-nh-o-ar-l1-r-r'-l2-d;
209、(q)-nh-nhc(o)-l1-r-r'-l2-d;
210、(q)-nh-nhc(o)-ar-l1-r-r'-l2-d;
211、(q)-nh-nh-l1-r-r'-l2-d;
212、(q)-nh-nh-ar-l1-r-r'-l2-d。
213、(ar)表示任选取代的芳基,所述任选取代的芳基包含但不限于任选取代的苯基、任选取代的苄基和任选取代的苯甲酰基。
214、在具体实施例中,考虑到酰基受体的相关化学,所产生的分子可以包括下式的任一者:
215、(q)-nh-ar-(l1-r-r'-l2-d)y 芳基胺;
216、(q)-nh-o-ar-(l1-r-r'-l2-d)y 芳基氨基氧基;
217、(q)-nh-nh-c(o)-ar-(l1-r-r'-l2-d)y芳基酰肼;
218、(q)-nh-nh-ar-(l1-r-r'-l2-d)y芳基肼;
219、其中y为2、3、4或5,具体地,2、3或4,具体地,2或3,最具体地,2。
220、l1、r、r'和d在每次出现时可以是相同的或不同的。
221、参考上文给出的r和r'的实例,r-r'可以例如为硫代马来酰亚胺(或卤代乙酰胺)加成的加成产物,例如,ns二取代的3-硫代-吡咯烷-2,5-二酮;施陶丁格连接的加成产物,例如n,3-或n,4取代的5-二苯基氧化膦-苯甲酰胺;胡伊斯根1,3-环加成(点击反应)的加成产物,例如ns二取代的3-硫代-吡咯烷-2,5-二酮、1,4二取代的1,2,3-三唑、3,5二取代的异噁唑或3,5二取代的四唑;狄尔斯-阿尔德环加成加合物,例如o或n取代的5-降冰片烯-2-羧酸酯或酰胺、n取代的5-降冰片烯-2,3-二羧酸酰亚胺、o或n取代的7-氧代降冰片烯-5-羧酸酯或胺、或n取代的7-氧代降冰片烯-5,6-二羧酰亚胺与9取代的蒽或3取代的1,2,4,5-四嗪之间的2,4-环加成产物;逆电子需求的狄尔斯-阿尔德环加成加合物,例如经取代的环丙烯基与3取代的1,2,4,5-四嗪之间的2,4-环加成产物;或任何高产率的选择性酰胺化或酰亚胺化反应的加成产物。
222、r-r'的实例包含:
223、
224、其中(*)表示l1与l2或d的连接位点。r-r'可以处于相对于其与l1和l2或d的连接的任一朝向上。
225、第二药物接头在邻近的经重塑的n-糖基化位点处的缀合
226、可以使用已用endos处理以将其修剪回到核心glcnac的n-糖基化位点以进行第二缀合。
227、在一个实施例中,此过程包括使用针对核心glcnac部分的与反应性基团r(r的实例参见先前章节)连接的糖衍生物(如叠氮化物)的酶加成。半乳糖基转移酶是催化半乳糖残基从经激活的糖核苷酸供体udp-gal加成为α1-3-、α1-4-、β1-3-或β1-4-键中的受体的酶。在一个具体实施例中,所述酶是β-1-4-半乳糖基转移酶(galt),如具有y298l突变的突变版本(ramakrishnan和qasba,2002,《生物化学杂志(the journal ofbiologicalchemistry)》277(23):20833-20839)。其它所关注的galt突变体包含galt y289n、galty289i、galt y289f、galt y289m、galt y289v、galt y289g、galt y289i和galt y289a。
228、通用术语“糖”在本文中用于表示单糖,例如葡萄糖(glc)、半乳糖(gal)、甘露糖(man)和岩藻糖(fuc)。术语“糖衍生物”在本文中用于表示单糖的衍生物,即包括取代基和/或官能团的单糖。
229、在一个实施例中,糖衍生物与反应性基团r一起是源自糖的糖衍生物su(a)x-p或包括x个官能团a的糖衍生物su,并且p为核苷单磷酸或二磷酸(p为用于酶促反应的糖衍生物底物的一部分,但其在反应期间被消耗以使糖衍生物su(a)x与核心glcnac残基链接)。糖衍生物su(a)x包括一个或多个官能团a。在su(a)x包括两个或更多个官能团a时,每个官能团a是独立选择的,即,一个su(a)x可以包括不同的官能团a。在一个实施例中,a独立地选自由以下组成的组:叠氮基、酮基和炔基,并且其中x为1、2、3或4;并且p为核苷单磷酸或二磷酸,如选自由以下组成的组的核苷单磷酸或二磷酸:尿苷二磷酸(udp)、鸟苷二磷酸(gdp)和胞苷二磷酸(cdp)。在一另外的实施例中,糖衍生物su(a)x优选地源自半乳糖(gal)、甘露糖(man)、n-乙酰葡糖胺(glcnac)、葡萄糖(glc)、n-乙酰半乳糖胺(galnac)、葡糖醛酸(gcu)、岩藻糖(fuc)和n-乙酰神经氨酸(唾液酸),具体地源自由以下组成的组:glcnac、glc、gal和galnac。在一又另外的实施例中,su(a)x源自gal或galnac,具体地,su(a)x源自galnac。
230、在一个实施例中,su(a)x中的一个或多个官能团a存在于糖或糖衍生物su的c2和/或c6上。
231、在a为叠氮基时,a通常与c2、c3、c4或c6键合。如上所描述的,su(a)x中的一个或多个叠氮化物取代基可以与糖或糖衍生物s的c2、c3、c4或c6而非羟基(oh)基团键合,或者在6-叠氮藻糖(6-azfuc)的情况下,而非与氢原子键合。可替代地或另外,氨基糖衍生物的n-乙酰基取代基可以被叠氮乙酰基取代基取代。在一个实施例中,su(a)x选自由以下组成的组:2-叠氮基乙酰胺基半乳糖(galnaz)、6-叠氮基-6-脱氧半乳糖(6-azgal)、6-叠氮基-6-脱氧-2-乙酰胺基半乳糖(6-azgalnac)、4-叠氮基-4-脱氧-2-乙酰胺基半乳糖(4-azgalnac)、6-叠氮基-6-脱氧-2-叠氮基乙酰胺基半乳糖(6-azgalnaz)、2-叠氮基乙酰胺基葡萄糖(glcnaz)、6-叠氮基-6-脱氧葡萄糖(6-azglc)、6-叠氮基-6-脱氧-2-乙酰胺基葡萄糖(6-azglcnac)、4-叠氮基-4-脱氧-2-乙酰胺基葡萄糖(4-azglcnac)和6-叠氮基-6-脱氧-2-叠氮基乙酰胺基葡萄糖(6-azglcnaz),具体地选自由以下组成的组:galnaz、6-azgal、6-azgalnac、4-azgalnac、glcnaz和6-azglcnac。
232、在a为酮基时,典型地,a与su的c2而非oh基键合。可替代地,a可以与氨基糖衍生物(优选地2-氨基糖衍生物)的n原子键合。糖衍生物然后包括-nc(o)r3取代基。r3优选地为任选取代的c2-c4烷基。
233、在一个实施例中,r3为乙基。在一另外的实施例中,su(a)选自由以下组成的组:2-脱氧-(2-氧代丙基)半乳糖(2-酮基gal)、2-n丙酰基半乳糖胺(2-n-丙酰基galnac)、2-n-(4-氧代戊酰基)半乳糖胺(2-n-levgal)和2-n-丁酰基半乳糖胺(2-n-丁酰基galnac),更优选地,2-酮基galnac和2-n-丙酰基galnac。
234、在a为炔基(具体地末端炔基或(杂)环炔基)时,典型地,所述炔基存在于2-氨基糖衍生物上。其中a为炔基的su(a)x的实例为2-(丁-3-炔酸胺基)-2-脱氧-半乳糖。
235、在一具体实施例中,su(a)x-p选自由以下组成的组:galnaz-udp、6-azgal-udp、6-azgalnac-udp、4-azgalnaz-udp、6-azgalnaz-udp、6-azglc-udp、6-azglcnaz-udp、2-酮基gal-udp、2-n-丙酰基-galnac-udp和2-(丁-3-炔酸胺基)-2-脱氧-半乳糖-udp。最具体地,s(a)x-p为galnaz-udp、4-azgalnac-udp或6-azgalnac-udp。
236、式su(a)x-p的若干种化合物是本领域已知的,其中核苷单磷酸或核苷二磷酸p与糖衍生物su(a)x连接。例如,wang等人,《欧洲化学杂志(chem.eur.j.)》2010,16,13343-13345;piller等人,《美国化学学会化学生物学杂志(acs chem.biol.)》2012,7,753;piller等人,《生物有机与药物化学快报(bioorg.med.chem.lett.)》2005,15,5459-5462;wo 2009/102820;wo2014/065661;wo2015/057063;wo2015/057065;以及wo2021/015622(所有文献都通过引用引入本文)公开了许多化合物su(a)x-p以及其合成。
237、适于使核心glcnac部分与包括反应性基团的糖衍生物在存在galt的情况下发生反应的条件描述于例如ep2,911,699;wo2016/022027;以及wo2016/170186中,所述文献全部通过引用并入本文。
238、在其中过程包括使用针对核心glcnac部分的与反应性基团r连接的糖衍生物的酶促加成并且其中糖衍生物与反应性基团r一起为如上文所定义的糖衍生物su(a)x-p的一个实施例中,所产生的含fc的多肽(如抗体)包括以下中的一种或多种:(n)-g-s-r,其中n为天冬酰胺残基,所述天冬酰胺残基存在于多肽的fc区中;g为任选岩藻糖基化的glcnac n-聚糖核;s为糖衍生物;并且r为反应性基团,其中s-r是如上文所定义的糖衍生物su(a)x。技术人员将理解,在此上下文中,核苷单磷酸或二磷酸p不保留在包括反应性基团的所产生的含fc的多肽(如抗体)中。
239、然后,包括反应性基团(如叠氮化物基团)的所产生的含fc的多肽(如抗体)可以与包括r'反应性基团的第二所关注部分(如药物接头)缀合(例如,如上文所描述的针对第一药物接头的两步过程)。
240、在一个实施例中,所产生的含fc的多肽缀合物(如抗体缀合物)包括以下中的一种或多种:(n)-g-s-r-r'-l-d或其药学上可接受的盐或溶剂化物;其中n为天冬酰胺残基,所述天冬酰胺残基存在于多肽的fc区中;g为任选岩藻糖基化的glcnac n-聚糖核;s为糖衍生物;r-r'为反应性基团r与互补反应性基团r'之间的反应产物;l为接头;并且d为药物部分。
241、为了区分在第一次缀合期间连接的接头与在第二次缀合期间连接的接头,前者可以被称为la,并且后者可以被称为lb。
242、在一个实施例中,s-r为如上文所定义的su(a)x。
243、r-r'、l(la和lb)和d如上文所定义,用于其中谷氨酰胺残基为缀合位点的过程的第一步。对于第一缀合,d可以被称为d1,并且对于第二缀合,d可以被称为d2。d1和d2在两次缀合中可以相同或不同,即,相同以增加特定药物的药物-抗体比(dar),或者不同以允许将两种不同药物同时靶向同一细胞,如具有不同作用模式的药物(例如微管蛋白抑制剂和dna结合剂)。在一优选实施例中,用于第二缀合的r-r'通常将被选择为不同于用于第一缀合反应的r-r',以避免任何交叉反应,即在谷氨酰胺残基处的第一缀合中,r-r'为r1-r1';并且在天冬酰胺-glcnac处的第二缀合中,r-r'为r2-r2';并且r1不与r2'发生反应,并且r2不与r1'发生反应。
244、因此,与用于所关注部分在谷氨酰胺残基处的加成的第一过程组合,在一个实施例中,含fc的多肽缀合物(如抗体缀合物)包括:
245、(i)(q)-nh-la-d1或其药学上可接受的盐或溶剂化物;其中q为谷氨酰胺残基,所述谷氨酰胺残基存在于所述多肽的fc区中;la为接头;并且d为药物部分;以及
246、(ii)(n)-g-s-r-r'-lb-d2或其药学上可接受的盐或溶剂化物;其中n为天冬酰胺残基,所述天冬酰胺残基存在于多肽的fc区中;g为任选岩藻糖基化的glcnac n-聚糖核;s为糖衍生物;r-r'为反应性基团r与互补反应性基团r'之间的反应产物;lb为接头;并且d为药物部分;并且
247、其中所述天冬酰胺残基邻近所述谷氨酰胺残基。
248、对于(i),上文描述的关于tgase反应的所有酰基受体变体都包含在内。
249、在使用两个位点的情况下,在不需要galt介导的反应之前连接完整的第一所关注部分构建体,一个位点基于在谷氨酰胺残基处使用tgase,并且另一个位点基于天冬酰胺-glcnac位点处的galt介导的反应。例如,可以使用tgase以连接酰基受体反应性部分(r),并且然后可以使用galt介导的反应将糖衍生物和第二反应性r基团与天冬酰胺-glcnac n-聚糖核连接。如果两个位点的r基团和r'基团被选择为不同,并且不具有交叉反应性,则第一所关注部分和第二所关注部分可以在“一锅”反应中同时或依序(如果优选的话)加成。
250、因此,可以产生以下中间体,所述中间体为含fc的多肽(如抗体),所述含fc的多肽包括:
251、(i)(q)-nh-l1-r1;其中q为谷氨酰胺残基,所述谷氨酰胺残基存在于多肽的fc区中;l1不存在或者为接头或间隔子部分,如peg;并且r1为反应性基团;以及
252、(ii)(n)-g-s-r2,其中n为天冬酰胺残基,所述天冬酰胺残基存在于多肽的fc区中;g为任选岩藻糖基化的glcnac n-聚糖核;s为糖衍生物;并且r2为反应性基团;
253、其中所述天冬酰胺残基邻近所述谷氨酰胺残基。
254、然后此中间体可以与(i)r1'-l2-d1;以及(ii)r2'-l2-d2发生反应,其中r1'和r2'为分别与r1和r2发生反应的互补反应性基团,并且具体地,即,r1不与r2'发生反应且r2不与r1'发生反应。举例来说,r1可以为四嗪,并且r1'为反式环辛烯(tco);r2可以为叠氮化物,并且r2'为二苯并环辛炔(dbco)。
255、此中间体可以与(i)r1'-l2-d1;以及(ii)r2'-l2-d2同时或按任意顺序依序发生反应。
256、“药学上可接受的盐”旨在意指本发明化合物的游离酸或碱的盐,所述盐是无毒的、生物学上可耐受的或以其它方式在生物学上适于施用于受试者。通常参见,g.s.paulekuhn等人,“基于橙皮书数据库分析选择活性药物成分盐的趋势(trends inactive pharmaceutical ingredient salt selection based on analysis oftheorange book database)”,《药物化学杂志(j.med.chem.)》,2007,50:6665-72;s.m.berge等人,“药物盐(pharmaceutical salts)”,《药物科学杂志(jpharm sci.)》,1977,66:1-19;以及《药物盐手册:特性、选择和用途(handbook ofpharmaceutical salts,properties,selection,and use)》,stahl和wermuth编辑,苏黎世的威利出版社和黑体化学学报(wiley-vch and vhca,zurich),2002。
257、药学上可接受的盐的实例是在药理学上有效并且适于与受试者的组织接触而没有过度的毒性、刺激或过敏反应的盐。本发明的化合物可以具有足够酸性的基团、足够碱性的基团或两种类型官能团,并因此可以与许多无机或有机碱以及无机和有机酸发生反应,以形成药学上可接受的盐。
258、药学上可接受的酸加成盐可以用无机酸和有机酸形成,例如乙酸盐、天冬氨酸盐、苯甲酸盐、苯磺酸盐、溴化物/氢溴化物、碳酸氢盐/碳酸盐、硫酸氢盐/硫酸盐、樟脑磺酸盐、氯化物/盐酸盐、氯茶碱、柠檬酸盐、乙二磺酸盐、富马酸盐、葡庚糖酸盐、葡糖酸盐、葡萄糖醛酸盐、马尿酸盐、氢碘化物/碘化物、羟乙基磺酸盐、乳酸盐、乳糖酸盐、十二烷基硫酸盐、苹果酸盐、马来酸盐、丙二酸盐、扁桃酸盐、甲磺酸盐、甲基硫酸盐、萘甲酸盐、萘磺酸盐、烟酸盐、硝酸盐、十八烷酸盐、油酸盐、草酸盐、棕榈酸盐、双氢萘酸盐、磷酸盐/磷酸氢盐/磷酸二氢盐、聚半乳糖醛酸盐、丙酸盐、硬脂酸盐、琥珀酸盐、磺基水杨酸盐、酒石酸盐、甲苯磺酸盐、三氟乙酸盐和三氟甲基磺酸。
259、可以衍生盐的无机酸包含例如盐酸、氢溴酸、硫酸、硝酸、磷酸等。可以衍生盐的有机酸包含例如乙酸、丙酸、乙醇酸、草酸、马来酸、丙二酸、琥珀酸、富马酸、酒石酸、柠檬酸、苯甲酸、扁桃酸、甲磺酸、乙磺酸、甲苯磺酸、三氟甲基磺酸、磺基水杨酸等。药学上可接受的碱加成盐可以用无机碱和有机碱形成。
260、可以衍生盐的无机碱包含例如元素周期表第i列至第xii列的铵盐和金属。在某些实施例中,所述盐衍生自钠、钾、铵、钙、镁、铁、银、锌和铜;具体地合适的盐包含铵盐、钾盐、钠盐、钙盐和镁盐。
261、可以衍生盐的有机碱包含例如伯胺、仲胺和叔胺,经取代的胺(包含天然存在的经取代的胺)、环胺、碱性离子交换树脂等。某些有机胺包含异丙胺、苄星(benzathine)、胆酸盐、二乙醇胺、二乙胺、赖氨酸、葡甲胺、哌嗪和氨丁三醇。
262、药学上可接受的盐的实例具体包含硫酸盐、焦硫酸盐、硫酸氢盐、亚硫酸盐、亚硫酸氢盐、磷酸盐、磷酸一氢盐、磷酸二氢盐、偏磷酸盐、焦磷酸盐、氯化物、溴化物、碘化物、乙酸盐、丙酸盐、癸酸盐、辛酸盐、丙烯酸盐、甲酸盐、异丁酸盐、己酸盐、庚酸盐、丙炔酸盐、草酸盐、丙二酸盐、琥珀酸盐、辛二酸盐、癸二酸盐、富马酸盐、马来酸盐、丁炔-1,4-二酸盐、己炔-1,6-二酸盐、苯甲酸盐、氯苯甲酸盐、甲基苯甲酸盐、二硝基苯甲酸盐、羟基苯甲酸盐、甲氧基苯甲酸盐、邻苯二甲酸盐、磺酸盐、二甲苯磺酸盐、苯乙酸盐、苯丙酸盐、苯丁酸盐、柠檬酸盐、乳酸盐、γ-羟基丁酸盐、乙醇酸盐、酒石酸盐、甲磺酸盐、丙磺酸盐、萘-1-磺酸盐、萘-2-磺酸盐和扁桃酸盐。
263、本发明的化合物或其药学上可接受的盐可以以溶剂化物的形式获得。溶剂化物包含由本发明化合物与一种或多种溶剂的相互作用或复合形成的溶剂,无论是呈溶液或固体或结晶形式。在一些实施例中,溶剂为水,并且溶剂化物为水合物。
264、药物组合物
265、本文所公开的包括一种或多种药物活性物质/药物的缀合物通常将经受一个或多个纯化步骤,例如,用于去除未使用的反应物和反应副产物的纯化步骤。此类纯化技术包含亲和纯化和尺寸排阻纯化中的一种或多种。然后可以将所产生的经纯化的缀合物与一种或多种药学上可接受的载体或稀释剂组合。这些缀合物通常包含以下中的一种或多种:缓冲剂,所述缓冲剂用于将ph维持在期望水平(如ph 5至ph 7);洗涤剂,如聚山梨酯;以及,尤其是在冻干制剂的情况下,冻干保护剂,如糖,例如蔗糖。
266、药物组合物可以用于治疗动物或人类受试者的疾病或病症,如增殖性病症,例如癌症。
本文地址:https://www.jishuxx.com/zhuanli/20241106/325494.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表