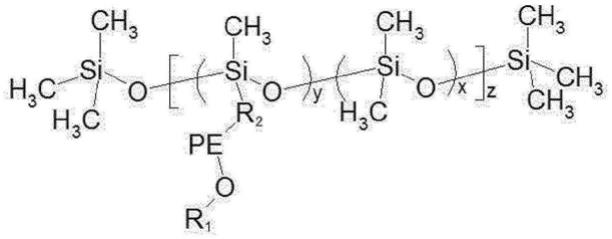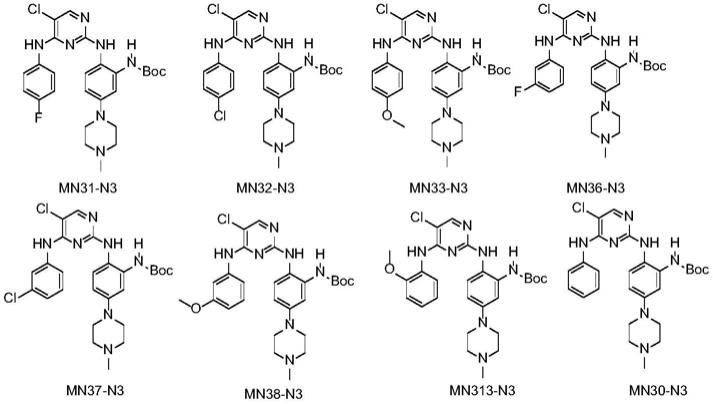
1.本发明涉及一种医药中间体(2-((5-氯-取代苯基氨基嘧啶-2-基)氨基)苯基)氨基甲酸叔丁酯类衍生物及合成方法。
背景技术:
2.成纤维细胞生长因子受体4(fgfr4)属于fgfr家族的四个受体酪氨酸激酶,其与成纤维细胞生长因子(fgf)相互作用,以调节关键的发育和生理过程[(a)turner,n.;grose,r.fibroblast growth factor signaling:from development to cancer.nat.rev.cancer 2010,10,116-129.(b)beenken,a.;mohammadi,m.the fgf family:biology,pathophysiology and therapy.nat.rev.drug discovery 2009,8,235-253.]。异常fgfr信号传导涉及许多癌症中,在非小细胞肺癌中包括fgfr1的生长障碍;fgfr2在胆管癌、子宫内膜和胃癌中;fgfr3在膀胱癌中;fgfr4在横纹肌肉瘤(rms)和肝细胞癌(hcc)中[(a)katoh,m.fibroblast growth factor receptors as treatment targets in clinical oncology.nat.rev.clin.oncol.2019,16,105-122.(b)ghedini,g.c.;ronca,r.;presta,m.;giacomini,a.future applications of fgf/fgfr inhibitors in cancer.expert rev.anticancer ther.2018,18,861-872.]。因此,已经进行了许多努力来鉴定fgfr抑制剂和多靶点激酶抑制剂(包括dovitinib,lenvatinib,regorafenib,sorafenib)[(a)roskoski,r.,jr.the role of fibroblast growth factor receptor(fgfr)protein-tyrosine kinase inhibitors in the treatment of cancers including those of the urinarybladder.pharmacol.res.2020,151,104567.(b)xue,w.-j.;li,m.-t.;chen,l.;sun,l.-p.;li,y.-y.recent developments and advances of fgfr as a potential target in cancer.future med.chem.2018,10,2109-2126.]。然而,fgfr抑制的程度导致这些多靶点抑制剂的安全性和功效性难以控制。已经开发了许多选择性泛fgfr抑制剂,其能够靶向激酶结构域内的atp结合位点,其可以被分为fgfr1-3激酶抑制剂[brameld,k.a.;owens,t.d.;verner,e.;venetsanakos,e.et al.discovery of the irreversible covalent fgfr inhibitor8-(3-(4-acryloylpiperazin-1-yl)propyl)-6-(2,6-dichloro-3,5-dimethoxyphenyl)-2-(methylamino)py rido[2,3-d]pyrimidin-7(8h)-one(prn1371)for the treatment of solid tumors.j.med.chem.2017,60,6516-6527.]。由于fgfr1-3激酶域具有高度同源性,因此基于结构的药物设计所获得抑制剂对fgfr1-3表现出良好的抑制作用。由于fgfr4的氨基酸序列与fgfr1-3存在较大差异,从而导致研发fgfr1-3抑制剂对fgfr4的抑制效果不佳。因此,选择性fgfr4抑制剂应运而生[bono,f.;de smet,f.;herbert,c.;de bock,k.;georgiadou,m.;fons,p.;tjwa,m.;alcouffe,c.et al.inhibition of tumor angiogenesis and growth by asmall-molecule multi-fgf receptor blocker with allosteric properties.cancer cell 2013,23,477-488.]。
[0003]
二苯胺基嘧啶类化合物是一类重要的氮杂环化合物,在医药和农药领域具有广泛用途。目前以二苯胺基嘧啶类为母核的抗肿瘤药物不断涌现,如2,4-二苯胺基嘧啶类小分子酪氨酸激酶抑制剂brigatinib、ceritinib、rilpivirine hydrochloride等合成一系列苯胺基嘧啶类化合物作为酪氨酸激酶抑制剂[(a)bartz,r.;fukuchi,k.;ohtsuka,t.;lange,t.;gruner,k.;watanabe,i.et al.abraham,r.preclinical development of u3-1784,a novel fgfr4 antibody against cancer,and avoidance of its on-target toxicity.mol.cancer ther.2019,18,1832-1843.(b)desnoyers,l.r.;pai,r.;ferrando,r.e.;k.;le,t.;ross,j.;carano,r.;d’souza,a.;qing,j.;mohtashemi,i.;ashkenazi,a.;french,d.m.targeting fgf19 inhibits tumor growth in colon cancer xenograft and fgf19 transgenic hepatocellular carcinoma models.oncogene 2008,27,85-97.]。可见以二苯胺基嘧啶为骨架的抗肿瘤化合物已引起科学家们的广泛关注。
技术实现要素:
[0004]
二苯胺基嘧啶母核是合成抗肿瘤化合物的关键中间体,在抗癌药,抗炎药,抗病毒药中该结构广泛存在且发挥着重要作用。
[0005]
本发明的(2-((5-氯-取代苯基氨基嘧啶-2-基)氨基)苯基)氨基甲酸叔丁酯类衍生物的结构式如下:
[0006][0007]
所述衍生物中典型结构包括如下:
[0008][0009]
所述(2-((5-氯-取代苯基氨基嘧啶-2-基)氨基)苯基)氨基甲酸叔丁酯类衍生物的合成路线如下:
[0010][0011]
其中,r1选自氢、c
1-5
烷基、c
3-6
环烷基、c
1-5
烷氧基、c
2-5
环氧烷基、哌啶基、哌嗪基、吗啉基、氰基、酯基、卤原子;
[0012]
r2为氢、c
1-5
烷基、c
1-3
烷氧基、c
3-6
环烷基、c
2-5
环氧烷基、卤原子、磺酰基、三氟甲基;
[0013][0014]
合成方法具体包括如下步骤:
[0015]
(2-((5-氯-取代苯基氨基嘧啶-2-基)氨基)苯基)氨基甲酸叔丁酯类衍生物的制备
[0016]
将化合物n2和m4放入装有溶剂的烧瓶中溶解,加入金属螯合配体和pd催化剂,在搅拌下加入碱性化合物制造碱性环境,在适宜温度下密封反应,tlc检测反应完成后,进行后处理,快速柱层析纯化,白色粉末固体。
[0017]
反应溶剂为二氯甲烷、二甲基亚砜、正丁醇、二甲苯、三氯甲烷、四氢呋喃、2-甲基四氢呋喃、乙醚、甲苯、苯、1,4-二氧六环、n-甲基吡咯烷酮、n,n-二甲基甲酰胺。优选为n,n-二甲基甲酰胺、二甲基亚砜、正丁醇、二甲苯、1,4-二氧六环;
[0018]
金属螯合配体为brettphos、ruphos、xphos、tbuxphos、me4tbuxphos、xantphos、tbubrettphos、sphos、davephos、johnphos、jackiephos,其中优选tbubrettphos、sphos、xphos、xantphos。
[0019]
钯为醋酸钯、氧化钯、四(三苯基膦)钯、三(二亚苄基丙酮)二钯、双(二亚苄基丙酮)钯、双(乙腈)氯化钯、二(三苯基膦)氯化钯、1,1-双(二苯基膦)二荗铁二氯化钯、[1,1'-双(二苯基膦)二茂铁]二氯化钯二氯甲烷络合物、二(氰基苯)二氯化钯、1,4-双(二苯基膦丁烷)二氯化钯,优选为:醋酸钯、氧化钯、四(三苯基膦)钯、三(二亚苄基丙酮)二钯、双(二亚苄基丙酮)钯、二(氰基苯)二氯化钯、1,4-双(二苯基膦丁烷)二氯化钯。
[0020]
反应温度60-130℃,优选80-100℃。
[0021]
化合物n2和m4,可根据现有技术进行制备。
[0022]
本发明得到中间体在用于制备蛋白酪氨酸激酶抑制剂,该类抑制剂用于作为癌症治疗药物。方面具有潜在的应用价值。
具体实施方式
[0023]
下面结合实施例对本发明做进一步说明,但本发明并不限于以下实施例。
[0024]
实施例1
[0025]
(5-氟-2-硝基苯基)氨基甲酸二叔丁酯(m2)的制备
[0026][0027]
将5-氟-2-硝基苯胺(10.95g,70.14mmol)和dmap(857mg,7mmol)加入80ml的dmf溶液中,向搅拌的反应液中加入二碳酸二叔丁酯(18.37g,7.01mmol),搅拌室温下反应4小时,tlc监控反应至完全,冰水析出,抽滤干燥得到黄色固体24.18g,产率97%。产物无需分离可直接进行下一步。1h nmr(400mhz,cdcl3)δ8.14(dd,j=9.1,5.4hz,1h),7.18(ddd,j=9.5,7.1,2.7hz,1h),7.04(dd,j=8.3,2.7hz,1h),1.40(s,18h).ms:356[m h]
[0028]
(5-(4-甲基哌嗪-1-基)-2-硝基苯基)氨基甲酸叔丁酯(m3)的制备
[0029][0030]
将m2(10g,28mmol)加入到80ml nmp中搅拌溶解,向搅拌的溶液中加入et3n(60mmol,8.5ml)和n-甲基哌嗪(30.8mmol,3.4ml),油浴110℃加热回流,反应8h。反应完毕,加入冰水析出,过滤,滤饼用石油醚洗涤,得到黄色固体9.4g,产率88%。1h nmr(400mhz,cdcl3)δ10.28(s,1h),8.13(d,j=9.7hz,1h),8.01(d,j=2.7hz,1h),6.48(dd,j=9.7,2.7hz,1h),3.60
–
3.46(m,4h),2.56(dd,j=6.9,3.4hz,4h),2.36(d,j=2.0hz,4h),1.54(d,j=1.2hz,9h).ms:337[m h]
。
[0031]
(2-氨基-5-(4-甲基哌嗪-1-基)苯基)氨基甲酸叔丁酯(m4)的制备
[0032][0033]
将m3(10g,29.6mmol)加入到80ml无水乙醇中溶解,加入干燥的钯碳(1g,9.4mmol),通入氢气保护下搅拌,室温下反应10h,结束反应。用硅藻土过滤钯碳,得到的滤液在在真空下干燥得到黑紫色固体8.4g,产率92%。1h nmr(400mhz,dmso-d6)δ10.28(s,1h),8.12(dd,j=9.7,1.7hz,1h),8.01(dd,j=2.9,1.5hz,1h),6.48(ddd,j=9.7,2.8,1.1hz,1h),3.51(dd,j=7.0,3.3hz,4h),2.85(d,j=1.2hz,2h),2.56(dd,j=6.9,3.4hz,4h),2.36(d,j=2.0hz,3h),1.54(d,j=1.2hz,9h).ms:307[m h]
。
[0034]
2,5-二氯-4-n-苯基嘧啶(n2)的制备
[0035]
[0036]
向乙醇(60ml)中加入2,4,5,三氯嘧啶(6g,33mmol)和苯胺(3.54g,38mmol),再加入na2co3(14g,132mmol),将混合物室温下搅拌反应5h。加水析出,抽滤得到滤饼,干燥得到白色固体(6.78g),产率86%。1h nmr(400mhz,dmso-d6)δ8.21(s,1h),7.68
–
7.60(m,2h),7.48
–
7.37(m,2h),7.29(d,j=4.0hz,1h),7.25
–
7.18(m,1h).ms:239[m h]
。
[0037]
(2-((5-氯-4-(苯基氨基)嘧啶-2-基)氨基)-5-(4-甲基哌嗪-1-基)苯基)氨基甲酸叔丁酯(mn30-n3)的制备
[0038][0039]
将化合物n2和m4放入装有溶剂的烧瓶中溶解,加入适量的金属螯合配体和pd催化剂,在搅拌下加入碱性化合物制造碱性环境,在适宜温度下密封反应,tlc检测反应完成后,进行后处理,快速柱层析纯化,白色粉末固体,产率52%。1h nmr(400mhz,dmso-d6)δ8.01(s,1h),7.72(dd,j=5.7,3.4hz,1h),7.63(s,1h),7.52
–
7.48(m,2h),7.23(d,j=8.0hz,1h),7.17(d,j=8.7hz,1h),7.08
–
7.03(m,2h),7.00(s,1h),6.62(dd,j=8.8,2.8hz,1h),6.46(s,1h),3.28
–
3.21(m,4h),2.58(t,j=5.0hz,4h),2.36(s,3h),1.45(s,9h).ms:509[m h]
。
[0040]
实施例2
[0041]
其他同实施例1的制备方法制备;
[0042]
(2-((5-氯-4-(苯基氨基)嘧啶-2-基)氨基)-5-(哌啶-1-基)苯基)氨基甲酸叔丁酯(mn10-n3)的制备(合成方法同mn30-n3);
[0043][0044]
白色固体,产率56%。1h nmr(400mhz,dmso-d6)δ8.68(s,1h),8.40(s,1h),8.22(s,1h),8.04(s,1h),7.69
–
7.62(m,2h),7.51
–
7.46(m,1h),7.29(d,j=8.8hz,1h),7.22(t,j=7.8hz,2h),7.17
–
7.12(m,1h),7.03(dd,j=8.1,6.6hz,1h),6.68(dd,j=8.8,2.8hz,1h),3.08(t,j=5.3hz,4h),1.69
–
1.58(m,6h),1.43(s,9h).ms:496[m h]
。
[0045]
实施例3
[0046]
其他同实施例1的制备方法制备;
[0047]
中间体mn11-n3:(2-((5-氯-4-((4-氟苯基)氨基)嘧啶-2-基)氨基)-5-(哌啶-1-基)苯基)氨基甲酸叔丁酯的制备(合成方法同mn30-n3)
[0048][0049]
黄色固体,产率49%。1h nmr(400mhz,dmso-d6)δ8.76(s,1h),8.35(s,1h),8.19(s,1h),8.03(s,1h),7.62(dd,j=8.8,5.1hz,2h),7.24(d,j=8.8hz,1h),7.15
–
7.11(m,1h),7.03(t,j=8.8hz,2h),6.67(dd,j=8.9,2.8hz,1h),3.12
–
3.04(m,4h),1.64
–
1.60(m,4h),1.53(d,j=4.5hz,2h),1.42(s,9h).ms:512[m h]
。
[0050]
实施例4
[0051]
其他同实施例1的制备方法制备;
[0052]
中间体mn18-n3:(2-((5-氯-4-((3-甲氧基苯基)氨基)嘧啶-2-基)氨基)-5-(哌啶-1-基)苯基)氨基甲酸叔丁酯的制备(合成方法同mn30-n3)
[0053][0054]
白色固体,产率59%。1h nmr(400mhz,dmso-d6)δ8.63(s,1h),8.41(s,1h),8.25(s,1h),8.05(s,1h),7.33(d,j=8.1hz,1h),7.30(d,j=8.8hz,2h),7.15
–
7.09(m,2h),6.64(ddd,j=14.9,8.5,2.6hz,2h),3.67(s,3h),3.07(t,j=5.3hz,4h),1.65
–
1.60(m,4h),1.56
–
1.51(m,2h),1.43(s,9h).ms:524[m h]
。
[0055]
实施例5
[0056]
其他同实施例1的制备方法制备;
[0057]
中间体mn20-n3:(2-((5-氯-4-(苯基氨基)嘧啶-2-基)氨基)-5-吗啉代苯基)氨基甲酸叔丁酯的制备(合成方法同mn30-n3)
[0058][0059]
黄色固体,产率54%。1h nmr(400mhz,dmso-d6)δ8.69(s,1h),8.43(s,1h),8.25(s,1h),8.05(s,1h),7.66(d,j=8.0hz,2h),7.48(d,j=7.5hz,2h),7.34(d,j=8.8hz,1h),7.23(t,j=7.8hz,2h),6.70(dd,j=8.9,2.8hz,1h),3.77
–
3.73(m,4h),3.05(dd,j=5.7,
3.8hz,4h),1.43(s,9h).ms:496[m h]
。
[0060]
实施例6
[0061]
其他同实施例1的制备方法制备;
[0062]
中间体mn21-n3:(2-((5-氯-4-((4-氟苯基)氨基)嘧啶-2-基)氨基)-5-吗啉代苯基)氨基甲酸叔丁酯的制备(合成方法同mn30-n3)
[0063][0064]
黄色固体,产率49%。1h nmr(400mhz,dmso-d6)δ8.78(s,1h),8.41(s,1h),8.23(s,1h),8.03(s,1h),7.63(dd,j=8.9,5.1hz,2h),7.30(d,j=8.8hz,1h),7.16(d,j=2.8hz,1h),7.04(t,j=8.7hz,2h),6.70(dd,j=8.9,2.8hz,1h),3.75(dd,j=5.9,3.7hz,4h),3.05(t,j=4.9hz,4h),1.42(s,9h).ms:514[m h]
。
[0065]
实施例7
[0066]
其他同实施例1的制备方法制备;
[0067]
中间体mn22-n3:(2-((5-氯-4-((4-氯苯基)氨基)嘧啶-2-基)氨基)-5-吗啉代苯基)氨基甲酸叔丁酯的制备(合成方法同mn30-n3)
[0068][0069]
黄色固体,产率51%。1h nmr(400mhz,dmso-d6)δ8.83(s,1h),8.38(s,1h),8.27(s,1h),8.06(s,1h),7.65(d,j=8.4hz,2h),7.27(d,j=8.8hz,1h),7.22(d,j=8.5hz,2h),7.20
–
7.16(m,1h),3.75(dd,j=6.0,3.5hz,4h),3.11
–
3.00(m,4h),1.41(s,9h).ms:530[m h]
。
[0070]
实施例8
[0071]
其他同实施例1的制备方法制备;
[0072]
中间体mn23-n3:(2-((5-氯-4-((4-甲氧基苯基)氨基)嘧啶-2-基)氨基)-5-吗啉代苯基)氨基甲酸叔丁酯的制备(合成方法同mn30-n3)
[0073][0074]
紫色固体,产率55%。1h nmr(400mhz,dmso-d6)δ8.62(s,1h),8.40(s,1h),8.15(s,1h),7.98(s,1h),7.53
–
7.44(m,2h),7.30(d,j=8.9hz,1h),7.13(d,j=2.5hz,1h),6.83
–
6.75(m,2h),6.68(dd,j=8.9,2.8hz,1h),3.74(dd,j=6.2,3.4hz,4h),3.72(s,3h),3.09
–
2.98(m,4h),1.42(s,9h).ms:526[m h]
。
[0075]
实施例9
[0076]
其他同实施例1的制备方法制备;
[0077]
中间体mn113-n3:(2-((5-氯-4-((2-甲氧基苯基)氨基)嘧啶-2-基)氨基)-5-(哌啶-1-基)苯基)氨基甲酸叔丁酯的制备(合成方法同mn30-n3)
[0078][0079]
白色固体,产率42%。1h nmr(400mhz,dmso-d6)δ8.40(s,1h),8.33(s,1h),8.14(s,1h),8.08(s,1h),7.99(s,1h),7.29(d,j=8.8hz,1h),7.16(s,1h),7.06(d,j=3.3hz,2h),6.79(s,1h),6.68(dd,j=8.8,2.8hz,1h),3.87(s,3h),3.09(t,j=5.3hz,4h),1.65(q,j=4.1,3.6hz,4h),1.54(q,j=5.9hz,2h),1.43(s,9h).ms:524[m h] 。
[0080]
本发明的合成方法有利于医药的探索和发现。
[0081]
以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明所述原则的前提下,本发明的实施方式还可以作出若干改进和修饰,这些改进和修饰也应视为本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。