一种英夫利昔单抗的定量检测方法
- 国知局
- 2024-07-30 11:17:47
本发明属于单抗检测,特别涉及一种英夫利昔单抗的定量检测方法。
背景技术:
1、英夫利昔(infliximab,又称英夫利西)单抗,为抗肿瘤坏死因子(tnfα)人-鼠嵌合单克隆抗体,作为tnfα拮抗剂,可与人体关键炎性因子tnfα的可溶形式和跨膜形式以高亲和力结合,抑制tnfα与受体结合,从而使tnfα失去生物活性,以避免其对人体组织产生的攻击作用。其适应症包括类风湿关节炎、成人及6岁以上儿童克罗恩病、瘘管性克罗恩病、强直性脊柱炎、银屑病及成人溃疡性结肠炎。1998年首次获fda批准在美国上市,2006年在国内获批上市,目前已有超过百万的患者接受了此药物的治疗。
2、然而,此药物同时也有较大的不良反应,常见呼吸道感染、头痛、肝功能异常、白细胞减少等,并会使得患者发生严重感染的风险增高甚至可导致死亡,这些风险与此抗体在人体内的血药浓度密切相关。而由于患者个体代谢差异的影响,患者间英夫利昔单抗的血药浓度有较大的差异,浓度过高则可能不良反应的风险增加,而浓度过低则可能导致治疗效果低下,而直接通过临床症状观察进行临床药物剂量优化有很大的局限性。另一方面,对于不同疾病甚至同一疾病不同治疗目标所需不同的英夫利昔单抗浓度。因此,为更好优化使用英夫利昔单抗,提高临床疗效,降低不良反应,推荐进行治疗药物监测。
3、目前已报道的测定人血样中英夫利昔单抗的方法绝大多数为酶联免疫吸附测定法等免疫学方法,相对液相色谱-串联色谱技术而言灵敏度低、特异性差、精密度差、分析范围窄,无法满足临床检验的实际需求。
技术实现思路
1、针对现有技术的缺陷,本发明所要解决的技术问题是提供一种英夫利昔单抗的定量检测方法。本发明能精确精准检测英夫利昔单抗,更符合临床对药物浓度监测的的实际需求。
2、本发明的一种英夫利昔单抗的检测方法,包括:利用液相色谱-串联质谱技术对待测样品进行检测,从而定量待测样品中英夫利昔单抗的含量;
3、其中液相色谱参数如下:
4、色谱柱:peptide xb-c18柱,100×2.1mm,粒径1.7μm;
5、流动相a:含0.1%甲酸的水;
6、流动相b:含0.1%甲酸的乙腈;
7、洗针液:50%甲醇;
8、采用梯度洗脱,流速为0.3ml/min,柱温为45℃,进样20μl;
9、其中质谱的条件包括:离子源:电喷雾离子源,正离子模式。
10、所述梯度洗脱包括:0-1.0min,流动相a体积分数保持90%,流动相b体积分数保持10%;1.0-7.5min,流动相a体积分数由90%下降至65%,流动相b体积分数由10%上升至35%;7.5-8.0min,流动相a体积分数由65%下降至10%,流动相b体积分数由35%上升至90%;8.0-10.0min,流动相a体积分数保持10%,流动相b体积分数保持90%;10.0-10.1min,流动相a体积分数由10%上升至90%,流动相b体积分数由90%下降至10%;保持流动相a和流动相b的体积分数到12.0min停止。
11、所述质谱的条件为:离子源:电喷雾离子源,正离子模式;毛细管电压:5500v;离子源温度(tem):500℃;离子源雾化气(gs1):55psi;离子源加热辅助气(gs2):50psi;气帘气(cur):30psi;碰撞气(cad):8psi;扫描模式:mrm。
12、质谱的化合物mrm扫描参数如下:
13、
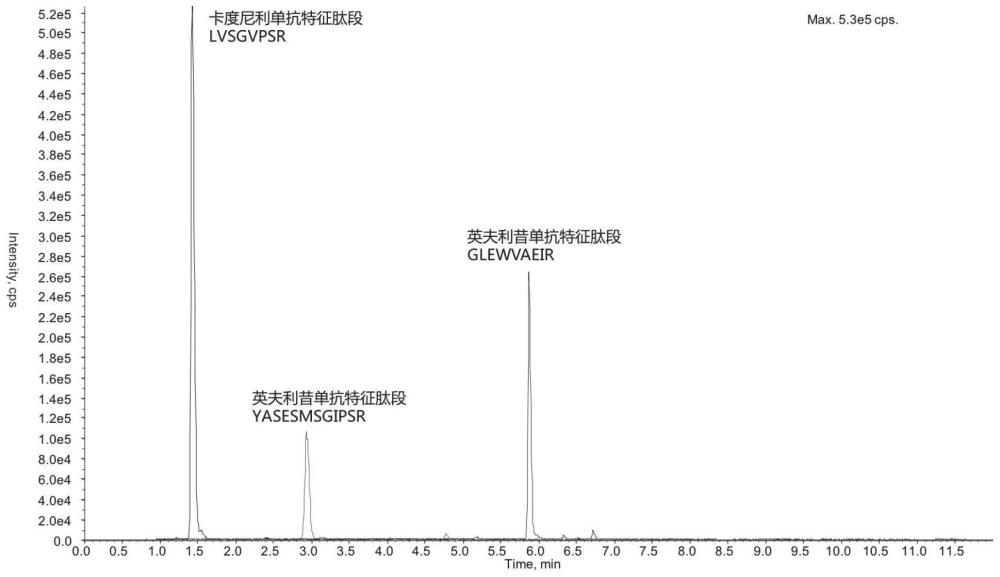
14、其中*标注为定量离子对;卡度尼利单抗作为内标。
15、所述待测样品为血清样品,对血清样本中的英夫利昔单抗进行磁珠富集、变性、酶解处理。
16、所述待测样品的制备包括:
17、(1)取proteing磁珠,加入pbs溶液清洗;
18、(2)向清洗完的磁珠中加入含0.05%吐温20的pbs溶液,再加入生物样品,再加入内标溶液,混匀;
19、(3)孵育1h,用含0.1%bsa的pbs溶液清洗,去离子水清洗;
20、(4)使用含0.25%的甲酸水溶液高速涡流,将单抗从磁珠上洗脱;
21、(5)取洗脱液,加入碳酸氢铵溶液,95℃振荡变性30min;
22、(6)将溶液晾至室温,向溶液中加入浓度为0.5mg/ml的胰酶溶液,37℃酶解2h;
23、(7)向酶解液中加入含甲酸的乙腈-水溶液,涡流混匀后离心,取上清进样分析。
24、所述步骤(2)中内标溶液为卡度尼利单抗的pbs溶液。
25、所述生物样品选自人血清样品。
26、进一步地,所述待测样品的制备方法:
27、(1)取60μlproteing磁珠,加入500μlpbs溶液清洗两次;
28、(2)向清洗完的磁珠中加入250μl含0.05%吐温20的pbs溶液,再加入20μl生物样本,再加入10μl内标溶液(50μg/ml卡度尼利pbs溶液),低速混匀;
29、(3)在滚轴混匀仪上孵育1h,依次用500μl含0.1%bsa的pbs溶液清洗两次,去离子水清洗两次;
30、(4)使用100μl含0.25%的甲酸水溶液高速涡流10min,将单抗从磁珠上洗脱;
31、(5)取90μl洗脱液,加入17μl 1mol/l的碳酸氢铵溶液,95℃振荡变性30min;
32、(6)将溶液晾至室温,向溶液中加入15μl浓度为0.5mg/ml的胰酶溶液,37℃酶解2h;
33、(7)向酶解液中加入23.3μl 50%乙腈-水溶液(含10%甲酸),涡流混匀后15000rpm离心5min,取上清进样分析。
34、所述检测方法还包括配制系列浓度标准品溶液;配制质控品溶液;然后分别进行磁珠富集、变性、酶解处理,然后采用液相色谱-串联质谱技术进行检测。
35、标准品溶液;配制质控品溶液的处理方法包括:
36、(1)根据标准品、质控品的量分别取proteing磁珠,分别加入pbs溶液清洗;
37、(2)分别向对应清洗完的磁珠中加入含0.05%吐温20的pbs溶液,加入标准品溶液、质控品溶液,再加入内标溶液,混匀;
38、(3)孵育1h,用含0.1%bsa的pbs溶液清洗,去离子水清洗;
39、(4)使用含0.25%的甲酸水溶液高速涡流,将单抗从磁珠上洗脱;
40、(5)取洗脱液,加入碳酸氢铵溶液,95℃振荡变性30min;
41、(6)将溶液晾至室温,向溶液中加入浓度为0.5mg/ml的胰酶溶液,37℃酶解2h;
42、(7)向酶解液中加入含甲酸的乙腈-水溶液,涡流混匀后离心,取上清进样液相色谱-串联质谱技术分析。
43、所述系列浓度标准品溶液的浓度为0.5~100μg/ml。
44、进一步地,所述标准品溶液的浓度为0.5μg/ml、1μg/ml、5μg/ml、10μg/ml、20μg/ml、50μg/ml、100μg/ml。
45、所述质控品溶液的浓度为0.5μg/ml、2μg/ml、15μg/ml、75μg/ml。
46、进一步地,所述标准曲线样品和质控品首先由混标储备液s0与空白基质稀释得到;所述混标储备液s0含英夫利昔单抗200μg/ml;所述空白基质为空白人血浆。
47、所述标准曲线工作液由s0与空白基质配制而成;充分混匀s0,用空白基质释得到s1、s2、s3、s4、s5、s6和s7;其中s7由50μls0和50μl空白基质组成;s6由25μl s0和75μl空白基质组成;s5由10μls0和90μl空白基质组成;s4由10μls0和190μl空白基质组成;s3由50μls4和50μl空白基质组成;s2由10μls4和90μl空白基质组成;s1由10μl s4和190μl空白基质组成。
48、所述质控品s0与空白基质配制而成;充分混匀s0,用空白基质稀释得到hqc、mqc、lqc和lloq;其中hqc由75μl s0和125μl空白基质组成;mqc由15μl s0和185μl空白基质组成;lqc由40μl mqc和260μl空白基质组成;lloq由50μl lqc和150μl空白基质组成。
49、有益效果
50、采用本发明的方法检测英夫利昔单抗的浓度,高灵敏度、高特异性,准确度与精密度满足要求,可用于血清中英夫利昔单抗的定量分析,为英夫利昔单抗浓度监测提供可靠的检测方法,从而对其临床用药进行指导作用。
本文地址:https://www.jishuxx.com/zhuanli/20240730/156104.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。