检测抗LAG-3抗体药物受体占位的方法与流程
- 国知局
- 2024-11-25 15:16:14
本申请涉及检测药物的受体占位率。具体地,本申请涉及检测抗lag-3抗体药物受体占位。
背景技术:
1、受体占位(ro)是评价药物与受体结合的重要研究内容,进行受体占位率研究是临床研究的重要内容,受体占位研究有助于验证药物的作用机理,选择最佳候选药物,并设计最佳给药剂量以保证临床研究的安全性及有效性。但该研究也面临许多技术和操作可行性方面的挑战。建立一个准确的可重复的ro方法需考虑诸多因素,如:选择合适的检测模式(直接法或间接法)、检测试剂、样品类型和目标细胞群等,还要充分考虑受体表达、受体调节以及样本稳定性等其他因素对实验结果的影响。
2、lag-3(淋巴细胞活化基因-3)属于免疫球蛋白超家族,主要表达在活化的t淋巴细胞。通过抑制lag-3及其配体分子的结合,可促进t细胞的活化和杀伤功能,最终有效促进免疫系统对于肿瘤细胞的杀伤。
3、不同于一般的其它抗体类受体占位研究,抗lag-3抗体药物的受体占位属于难度很高的一种。该研究面临的挑战主要包括正常人靶点水平表达很低,基质干扰非常大,该类细胞类生物分析的变异度较大,导致结果会出现非常大的差异,无法获得有效的数据来建立可靠的方法。
4、目前针对lag-3靶点抗体药物还未发现有解决方法的报道,受困于该类方法的难题,很多该类药物无法提供受体占位的数据,无法为早期临床的安全性及有效性评价提供数据支持。
技术实现思路
1、第一方面,本申请提供了用于检测施用抗lag-3抗体药物后的受试者的血液样品中的所述抗lag-3抗体药物的受体占位率的方法,所述方法包括:
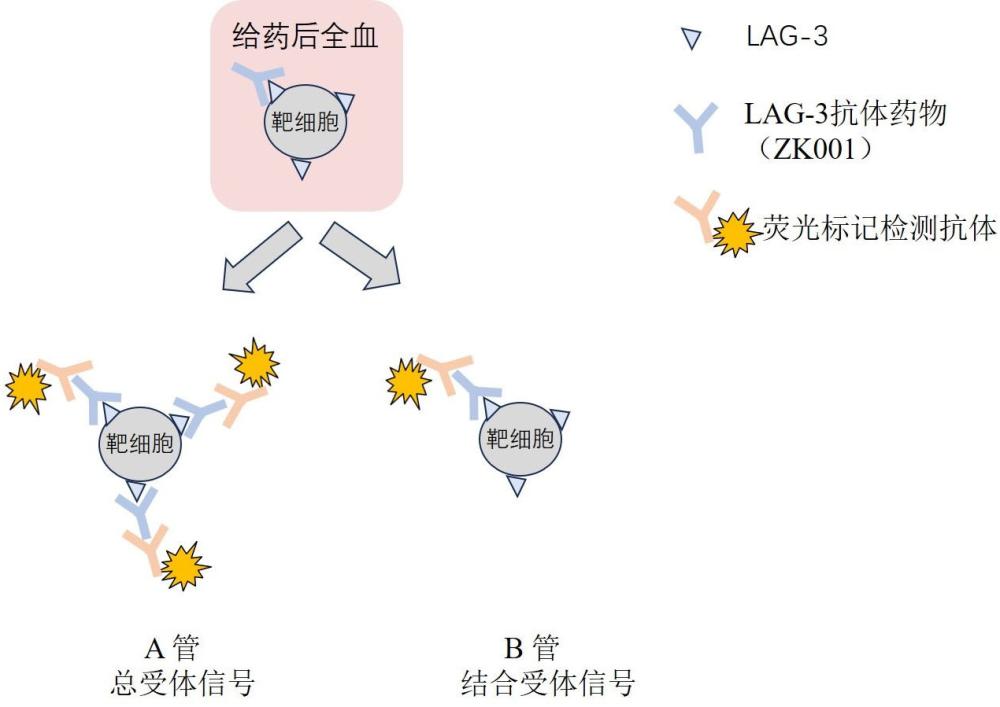
2、(1) 从所述血液样品获得白细胞数量基本相同的第一白细胞样品和第二白细胞样品,所述第一白细胞样品用于获得测试信号强度,所述第二白细胞样品用于获得总信号强度;其中,
3、获得所述测试信号强度包括:
4、(a) 向所述第一白细胞样品中加入带有可检测标记的所述抗lag-3抗体药物的检测抗体,所述检测抗体特异性针对所述抗lag-3抗体的igg亚型并与所述抗lag-3抗体药物的恒定区结合;
5、(b) 以单个细胞为检测单元,检测所述第一白细胞样品的可检测标记的信号强度,获得所述测试信号强度;
6、获得所述总信号强度包括:
7、(c) 向所述第二白细胞样品中加入足以饱和式结合所述第二白细胞样品中的白细胞上的lag-3靶点的量的所述抗lag-3抗体药物;
8、(d) 加入带有可检测标记的所述抗lag-3抗体药物的检测抗体;
9、(e) 以单个细胞为检测单元,检测所述第二白细胞样品的可检测标记的信号强度,获得所述总信号强度;
10、(2) 比较所述测试信号强度与所述总信号强度,以确定所述抗lag-3抗体药物的受体占位率。
11、在一些实施方案中,血液样品是全血样品,方法还包括在步骤(1)之前,对所述全血样品进行红细胞裂解处理,以获得白细胞。
12、在一些实施方案中,以1:20至1:40的体积比加入1%的氯化铵裂解液以进行红细胞裂解处理。
13、在一些实施方案中,以1:30的体积比加入1%的氯化铵裂解液以进行红细胞裂解处理。
14、在一些实施方案中,通过流式细胞术进行步骤(b)或步骤(e)。
15、在一些实施方案中,步骤(a)至步骤(b)先于步骤(c)至步骤(e)进行,或者步骤(a)至步骤(b)后于步骤(c)至步骤(e)进行,或者步骤(a)至步骤(b)同时与步骤(c)至步骤(e)进行。
16、在一些实施方案中,所述可检测标记是荧光标记试剂。
17、在一些实施方案中,所述可检测标记是af647、fitc、bv421或bv785。
18、在一些实施方案中,所述抗lag-3抗体药物是非igg1型抗体药物。
19、在一些实施方案中,所述抗lag-3抗体药物是igg4型抗体药物,且所述带有可检测标记的所述抗lag-3抗体药物的检测抗体是缀合af647的igg4型抗体的抗抗体。
20、在一些实施方案中,以单个细胞为检测单元检测白细胞样品的可检测标记的信号强度时,检测cd3阳性t细胞、cd8阴性t细胞或cd8阳性t细胞的可检测标记的信号强度。
21、在一些实施方案中,检测抗体包含5 μg/ml的fitc-cd45、0.5 ug/ml的bv421-cd3、1 ug/ml的bv785-cd8和1.65 ug/ml的af647-igg4。
技术特征:1.用于检测施用抗lag-3抗体药物后的受试者的血液样品中的所述抗lag-3抗体药物的受体占位率的方法,所述方法包括:
2.如权利要求1所述的方法,其中所述血液样品是全血样品,所述方法还包括在步骤(1)之前,对所述全血样品进行红细胞裂解处理,以获得白细胞。
3.如权利要求2所述的方法,其中以1:20至1:40的体积比加入1%的氯化铵裂解液以进行红细胞裂解处理。
4.如权利要求2所述的方法,其中以1:30的体积比加入1%的氯化铵裂解液以进行红细胞裂解处理。
5.如权利要求1所述的方法,其中通过流式细胞术进行步骤(b)或步骤(e)。
6.如权利要求1所述的方法,其中所述可检测标记是荧光标记试剂。
7.如权利要求1所述的方法,其中所述可检测标记是af647、fitc、bv421或bv785。
8.如权利要求1所述的方法,其中所述抗lag-3抗体药物是非igg1型抗体药物。
9.如权利要求1所述的方法,其中,
10.如权利要求1所述的方法,其中,
11. 如权利要求1所述的方法,其中所述检测抗体包含5 μg/ml的fitc-cd45、0.5 ug/ml的bv421-cd3、1 ug/ml的bv785-cd8和1.65 ug/ml的af647-igg4。
技术总结本申请涉及用于检测施用抗LAG‑3抗体药物后的受试者血液样品中的抗LAG‑3抗体药物的受体占位率的方法。技术研发人员:王芳,董立厚,刘兴娟,王变珍,孙云娟受保护的技术使用者:军科正源(北京)药物研究有限责任公司技术研发日:技术公布日:2024/11/21本文地址:https://www.jishuxx.com/zhuanli/20241125/337014.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表