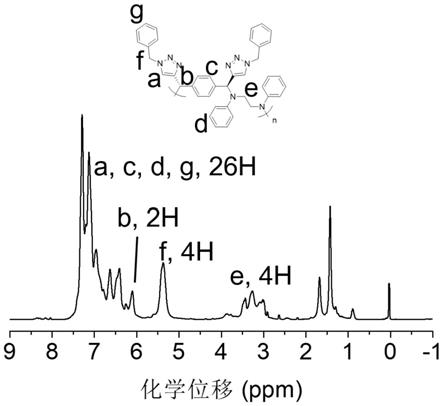
带电荷链接体及其在共轭反应上的应用
本案是申请日为2014年2月28日,发明名称为带电荷链接体及其在共轭反应上的应用,申请号为cn201480076320.3的案件的分案申请。
1.技术领域
1.本发明描述了一类应用于药物,特别是细胞毒素分子和生物分子共轭结合的新型带电荷链亚膦酸盐基团接体,同时描述了细胞结合分子-药物分子(细胞毒素分子)共轭体的制备方法。该方法可以是先用这类带电荷性链接体修饰药物分子,然后与细胞结合分子反应,也可以是先用链接体修饰细胞结合分子然后再与药物分子反应。
2.技术背景
2.靶向药物输送(muller,r;keck,c(2004).j.biotech.113,151),其目的是延长,定位,靶向和具有某一保护的药物与病变组织相互作用,在过去30年来已被进行了大量研究。目前有许多不同的药物输送工具,如,抗体,蛋白质,维生素,肽,聚合物胶束,脂质体,脂蛋白为基础的药物载体,纳米颗粒的药物载体,树枝状等。理想的药物释放工具必须是无毒、生物相容性、无免疫原性,可生物降解(scott,r;crabbe,d;et al(2008)expert opin.drugdeli.5,459)和避免宿主的防御机制的识别(saltzman,w.;torchilin,v.(2008).
″
drugdelivery systems
″
access science.mcgraw-hill co.)。药物在输送工具上的链接,特别是,抗体和细胞杀伤分子之间的链接起着至关重要的作用,在靶向给药系统的构建中起到决定性作用,因为连接体的性质显着影响着偶联物的疗效、选择性和它的药代动力学 (zhao,r.;wilhelm,s.et al,(2011)j.med.chem.36,5404;doronina,s.;mendelsohn,b.; et al,(2006)bioconjug chem,17,114;hamann,p.;hinman,l;et al.(2005)bioconjugchem.16,346)。已经有四类用于细胞结合分子-药物分子共轭体的联接体进入临床上应用: (a)酸不稳定联接体,它利用细胞核内和溶酶体内酸性微环境;(b)能被溶酶体蛋白水解酶切断的联接体;(c)化学特性稳定的硫醚联接体,抗体在细胞内被酶降解后可释放赖氨酰基加合物;(d)双硫键联接体,和细胞内被巯基接触后被切断(zhao,r.;wilhelm,s.et al, 2011j.med.chem.36,5404)。
3.细胞结合分子和药物分子或者各种修饰过的化合物通过上述各类链接体而形成的共轭体可见于各类文献(美国专利号4,680,338,5,122,368,5,141,648,5,208,020,5, 416,064;5,475,092,5,543,390,5,563,250 5,585,499,5,880,270,6,214,345,6,436, 931,6,372,738,6,340,701,6,989,452,7,129,261,7,375,078,7,498,302,7,507,420,7, 691,962,7,910,594,7,968,586,7,989,434,7,994,135,7,999,083,8,153,768,8,236, 319,zhao,r.;et al,(2011)j.med.chem.36,5404;doronina,s.;et al,(2006)bioconjugchem,17,114;hamann,p.;et al.(2005)bioconjug chem.16,346)。一般而言,在这些共轭体中,细胞结合分子首先被一种双功能团试剂,如spdp(n-琥珀酰亚胺3-(2-吡啶双硫)丙酸酯),或者smcc(琥珀酰亚胺-4-(n-马来酰亚胺甲基)环己烷-1-羧酸酯),或者spdb(n-琥珀酰亚胺4-(2-吡啶双硫)丁酸酯)所修饰,以引入活性双硫基或者琥珀亚胺基,然后和含巯基
的细胞毒素药物分子的反应生成共轭体,由此,细胞结合分子如单克隆抗体,就和药物分子通过双硫键或者硫醚键链接起来。
4.然而,细胞结合分子-药物分子共轭体,如抗体-药物共轭体(adc)在各种肿瘤治疗方法的开发上的应用受限于以下两方面:特殊靶向试剂(载体)的不可得以及当和载体相连接的药物分子数量增加时,现有的共轭结合方法容易形成蛋白质共聚体。通常当与疏水性的联接体进行共轭反应时,生成的细胞毒素药物共轭体发生聚合的问题最为严重。由于高的药物荷载意味着高的共轭体的内在活性,因此只要能保持载体蛋白的亲和性能不变,它上面荷载的药物分子越多越好。聚合蛋白质可能具有非特异性毒性,免疫原性的,因此必须在用于治疗用途之前除去,这样会使得生产的放大更加困难,也降低了其产率。
5.因此,改善现有的药物/毒素分子和载体(细胞结合分子)的共轭结合方法,通过运用新的带电荷性链接体以减少蛋白聚合,尽可能地提高药物分子的荷载量,成为一项非常迫切的需求。
3.发明总结
6.本发明描述了含亚膦酸盐基团带电荷链接体用于链接药物分子和细胞结合分子 (如抗体)链接。首选的共轭结构细胞结合分子-带电荷链接体-药物的分子式可以表达为: cb-(-l-drug)n,其中cb为细胞结合分子,l为带电荷链接体,drug为药物分子,n是1至20间的整数。在细胞-药物共轭体上应用带电荷链接体的优越性在于:a)减少了共轭体在水基介质中的聚合;b)能够实现更大的药物/细胞结合分子的比率,提高共轭体的活性;c)共轭体上药物-链接体断链后能停留在目标细胞内,对抗具有渗透性糖蛋白(pgp)表达的多药耐药性(mdr)细胞。
7.在一方面,本发明中的带电荷链接体可以表达为结构式(i),其中y可以和细胞结合分子反应,z与细胞毒素药物反应:
[0008][0009]
其中,y代表一种能与细胞结合分子反应的官能团;
[0010]
z指一种能与细胞毒素分子通过下列结构链接的官能团:双硫键,硫醚,硫酯,多肽,腙,醚,酯,氨基甲酸酯,碳酸酯,(二级三级或四级)胺,亚胺,环杂烷基,杂芳基,烷基肟或者酰胺;
[0011]
r1,r2,r3,r4,r5和r6为相同或不同的h,含1-6个碳原子的线性烷基,含3-6个碳原子的支链或环烷基,线性,支链或者环烯基,环炔基,或者含1-6个碳原子的酯,醚,酰胺或者具有(och2ch2)p结构式的聚乙二醇单元,其中p为从0至1000的整数,或者上述基团的组合。
[0012]
除此以外,r1,r2,r3和r4分别为从c,n,o,s,si和p中选取的原子组成的化学链,它们共价连接细胞表面结合配体,亚膦酸酯或磺酰基,药物分子,或者自己(r1,r2,r3和r4)。用于形成带电荷链接体的原子可以以任何在化学上可能的方式组合,比如形成亚烃基,亚烯基,亚炔基,醚,聚氧化烯烃基,酯,胺,亚胺,聚胺,联胺,腙,酰胺,脲,氨基脲,二肼羰,烷氧基胺,聚氨酯,氨基酸,多肽,酰氧胺,氧肟酸或者它们的组合。
[0013]
m为h,na,k或者n
r1r2r3或者一种药物学上的盐。r1,r2和r3的定义如上所述。
[0014]
另一方面,本发明描述了一类如结构式(ii)的细胞结合分子-药物分子共轭体。其中,细胞结合分子cb和药物分子drug分别在带电荷链接体的两端反应:
[0015][0016]
其中,cb代表细胞结合分子;n是1~12.
[0017]
drug代表通过带电荷链接体以下列官能团链接在细胞结合分子上的药物分子:双硫键,硫醚,硫酯,多肽,腙,醚,酯,氨基甲酸酯,碳酸酯,环杂烷基,杂芳基,烷基肟或者酰胺;
[0018]
r1,r2,r3,r4,r5,r6和m的定义同结构式(i)所描述。
[0019]
进一步,本发明描述了一类如结构式(iii)的修饰过的细胞结合分子,它们由原始细胞结合分子cb与带电荷链接体反应生成,该链接体还含有一个能与药物分子继续反应的功能团z:
[0020][0021]
其中的取代基团定义同上文所述。
[0022]
更进一步,本发明描述了一类如结构式(iv)的修饰过的药物分子,它们由原始药物分子drug和带电荷链接体反应生成,该链接体还含有一个能与细胞结合分子继续反应的功能团y:
[0023][0024]
其中的取代基团定义同上文所述。
[0025]
本发明还描述了一种制备如结构式(ii)所示的共轭体的方法,其中的药物分子通过带电荷链接体与细胞结合分子相连接。
[0026]
本发明也描述了一种制备如结构式(iii)所示的,通过细胞结合分子与带电荷链接体反应得到修饰的细胞结合分子的方法。
[0027]
本发明还描述了一种制备如结构式(iv)所示的,通过药物分子与带电荷链接体反应得到修饰的药物分子的方法。
[0028]
4.附图说明
[0029]
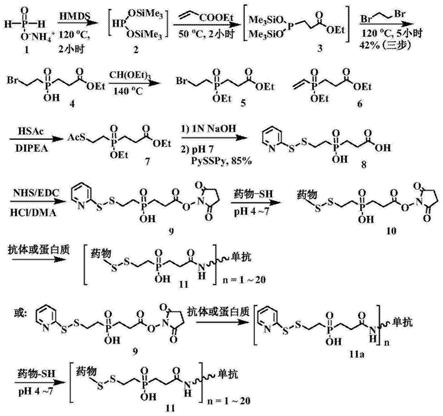
图1.展示含有吡啶双硫键和活性羧酸酯的亚膦酸盐链接体的合成及其与抗体的共轭链接。亚磷酸胺首先被转换成双(三甲基硅)膦酸酯,然后与丙烯酸酯进行迈克尔 (michael)加成反应,随后与过量的1,2-二溴乙烷发生取代反应生成(2-溴乙基)(3-乙氧基-3-氧丙烷基)次膦酸(4)。次磷酸首先被三乙氧基甲烷保护,然后溴乙基片段被硫代乙酸酯取代,碱性水解后再次与过量的2,2
’‑
二硫代二吡啶发生亲核取代。得到的酸(8)在缩合
剂edc的作用下,在酸性条件与n-羟基丁二酰亚胺(nhs)缩合,产生次磷酸链接体,用以制备抗体-小分子药物共轭体。
[0030]
图2展示含有吡啶双硫键和活性羧酸酯的次磷酸酯链接体的合成。该合成路线不进行次磷酸的保护,直接让硫代乙酸酯与溴乙基次磷酸酯或者羧基反应。获得的链接体可以通过双硫键和抗体偶联。
[0031]
图3展示含有活性羧酸酯和马来酰亚胺取代基的次磷酸酯链接体的合成,它可以通过硫醚键和抗体或蛋白质相连。
[0032]
图4展示通过1,4-二溴丁烷的取代反应制备含有吡啶双硫键和活性羧酸酯的次磷酸酯链接体。它可以通过双硫键和抗体或蛋白质相连。
[0033]
图5展示通过1,3-二溴丁烷的取代反应制备次磷酸酯链接体,它包含具有空间位阻的吡啶双硫键和活性羧酸酯,可以通过具有空间位阻的双硫键和抗体或蛋白质共轭相连。
[0034]
图6展示通过1,3-二溴-3-甲基丁烷的取代反应制备次磷酸酯链接体,它包含具有极大空间位阻的吡啶双硫键和活性羧酸酯。
[0035]
图7展示通过2-溴-2-甲基丁基次磷酸酯和乙基黄原酸钾的取代反应制备包含具有空间位阻的吡啶双硫键和活性羧酸酯的次磷酸酯链接体。
[0036]
图8展示通过次磷酸和双键的加成反应制备含有吡啶双硫键和活性羧酸酯的次磷酸酯链接体。它可以通过双硫键和抗体或蛋白质共轭相连。
[0037]
图9展示通过次磷酸和烯丙基丙二酸二乙酯的加成反应制备包含有位阻的吡啶双硫键和活性羧酸酯的次磷酸酯链接体。它可以通过有位阻的双硫键和抗体或蛋白质共轭相连。
[0038]
图10展示通过黄原酸和具有空间位阻的溴化物的取代反应制备包含具有位阻的吡啶双硫键和活性羧酸酯的次磷酸酯链接体。
[0039]
图11展示通过溴代烷烃和次磷酸铵的取代反应制备包含吡啶双硫键和活性羧酸酯的次磷酸酯链接体。
[0040]
图12展示含有活性羧酸酯和马来酰亚胺取代基的次磷酸酯链接体的合成,它可以通过硫醚键共轭连接细胞结合分子和药物。
[0041]
图13展示应用本专利次磷酸酯链接体制备抗体-链接体,双硫键被还原,然后与具有巯基反应活性的药物反应,合成抗体-药物共轭体。
[0042]
图14展示含有吡啶双硫基,聚乙二醇链和活性羧酸酯的次磷酸酯链接体的合成,它可以通过硫醚键共轭连接细胞结合分子。
[0043]
图15展示含有叠氮基和活性羧酸酯的次磷酸酯链接体的合成,它可以click反应共轭连接细胞结合分子和小分子药物。
[0044]
图16展示含有酮基和n-羟基琥珀酰亚胺脂的次磷酸酯链接体的合成,它可以通过腙键使细胞结合分子和小分子药物共轭连接。
[0045]
图17展示含有肼和马来酰亚胺基团的次磷酸酯链接体的合成,它可以通过腙键使抗体和小分子药物共轭连接。
[0046]
图18展示含有酮基和n-羟基琥珀酰亚胺脂的次磷酸酯链接体的合成,它可以通过腙键使细胞结合分子和含肼基的小分子药物共轭连接。
[0047]
图19展示含有氨基和马来酰亚胺基团的次磷酸酯链接体的合成,它可以通过硫醚键和酰胺键使抗体和小分子药物共轭连接。
[0048]
图20展示含有烷氧氨基和马来酰亚胺基团的次磷酸酯链接体的合成,它可以通过硫醚键和肟键使抗体和含酮或醛的小分子药物共轭连接。
[0049]
图21展示应用本专利带电荷链接体和典型的细胞毒性分子(tubulysin类,卡奇霉素类(calicbeamicin),美登素类(maytansinoid),阿里他汀类(auristatin),阿霉素类(doxorubicin),cc-105同系物,吡咯并苯二氮卓(pyrrolobenzodiazepine)二聚体)制得的抗体-药物共轭体。
[0050]
图21-a带电荷链接体通过硫醚键连接tubulysin同系物产生的adc结构。
[0051]
图21-b带电荷链接体通过双硫键连接tubulysin同系物产生的adc结构。
[0052]
图21-c带电荷链接体通过双硫键连接tubulysin同系物产生的adc结构。
[0053]
图21-d带电荷链接体通过腙键和双硫键连接卡奇霉素同系物产生的adc结构。
[0054]
图21-e带电荷链接体通过双硫键连接卡奇霉素同系物产生的adc结构。
[0055]
图21-f带电荷链接体通过硫醚键连接卡奇霉素同系物产生的adc结构。
[0056]
图21-g带电荷链接体通过双硫键连接美登素化合物dm1产生的adc结构。
[0057]
图21-h带电荷链接体通过硫醚键连接美登素化合物dm1产生的adc结构。
[0058]
图21-i带电荷链接体通过双硫键连接美登素化合物dm4产生的adc结构。
[0059]
图21-j带电荷链接体通过硫醚键和瓜氨酸-缬氨酸肽键连接单甲基阿里他汀e (mmae)产生的adc结构。
[0060]
图21-k带电荷链接体通过硫醚键和瓜氨酸-缬氨酸肽键连接单甲基阿里他汀f (mmaf)产生的adc结构。
[0061]
图21-1带电荷链接体通过硫醚键和瓜氨酸-缬氨酸肽键连接阿里他汀化合物 (mmaf-ome)产生的adc结构。
[0062]
图21-m带电荷链接体通过双硫键和瓜氨酸-缬氨酸肽键连接阿里他汀化合物 (mmaf-ome)产生的adc结构。
[0063]
图21-n带电荷链接体通过双硫键连接阿霉素化合物产生的adc结构。
[0064]
图21-o带电荷链接体通过腙键连接阿霉素化合物产生的adc结构。
[0065]
图21-p带电荷链接体通过腙键连接阿霉素化合物产生的adc结构。
[0066]
图21-q带电荷链接体通过肼基甲酸酯键连接cc-1065同系物产生的adc结构。
[0067]
图21-r带电荷链接体通过酰肼键连接吡咯并苯二氮卓二聚体前药产生的adc结构。
[0068]
图21-s带电荷链接体通过双硫键连接吡咯并苯二氮卓二聚体前药产生的adc结构。
[0069]
图21-t带电荷链接体通过双硫键连接吡咯并苯二氮卓(托马霉素)二聚体前药产生的adc结构。
[0070]
图21-u带电荷链接体通过烷基肟键连接吡咯并苯二氮卓二聚体前药产生的adc结构。
[0071]
图21-v带电荷链接体通过烷基肟键连接吡咯并苯二氮卓二聚体前药产生的adc结构。
[0072]
图21-w带电荷链接体通过烷基肟键连接吡咯并苯二氮卓二聚体前药产生的adc结构。
[0073]
图21-x带电荷链接体通过烷基肟键连接吲哚并苯二氮卓二聚体前药产生的adc结构。
[0074]
图21-y带电荷链接体通过多肽键连接多卡霉素同系物产生的adc结构。
[0075]
图22展示应用带电荷次磷酸酯链接体修饰细胞结合剂(抗her2抗体)和产生的相应细胞结合剂-药物共轭体。
[0076]
图23展示次磷酸酯链接体连接的具有不同药物荷载比的抗cd22-tz041的体外细胞毒性实验结果。图24展示tz041药物和抗体以亚膦酸盐链接体相连的共轭体结构。
[0077]
5.
技术实现要素:
[0078]
5.1.定义
[0079]“烷基”指一类含有1至8个碳原子的线性或者环状直链或者支链脂肪烃。支链指在线性的烷基上有一个或者多个低级烷基,比如甲基,乙基或者丙基相连接。烷基实施例包括甲基,乙基,正丙基,异丙基,正丁基,叔丁基,正戊烷基,3-戊烷基,辛烷基,壬烷基,癸烷基,环戊烷基,环己烷基,2,2-二甲基丁基,2,3-二甲基丁基,2,2-二甲基戊基,2,3-二甲基戊基,3,3-二甲基戊基,2,3,4-三甲基戊基,3-甲基己基,2,2-二甲基己基,2,4-二甲基己基, 2,5-二甲基己基,3,5-二甲基己基,2,4-二甲基戊基,2-甲基庚基,3-甲基庚基,正庚基,异庚基,正辛烷基和异辛烷基。c
1-c8烷基可以是未被取代或者被以下,但不限于以下的一个或者多个基团取代:c
1-c8烷基,c
1-c8烷氧基,芳基,-c(o)r’,-oc(o)r’,-c(o)or’,-c(o)nh2,-c (o)nhr’,-c(o)n(r’)
2-nhc(o)r’,-s(o)2r’,-s(o)r’,-oh,卤素(-f,-cl,-br,或-i),-n3,
‑ꢀ
nh2,-nh(r’),-n(r’)2及-cn;其中r’指各自独立的c
1-c8烷基或者芳基。
[0080]“c3~c8碳环”指含3,4,5,6,7,8个碳原子的饱和或不饱和的非芳烃环状化合物。典型的c
3-c8碳环包括,但不限于环丙基,环丁基,环戊基,环戊二烯基,环己基,环己烯基,1,3
‑ꢀ
环己二烯基,1,4-环己二烯基,环庚基,1,3-环庚二烯基,1,3,5-环庚三烯基,环辛基及环辛二烯基。c3~c8碳环可以是未被取代或者被以下,但不限于以下的一个或者多个基团取代: c
1-c8烷基,c
1-c8烷氧基,芳基,酰基,酰氧基,酯基,-c(o)nh2,-c(o)nhr’,-c(o)n(r’)2,-nhc (o)r’,-s(o)2r’,-s(o)r’,-oh,卤素(-f,-cl,-br,-i),-n3,-nh2,-nhr’,-n(r’)2及-cn;其中r’指各自独立的c
1-c8烷基或者芳基。
[0081]“c3~c8碳环基”指上述c3-c8碳环上其中一个氢原子被化学键所取代而产生的基团。
[0082]“杂环”指一类芳香性或者非芳香性含3至14个碳的杂环,其中环上1至4个碳原子各自独立地被杂元素,如o,n,s,se和p所取代。优选杂元素为o,n和s。相关杂环的说明亦可参见于the handbook of chemistry and physics,78
th
edition,crc press,inc..1997
‑ꢀ
1998,p.225至226,以及该书引述的文献内
[0083]
优选的非芳香杂环基包括但不限于吡咯烷基,吡唑烷基,咪唑烷基,环氧乙烷基,四氢呋喃基,二氧戊环基,四氢吡喃基,二氧杂环己烷基,哌啶基,哌嗪基,吗啉基,吡喃基,咪唑啉基,吡咯啉基,吡唑啉基,噻唑烷基,四氢硫吡喃基,二噻烷基,硫吗啉基,二氢吡喃基,四氢吡喃基,四氢吡啶基,二氢吡啶基,四氢嘧啶基,二氢硫吡喃基,氮杂环庚烷基以及
他们与苯基生成的稠环。
[0084]“烷基”,“环烷基”,“烯烃基”,“炔烃基”,“芳基”,“杂芳基”,“杂环”及诸如此类的术语也指由相应的烃失去两个氢原子生成的“亚烷基”,“环亚烷基”,“亚烯基”,“亚炔基”,“亚芳基”,“杂亚芳基”,“杂亚环”等。
[0085]
卤素原子指氟,氯,溴,碘原子,优选溴和氯。
[0086]“药学的”或者“药学上可接受的”指分子实体及组合物,视情形在动物或人体上应用时,不产生有害的,过敏性的或者其他不良反应。
[0087]“药学上可接受的辅料”包括所有载体,稀释剂,佐剂或者赋形剂,比如防腐剂,抗氧化剂,填料,崩解剂,润湿剂,乳化剂,悬浮剂,溶剂,分散介质,涂层,抗菌剂,抗真菌剂,等渗和吸收延缓剂,和类似这些的试剂等。在药物活性物质中加入这些介质和试剂在本领域是已知的。所有常规的介质和试剂,除非它们与药物活性组分不相容,在药物组合物里的应用也有被考虑。辅助活性组分也可以被加入中以获得合适的药物组合。
[0088]
在本发明中,“药用盐”指已经公开的化合物的一类衍生物,为母系化合物被修饰后产生的酸或碱加成盐。药学上可以接受盐包括从非毒性无机或者有机酸衍生的常规非毒性的盐以及季铵盐。这些成盐的无机酸包括盐酸,氢溴酸,硫酸,氨基磺酸,磷酸,硝酸等,有机酸如乙酸,丙酸,丁二酸,酒石酸,柠檬酸,甲磺酸,苯磺酸,葡萄糖醛酸,谷氨酸,苯甲酸,水杨酸,甲苯磺酸,草酸,富马酸,乳酸等。其他的加成盐包括由氨基丁三醇,甲葡胺,吡咯乙醇等生成的铵盐以及钠,钾,钙,锌,镁等金属盐。
[0089]
本发明中的药用盐可以从包含酸性或者碱性片段的母系化合物,用常规化学方法合成。通常,这些盐可以通过在这些化合物的游离酸或碱的水溶液或者有机溶液,或者两者的混合溶液中,加入等当量的适当的碱或酸,而反应生成。通常优选的非水相反应介质为醚,乙酸乙酯,乙醇,异丙醇或者乙腈。所有可适用盐的列表可参见于《瑞明顿的药物科学》第17版,马克出版公司,美国宾夕法尼亚州易斯顿,1985,第1418页(remington’spharmaceutical sciences,17
th
ed.mack publishing company,easton,pa,1985, p.1418),以及该书引述的文献内。
[0090]
本发明所描述的是应用亲水性亚磷酸盐链接体合成的新型共轭体,部分结构和它们的合成如图1至23所示。
[0091]
5.2.带电荷链接体
[0092]
本发明的亚磷酸盐带电荷链接体的合成路线以及由药物分子和细胞结合分子的制备共轭体的方法如图1-20所示。此带电荷链接体包含有三个部分:a)一种带电荷亚膦酸盐,b)能够与细胞结合分子反应的基团,如n-羟基琥珀酰亚胺酯,马来酰亚胺基,卤代乙酰基,酰肼,c)能够与药物分子反应的基团,比如,但不限于双硫基,马来酰亚胺,卤代乙酰基,醛,酮,叠氮化物,胺基,烷氧胺,酰肼。带电荷亚磷酸盐取代基可以用如下的方法引入:通过用市场上可获得的亚膦酸胺与丙烯酸酯进行迈克尔(michael)加成反应然后用过量的二溴烷烃取代生成。另外带电荷亚磷酸盐取代基可以如图11所示用亚磷酸盐对卤代烷烃双进行取代。更加具体的合成带电荷亚磷酸盐条件以及他们在细胞结合配体-药物共轭体制备的应用在图1-20中有进一步说明。
[0093]
优选的带电荷链接体为具有结构式(i)的化合物:
[0094][0095]
其中,y代表一种能与细胞结合分子反应的官能团;
[0096]
z代表一种能与细胞毒素分子通过下列结构链接的官能团:双硫键,硫醚,硫酯,多肽,腙,醚,酯,氨基甲酸酯,碳酸酯,二级三级或四级胺,亚胺,肟,环杂烷基,杂芳基,或者酰胺;
[0097]
m是h,或na,或k,或n
r1r2r3或一个药用的盐.
[0098]
r1,r2,r3,r4,和r5为相同或不同的h,含1-6个碳原子的线性烷基,含3-6个碳原子的支链或环烷基,线性,支链或者环烯基,环炔基,或者含1-6个碳原子的酯,醚,酰胺或者具有 (och2ch2)p结构式的聚乙二醇单元,其中p为从0至1000的整数,或者上述基团的组合。
[0099]
在另一实施例中,r1,r2,和r3分别为从c,n,o,s,si和p中选取的原子组成的化学链,它们共价连接细胞表面结合配体,亚膦酸酯,磺酰基或者亚砜,药物分子,和自己(r1,r2,和r3)。用于形成带电荷链接体的原子可以以任何在化学上可能的方式组合,比如形成亚烃基,亚烯基,亚炔基,醚,聚氧化烯烃基,酯,胺,亚胺,聚胺,联胺,腙,酰胺,脲,氨基脲,二肼羰,烷氧基胺,聚氨酯,氨基酸,酰氧胺,氧肟酸或者其他结构。另外,形成链接体的原子可以处于饱和或者不饱和状态,可以为自由基,可以在链接体内相互环化形成二阶环结构,包括环烷烃,环醚,环胺,亚芳烃,杂亚芳烃和他们的类似物等。
[0100]
能与细胞结合分子反应的官能团y的例子包括与胺反应基团,包括但不限于n-羟基琥珀酰亚胺酯,p-硝基苯基酯,双硝基苯基酯,五氟苯基酯;与巯基反应基团,包括但不限于吡啶双硫基,硝基吡啶双硫基,马来酰亚胺,卤代醋酸酯,羧酸卤化物。
[0101]
能链接细胞毒素药物分子的官能团z包含能与下列官能团成键的基团:双硫键,硫醚,硫酯,多肽,腙,酯,氨基甲酸酯,碳酸酯,烷基肟或者酰胺。这样的官能团包括,但不限于巯基,双硫基,氨基,羧基,醛,马来酰亚胺,卤代乙酰基,肼和羟基。
[0102]
在优选实施例中,r1,r2,和r3为含1-6个碳原子的线性烷基,或者具有(och2ch2)p结构式的聚乙二醇单元,p=1~100。
[0103]
结构式(i)中,含2-双硫-吡啶的链接体的合成如图1,2,4,5,6,7,8,9,10,11,13,和14所示;含马来酰亚胺的带电荷链接体的合成如图3和12所示;含聚乙二醇单元的带电荷链接体的合成如图14所示;含叠氮官能团,可以和炔烃进行huisgen 1,3-双极性环加成的带电荷链接体的合成如图15所示;含肼能生成易酸解键的带电荷链接体的合成如图16,17 和18所示;含烷氧胺片段,能生成烷基肟键的带电荷链接体的合成如图20所示。
[0104]
5.3细胞结合分子-药物分子共轭体
[0105]
本发明的共轭体可以用以下的结构式来表示:cb-(-l-drug)n,其中cb为细胞结合分子,l为带电荷链接体,drug为药物分子,n为1至20。
[0106]
带电荷链接体l可以由一个或者多个链接体单元所构成。这样的单元如6-马来酰亚胺己酰基(mc),马来酰亚胺丙酰基(mp),缬氨酸-瓜氨酸(val-cit或vc),丙氨酸-苯丙氨酸(ala-phe或af),p-氨基苄氧基羰基(pab),4-硫戊酸酯(spp),4-(n-马来酰亚胺甲基)环己基-1-羧酸酯(mcc),(4-乙酰)氨基苯甲酸酯(siab),4-硫-丁酸酯(spdb),4-硫-2-羟基磺
酰基-丁酸酯(2-sulfo-spdb),一个或多个乙烯氧基(-ch2ch2o-)单元(eo或peo)。其他的链接体单元在当前文献中已知,部分在本发明中也有描述。
[0107]
这些链接体单元的结构式如下所示:
[0108][0109][0110][0111][0112][0112][0113][0114][0115]
优选地,共轭体具有如(ii)的结构式:
[0116][0117]
其中,cb代表细胞结合分子;
[0118]
drug代表通过本发明中带电荷链接体,同下列官能团链接在细胞结合分子上的药物分子:双硫键,硫醚,硫酯,多肽,腙,醚,酯,氨基甲酸酯,碳酸酯,杂环烃,胺,亚胺,烷基肟或者酰胺;
[0119]
n为1-20;r1,r2,r3,r4,r5,和m的定义同结构式(i)所描述。
[0120]
如下文所详述,药物分子可以为各种小分子药物,包括但不限于,tubulysin,刺孢霉素(calicheamicin),阿里他汀类(auristatin),美登素类(maytansinoid),cc-105同系物,柔红霉素和阿霉素类(morpholinos)doxorubicin),紫杉醇类(taxane),cryptophycin, epothilone,苯二氮卓类(benzodiazepine)二聚物(如吡咯并苯二氮卓 (pyrrolobenzodiazepine)或托马霉素(tomaymycin)的二聚物)、吲哚啉并苯二氮卓 (indolinobenzodiazepine)、咪唑并苯二氮卓(imidazobenzothiadiazepine)或者恶唑烷并苯二氮卓(oxazolidinobenzodiazepine)的二聚体。
[0121]
在合成共轭体时,可以首先用本发明所描述的带电荷链接体修饰细胞结合分子,引入具有反应活性的双硫基团,马来酰亚胺,卤代乙酰基,叠氮化物,1-炔烃基,酮或者肼的官能团。以双硫键相连接的细胞结合分子-药物分子共轭体是通过修饰的细胞结合分子上的双硫键与药物分子上的自由硫醇进行硫交换而得到的。以硫醚键相连接的细胞结合分子-药物分子共轭体是通过修饰的细胞结合分子上的马来酰亚胺,卤代乙酰基或者乙基磺酰基与药物分子上的自由硫醇反应而得到的。含有对酸敏感的肼的共轭体的合成是用文献已知的方法(比如,p.hamann et al.,hinman,l.m.,et al,cancer res.53,3336-334, 1993;b.laguzza et al.,j.med.chem.,32;548-555,1959;p.trail et al.,cancer res., 57;100-105,1997)通过一个羰基基团和链接体上的肼反应而实现的。
[0122]
另外,药物分子可以首先与本专利所描述的带电荷链接体反应,产生一个如结构式(iv)的含有能与细胞结合分子反应的官能团的修饰药物。比如,含有巯基的药物可以与含有马来酰亚胺,卤代乙酰基或乙基磺酰基德如结构式(i)中的带电荷链接体在中性ph的水相中反应,而产生新的通过硫醚键连接有带电荷链接体的新的药物分子。含巯基的药物可以与带有吡啶双硫基片段的带电荷链接体进行双硫交换,产生通过双硫键连接有带电荷链接体的修饰药物分子。含羟基或巯基的药物还可以与本发明中含卤素的带电荷链接体在温和碱的作用下反应,产生含有醚或者硫醚的修饰药物分子。含有羟基的药物可以与结构式(i)中的带电荷链接体上的羧基缩合,在脱水剂(如hedc或者dcc)的作用下生成酯键。类似的,含有胺基的药物可以与结构式(i)中的带电荷链接体上的羧基缩合,成酰胺键。
[0123]
共轭体可以通过常规的生物化学的方法纯化,如sephadex g25或者sephacryls300柱凝胶过滤,吸附色谱,离子色谱或者渗析纯化。在某些情形下(如叶酸,黑素细胞刺激激素,egf等),细胞结合分子-药物共轭体可以通过柱色谱如hplc,中压柱色谱或者离子交换色谱而纯化。
[0124]
5.4修饰的细胞结合分子
[0125]
细胞结合分子通过本发明中的链接体被修饰,其结构如结构式(iii):
[0126][0127]
其中,所含有各取代基的同在前文中带电荷链接体体和共轭体里的描述。
[0128]
在优选的实施例中,z为双硫基,马来酰亚胺,卤代乙酰基或者n-羟基琥珀酰亚胺酯,cb通过硫醚,酰胺或者双硫键与r1相连接。用带电荷链接体同细胞结合分子反应修饰的细胞结合分子的制备如同已知的其他链接体修饰细胞结合分子相关文献中的各种方法(美
国专利号5,846,545,5,585,499,5,475,092,5,414,064,5,208,020,和4,563,304; carlsson,j.et al.biochem.j.(1978)173,723-737(1978);goff,d.a.,bioconjugatechem.(1990),1,381-386;l.delprino et al.j.pharm.sci.(1993),82,506-512; s.arpicco et al.,bioconjugate chem(1997),8,327-337)。
[0129]
优势上,由于带电荷链接体体上的亚膦酸盐可溶于水或者只需要少量的有机溶剂辅助即可溶解在水相,细胞结合分子和链接体的反应可以很便利地在水溶液里进行。首先链接体溶解在水相缓冲溶液中,或者含有少量(一般小于10%的体积比)可以与水互溶的极性有机溶剂,如各种醇(甲醇,乙醇,丙醇),二甲基甲酰胺(dmf),二甲基乙酰胺(dma),二甲亚砜(dmso)的缓冲液中,配成较高浓度的溶液,比如1-100mm,然后取适量的液滴加入含有细胞结合分子的水相缓冲溶液里。适量的液滴指的是能够在每一个细胞结合分子上引入1 至10个,优选1至5个链接体体的量,其体积不应当超过细胞结合分子体积的10%,最好不超过5%,最优是在0-3%以内。细胞结合分子缓冲水溶液ph在6至9,最优在6.5至7.5,可以包含任何适于调节ph值的非亲核性盐。典型的缓冲液体系包括磷酸,三乙醇胺盐酸,hepes和 mops,其中可以包含有额外的组分,如环糊精,蔗糖和盐,比如nacl和kcl。加入完成以后,反应在4至40度,最优是室温。反应的进程可以通过测量反应溶液在325nm或者其他合适波长的吸光度,进行监测。反应完成之后,修饰的细胞结合分子可以用常规的方法分离,比如凝胶过滤和吸附色谱分离。
[0130]
细胞结合分子的修饰可以通过测量反应释放的小分子基团的吸光度进行评价,比如硝基吡啶硫酮,双硝基吡啶双硫酮,吡啶硫酮,吡啶甲酰胺双硫酮和双吡啶甲酰胺双硫酮。图22描述了细胞结合分子her2抗体被本发明中一种带电荷链接体修饰的结果,链接体/ 抗体(l/a)的结合进程与链接的药物分子/抗体(d/a)一并显示。这里所描述的带电荷链接体包含有多种类的官能团,它们可以和任何具有合适基团的细胞结合分子反应。比如含有氨基或羟基的细胞结合分子可以与含n-羟基琥珀酰亚胺酯的链接体反应,含巯基的细胞结合分子可以与含马来酰亚胺或者卤代乙酰基的链接体反应,含羰基的细胞结合分子可以与含肼或者羟胺的链接体反应。有经验技术的操作者可以依据细胞结合分子上官能团的反应性,很容易地决定应当使用的链接体。
[0131]
5.5修饰的细胞毒素药物分子
[0132]
以本发明中的链接体所修饰的细胞毒素药物分子可以最好地用结构式(iv)表示:
[0133][0134]
其中各取代基的定义如前文所描述。
[0135]
在最优的实施例中,y是双硫键,马来酰亚胺,卤代乙酰基或者n-羟基琥珀酰亚胺酯。
[0136]
结构式如(iv)的修饰的药物分子可以通过药物和本发明中的链接体反应制备,它包含有一个能与细胞结合分子反应的官能团。比如,含巯基的药物分子可以和如结构式(i) 的含马来酰亚胺基团的链接体,在中性缓冲溶液中反应,得到一个通过硫醚键连接带电荷链接体的修饰药物分子。含巯基的药物分子也可以通过双硫交换反应和含吡啶双硫基团的
链接体反应,得到一个通过硫醚键连接带电荷链接体的修饰药物分子。含羟基的药物分子可以和含卤素原子的链接体,在弱碱存在时反应,得到一个含醚键的修饰药物分子。含羟基的药物分子也可以和如结构式(i)的含羧基的链接体,在脱水剂如二环己基碳化二亚胺 (dcc)存在时反应,得到一个含酯的修饰药物分子。含氨基的药物分子可以含羧基的链接体进行缩合反应,生成酰胺键。修饰的药物分子可以用标准方法纯化,如硅胶或氧化铝柱色谱,结晶,制备薄层色谱,离子交换色谱或者hplc。
[0137]
5.6细胞结合分子
[0138]
本发明所述构成共轭体的细胞结合体分子和修饰过的细胞结合分子可以是任何一种已知的或可知的能够与目标细胞上的位点结合、络合或反应的分子。目标细胞系指需要被治疗的或被原生物学上修饰的细胞。细胞结合体分子通过与目标细胞结合、络合或反应,细胞结合体分子把抗有丝分裂剂传送到目标细胞。
[0139]
细胞结合分子包括但不限于大分子量的蛋白,例如完整抗体(多克隆或者单克隆);单链抗体;抗体片段如fab,fab’,f(ab’)2,fv[parham,j.immunol.131,2895-10 2902 (1983)],fab表达库产生的片段,抗个体遗传型的抗体(anti-id),cdr’s,任何能与癌细胞的抗原表位、病毒抗原表位或微生物抗原表位特异结合或通过识别并结合特异抗原产生一系列生物活性的上述物的片段;(miller et al(2003)j.of immunology 170:4854-4861);干扰素(i,ii,iii型);多肽;淋巴因子如il-2,il-3,il-4,il-6,gm-csf,或ifn-γ;激素如胰岛素,促甲状腺激素释放激素(trh),黑素细胞刺激激素(msh),类固醇激素如雄激素,雌激素,或促黑激素(msh);生长因子和集落刺激因子如表皮生长因子(efg),粒细胞巨噬细胞集落刺激因子(gm-csf),转化生长因子(tgf)如tgfα,tgfβ,胰岛素和类胰岛素生长因子 (igf-i,igf-ii)g-csf,m-csf和gm-csf[burgess,immunology today,5,155-158(1984)] 等;疫苗生长因子(vgf);成纤维细胞生长因子(fgfs);小分子量蛋白,多肽,肽和肽激素,例如蛙皮素,胃泌激素和胃泌素释放肽;血小板源生长因子;白细胞介素和细胞因子如白细胞介素-2(il-2),白细胞介素-6(il-6),白血病抑制因子,粒细胞巨噬细胞集落刺激因子(gm
‑ꢀ
csf)和维生素如叶酸;脱辅基蛋白和醣蛋白如转铁蛋白[o’keefe et al,j.bio.chem.260, 932-927(1985)];糖结合蛋白或脂蛋白如凝集素;细胞营养传送分子;以及小分子抑制剂如前列腺特异性膜抗原(psma)抑制剂,小分子酪氨酸激酶抑制剂(tki),非肽或其它细胞结合分子或物质,例如生物活性高分子(dhar,et al,proc.natl.acad.sci.2008,105,17356
‑ꢀ
61),树形高分子(lee,et al,nat.biotechnol.2005,23,1517-26;almutairi,et al; proc.natl.acad.sci.2009,106,685-90),纳米颗粒(liong,et al,acs nano,2008,19, 1309-12;medarova,et al,nat.med.2007,13,372-7;javier,et al,bioconjugatechem.2008,19,1309-12),脂质体(medinai,et al,curr.phar.des.2004,10,2981-9),病毒衣壳(flenniken,et al,viruses nanotechnol.2009,327,71-93)。一般地说,如果有合适的单克隆抗体,单克隆抗体是最好的细胞结合体。抗体可以是鼠源、人源,经过人源化改造,嵌合类或者其他物种。
[0140]
本发明中抗体的生产方式包括其在生物体内、体外的产生过程或者三者的组合过程。抗受体肽段的的多克隆抗体的生产方法已是众所周知,如美国专利编号4,493,795 (nestor等)。制备单克隆抗体的经典方法是采用特定抗原免疫小鼠,分离得到的小鼠脾细胞与骨髓瘤细胞融合(g.;milstein,c.(1975).nature 256:495-497)。详细的操作
dacetuzumab(抗-cd40抗体),达利珠单抗(别名:赛尼哌,抗cd25(il-2受体的α链)抗体), daratumumab(抗-cd38(环化adp核糖水解酶)抗体),,狄诺塞麦(别名:prolia,抗rankl抗体),地莫单抗(抗b-淋巴瘤细胞抗体),阿托度单抗,dorlixizumab,ecromeximab(抗-gd3神经节苷脂抗体),依库丽单抗(别名:soliris,抗-c5抗体),埃巴单抗(抗内毒素抗体),依决洛单抗(别名:panorex,mab17-1a,抗-epcam抗体),依法利珠单抗(别名:raptiva,抗lfa-1 (cd11a)抗体),依芬古单抗(别名:mycograb,抗hsp90抗体),elotuzumab(抗slamf7抗体),伊斯利莫(抗il-6抗体),恩莫单抗(抗icam-1(cd54)抗体),epitumomab(抗episialin抗体),依帕珠单抗(抗-cd22抗体),erlizumab(抗itgb2(cd18)抗体),ertumaxomab(别名: rexomun,抗her2/neu,cd3抗体),伊瑞西珠(别名:abegrin,抗整合素αvβ3抗体),艾韦单抗(抗乙型肝炎表面抗原抗体),fanolesomab(别名:neutrospec,抗cd15抗体),法拉莫单抗 (抗干扰素受体抗体),farletuzumab(抗叶酸受体1抗体),felvizumab(抗呼吸道合胞病毒抗体),fezakinumab(抗il-22抗体),figitumumab(抗igf-1受体抗体),fontolizumab(抗 ifn-γ抗体),夫瑞韦如(抗狂犬病毒糖蛋白抗体),fresolimumab(抗tgf-β抗体),加利昔单抗(抗cd80抗体),gantenerumab(抗-β淀粉样蛋白抗体),gavilimomab(抗-cd147(basigin) 抗体),吉妥单抗(抗cd33抗体),girentuximab(抗碳酸酐酶9抗体),glembatumumab 5(别名:cr011,抗gpnmb抗体),戈利木单抗(别名:simponi,抗tnf-α抗体),gomiliximab(抗cd23 (ige受体)抗体),ibalizumab(抗cd4抗体),替伊莫单抗(抗cd20抗体),伊戈伏单抗(别名: indimacis-125,抗ca-125抗体),英西单抗(别名:myoscint,抗心肌肌球蛋白抗体),英夫利昔单抗(别名:英利昔单抗,抗tnf-α抗体),intetumumab(抗cd51抗体),伊诺莫单抗(抗cd25 (il-2受体α链)抗体),inotuzumab(抗cd22抗体),易普利姆玛(抗cd152抗体),iratumumab (抗cd30(tnfrsf8)抗体),keliximab(抗cd4抗体),labetuzumab(别名:cea-cide,抗cea抗体),lebrikizumab(抗il-13抗体),lemalesomab(抗nca-90(粒细胞抗原)抗体),乐德木单抗(抗tgfβ-2抗体),来沙木单抗(抗trail-r2抗体),利韦单抗(抗乙型肝炎表面抗原抗体),林妥珠单抗(抗cd33抗体),lucatumumab(抗cd40抗体),鲁昔单抗(抗cd23(ige受体)抗体), mapatumumab(抗trail-r1抗体),马司莫单抗(抗t-细胞受体抗体),马妥珠单抗(抗-egfr抗体),美泊利单抗(别名:bosatria,抗il-5抗体),metelimumab(抗tgfβ-1抗体), milatuzumab(抗cd74抗体),minretumomab(抗tag-72抗体),米妥莫单抗(别名bec-2,抗
‑ꢀ
gd3神经节苷脂抗体),morolimumab(抗恒河猴因子抗体),莫维珠单抗(别名:numax,抗呼吸道合胞病毒抗体),莫罗单抗-cd3(别名:okt30rthoclone,抗cd3抗体),他那可单抗(抗c242 抗体),他那莫单抗(抗5t4抗体),那他珠单抗(别名:tysabri,抗整合素α4抗体),奈巴库25 单抗(抗内毒素抗体),necitumumab(抗egfr抗体),nerelimomab(抗tnf-α抗体),尼妥珠单抗(别名:theracim,theraloc,抗egfr抗体),nofetumomab,ocrelizumab(抗cd20抗体),奥度莫单抗(别名:afolimomab,抗lfa-1(cd11a)抗体),木单抗(别名:arzerra,抗cd20抗体), olaratumab(抗pdgf-rα抗体),奥马珠单抗(别名:索雷尔,抗ige fc区抗体),oportuzumab (抗epcam抗体),奥戈伏单抗(别名:ovarex,抗ca-125抗体),otelixizumab(抗cd3抗体),帕吉昔单抗(抗脂磷壁酸抗体),帕利珠单抗(别名:synagis,abbosynagis,抗呼吸道合胞病毒抗体),帕尼单抗(别名:维克替比,abx-egf,抗-egfr抗体),panobacumab(抗绿脓杆菌抗体),pascolizumab(抗il-4抗体),pemtumomab(别名:theragyn,抗muc1抗体),帕妥珠单抗 (别名:omnitarg,2c4,抗her2/neu抗体),培克珠单抗(抗c5抗体),pintumomab(抗腺癌抗原
抗体),普立昔单抗(抗cd4抗体),普托木单抗(抗波形蛋白抗体),pr0140(抗ccr5抗体), racotumomab(别名:1e10,抗-(n-羟乙酰神经氨酸(neugc,ngna)-神经节苷脂gm3)抗体),瑞非韦鲁(抗狂犬病毒糖蛋白抗体),ramucirumab(抗vegfr2抗体),雷珠单抗(别名: lucentis,抗vegf-a抗体),瑞西巴库(抗炭疽毒素,保护性抗原抗体),瑞加韦单抗(抗巨细胞病毒的糖蛋白b抗体),reslizumab(抗il-5抗体),rilotumumab(抗hgf抗体),利妥昔单抗 (别名:美罗华,rituxanmab,抗cd20抗体),robatumumab(抗igf-1受体抗体),rontalizumab (抗ifn-α抗体),rovelizumab(别名:leukarrest,抗cd11,cd18抗体),ruplizumab(别名: antova,抗cd154(cd40l)抗体),沙妥莫单抗(抗tag-72抗体),司韦单抗(抗巨细胞病毒抗体),sibrotuzumab(抗fap抗体),sifalimumab(抗ifn-α抗体),siltuximab(抗il-6抗体),siplizumab(抗cd2抗体),(smart)mi95(抗cd33抗体),solanezumab(抗β-淀粉样蛋白抗体),sonepcizumab(抗神经鞘氨醇-1-磷酸抗体),索土珠单抗(抗episialin抗体),司他莫鲁(抗肌肉生长抑制素抗体),硫索单抗(别名:leukoscan,(抗-nca-90(粒细胞抗原)抗体))),tacatuzumab(抗α-甲胎蛋白抗体),他度珠单抗(抗整合素αiibβ3抗体),他利珠单抗 (抗ige抗体),他尼珠(抗ngf抗体),taplitumomab(抗cd19抗体),tefibazumab(别名: aurexis,抗聚集因子a抗体),阿替莫单抗,tenatumomab(抗固生蛋白c抗体),替奈昔单抗 (抗cd40抗体),teplizumab(抗cd3抗体),tgn1412(抗cd28抗体),ticilimumab(别名: tremelimumab(抗ctla-4抗体),tigatuzumab(抗trail-r2抗体),tnx-650(抗il-13抗体),托珠单抗(别名atlizumab,actemra,roactemra,(抗il-6受体抗体),toralizumab(抗cd154 (cd40l)抗体),托西莫单抗(抗cd20抗体),曲妥珠单抗(赫赛汀,(抗her2/neu蛋白抗体), tremelimumab(抗ctla-4抗体),tucotuzumab celmoleukin(抗epcam抗体),妥韦单抗(抗b 型肝炎病毒抗体),urtoxazumab(抗大肠杆菌抗体),优斯它单抗(别名:stelara,抗il-12, il-23抗体),伐利昔单抗(抗aoc3(vap-1)抗体),vedolizumab,(抗整合素α4β7抗体), veltuzumab(抗cd20抗体),维帕莫单抗(抗aoc3(vap-1)抗体,visilizumab(别名:nuvion,抗cd3抗体),vitaxin(抗血管整合素avb3抗体),volociximab(抗整合素α5β1),伏妥莫单抗 (别名:humaspect,抗肿瘤抗原ctaa16.88抗体),扎妥木单抗(别名:humax-egfr,(抗egfr抗体),zanolimumab(别名:humax-cd4,抗cd4抗体),ziralimumab(抗cd147(基础免疫球蛋白) 抗体),阿佐莫单抗(抗cd5抗体),依那西普(),阿法赛特(),阿巴西普(),利纳西普(arcalyst),14f7[抗irp-2(铁离子调节蛋白2)抗体],14g2a(抗gd2神经节苷脂抗体,治疗黑色素瘤和实体瘤,nat.cancer inst.),j591(抗 psma抗体,治疗前列腺癌,威尔康乃尔医学院),225.28s[抗hmw-maa(高分子量黑色素瘤相关抗原)抗体,索林radiofarmaci srl(意大利米兰)治疗黑色素瘤],col-1(抗ceacam3抗体,cgm1,nat.cancer inst.。美国用于治疗大肠癌和胃癌),cyt-356(,治疗前列腺癌),hnk20(oravax公司,用于治疗呼吸道合胞病毒),immurait(来自immunomedics治疗非霍奇金淋巴瘤),lym-1(抗hla-dr10抗体,百富勤医药,用于癌症),mak-195f[抗tnf抗体(又称:肿瘤坏死因子;tnfa,肿瘤坏死因子-α;tnfsf2),阿伯特/诺尔,用于治疗败血症中毒性休克],medi-500[别名:t10b9,抗cd3抗体,trαβ(t细胞受体α/β),复合物,medimmune公司用于治疗移植物抗宿主病],ring scan[抗tag72(肿瘤相关糖蛋白72抗体),neoprobe集团,用于治疗乳腺癌、结肠癌和直肠癌。avicidin(抗-epcam抗体(上皮细胞粘附分子),抗 tacstd1抗体(肿瘤相关钙信号转导1),抗ga733-2(胃肠肿瘤相关蛋白2),抗egp-2抗体(上皮糖蛋白
2);抗ksa抗体;ks1/4抗原;m4s;肿瘤抗原17-1a;cd326,来自neorx公司用于治疗结肠癌,卵巢癌,前列腺癌和非霍奇金淋巴瘤;lymphocide(immunomedics公司,nj),smartid10(protein design labs),oncolym(techniclone公司,加利福尼亚州),allomune (biotransplant,ca),抗vegf抗体(genentech公司,ca);ceacide(immunomedics公司,nj), imc-1c11(imclone,nj)和西妥昔单抗(imclone公司,美国新泽西州)。
[0150]
其它与配体结合的抗体,此抗体具有抗下述抗原(但不仅限于此):氨肽酶n (cd13),膜联蛋白a1,b7-h3(cd276,各种癌症),ca125,ca15-3(癌),ca19-9(癌),l6(癌), lewis y(癌),lewis x(癌),甲胎蛋白(癌),ca242,胎盘碱性磷酸酶(癌),前列腺特异性抗原(前列腺癌),前列腺酸性磷酸酶(前列腺),表皮生长因子(癌),cd2(霍奇金病,非霍奇金淋巴瘤的淋巴瘤,多发性骨髓瘤),cd3的ε(t细胞淋巴瘤,肺癌,乳腺癌,胃癌,卵巢癌,自身免疫性疾病,恶性腹水),cd19(b细胞恶性肿瘤),cd20(非霍奇金淋巴瘤),cd22(白血病,淋巴瘤,多发性骨髓瘤,系统性红斑狼疮),cd30(霍奇金淋巴瘤),cd33(白血病,自体免疫疾病),cd38(多发性骨髓瘤),cd40(淋巴瘤,多发性骨髓瘤,白血病),cd51(转移性黑素瘤,肉瘤),cd52(白血病),cd56(小细胞肺癌癌,卵巢癌,merkel细胞癌,以及液体肿瘤,多发性骨髓瘤),cd66e(癌症),cd70(转移性肾细胞癌和非霍奇金淋巴瘤),cd74(多发性骨髓瘤), cd80(淋巴瘤),cd98(癌症),粘蛋白(癌),cd221(实体瘤),cd227(乳腺癌,卵巢癌),cd262 (非小细胞肺癌和其他癌),cd309(卵巢癌),cd326(实体瘤),ceacam3(大肠癌,胃癌), ceacam5(癌胚抗原;cea,cd66e)(乳腺癌,结肠直肠癌和肺癌),dll3(δ状-3),egfr(表皮生长因子受体,各种癌症),ctla4(黑色素瘤),cxcr4(cd184,血红素肿瘤,实体肿瘤),内皮糖蛋白(cd105,实体瘤),epcam(上皮细胞粘附分子,膀胱癌,头,颈,结肠,前列腺非霍奇金淋巴瘤,和卵巢癌),erbb2(表皮生长因子受体2;肺癌,乳腺癌,前列腺癌),fcgr1(自身免疫性疾病),folr(叶酸受体,卵巢癌),gd2神经节苷脂(癌症),g-28(一种细胞表面抗原 glyvolipid,黑素瘤),独特型gd3(癌症),热休克蛋白(癌症),her1(肺,胃癌),her2(乳腺癌,肺癌和卵巢癌),hla-dr10(nhl),hla-drb(非霍奇金淋巴瘤,b细胞白血病),人绒毛膜促性腺激素(癌),igf1r(胰岛素样生长因子1受体,实体瘤,血液癌症),il-2受体(白细胞介素 2受体,t-细胞白血病和淋巴瘤),il-6r(白细胞介素6受体,多发性骨髓瘤,类风湿性关节炎,castleman病,il6依赖性肿瘤),整合素(αvβ3,α5β1,α6β4,αllβ3,α5β5,αvβ5细胞附着因子,对各种癌症),mage-1(癌),mage-2(癌),mage-3(癌),mage 4(癌),抗转铁蛋白受体 (癌),p97(黑色素瘤),ms4a1(跨膜域4亚科a成员1,非霍奇金b细胞淋巴瘤,白血病),muc1或 muc1-klh(乳腺癌,卵巢癌,子宫颈癌,支气管和胃肠道癌症),muc16(ca125)(卵巢癌),cea (大肠),gp100(黑色素瘤),mart1(黑色素瘤)mpg(黑色素瘤),ms4a1(跨膜域4蛋白a,小细胞肺癌,非霍奇金淋巴瘤),核仁,神经癌基因产物(癌),p21(癌),抗(n-羟乙酰神经氨酸,乳腺癌,黑色素瘤的癌症),plap样睾丸碱性磷酸酶(卵巢癌,睾丸癌),psma(前列腺肿瘤),psa (前列腺),rob04,tag 72(肿瘤相关糖蛋白72,白血病,胃癌,结肠直肠癌,卵巢癌)中,t细胞的跨膜蛋白(癌症),tie(cd202b),tnfrsf10b(肿瘤坏死因子受体超家族成员10b,癌症), tnfrsf13b(肿瘤坏死因子受体超家族成员13b,多发性骨髓瘤,非霍奇金淋巴瘤,以及其他癌症,类风湿性关节炎和系统性红斑狼疮),tpbg(滋养层糖蛋白,肾细胞癌),trail-r1(肿瘤坏死凋亡诱导配体受体1,淋巴瘤,非霍奇金淋巴瘤,大肠癌,肺癌),vcam-1(cd106,黑色素瘤),血管内皮生长因子,血管内皮生长因子-a,vegf-2(cd309)(各种癌症)。通过抗体识
别的一些其他的肿瘤相关抗原已审阅(gerber等,mabs 1:3,247-253(2009);novellino等, cancer immunol immunother.54(3),187-207(2005),franke等,cancerbiother.radiopharm.2000,15,459-76)。还有抗许多其他的抗原是:其他不同的集群(cd4, cd5,cd6,cd7,cd8,cd9,cd10,cd11a,cd11b,cd11c,cd12w,cd14,cd15,cd16,cdw17,cd18, cd21,cd23,cd24,cd25,cd26,cd27,cd28,cd29,cd30,cd31,cd32,cd33,cd34,cd35,cd36, cd37,cd38,cd41,cd42,cd43,cd44,cd45,cd46,cd47,cd48,cd49b,cd49c,cd53,cd54,cd55, cd56,cd58,cd59,cd61,cd62e,cd62l,cd62p,cd63,cd68,cd69,cd70,cd71,cd72,cd79, cd81,cd82,cd83,cd86,cd87,cd88,cd89,cd90,cd91,cd95,cd96,cd100,cd103,cd105, cd106,cd109,cd117,cd120,cd127,cd133,cd134,cd135,cd138,cd141,cd142,cd143,cd144,cd147,cd151,cd152,cd154,cd156,cd158,cd163,cd166,cd168,cd184,cdw186, cd195,cd202(a,b),cd209,cd235a,cd271,cd303,cd304),ap02,aslg659,bmpr1b(骨形态发生蛋白受体),cripto,膜联蛋白a1,核仁,内皮糖蛋白(cd105),robo4,氨基肽酶n,δ-样4 (dll4),vegfr-2(cd309),cxcr4 9cd184),tie2,b7-h3,wt1,muc1,lmp2,hpv e6e7, egfrviii,her-2/neu,her3,hla-dob(mhcii类分子ia抗原),整合素,irta2,mpf(mpf, msln,smr,巨核细胞强化因子,间皮素),cripto,sema 5b(flj10372,kiaa1445,mm42015, sema5b,5emag,semaphoring 5bhlog,sdema域,七个血小板重复序列,胞浆区),个体基因型,mage a3,p53nonmutant,ny-eso-1,gd2,cea,melana/mart1,napi3b(napi-3b,nptiib, slc34a2,溶质载体家族34,成员2,ii型钠依赖的磷转运3b),ras突变,gp100,p53突变体, proteinase3(pr1),bcr-abl,酪氨酸酶,生存素,htert,肉瘤易位断点,epha2,pap,ml-iap, afp,epcam,erg(tmprss2ets融合基因),na17,pax3,alk,雄激素受体,细胞周期素b1,聚唾液酸,mycn,rhoc,trp-2,gd3,岩藻糖神经节苷脂,间皮素,steap1(6个跨膜上皮前列腺抗原),和steap2(hgnc 8639,ipca-1,pcanp1,stamp1,steap2,stmp,前列腺),psca,mage a1, sle(a),cyp1b1,plac1,gm3,boris,tn,globoh,etv6-aml,ny-br-1,rgs5,sart3,stn,碳酸酐酶ix,pax5,oy-25tes1,精子蛋白17,lck,hmwmaa,akap-4,ssx2,xage 1,b7h3,豆荚蛋白, tie 2,page4,vegfr2,mad-ct-1,fap,pdgfr-β,mad-ct-2,fos蛋白相关抗原1。
[0151]
在另一具体实施例中,本发明采用带电荷连接体的细胞结合分子-药物共轭体可以用来治疗癌症。这些癌症包含,并不限于,肾上腺皮质癌,直肠癌,膀胱癌,脑肿瘤(成人:脑干胶质瘤,儿童,小脑星形细胞瘤,星形细胞瘤,室管膜瘤,髓母细胞瘤,幕上原始神经外胚层肿瘤,松果体,视觉通路和下丘脑胶质瘤),乳腺癌,类癌肿瘤,胃肠道,未知原发癌,宫颈癌,结肠癌,子宫内膜癌,食管癌,肝外胆管癌,尤文家族肿瘤(pnet),颅外恶性生殖细胞肿瘤,眼癌,眼内黑色素瘤,胆囊癌,胃癌(胃),生殖细胞肿瘤,性腺外,妊娠滋养细胞肿瘤,头颈部肿瘤,下咽癌,胰岛细胞癌,肾癌(肾细胞癌),喉癌,白血病(急性淋巴细胞,急性髓细胞,慢性淋巴细胞,慢性髓细胞,多毛细胞),唇和口腔癌,肝癌,肺癌(非小细胞,小细胞,淋巴瘤(爱滋病相关,中枢神经系统,皮肤t细胞,霍奇金病,非霍奇金病,恶性间皮瘤,黑色素瘤,默克尔细胞癌,原发性隐匿性鳞状颈部转移癌,多发性骨髓瘤和其他浆细胞肿瘤,蕈样肉芽肿,骨髓增生异常综合征,骨髓增殖性疾病,鼻咽癌,神经母细胞瘤,口腔癌,口咽癌,骨肉瘤,卵巢癌(上皮细胞,生殖细胞瘤,低度恶性潜能肿瘤),胰腺癌(外分泌,胰岛细胞癌),鼻窦和鼻腔癌,甲状旁腺癌,阴茎癌,嗜铬细胞瘤癌,垂体肿瘤,浆细胞肿瘤,前列腺癌横纹肌肉瘤,直肠癌,肾细胞癌(肾癌),肾盂和输尿管(移行细胞),涎腺癌,塞扎综合症,皮肤癌,
皮肤癌(皮样t细胞淋巴瘤,卡波西氏肉瘤,黑色素瘤),小肠癌,软组织肉瘤,胃癌,睾丸癌,胸腺瘤(恶性),甲状腺癌,尿道癌,子宫癌(肉瘤),儿童异常肿瘤,阴道癌,外阴癌,肾母细胞瘤。
[0152]
在另一具体实施例中,本发明采用带电荷连接体的细胞结合分子-药物共轭体通过其组分和方法可以用来治疗或预防自身免疫疾病。自身免疫疾病包括,但不限于,胃酸缺乏自身免疫性慢性活动性肝炎,急性播散性脑脊髓炎,急性出血性脑白质炎,阿狄森氏病,丙种球蛋白血症,斑秃,肌萎缩性侧索硬化症,强直性脊柱炎,抗肾小球基底膜/肾小管基底膜肾炎,抗磷脂综合征,抗合成酶综合征,关节炎,异位性过敏症,过敏性皮炎,自身免疫性再生障碍性贫血,自身免疫性心肌病,自身免疫性溶血性贫血,自身免疫性肝炎,自身免疫性内耳病,自身免疫性淋巴组织增生综合征,自身免疫性周围神经系统疾病,自身免疫性胰腺炎自体免疫多内分泌症i,ii,iii型,自身免疫性孕酮皮炎,自身免疫性血小板减少性紫癜,自身免疫性色素层炎,巴洛病/巴洛同心性硬化,黑奇特综合征,berger病,bickerstaff 脑干脑炎,blau综合征,大苞性类天苞疮,巨淋巴结增生,美洲锥虫病,慢性疲劳免疫功能紊乱综合征,慢性炎症性脱髓鞘性多发神经病,慢性复发性多病灶性骨髓炎,慢性莱姆病,慢性阻塞性肺疾病,变应性肉芽肿性血管炎,瘢痕性类天疱疮,腹部疾病,耳蜗前庭综合征,冷凝集素病,补体c2缺乏症,颅动脉炎,肢端硬皮综合征,克隆氏病(一种特发性炎症性肠病),柯兴氏症,皮肤白细胞碎裂性血管炎,恶性萎缩性丘疹病,痛性肥胖病,疱疹样皮炎,皮肌炎,1型糖尿病,弥漫性皮肤硬皮病,心肌梗塞后综合征,盘状红斑狼疮,湿疹,子宫内膜异位症,幼年特发性关节炎,嗜酸细胞性筋膜炎,嗜酸细胞性筋膜炎,结节性红斑,特发性混合性冷球蛋白血症,埃文斯综合征,渐进性骨化性纤维组织结构不良,纤维肌痛,纤维肌炎,纤维性肺泡炎,胃炎,胃肠类天疱疮,巨细胞动脉炎,肾小球肾炎,肺出血肾炎综合征,格雷夫斯氏病,格林-巴利神经根炎,桥本脑炎,淋巴瘤性甲状腺肿,溶血性贫血,过敏性紫癜多,妊娠期疱疹,化脓性汗腺炎,休斯综合症(抗磷脂抗体综合征),低丙球蛋白血症,特发性炎性脱髓鞘疾病,特发性肺纤维化,特发性血小板减少性紫癜(自身免疫性血小板减少性紫癜), iga肾病(berger病),包涵体肌炎,发炎性脱髓鞘病变,间质性膀胱炎,肠易激综合征,幼年特发性关节炎,幼儿型类风湿性关节炎,皮肤粘膜淋巴结综合征,兰伯特肌无力综合征,白细胞分裂性血管炎,扁平苔藓,硬化性苔藓,线状iga病(lad),肌萎缩性侧索硬化症,狼疮样肝炎,红斑狼疮,马吉德综合征,美尼尔氏综合症,显微镜下多血管炎,米勒
·
费希尔综合征,混合性结缔组织病,硬斑病,穆哈二氏病,韦尔斯综合征,多发性骨髓瘤,多发性硬化症,重症肌无力,肌炎,发作性睡病,视神经脊髓炎(德维克病),神经性肌强直,眼部瘢痕性类天疱疮,眼阵挛-肌阵挛综合征,奥德氏甲状腺炎,复发性风湿病,熊猫症候群(合并链球菌感染的儿童自体免疫神经精神异常),类肿瘤性小脑变性,阵发性睡眠性血红蛋白尿症,进行性一侧面萎缩,巴-特二氏综合征,睫状体扁平部炎,天疱疮,寻常型天疱疮,恶性贫血,静脉周围炎,poems综合征,结节性多动脉炎,风湿性多肌痛,多发性肌炎,原发性胆汁性肝硬化,原发性硬化性胆管炎,进行性炎性神经病变,银屑病,银屑病关节炎,坏疽性脓皮,纯红细胞再生障碍性贫血,罗斯默森氏脑炎,雷诺病,复发性多软骨炎,莱特尔综合征,腿多动综合征,腹膜后纤维化,类风湿关节炎,类风湿发热,结节病,精神分裂症,施密特综合征,施尼茨勒综合征,巩膜炎,硬皮病,干燥综合征,脊椎关节病,粘血综合征,斯蒂尔病,僵人综合征,亚急性细菌性心内膜炎,susac氏综合征,急性热性嗜中性皮肤病,西德纳姆舞蹈病,交感性
眼炎,高安氏动脉炎,颞动脉炎(巨细胞动脉炎),痛性眼肌麻痹综合征,横贯性脊髓炎,溃疡性结肠炎(一种特发性炎症性肠疾病),未分化的结缔组织病,未分化脊柱关节病,血管炎,白癜风,韦格纳氏肉芽肿病,威尔逊氏综合征,威斯科特-奥尔德里奇综合征。
[0153]
在另一具体实施方案中,通过本发明的亲水链接体链接的用于治疗或预防自身免疫疾病的细胞结合分子包括,但不限于:抗弹性蛋白抗体;abys抗上皮细胞抗体;抗基底膜 iv型胶原蛋白抗体;抗核抗体;抗双链dna抗体;抗单链dna抗体,抗心肌磷脂抗体igm,igg;抗celiac(anti-celiac antibody)抗体;抗磷脂抗体igk,igg;抗核糖蛋白抗体;抗线粒体抗体;甲状腺抗体;微粒体抗体,t-细胞抗体;甲状腺球蛋白抗体,抗硬皮病-70抗体(anti
‑ꢀ
scl-70);人抗jo抗体(anti-jo);抗系统性红斑狼疮患者自身抗体;抗干燥综合症抗体(anti-la/ssb);抗系统性红斑狼疮抗体;抗壁细胞抗体;抗组蛋白抗体;抗核糖核蛋白抗体 (anti-rnp);中性粒细胞胞质抗体(c-anca);细胞核周围抗中性粒细胞抗体(p-anca);抗着丝粒抗体;抗核纤维蛋白抗体,以及抗肾小球基底膜抗体(gbm)抗体,抗神经节苷脂(anti
‑ꢀ
ganglioside)抗体;抗桥粒芯糖蛋白3抗体(anti-desmogein 3);抗人p62抗体;抗人sp100 抗体;抗线粒体m2抗体;类风湿因子抗体;抗突变型瓜氨酸波形蛋白抗体(anti-mcv);抗拓扑异构酶抗体;抗中性粒细胞胞浆(canca)抗体。
[0154]
在某些优选的实施方案中,本发明中用于共轭偶联的结合分子,可以与自身免疫性疾病相关的活化淋巴细胞表达的受体或受体复合物结合。包括免疫球蛋白基因超家族成员(如cd2,cd3,cd4,cd8,cd19,cd20,cd22,cd28,cd30,cd37,cd38,cd56,cd70,cd79,cd90, cd125,cd152/ctla-4,pd-1,pdl-1,或icos),tnf受体超家族成员(如cd27,cd40,cd95/fas, cd134/ox40,cd137/4-1bb,inf-r1,tnfr-2,rank,taci,bcma,骨保护素,apo2/trail-r1, trail-r2,trail-r3,trail-r4,apo-3),整联蛋白,细胞因子受体,趋化因子受体,主要组织相容性蛋白,凝集素(c型,s型或i型)或补体调控蛋白。
[0155]
在另一特定实施方案中,对病毒性或细菌性抗原具有免疫特异性的有用的结合体是人源化的或人源单克隆抗体。本文所用术语“病毒性抗原”包括,但不限于:任何能诱发免疫反应的病毒肽段,多肽蛋白(例如,hivgp120,hiv nef,rsv f糖蛋白,流感病毒神经氨酸酶,流感病毒血凝素,人类t淋巴细胞病毒感染调节因子tax,单疱疹病毒糖蛋白(例如,gb, gc,gd和ge)和乙型肝炎表面抗原)。本文所用的术语“细菌性抗原”包括,但不限于:任何能诱发免疫反应的微生物肽段,多肽蛋白,糖类,多糖,脂质分子(例如,细菌,真菌,致病性原生动物,酵母多肽包括,例如,脂多糖和荚膜多糖5/8)。可用于治疗病毒性或细菌性感染的抗体包括,但不限于:帕利珠单抗,一种用于治疗rsv感染的人源的抗呼吸道合胞体病毒单克隆抗体;pro542,一种用于治疗hiv感染的cd4融合抗体;ostavir,一种治疗乙肝病毒人源性抗体;protvir,一种用于治疗巨细胞病毒人源化免疫球蛋白亚型i抗体,还有抗脂多糖 (anti-lps)抗体。
[0156]
通过本发明带电荷连接体的制备的细胞结合分子-药物共轭体可以用于治疗传染性疾病。这些传染病包括,但不限于:不动杆菌感染,放线菌病,非洲昏睡病(非洲锥虫病),艾滋病(获得性免疫缺陷综合症),阿米巴病,微粒孢子虫病,炭疽,溶血隐秘杆菌感染,阿根廷出血热,蛔虫病,曲霉菌病,星状病毒感染,巴贝虫病,蜡样芽胞杆菌感染,细菌性肺炎,细菌性阴道病,类杆菌感染,小袋虫病,贝利蛔线虫感染,bk病毒感染,黑色发结节病,人芽囊原虫感染,芽生菌,玻利维亚出血热,疏螺旋体感染,肉毒中毒(和婴儿肉毒中毒),巴西出血
热,布氏杆菌病,伯霍尔德杆菌感染,布鲁里溃疡,感染杯状病毒(诺罗病毒和札幌病毒),弯曲菌病,念珠菌感染(念珠菌病,鹅口疮),猫抓病,蜂窝组织炎,查格斯病(美洲锥虫病),软下疳,水痘,衣原体,肺炎衣原体感染,霍乱,着色真菌病,肝吸虫病,难辨梭状芽孢杆菌感染,球孢子菌病,科罗拉多蜱热,普通感冒(急性病毒鼻咽炎;急性鼻炎),克雅氏病,克里米亚-刚果出血热,隐球菌病,隐孢子虫病,皮肤幼虫移行症,环孢子虫感染,囊虫病,巨细胞病毒感染,登革热,双核阿米巴病,白喉,裂头绦虫,龙线虫病,埃博拉出血热,包虫病,埃里希体病,蛲虫病(蛲虫感染),肠球菌感染,肠病毒感染,流行性斑疹伤寒,传染性红斑(第五病),幼儿急疹,姜片虫病,家族致命性失眠症,丝虫病,产气荚膜梭菌引起的食物中毒,非寄生阿米巴感染,梭杆菌感染,气性坏疽(梭菌性肌坏死),地丝菌病,吉斯特曼-施特劳斯综合征,贾第虫病,马鼻疽,腭口线虫病,淋病,腹股沟肉芽肿,a组链球菌感染,b组链球菌感染,流感嗜血杆菌感染,手足口病(hfmd),汉坦病毒肺综合征,幽门螺杆菌感染,溶血性尿毒综合征,出血热肾病综合征,甲型肝炎,乙型肝炎,丙型肝炎,丁型肝炎,戊型肝炎,单纯疱疹,组织胞浆菌病,钩虫感染,人鲍坎病毒感染,人埃文氏埃立克体病,人粒细胞无形体病,人类偏肺病毒感染,人体单核细胞埃立克体病,人乳头状瘤病毒感染,人副流感病毒感染,膜壳绦虫病,爱泼斯坦-巴尔病毒传染性单核细胞增多症(单一),流感,等孢子球虫病,川崎病,角膜炎,金氏金氏杆菌感染,库鲁病,拉沙热,军团杆菌病(退伍军人协会会员病),军团杆菌病(庞蒂亚克热),利什曼病,麻风病,钩端螺旋体病,李氏杆菌病,莱姆病(莱姆疏螺旋体病),淋巴丝虫病(象皮肿),淋巴细胞性脉络丛脑膜炎,疟疾,马尔堡出血热,麻疹,类鼻疽 (惠特莫尔氏病),脑膜炎,脑膜炎球菌病,后殖吸虫病,微孢子虫病,传染性软疣,流行性腮腺炎,斑疹伤寒(地方性斑疹伤寒),支原体肺炎,足菌肿,蝇蛆病,新生儿结膜炎(新生儿眼炎),克-亚综合征(vcjd,nvcjd),诺卡氏菌病,盘尾丝虫病(河盲症),副球孢子菌病(南美芽生菌病),肺吸虫病,巴氏杆菌病,头虱病(头虱),体虱病(体虱),阴虱病(阴虱),盆腔炎,百日咳,鼠疫,肺炎球菌感染,肺孢子虫性肺炎,肺炎,脊髓灰质炎,普氏菌感染,原发性阿米巴脑膜脑炎,进行性多病灶脑白质病,鹦鹉热,q热,狂犬病,鼠咬热,呼吸道合胞病毒感染,鼻孢子菌病,鼻病毒感染,立克次体感染,立克次氏体,裂谷热,洛矶山斑疹热,轮状病毒感染,风疹,沙门氏菌病,sars(严重急性呼吸系统综合症),疥疮,血吸虫病,败血症,痢疾(菌痢),带状疱疹(带状疱疹),天花(天花),孢子丝菌病,葡萄球菌食物中毒,葡萄球菌感染,线虫,梅毒,绦虫病,破伤风(牙关紧闭症),须癣,头癣,体癣,股癣,手癣,黑糠疹,足癣,甲癣,花斑癣,弓蛔虫病(眼幼虫移行症),弓蛔虫病(内脏幼虫移行症),弓形体病,旋毛虫病,滴虫病,鞭虫病(鞭虫感染),肺结核,兔热病,尿素分解尿素支原体感染,委内瑞拉马脑炎,委内瑞拉出血热,病毒性肺炎,西尼罗热,白色毛结节菌病(白色毛结节菌病),假结核菌感染,耶尔森菌病,黄热病,接合菌病。
[0157]
在本专利中被描述的细胞结合分子主要倾向为抗体。这些抗体可用来对抗致病菌。所对抗的致病菌包括,但不限于:鲍曼不动杆菌,以色列放线菌,戈氏放线菌和丙酸丙酸盐杆菌,布氏锥虫,hiv(人类免疫缺陷病毒),溶组织内阿米巴,无形体属,炭疽杆菌,溶血隐秘杆菌,胡宁病毒,蛔虫,曲霉属,星状病毒家庭,巴贝斯虫属,蜡样芽胞杆菌,多杆菌,类杆菌属,结肠小袋纤毛虫,贝利蛔线虫属,bk病毒,何德毛结节菌,人芽囊原虫,皮炎芽生菌,沙粒病毒,疏螺旋体属,肉毒梭菌,清风藤,布鲁菌属,通常洋葱伯克霍尔德菌和其他伯克霍尔德杆菌种,溃疡分枝杆菌,杯状病毒科家族,弯曲杆菌属,通常是白色念珠菌和其他念珠菌
属,巴尔通体,a组链球菌和葡萄球菌,克氏锥虫,杜克雷嗜血杆菌,水痘带状疱疹病毒 (vzv),沙眼衣原体,肺炎衣原体,霍乱弧菌,裴氏着色霉,华支睾吸虫,难辨梭状芽孢杆菌,粗球孢子菌和coccidioides posadasli,科罗拉多蜱热病毒,鼻病毒,冠状病毒,朊病毒克雅氏病,克里米亚-刚果出血热病毒,新型隐球菌,隐孢子虫属,猫钩虫;multipleparasites,环孢子,猪带绦虫,巨细胞病毒,登革热病毒(den-1,den-2,den-3和den-4)虫媒病毒,脆弱双核阿米巴,白喉棒状杆菌,裂头属,麦地那龙线虫,埃博拉病毒,棘球属,埃立克体属,蛲虫,肠球菌属,肠道病毒属,普氏立克次体,细小病毒b19,人类疱疹病毒6型和人类疱疹病毒7型,布氏姜片吸虫,肝片吸虫和大片吸虫,ffi朊病毒,丝虫目超家族,产气荚膜杆菌,梭杆菌属,产气荚膜梭菌,其他梭菌属,白地霉,gss朊病毒,肠贾第鞭毛虫,鼻疽伯克霍尔德氏菌,棘颚口线虫和刚棘颚口虫,淋病奈瑟菌,肉芽肿杆菌,化脓性链球菌,无乳链球菌,流感嗜血杆菌,肠道病毒,大多数柯萨奇a病毒和肠病毒71型,辛诺瓦病毒,幽门螺旋杆菌,大肠杆菌o157:h7,布尼亚病毒科家族,甲型肝炎病毒,乙型肝炎病毒,丙型肝炎病毒,丁型肝炎病毒,戊型肝炎病毒,单纯疱疹病毒1型,单纯疱疹病毒2型,组织胞浆菌,十二指肠钩虫和美洲板口线虫,流感嗜血杆菌,人类博卡病毒,埃文氏埃立克体,无形体科,人类偏肺病毒,沙费埃里希体,人乳头瘤病毒,人副流感病毒,微小膜壳绦虫和缩小包膜绦虫,eb病毒,正粘病毒科,贝利等孢球虫,金氏金氏杆菌,肺炎克雷伯菌,klebsiella ozaenas,库鲁病朊病毒,拉沙病毒,嗜肺军团菌,嗜肺军团菌,利什曼原虫属,麻风分枝杆菌和弥漫型痳疯分枝杆菌,钩端螺旋体属,李斯特菌,博氏包柔螺旋体和其他疏螺旋体属,班氏丝虫和马来丝虫,淋巴细胞性脉络丛脑膜炎病毒(lcmv),疟原虫属,马尔堡病毒,麻疹病毒,类鼻疽伯克氏菌,脑膜炎奈瑟菌,横川后殖吸虫,微孢子虫门,传染性软疣病毒(mcv),腮腺炎病毒,立克次体杆菌,肺炎支原体,多种细菌(马杜拉分枝菌病)和真菌(马杜拉分枝菌病),寄生双翅目蝇蛆,沙眼衣原体和淋球菌,vcjd朊病毒,星状诺卡氏菌和其他诺卡氏菌属物种,旋盘尾丝虫,巴西芽生菌,卫氏并殖吸虫和其他并殖吸虫属,巴斯德氏菌属,虱头癣,体虱,阴虱,百日咳博德特氏菌,鼠疫耶尔森氏菌,肺炎链球菌,卡氏肺囊虫,脊髓灰质炎病毒,普雷沃氏菌属,福氏耐格里阿米巴,jc病毒,鹦鹉热衣原体,立克次体,狂犬病毒,念珠状链杆菌和鼠咬热螺旋体,呼吸道合胞病毒,西伯鼻孢子虫,鼻病毒,立克次体属,螨立克次体,立夫特山谷热病毒,立氏立克次体,轮状病毒,风疹病毒,沙门氏菌属,非典型肺炎冠状病毒,疥螨,血吸虫属,志贺氏菌属,水痘带状疱疹病毒,重型天花或类天花,申克孢子丝菌,葡萄球菌属,金黄色葡萄球菌,化脓性链球菌,粪类圆线虫,梅毒螺旋体,绦虫属,破伤风梭菌,毛癣菌属,断发毛癣菌,发癣菌属,絮状表皮癣菌,红色毛癣菌和须癣毛癣菌,威尼克外瓶霉,毛癣菌属,马拉色菌属,犬弓首蛔虫或猫弓蛔虫,弓形虫,旋毛虫,阴道毛滴虫,鞭虫,结核杆菌,土拉热弗朗西丝菌,解脲支原体,委内瑞拉马脑炎病毒,霍乱弧菌,瓜纳瑞托病毒,西尼罗病毒,白色毛孢子菌,假结核耶尔森菌,小肠结肠炎耶尔森菌,黄热病毒,毛霉目(毛霉菌病)和虫霉目 (虫霉菌病),铜绿假单胞菌,胎儿弯曲杆菌(弧菌),嗜水气单胞菌,迟缓爱德华氏菌,耶尔森菌,志贺痢疾杆菌,福氏痢疾杆菌,宋内志贺氏菌,鼠伤寒沙门氏菌,雅司螺旋体,treponemacarateneum,奋森疏螺旋体,博氏包柔螺旋体,出血性黄疸钩端螺旋体,卡氏肺囊虫,布鲁氏菌,猪布鲁氏菌,布氏杆菌,支原体属,斑疹伤寒病原体,rickettsia tsutsugumushi,披衣菌属;病原真菌(曲霉,白色念珠菌,荚膜组织胞浆菌);原生动物(溶组织内阿米巴,阴道毛滴虫,人毛滴虫,tryoanosoma gambiense,罗得西亚锥虫,杜氏利什曼原虫,热带利什曼原
虫,巴西利什曼原虫,肺囊虫肺炎,间日疟原虫,恶性疟原虫,恶性疟疾)或蠕虫(日本血吸虫,曼氏血吸虫,埃及血吸虫和钩虫)。
[0158]
其他作为细胞结合配体的抗体在本发明中用于治疗多种病毒性疾病包括,但不限于:抗体作用于病原病毒的抗原包括以下例子但不限于:天花病毒,疱疹病毒,腺病毒,乳多空病毒科,肠道病毒科,细小rna病毒科,细小病毒科,呼肠孤病毒,逆转录病毒科,流感病毒,副流感病毒,腮腺炎,麻疹,呼吸道合胞病毒,风疹,虫媒病毒,弹状病毒,沙粒病毒科, non-a/non-b肝炎病毒,鼻病毒,冠状病毒,轮状病毒科,肿瘤病毒[例如,乙型肝炎病毒(肝细胞癌),人乳头状瘤病毒(宫颈癌,肛门癌),卡波西肉瘤相关疱疹病毒(卡波济氏肉瘤),eb 病毒(鼻咽癌,伯基特淋巴瘤,原发性中枢神经系统淋巴瘤),mcpyv(梅克尔细胞癌),sv40 (猿猴病毒40),丙型肝炎病毒(肝癌),人类嗜t淋巴细胞病毒1型(成人t细胞白血病/淋巴瘤),免疫失调引起病毒:[如人类免疫缺陷病毒(艾滋病)];中枢神经系统病毒:[如,jcv(进行性多病灶脑白质病),mev(亚急性硬化性全脑炎),lcv(淋巴细胞性脉络丛脑膜炎),虫媒病毒性脑炎,正粘病毒科(可能的)(昏睡性脑炎),rv(狂犬病),水疱性口炎-印度病毒属,疹病毒性脑膜炎,拉姆齐
·
亨特综合征ii型;脊髓灰质炎(小儿麻痹症,后小儿麻痹症候群),人类嗜t淋巴细胞病毒1型(热带痉挛性截瘫)];巨细胞病毒(巨细胞病毒性视网膜炎,hsv (疱疹性角膜炎));心血管病病毒[如柯萨奇病毒(心包炎,心肌炎)];呼吸系统/急性鼻咽炎病毒/病毒性肺炎:[非洲淋巴细胞瘤病毒(疱疹病毒4型感染/传染性单核细胞增多),巨细胞病毒;sars冠状病毒(严重急性呼吸器官综合征)正粘病毒:流感病毒a/b/c(流感/禽流感),副粘病毒:人类副流感病毒(副流感),呼吸道合胞病毒(人类呼吸道合胞病毒),肺病毒];消化系统病毒[muv(腮腺炎),巨细胞病毒(巨细胞病毒性食管炎);腺病毒(腺病毒感染);轮状病毒,诺如病毒,星状病毒,冠状病毒;hbv(乙肝病毒),柯萨奇病毒,甲型肝炎(甲肝病毒),hcv(丙型肝炎病毒),hdv(丁型肝炎病毒),hev(戊型肝炎病毒),hgv(庚型肝炎病毒)];泌尿生殖系统的病毒[如,bk病毒,muv(腮腺炎)]。
[0159]
按照更进一步的目标,由本发明的亲水链连接的共轭体包含药学上可接受的载体组分共同用来治疗癌症或自身免疫疾病。治疗癌症和自身免疫疾病的方法包括体外,体内或离体疗法。体外疗法应用实例,包括药物处理体外培养细胞,杀死除了没有表达目标抗原的细胞以外的所有细胞;或者杀死表达非想要的抗原的细胞。作为离体疗法的治疗方法的一个示例:在体外处理造血干细胞,杀死患病或恶性细胞后输回原患者体内。例如,临床上先通过间接体内治疗除去骨髓中的肿瘤细胞或淋巴细胞然后输回原患者来治疗癌症和自体免疫疾病,或者在移植前去除骨髓中的t细胞和其它淋巴细胞以防止对移植物的免疫拮抗反应。实施方法如下:从病人或其他个体获取骨髓细胞,然后在加入本发明共轭药物的含血清培养基中37℃培养,药物浓度范围为1pm到0.1mm,培养时间为30分钟左右到48小时左右。药物具体浓度和培养时间由经验丰富的临床医生决定。培养结束后,骨髓细胞用含血清培养基洗涤后,按照已知方法通过静脉注射输回人体内。如果病人在获取骨髓细胞和回输处理前需要接受其它治疗,比如烧蚀化疗或全身放射疗法的情况下,处理后的骨髓细胞可以保存在合格的液氮医疗设备中。
[0160]
用于体内临床应用时,由本发明的链接体连接的共轭体药物将以溶液或能被无菌水溶解后注射的冻干固体的形式提供。合适的共轭药物给药方法实施例如下:共轭药物每星期通过静脉注射一次,持续8星期。单次剂量通过溶解于50到500毫升的生理盐水,生理盐
水可以加入人血清白蛋白(例如,0.5到1毫升的100mg/ml的浓缩人血清白蛋白)。药物剂量每星期大概在50μg到20mg每千克体重,静脉注射(每次注射范围10ug到200mg/kg体重)。8周的治疗结束后,病人可以再接受新一轮的治疗。详细的治疗方法包括给药途径,赋形剂,稀释剂,药物剂量,治疗时间等等可以由有经验的临床医生决定。
[0161]
可以通过体内或离体的方法选择性杀死细胞群来治疗疾病的例子包括任何种类的恶性肿瘤,自体免疫疾病,移植排斥和感染(包括病毒,细菌或寄生虫)。
[0162]
达到理想的生物学效果而需要的共轭药物的量,将因多个因素而各异,这些因素包括化合物的性质特点,疗效和共轭药物的生物利用度,疾病的类型,病人的种族,病人患病的状态,给药的途径,所有这些因素共同决定给药时间表和给药方式。
[0163]
概括的说,通过本发明中的链连接的共轭药物可以通过以0.1到10%质量体积比溶解在生理缓冲液中用于非肠道给药。典型的药物剂量范围从每天1ug到0.1g每千克体重;推荐的药物剂量范围从每天0.01mg到20mg每千克体重或者等效剂量的儿童用量。推荐的给药量取决于多个变量,包括疾病或功能紊乱的类型,病人个体的整体的健康状态,偶联药物的相对生物学活性,化合物的剂型,给药的方式(静脉注射,肌肉注射,或其它),在选中给药方式下的药物动力学特性,以及给药的速度(单次注射或者连续滴注)和给药的时间表(在一定时间内重复给药的次数)。
[0164]
由本发明的链连接的共轭药物同样可以以单位剂量的形式给药,这里的“单位剂量”是指一个病人一次给药的剂量,单位剂量的药物可以简单方便地包装和使用,单位剂量的药物是保持物理和化学稳定的活性共轭药物本身,或者是像以下介绍的药学上可接受的混合物。典型的一天的剂量范围从0.01mg到100mg每千克体重。一般而言,人每天的单位剂量范围从1mg到3000mg。推荐的单位剂量范围是1mg到500mg,每天给药一到四次,或者更理想的每天一次10mg到500mg。本发明的共轭药物可以通过加入一种或多种药学上可接受的辅料,制成药物制剂。此单位剂量的药物可以用于口服给药,比如是片剂,简单的胶囊或软胶囊;或鼻内给药,比如粉末状,滴鼻剂,或喷雾剂;或者通过皮肤给药,比如局部软膏剂,乳膏剂,洗液,凝胶剂或喷雾剂或皮肤贴片。
[0165]
5..7药物/细胞毒素制剂
[0166]
药物是指可以直接或修饰后通过本发明连接到细胞结合分子上的小分子药物包括细胞毒素。这里的“小分子药物”广泛的指分子量在100到1800的有机的,无机的或者有机金属的化合物,更适当的分子量是120到1400.对于小分子药物的更好的定义可以参见 w005058367a2和美国专利no.4,956,303,以及其它的文献,这里小分子药物的定义包含所有参考文献对小分子药物的定义。这里的药物包括所有已知的药物以及所有可能成为药物的药物。
[0167]
已知的药物包括,但不限于,
[0168]
1).化学治疗药物试剂a).烷基化试剂:比如氮芥类:苯丁酸氮芥,萘氮芥,环磷酰胺,达卡巴嗪,雌氮芥,异环磷酰胺,二氯甲基二乙胺,盐酸甲氧氮芥,甘露醇氮芥,二溴甘露醇,美法仑,二溴卫矛醇,哌血生,新恩比兴,苯芥胆甾醇,泼尼氮芥,噻替派,曲洛磷胺,尿嘧啶氮芥;cc-1065(包括它的阿多来新、卡折来新、比折来新合成类似物);倍癌霉素(包括合成类似物kw-2189和cbi-tmi);苯二氮卓二聚体(比如吡咯并苯二氮卓(pbd),或托马霉素,吲哚啉并苯二氮卓,咪唑并苯二氮卓,或者恶唑烷并苯二氮卓的二聚体);亚硝基脲:(卡莫
plx4032,sta-9090,stimuvax,allovectin-7,xegeva,provenge,yervoy,异戊二烯化抑制剂(如洛伐他汀),多巴胺能神经毒素(如1-甲基-4-苯基吡啶离子),细胞周期抑制剂(如星形孢菌素),放线菌素(如放线菌素d,放线菌素),平阳霉素(如博莱霉素博莱霉素a2,b2,培洛霉素),蒽环类药物(如柔红霉素,阿霉素(亚德里亚霉素),伊达比星,表阿霉素,吡柔比星,柔红霉素苯腙,mtoxantrone,mdr抑制剂(如维拉帕米),ca2 atp酶抑制剂(如毒胡萝卜素),组蛋白去乙酰化酶抑制剂(vorinostat,罗米地辛,帕比司他,丙戊酸,mocetinostat (mgcd0103),belinostat,pci-24781,entinostat,sb939,resminostat,givinostat,ar
‑ꢀ
42,cudc-10,萝卜硫素,曲古抑菌素a);毒胡萝卜素,塞来昔布,格列酮类,表没食子儿茶素没食子酸酯,双硫仑,salinosporamide a.;antiadrenals,如氨鲁米特,米托坦,曲洛司坦;酰葡醛内酯;醛磷酰胺糖苷;乙酰丙酸;吖啶;阿糖胞苷,bestrabucil;比生群,edatraxate; defofamine;秋水仙碱;二氮化合物;依氟鸟氨酸(dfmo),elfomithine;依利醋铵,乙环氧啶;硝酸镓;gacytosine,羟基脲;伊班膦酸钠,香菇多糖;氯尼达明;丙脒腙;米托蒽醌;单哌潘生丁;nitracrine;喷司他丁;蛋氨氮芥;吡柔比星;鬼臼酸;乙肼;甲基苄肼;雷佐生;根瘤菌素;西佐喃;螺旋锗;tenuazonic酸;triaziquone;2,2’,2
’‑ꢀ
trichlorotriethylamine;(特别是t-2毒素,单端孢verrucarin a,roridina a和 anguidine);聚氨酯,sirna,反义药物,和nucleolytic酶。
[0169]
2).一种抗自身免疫病剂包括,但不限于,环孢素,环孢素a,硫唑嘌呤,氨基己酸,溴隐亭,苯丁酸氮芥,氯喹,环磷酰胺,糖皮质激素(如激素类药,倍他米松,布地奈德,氟尼缩松,氢化可的松,丙酸氟替卡松,氟考龙,地塞米松,曲安奈德,丙酸倍氯米松),脱氢表雄酮,enanercept,羟氯喹,英夫利昔单抗,美洛昔康,甲氨蝶呤,吗替麦考酚酯,西罗莫司,他克莫司,强的松。
[0170]
3).抗传染病剂包括,但不限于,a).氨基糖苷类:丁胺卡那霉素,武夷霉素,庆大霉素(奈替米星,西索米星,异帕米星),潮霉素b,卡那霉素(阿贝卡星,阿米卡星,卡那霉素b,地贝卡星,妥布霉素),新霉素,(巴龙霉素,新霉素b,核糖霉素),乙基西梭霉素,大观霉素,链霉素,妥布霉素,甲基姿苏霉素;b).氯霉素类抗生素类:叠氮氯霉素,氯霉素,氟苯尼考,甲砜霉素;c).安莎类抗生素类:格尔德霉素,除莠霉素;d).碳青霉烯类抗生素类:比阿培南,多尼培南,厄他培南,亚胺培南/西司他丁,美罗培南,帕尼培南;e).头孢类:碳头孢烯 (氯碳头孢),头孢乙腈,头孢克罗,头孢拉定,头孢羟氨,头孢洛宁,头孢噻啶,先锋霉素i或头孢噻吩,头孢氨苄,头孢来星,头孢羟唑,头孢匹林,头孢曲嗪,头孢氮氟,头孢西酮,头孢唑啉,头孢拉宗,头孢卡品,头孢达肟,头孢吡肟,头孢米诺,头孢西丁,头孢丙烯,头孢沙定,头孢替唑,头孢呋辛,头孢克肟,头孢地尼,头孢妥仑,头孢他美,头孢甲肟,头孢地嗪,头孢尼西,头孢哌酮,头孢雷特,头孢噻肟,头孢替安,头孢唑兰,头孢咪唑,头孢匹胺,头孢匹罗,头孢泊肟,头孢喹肟,头孢磺啶,头孢他啶,头孢特仑,头孢布烯,头孢噻林,头孢唑肟,头孢吡普,头孢曲松,头孢唑喃,头霉素(头孢西丁,头孢替坦,头孢美唑),氧头孢烯(氟氧头孢,拉氧头孢);f).糖肽类:万古霉素(博莱霉素,奥利万星,特拉万星),替考拉宁(达巴万星),雷莫拉宁;g).甘氨酰环类:如替加环素;h).β-内酰胺酶抑制剂类:青霉烷(舒巴坦,他唑巴坦),clavam(克拉维酸);i).林可酰胺类:克林霉素,林可霉素;j).脂肽:达托霉素,a54145,钙依赖性抗生素(cda);k).大环内酯类抗生素红霉素,阿奇霉素,克拉霉素,地红霉素,红霉素,罗红霉素,交沙霉素,酮内酯(泰利霉素,喹红霉素),麦迪霉素,美地霉素,竹桃霉素,利
福霉素(利福平,利福布丁,利福喷丁),罗他霉素,罗红霉素,大观霉素,螺旋霉素,他克莫司 (fk506),醋竹桃霉素,泰利霉素;l).单环β-内酰胺类:氨曲南,tigemonam,m).恶唑烷酮类:利奈唑胺;n).青霉素类抗生素:阿莫西林,氨比西林(匹氨西林,海他西林,巴氨西林,美坦西林,酞氨西林),叠氮西林,阿洛西林,青霉素g,苄星青霉素,苄星青霉素,苄星苯氧甲基青霉素,氯甲西林,普鲁卡因苄青霉素,羧苄青霉素(卡茚西林),氯唑西林,双氯西林,依匹西林,氟氯西林,美西林(匹美西林),美洛西林,甲氧西林,萘夫西林,苯唑西林,培那西林,盘尼西林,非奈西林,青霉素v,哌拉西林,丙匹西林,磺苄西林,替莫西林,替卡西林;o).多肽类:杆菌肽,粘杆菌素,多粘菌素b;p).喹诺酮类:阿拉沙星,巴洛沙星,环丙沙星,克林沙星,依诺沙星,恩诺沙星,达氟沙星,二氟沙星,氧氟沙星,加雷沙星,加替沙星,吉米沙星,格帕沙星,卡诺曲伐沙星,左氧氟沙星,洛美沙星,麻保沙星,那氟沙星,莫西沙星,奥比沙星,诺氟沙星,氧氟沙星,培氟沙星,曲伐沙星,西他沙星,司帕沙星,格帕沙星,替马沙星,托氟沙星,曲伐沙星;q).阳菌素类:普那霉素,奎奴普丁/达福普汀)r).磺胺类:磺胺米隆,偶氮磺胺,磺胺醋酰,磺胺甲二唑,柳氮磺胺吡啶,磺胺异恶唑,甲氧苄啶,磺胺甲恶唑(复方新诺明);s).甾体类抗菌药:例如,夫西地酸;t).四环素类抗生素:多西环素,氯羟四环素,氯四环素,赖甲环素,去甲金霉素,土霉素,米诺环素,氯甲烯土霉素,氧四环素,青哌环素,吡甲四环素,四环素,甘氨酰(例如替加环素);u).其他的类型的抗生素:番荔枝素,砷凡纳明,细菌萜醇抑制剂(杆菌肽),dadal/ar抑制剂(环丝氨酸),dictyostatin,圆皮海绵内酯,艾榴塞洛素,埃博霉素,乙胺丁醇,依托泊苷,法罗培南,夫西地酸,呋喃唑酮,异烟肼, laulimalide,甲硝唑,莫匹罗星,mycolactone,nam合成抑制剂(如磷霉素),硝基呋喃妥因,紫杉醇,平板霉素,吡嗪酰胺,奎奴普丁/达福普汀,利福平(甲哌利福霉素),他唑巴坦磺甲硝咪唑,番荔枝内酯;
[0171]
4).抗病毒药物:a).输入/融合抑制剂:aplaviroc,maraviroc,vicriviroc,gp41 (恩夫韦肽),pro140,cd4(ibalizumab);b).整合酶抑制剂:雷特格韦,埃替拉韦, globoidna n a;c).成熟抑制剂:bevirimat,vivecon;d).神经氨酸酶抑制剂:奥司他韦,扎那米韦,帕拉米韦;e).核苷及核苷酸:阿巴卡韦,阿昔洛韦,阿德福韦酯,氨多索韦,阿普瑞西他滨,溴夫定,西多福韦,右艾夫他滨,克拉夫定,地达诺新(ddi),艾夫他滨,恩曲他滨 (ftc),恩替卡韦,泛昔洛韦,氟二氧嘧啶(5-fu),3
’‑
氟-取代的2’,3
’‑
二脱氧核苷类似物, (例如,3
’‑
氟-2’,3
’‑
二脱氧胸苷(flt),3
’‑
氟-2’,3
’‑
双脱氧鸟苷(flg),福米韦生,更昔洛韦,碘苷,拉米夫定(3tc),1-核苷(比如.β-1-胸苷和β-1-2
’‑
脱氧胞苷)喷昔洛韦,racivir,利巴韦林,stampidine,司他夫定(d4t),taribavirin(viramidine),替比夫定,替诺福韦,三伐昔洛韦,缬更昔洛韦,扎西他滨(ddc),齐多夫定(azt);f).非核苷类药物:金刚烷胺, ateviridine,卡普韦林,二芳基嘧啶类化合物(依曲韦林,利匹韦林),地拉韦啶,廿二醇,乙米韦林,依法韦仑,膦甲酸(膦甲酸),咪喹莫特,alfa-干扰素,洛韦胺,洛德腺苷,甲吲噻腙,奈韦拉平,nov-205,聚乙二醇干扰素alfa,足叶草毒素,利福平,金刚烷乙胺,瑞喹莫德(r
‑ꢀ
848),g).蛋白酶抑制剂:安普那韦,阿扎那韦,博赛泼维,地瑞纳韦,福沙那韦,茚地那韦,洛匹那韦,奈非那韦,利托那韦,普拉康纳利,沙奎那韦,特拉匹韦(vx-950),替拉那韦;h).其他类型抗病毒药物:抗体酶,阿比朵尔,胡桐内酯a,ceragenin,蓝藻抗病毒蛋白n,二芳基嘧啶类化合物,表没食子儿茶素没食子酸酯(egcg),膦甲酸,griffithsin,塔利韦林 (viramidine),羟基脲,kp-1461,米替福新,普拉康纳利,portmanteau inhibitors,利巴韦
林,seliciclib。
[0172]
5).本发明中通过带电荷连接体链接的的药物还包括下列放射性同位素。例放射性同位素(放射性核素)是3h,
11
c,
14
c,
18
f,
32
p,
35
s,
64
cu,
68
ga,
86
y,
99
tc,
111
in,
123
i,
124
i,
125
i,
131
i,
133
xe,
177
lu,
211
at,和
213
bi。放射性同位素标记的抗体在受体靶向成像实验中非常有用或可直接用于有针对性的靶向治疗,如抗体药物缀合物的发明(wuetal(2005)naturebiotechnology23(9):1137-1146)。细胞结合的分子,如抗体,前面描述的那样:可以通过本专利亲水链接体结合、螯合或形成其他复杂的放射性同位素金属结合作用来被标记,此标记技术描述于currentprotocolsinimmunology,volumesland2,coligenetal,ed.wiley-interscience,newyork,n.y.,pubs.(1991)。能生成复杂金属络合物的螯合剂包括dota,dotp,dotma,dtpa和teta(macrocyclics,dallas,tex.).
[0173]
6).药学上上述任何化合物可接受的盐、酸以及上述任何药物的衍生物。
[0174]
本专利优选的通过此带电荷链接体共轭连接到细胞结合分子的细胞毒性药物是tubulysins,美登素类,taxanoids(紫杉醇),cc-1065类似物,柔红霉素和阿霉素的化合物,苯二氮卓类二聚体(例如,吡咯并苯二氮卓(pbd)二聚体,托马霉素二聚体,氨茴霉素二聚体,吲哚啉并苯二氮卓二聚体,咪唑并苯二氮卓二聚体,或者恶唑烷并苯二氮卓的二聚体),刺孢霉素和烯二炔类抗生素,放线菌素,重氮丝氨酸(azaserines),博莱霉素,表柔比星(表阿霉素),他莫昔芬,伊达比星,海兔毒素(多拉司他汀)/阿里他汀(auristatins)(如单甲基auristatine,mmae,mmaf,auristatinpye,auristatintp,auristatins2-aq,6-aq,eb(aeb),和efp(aefp)),多卡米星(duocarmycins),塞替派,长春新碱,hemiasterlins,esperamicins,以及它们的类似物和衍生物。
[0175]
本发明专利中,tubulysins是优选用作共轭(偶联)药物的一类化合物,其可以从天然产物中提取或者通过已知的方法进行合成(例如:.balasubramanian,r.;etal.j.med.chem.,2009,52,238-240.wipf,p.;etal.org.lett.,2004,6,4057-4060.pando,o.;etal.j.am.chem.soc.,2011,133,7692-7695.reddy,j.a.;etal.mol.pharmaceutics,2009,6,1518-1525.raghavan,b.;etal.j.med.chem.,2008,51,1530-1533.patterson,a.w.;etal.j.org.chem.,2008,73,4362-4369.pando,o.;etal.org.lett.,2009,11(24),pp5567-5569.wipf,p.;etal.org.lett.,2007,9(8),1605-1607.friestad,g.k.;org.lett.,2004,6,pp3249-3252.hillarym.peltier,h.m.;etal.j.am.chem.soc.,2006,128,16018-16019.chandrasekhar,s.;etal.j.org.chem.,2009,74,9531-9534.liu,y.;etal.mol.pharmaceutics,2012,9,168-175.friestad,g.k.;etal.org.lett.,2009,11,1095-1098.kubicek,k.;etal.,angewchemintedengl,2010.49:p.4809-12.chai,y.;etal.,chembiol,2010,17:296-309.ullrich,a.;etal.,angewchemintedengl,2009,48,4422-5.sani,m.;etal.angewchemintedengl,2007,46,3526-9.domling,a.;etal.,angewchemintedengl,2006.45,7235-9.patentapplications:zanda,m.;etal,can.pat.appl.ca2710693(2011).chai,y.;etal.eur.pat.appl.2174947(2010),wo2010034724.leamon,c.;etal,wo2010033733,wo2009002993.ellman,j.;etal,wo2009134279;wo2009012958,usappl.20110263650,20110021568,matschiner,g.;etal,wo2009095447.vlahov,i.:etal,wo2009055562,wo2008112873.low,p.;etal,wo2009026177.richter,w.,wo2008138561.kjems,j.;et
736;8,153,627;8,034,808;7,834,005;7,741,319;7,704,924;7,691,848;7,678,787;7, 612,062;7,608,615;7,557,099;7,528,128;7,528,126:7,511,032;7,429,658;7,407, 951;7,326,700;7,312,210;7,265,105;7,202,239;7,189,710;7,173,026;7,109,193;7, 067,511;7,064,120;7,056,913;7,049,311;7,022,699;7,015,215;6,979,684;6,951, 853;6,884,799;6,800,622;6,747,144;6,660,856;6,608,192;6,562,806;6,977,254;6, 951,853;6,909,006;6,344,451;5,880,122;4,935,362;4,764,616;4,761,412;4,723, 007;4,723,003;4,683,230;4,663,453;4,508,647;4,464,467;4,427,587;4,000,304;美国申请专利:20100203007,20100316656,20030195196。
[0183]
本发明专利中,所描述的细胞毒性药物/药剂的类似物及衍生物可以通过本发明带电荷链接体试剂进行偶联。在本行业领域中,对细胞毒性药物/试剂有一点是广为被技术人员所知的:每一种细胞毒性药物/试剂都能够在保持化合物起始的特异性/活性的条件下对其进行修饰。同样,很多化合物可以被用于替代本发明专利中所描述的细胞毒性药物/药剂。因此,本发明专利中的药物/药剂包括了所述化合物的类似物及衍生物。
[0184]
本发明专利中所引用的文献以及实例都明确地并入例子里进行了说明。
[0185]
6.实例
[0186]
本发明专利用下面的实例进行了进一步的说明,这些实例的内容不限制本发明专利的范围。在实例中所描述的细胞系的培养条件,除了特殊说明之外,均是依据美国菌种保藏中心(atcc)或者德国菌种保藏中心(dsmz)特定条件。除了特殊说明外,细胞培养试剂来自于invitrogen公司。所有的无水试剂均由商业途径获得,并储存于充氮密封瓶中。其他的试剂和溶剂均按照最高规格购买,使用时未经进一步的处理。nmr数据由varian mercury300mhz检测得出,化学位移以ppm为单位,四甲基硅烷为标准,耦合常数(j)的单位是hz。低分辨率质谱数据由waters micromass zmd质谱仪连接waters 2795hplc高效液相分离器以及2996光电二极管阵列检测器联合检测得出。
[0187]
实例1:(2-溴乙基)(3-乙氧基-3-氧代丙基)次膦酸(或乙基3-[2-溴乙基-(羟基) 氧膦基]丙酸乙酯)(4)
[0188][0189]
在n2保护下,将次膦酸胺(8.00g,96mmol)和六甲基二硅氮烷(20.0ml,96mmol)于 120℃反应1h。将反应物混合物冷却至0℃,小心滴加丙烯酸乙酯(10.4ml,96mmol),滴加完毕后,将反应液升温至50℃,搅拌2h。反应结束后,将反应混合物冷却至室温,加入二溴乙烷(40.0ml),再将反应混合液升温至120℃反应5h。将反应生成的三甲基溴硅烷和过量的二氯甲烷减压蒸掉,滴加入100ml乙醇水溶液(1∶1),回流0.5h。将反应混合液减压蒸馏,残余物用乙酸乙酯萃取,有机相用无水硫酸镁干燥后减压浓缩,得到目标化合物4(10.85g,产率 41%).1h nmr(300mhz,cd3od):δ1.26(t,j=7.1hz,3h),2.07(m,2h),2.42(m,2h),2.62(m, 2h),3.59(m,2h),4.15(q,j=7.1hz,2h).
31
p nmr(100mhz,cd3od):δ49.5;esi ms m/z
‑ꢀ
c7h
13
bro4p(m-h),计算值:271.98,测定值:271.97。
[0190]
实例2:3-[2-溴乙基(乙氧基)膦基]丙酸乙酯(5)和3-[乙氧基(乙烯基)膦基]丙酸乙酯(6)
[0191][0192]
向化合物4(10.84g,20mmol)中加入原甲酸三乙酯(100.0ml),反应混合液升温至回流,用dean-stark分水器除去生成的乙醇和甲酸乙酯。反应结束后,将多余的原甲酸三乙酯减压除去,得到5和6([39.2:60.8,
31
pnmr比例],11.83g)。6:1hnmr(300mhz,cd3od)δ1.27(m,6h),2.19(m,2h),2.57(m,2h),4.11(m,4h),6.36(m,3h).
31
pnmr(100mhz,cd3od):δ44.9;5:
31
pnmr(100mhz,cd3od)δ53.3;esimsm/z ,5:323.01(m na),6:243.09(m na).
[0193]
实例3.乙基(3-(2-(乙酰巯基)乙基)(乙氧基)磷酰基)丙酸酯(7).
[0194][0195]
在100毫升化合物5和6的(10克,38.4毫摩尔,以上比例估计)四氢呋喃溶液中,20℃下1.5小时内逐滴加入硫代乙酸(3毫升,42毫摩尔)和二异丙基乙胺(8.5毫升,48.9毫摩尔)溶于50毫升无水thf的混合溶液。反应在氩气下搅拌24小时,然后浓缩,用乙酸乙酯/正己烷稀释,用1m磷酸二氢钠洗涤,mgso4干燥,过滤,蒸发,sio2色谱纯化(1∶12至1∶10乙酸乙酯/正己烷)得化合物7(10.01克(88%收率)。esimsm/z
319.08(m na).
[0196]
实例4.3-(羟基(2-(吡啶-2-双硫)乙基)磷酰基)丙酸(8).
[0197][0198]
在100毫升化合物7(5克,16.89毫摩尔)的甲醇溶液中加入50毫升的3m的naoh溶液。在氩气下搅拌3h后,混合物在氩气下用3m磷酸中和至ph7.2,然后滴加至200ml2,2
’‑
二硫(5-硝基吡啶)(20克,64.4毫摩尔)的甲醇溶液。在氩气下搅拌4h后,反应有机溶剂被浓缩,乙酸乙酯/正己烷稀释(1∶1),水相被分离,有机相用水洗(3x25毫升)。合并水相用乙酸乙酯/正己烷洗涤(1∶1,35毫升),以盐酸/醋酸酸化至ph3-4,浓缩至约10毫升,加乙腈(60毫升),超声(或快速搅拌)1小时,过滤,滤饼用水/乙腈(1∶10)洗涤。然后将滤液浓缩用sio2柱纯化(水/乙腈/醋酸1∶10∶0.01洗脱),收集相应组分,加入dmf(约5毫升),蒸发至干,得化合物8(4.41克,85%收率)。esims,m/z-306.01(m-h).
[0199]
实例5.(3-((2,5-二氧吡咯-1-基)氧基)-3-氧代丙基)(2-(2-吡啶基二硫)乙基)次磷酸(9).
[0200][0201]
在50毫升化合物8(2.20克,7.16毫摩尔)的dma溶液中加入0.2毫升浓盐酸,浓缩,然后再溶解干dma(60毫升)中。加入nhs(0.90克,7.82毫摩尔)和edc(3克,15.62毫摩尔),将混合物在氩气下搅拌过夜,蒸干,用sio2硅胶柱纯化,洗脱液4∶1∶1丙酮/dcm/醋酸,汇集的馏分蒸干,加入乙醇/甲苯/正己烷混合溶液,固化后得标题化合物(2.11克,73%收率)。1h
nmr(dms0-d6,300mhz)8.39(dd,1h,j=3.5,4.7hz),7.84(m,2h),7.24(m,1h),2.93-2.89 (m,2h),2.74(s,4h),2.41-2.37(m,2h),2.09-2.03(m,4h);ms m/z-403.2(m-h).
[0202]
实例6. 3,6-桥内环氧-δ-四氢酞酰亚胺(15)
[0203][0204]
马来酰亚胺(10.0g,103.0mmol)溶于乙醚(350ml)后,加入呋喃(11.0ml,151.2mmol)。混合物置于1升的高压反应釜中,在100℃下加热8小时。反应釜冷至室温,将釜内反应固体用甲醇溶解,转移至反应瓶中,浓缩,用乙酸乙酯/正己烷重结晶,得目标化合物 16.9g(产率99%)。1h nmr(dmf-d7,300mhz):11.06(s,1h)(nh),6.61(m,2h),5.15(m,2h),2.97(m,2h).13c nmr 178.86,137.72,82.05,49.93.ms m/z 188.4(m na).
[0205]
实例7.乙基(3,6-桥内环氧-δ-四氢苯酞)-乙基)(乙氧基)磷酰基)丙酸酯(16)
[0206][0207]
在60毫升3,6-桥内环氧-δ-四氢酞酰亚胺(2.40g,14.55mmol)dma溶液中加入 k2co3(4.2克,30.39毫摩尔)和ki(0.40克,3.45毫摩尔)。在氩气下搅拌1小时后,加入10毫升的化合物5和6(2.6克,10毫摩尔)的dma溶液。将混合物在氩气下搅拌过夜,浓缩,重新溶解在乙酸乙酯中(100毫升),用水(2
×
50毫升)和1m磷酸二氢钠(2
×
50毫升)洗,na2so4干燥,过滤,浓缩后用sio2色谱柱纯化,洗脱液乙酸乙酯/正己烷(1∶15-1∶8),得标题化合物(3.11 克,81%收率)。esi ms m/z
408.20(m na).
[0208]
实例8. 3-((2-(2,5-双氧-2,5-二氢-1h-吡咯-1-基)乙基)(羟基)或磷酰基)丙酸 (17)
[0209][0210]
化合物16(3克,7.79毫摩尔)与20毫升dma,20毫升甲苯和10毫升8n盐酸的混合物在120-140℃加热8小时。在反应进行时,5
×
10毫升的水逐步加入,使反应体积至40毫升左右。反应浓缩,sio2硅胶柱纯化,洗脱液1∶10∶0.01至1∶8∶0.01水/乙腈/醋酸,得标题化合物 (1.55克,76%收率)。esi ms m/z-260.10(m-h).
[0211]
实例9.(2-(2,5-双氧-2,5-二氢-1h-吡咯-1-基)乙基)(3-((2,5-双氧吡咯-1-基) 氧基)-3-氧代丙基)次膦酸(18)
[0212][0213]
化合物17(1.5克,5.74毫摩尔)溶于50毫升dma,向其中添加0.1毫升的浓hcl,浓缩至干,然后重新溶于40毫升无水dma,然后与nhs(0.71克,6.01毫摩尔)和edc(3克,15.62毫
摩尔)在氩气下搅拌过夜。反应溶液蒸干后用硅胶柱纯化,洗脱液4∶1∶1丙酮/dcm/乙酸,收集的组分蒸干后,加入乙醇/甲苯/正己烷,固化得标题化合物(1.56克,76%收率)。esimsm/z-357.20(m-h).
[0214]
实例10.(3-溴化丁基)(3-乙氧基-3-氧代丙基)次磷酸(29)
[0215][0216]
次磷酸铵(8克,96毫摩尔)和1,1,1,3,3,3-六甲基二硅氮烷(20毫升,96毫摩尔)的混合物在氩气中120℃加热1小时。冷却至0℃后,逐滴加入乙基丙烯酸酯(10.4毫升,96毫摩尔),反应溶液在50℃搅拌2小时,然后冷却至室温,加入1,3-二溴丁烷(40.0毫升),反应物在120℃加热5小时。反应生成的三甲基溴化硅烷在真空下被去除,然后逐滴加入100毫升的水和乙醇(1∶1)的混合溶液,回流0.5小时,然后真空浓缩。反应用水稀释,用0.1mnaoh中和至ph7,用正己烷(2
×
80毫升)洗。水层的ph值调节至~3,用乙酸乙酯萃取(3
×
80毫升)。有机层(乙酸乙酯)是在硫酸镁上干燥,过滤,减压浓缩,在硅胶柱上纯化,用丙酮/二氯甲烷(4∶1)洗脱,得目标化合物29(12.38克,43%收率)。esimsm/z-299.20(m-h).
[0217]
实例11.3-(3-溴丁基)(乙氧基)乙氧基磷酰基)-丙酸乙酯(30)和3-(2-丙烯-1-基(乙氧基)磷酰)丙酸乙酯(31)
[0218][0219]
化合物29(12.20克,40.66毫摩尔)与原甲酸三乙酯(100毫升)混合,回流,用dean-stark分水器除去乙醇和甲酸乙酯。过量的原甲酸三乙酯在真空下被去除,得到30和31(21.8:79.2
31
p核磁比率,10.13克,93%收率)。esimsm/z
30:c
11h22
brnao4p计算值351.04,实测值351.20;31:c
11h21
nao4p计算值271.12,实测值271.20.
[0220]
实例12.3-(3-(乙酰巯基)丁基)(乙氧基)磷酰基)丙酸乙酯(32)
[0221][0222]
在30和31(6.1克,22.76毫摩尔,从上比率估计)的四氢呋喃溶液(100毫升)中逐滴加入硫代乙酸(3.0毫升,42.0毫摩尔)和dipea(8.5毫升,48.9毫摩尔)的thf溶液(50毫升)。在氮气下,50℃搅拌24h后,反应液被浓缩,用正己烷和乙酸乙酯稀释,1.0m磷酸二氢钠洗,在硫酸镁上干燥,过滤,蒸干,用硅胶柱纯化(1∶12至1∶10正己烷/乙酸乙酯洗脱),得到目标化合物32(5.23克,71%收率)。esimsm/z
347.20(m na).
[0223]
实例13.(3-羟基-(3-(2-吡啶-2-双硫)丁基)磷酰基)丙酸(33)
[0224]
[0225]
在化合物32(5.20克16.04毫摩尔)的甲醇溶液(100毫升)中加入50毫升3n的氢氧化钠溶液。在氩气下搅拌3h后,混合物用3m磷酸中和至ph 7.2,然后滴加至2,2
’‑
二硫双(5
‑ꢀ
硝基吡啶)(20克,64.4毫摩尔)的甲醇溶液(200毫升)。在氩气下搅拌24h后,反应液被浓缩,用乙酸乙酯/正己烷(1∶1)稀释,水相被分离,有机相用水洗(3
×
25ml),所有的水相用正己烷-乙酸乙酯(1∶1,35毫升)洗,然后用盐酸/乙酸酸化至ph值3~42,浓缩至~10毫升,用乙腈(60毫升)稀释,超声震荡(或快速搅拌)1小时,过滤,滤饼用水和乙腈(1∶10)洗。滤液被浓缩然后用硅胶柱纯化,洗脱液水/乙腈/乙酸(1∶10∶0.01),在收集的组分中加入dmf(5毫升),浓缩至干,得到目标化合物33(4.40克,81%产率)。esi ms,m/z-334.10(m-h).
[0226]
实例14.(3-((2,5-双氧吡咯-1-基)氧基)-3-氧代丙基)(3-(2-吡啶-双硫)丁基次膦酸)(34)
[0227][0228]
在化合物33(2克,6.56毫摩尔)的dma溶液(50毫升)中加入0.2毫升的浓hcl,浓缩至干,然后重新溶解在无水dma(60毫升)中,向其中加入nhs(0.85克,7.39毫摩尔)和edc(3 克,15.62毫摩尔)在氩气下搅拌过夜。浓缩,硅胶柱纯化,4∶1∶0.01的丙酮/dcm/乙酸洗脱液,组分收集后旋干,加入乙醇/甲苯/正己烷的混合溶液,固化得目标化合物(1.98克,70%收率)。esi ms m/z-431.2(m-h).
[0229]
实例15.(3-溴-3-甲基丁基)(3-乙氧基-3-氧代丙基)次磷酸(37)
[0230][0231]
次磷酸铵(8克,96毫摩尔)和1,1,1,3,3,3-六甲基二硅氮烷(20毫升,96毫摩尔)的混合物在氩气中120℃加热1小时。冷却至0℃后,逐滴加入乙基丙烯酸酯(10.4毫升,96毫摩尔),反应溶液在50℃搅拌2小时,然后冷却至室温,加入1,3-二溴-3-甲基丁烷(44.0毫升),反应物在120℃加热5小时。反应生成的三甲基溴化硅烷在真空下被去除,然后逐滴加入100 毫升的水和乙醇(1∶1)的混合溶液,回流0.5小时,然后真空浓缩。反应用水稀释,用0.1m naoh中和至ph 7,用正己烷(2
×
80毫升)洗。水层的ph值调节至~3,用乙酸乙酯萃取(3
×
80 毫升)。有机层(乙酸乙酯)是在硫酸镁上干燥,过滤,减压浓缩,在硅胶柱上纯化,用丙酮/二氯甲烷(4∶1)洗脱,得目标化合物37(12.95克,43%收率)。esi ms m/z-313.10(m-h).
[0232]
实例16. 3-(3-溴-3-甲基丁基)(乙氧基)磷酰基)丙酸乙酯(38)和3-(乙氧基(3
‑ꢀ
甲基丁-2-烯-1-基)磷酰)丙酸乙酯(39)
[0233][0234]
化合物37(12.90克,41.07毫摩尔)与原甲酸三乙酯(100毫升)混合,回流,用dean
‑ꢀ
stark分水器除去乙醇和甲酸乙酯。过量的原甲酸三乙酯在真空下被去除,得到38和39 (12.5:87.5
31
p核磁比率,9.89克,89%收率)。esi ms m/z
38:c
12h24
brnao4p计算值365.06,
实测值365.10;39:c
12h23
nao4p计算值283.13,实测值285.20.
[0235]
实例17. 3-(3-(乙酰巯基)-3-甲基丁基)(乙氧基)磷酰基)丙酸乙酯(40)
[0236][0237]
在38和39(8.5克,31.25毫摩尔,从上比率估计)的四氢呋喃溶液(100毫升)中逐滴加入硫代乙酸(5.0毫升,70.0毫摩尔)和dipea(12.5毫升,71.9毫摩尔)的thf溶液(80毫升)。在氮气下,70℃搅拌35h后,反应液被浓缩,用正己烷和乙酸乙酯稀释,1.0m磷酸二氢钠洗,在硫酸镁上干燥,过滤,蒸干,用硅胶柱纯化(1∶12至1∶10正己烷/乙酸乙酯洗脱),得到目标化合物40(6.55克,62%收率)。esi ms m/z
361.20(m na).
[0238]
实例18.((3-羟基-3-甲基-3-(2-吡啶-2-双硫)丁基)磷酰基)丙酸(41)
[0239][0240]
在化合物40(6.50克,19.22毫摩尔)的甲醇溶液(100毫升)中加入50毫升3n的氢氧化钠溶液。在氩气下搅拌3h后,混合物用3m磷酸中和至ph 7.2,然后滴加至2,2
’‑
二硫双(5
‑ꢀ
硝基吡啶)(20克,64.4毫摩尔)的甲醇溶液(200毫升)。在氩气下搅拌24h后,反应液被浓缩,用乙酸乙酯/正己烷(1∶1)稀释,水相被分离,有机相用水洗(3
×
25ml),所有的水相用正己烷-乙酸乙酯(1∶1,35毫升)洗,然后用盐酸/乙酸酸化至ph值3~4,浓缩至~10毫升,用乙腈 (60毫升)稀释,超声震荡(或快速搅拌)1小时,过滤,滤饼用水和乙腈(1∶10)洗。滤液被浓缩然后用硅胶柱纯化,洗脱液水/乙腈/乙酸(1∶10∶0.01),在收集的组分中加入dmf(5毫升),浓缩至干,得到目标化合物41(5.16克,77%产率)。esi ms,m/z-348.12(m-h).
[0241]
实例19.(3-((2,5-双氧吡咯-1-基)氧基)-3-氧代丙基)(3-甲基-3-(2-吡啶-双硫)丁基次膦酸(42)
[0242][0243]
在化合物41(2.10克,6.01毫摩尔)的dma溶液(50毫升)中加入0.2毫升的浓hcl,浓缩至干,然后重新溶解在无水dma(60毫升)中,向其中加入nhs(0.80克,6.96毫摩尔)和edc (3克,15.62毫摩尔)在氩气下搅拌过夜。浓缩,硅胶柱纯化,4∶1∶0.01的丙酮/dcm/乙酸洗脱液,组分收集后旋干,加入乙醇/甲苯/正己烷的混合溶液,固化得目标化合物(1.93克,72%收率)。esi ms m/z-445.10(m-h).
[0244]
实例20.次磷酸链接体修饰抗体
[0245]
抗her2抗体(8mg/ml)与10倍摩尔当量的次磷酸链接体(用dma配成30mm贮备溶液) 反应。该反应是在25℃,含5%dma(v/v)的100mm磷酸二氢钠缓冲液(ph7.4)中进行,反应时间分别为15,30,60,120和240分钟。修饰后的抗her2产物经g25凝胶层析(50mm磷酸二氢钠,50mm氯化钠和2mm edta,ph6.5),以除去未反应的链接体。
[0246]
实例21.共轭(偶联)体的制备
[0247]
将含吡啶硫醇(spp)的带电荷链接体溶解在dma中,浓度约10mm。抗体透析到缓冲液a(50mm磷酸二氢钠,氯化钠50mm和2mm edta,ph 6.5)中。8mg/ml抗体和4摩尔当量的链接体混合于含5%dma(v/v)的缓冲液,于环境温度下反应90分钟。未反应的链接体通过 sephadex g25凝胶过滤除去。过滤柱的缓冲液选用缓冲液a(50mm磷酸二氢钠,50mm氯化钠和2mm edta,ph 6.5或150mm磷酸钾和100mm氯化钠,ph7.4)。对于含spp的抗体-链接体产物分析,先使用50mm dtt处理以释放吡啶-2-硫酮再如下所述测量343nm处吸光度(释放出的游离吡啶-2-硫酮的ε
343
=8080m-1
cm-1
)。含巯基的药物(如tubulysin-tz041)溶解在dma(n, n-二甲基乙酰胺)中,浓度约10mm。将相对于抗体-链接体1-1.5倍摩尔当量(相对于抗体上连接体)的药物在搅拌中缓慢地加入到上述含2.5mg/ml抗体连接体的缓冲液a(ph 6.5或 7.4)中,且dma的终浓度为3%(v/v)。该反应在环境温度下持续特定的时间。药物-抗体偶联物用缓冲液b(pbs(磷酸二氢钠),ph 6.5)平衡的sephadex 625柱纯化。药物偶联的程度可通过测量偶联物的a
254
和a
280
来计算。
[0248]
实例22通过含次磷酸基团的二硫键链接体偶联的tubulysin(zt041)-抗体偶联物的体外细胞毒性实验评价
[0249]
靶细胞(如ramos,20000个细胞)与系列梯度浓度稀释的裸抗体或抗体-药物偶联物孵育96小时后,通过碘化丙啶染色和becton dickinson facs(becton dickinson,富兰克林湖区,新泽西州)流式细胞术分析。细胞经488nm激发,测定红色荧光强度(617nm发射, fl2通道)。通过调节前向角和侧向角散射光设定活细胞于某区域(门控区)。失去活力的细胞为偏离门控区的细胞。活细胞数目取六次重复测定的平均值。由活细胞比例所对应的偶联药物的浓度可求得偶联药物的ic
50
值(半数细胞致死浓度)。
[0250]
7.参考文献
[0251]
u.s.专利号.4,680,338,5,122,368,5,141,648,5,208,020,5,416,064;5,475, 092,5,543,390,5,563,250 5,585,499,5,880,270,6,214,345,6,436,931,6,372,738,6, 340,701,6,989,452,7,129,261,7,375,078,7,498,302,7,507,420,7,691,962,7,910, 594,7,968,586,7,989,434,7,994,135,7,999,083,8,153,768,8,236,319.
[0252]
albrecht,h.;et al.j immunol methods 2006,310,100.
[0253]
alley,s.c.;et al.curr opin chem biol 2010,14,529.
[0254]
anderson,d.c.;et al.bioconjug chem 1993,4,10.
[0255]
antczak,c.;et al.bioconjug chem 2006,17,1551.
[0256]
aoki,s.;et al.bioorg med chem 2009,17,3405.
[0257]
austin,c.d.;et al.proc natl aead sci u s a 2005,102,17987.
[0258]
barbour,n.p.;et al.pharm res 1995,12,215.
[0259]
beeson,c.;et al.bioconjug chem 2003,14,927.
[0260]
bickel,u.;et al.bioconjug chem 1995,6,211.
[0261]
chen,j.;et al.expert opin drug deliv 2005,2,873.
[0262]
dijoseph,j.f.;et al.blood 2004,103,1807.
[0263]
doronina,s.o.;et al.bioconjugate chem.,2006,17,114.
[0264]
doronina,s.o.;et al.bioconjug chem 2008,19,1960.
[0265]
ebner,a.;et al.bioconjug chem 2007,18,1176.
[0266]
erickson,h.k.;et al.bioconjug chem 2010,21,84.
[0267]
garsky,v.m.;et al.j.med.chem.,2001,4216.
[0268]
greenwald,r.b.;et al.j.med.chem.,1999,42,3657.
[0269]
haenseler,e.;et al.biochemistry,1992,31,891.
[0270]
hamann,p.r.;et al.bioconjugate chem.,2002,13,40.
[0271]
hamann,p.r.;et al.bioconjugate chem.,2005,16,354.
[0272]
jeffrey,s.c.;et al.j.med.chem.,2005,48,1344
[0273]
johnson,d.a.;et al.cancer res 1991,51,5774.
[0274]
jones,d.s.;et al.bioconjug chem 2001,12,1012.
[0275]
jones,d.s.;et al.bioconjug chem 1999,10,480.
[0276]
jones,d.s.;et al.bioconjug chem 1994,5,390.
[0277]
kashef,n.;et al.j med microbiol 2006,55,1441.
[0278]
kellogg,b.a.;et al.bioconjug chem 2011,22,717.
[0279]
kelly,r.k.;et al.eur j cancer 2011,47,1736.
[0280]
king,h.d.;et al.bioconjug chem 1999,10,279.
[0281]
king,h.d.;et al,j.med.chem.,2002,45,4336
[0282]
klussman,k.;et al.bioconjug chem 2004,15,765.
[0283]
m.;et al.bioconjugate chem.,2002,13,206.
[0284]
kratz,f.,et al.j.med.chem.,2002,45,5523.
[0285]
kumaresan,p.r.;et al.bioconjua chem 2008,19,1313.
[0286]
kumaresan,p.r.;et al.bioconjug chem 2007,18,175.
[0287]
lee,l.s.;et al.bioconjug chem 1999,10,973.
[0288]
li,l.;et al.bioconjug chem 2002,13,985.
[0289]
lipinski,t.;et al.glycoconj j 2011,28,149.
[0290]
meyer-losic,f.;et al.j.med.chem.,2006,49,6908
[0291]
mikolajczyk,s.d.;et al.bioconjua chem 1994,5,636.
[0292]
miller,m.l.;et al.j.med.chem.,2004,47,4802
[0293]
mitchell,j.s.;et al.bioconjug chem 2007,18,268.
[0294]
moon,s.-j.;et al.j.med.chem.,2008,51,6916
[0295]
ojima,i.;et al.j.med.chem.,2002,45,5620
[0296]
ruppert,c.;et al.bioconjug chem 2002,13,804.
[0297]
safavy,a.;et al.bioconjug chem 2003,14,302.
[0298]
safavy,a.;et al.bioconjug chem 2004,15,1264.
[0299]
senter,p.et al.photochem.photobio.,1985,42,231.
[0300]
scott,c.f.,jr.;et al.j natl cancer inst 1987,79,1163.
[0301]
sharkey,r.m.;et al.mol cancer ther 2012,11,224.
[0302]
siiman,o.;et al.bioconjugate chem.,2000,11,549.
[0303]
skwarczynski,m.;et al.j.med.chem.,2006,49,7253
[0304]
srinivasachar,k.;neville,d.m.,jr.biochemistry 1989,28,2501.
[0305]
studer,m.;et al.bioconjug chem 1992,3,424.
[0306]
sun,x.;et al.bioconjug chem 2011,22,728.
[0307]
suzawa,t.;et al.bioorg med chem 2000,8,2175.
[0308]
tadayoni,b.m.;et al.bioconjug chem 1993,4,139.
[0309]
ten hoeve,w.;et al.bioconjug chem 1997,8,257.
[0310]
tsai,n.m.;et al.biotechniques 2001,30,396.
[0311]
walker,m.a.;rt al.bioorg med chem lett 2004,14,4323.
[0312]
wilbur,d.s.;et al.bioconjug chem 2011,22,1089.
[0313]
widdison,w.c.;et al.j.med.chem.,2006,49,4392.
[0314]
zhao,r.y.;et al.j.med.chem.,2011,54,3606
[0315]
zhao,r.y.;et al.j.med.chem.,2012,55,766
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。