磷苯妥英钠固体组合物、冻干方法、及其用途与流程
- 国知局
- 2024-07-12 10:31:16
本发明涉及磷苯妥英钠固体组合物、冻干方法、及其用途。
背景技术:
1、磷苯妥英钠是苯妥英的磷酸酯前药,于1996年9月美国fda批准上市,用于治疗和控制癫痫和其他类型的惊厥状态。在体内转化为苯妥英之前,磷苯妥英钠没有药理活性。因此其药理作用归因于苯妥英。
2、
3、开发磷苯妥英钠旨在替代苯妥英。市场上销售的苯妥英钠注射剂配方中含有过量的丙二醇和较高高的ph值(12),会引起给药部位的严重疼痛,低血压,输液部位远端进行性肢体缺血以及其他血管并发症,包括“紫色手套综合征(purple glove syndrome)”。使用磷苯妥英钠可避免苯妥英钠相关的问题。
4、目前,市售的磷苯妥英钠剂型为注射液,该制剂需要在2-8℃保存,室温保存不能超过48小时。由于磷苯妥英钠注射液室温下不稳定,容易发生降解,产生降解杂质,如二苯基甘氨酸、二苯基海因酸以及苯妥英,从而影响其临床使用的有效性。此外,2-8℃的储存条件增加了磷苯妥英钠注射液的运输和保存成本。磷苯妥英钠在保存中产生的主要降解杂质结构如表1所示:
5、表1磷苯妥英钠降解杂质结构
6、
7、
8、鉴于此,亟需开发磷苯妥英钠的替代剂型,以解决上述技术问题。
9、美国专利文献us 4,925,860中公开了磷苯妥英钠的药物组合物。该专利文献中描述了磷苯妥英钠易于降解,降解产物包括甲醛,5,5-二苯基-4-咪唑啉酮(diz),二苯基甘氨酰胺,二苯甲酮,杂质a和杂质c。该专利文献中表明,ph下降会导致苯妥英的生成速率增加,同时在较低的ph值下杂质c溶解度会降低。由于杂质c是水不溶性的,这使得磷苯妥英钠水性制剂中产生杂质c沉淀,降低了磷苯妥英钠的保存期限,并导致可见颗粒物的问题。该专利文献中教导了使用合适的有机缓冲液如氨丁三醇将ph维持在8.3至9.4,该ph范围可以使得磷苯妥英钠的降解产物主要为二苯基甘氨酰胺,而使得杂质c的产生最小化,从而延长磷苯妥英钠的保质期。该组合物ph范围满足美国药典(usp 28)要求。然而,该专利并未教导如何避免磷苯妥英钠的降解,也没有教导如何获得可以在室温保存的磷苯妥英钠制剂。
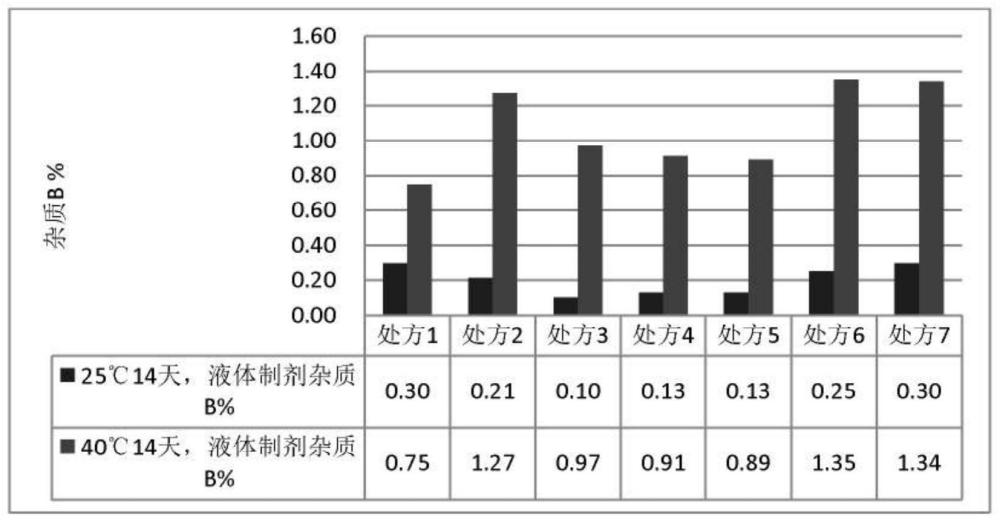
10、本发明人研究发现,按照专利文献us 4,925,860中处方制得的药物组合物,在25℃和40℃条件下存储不稳定,会产生杂质b。
11、欧洲专利文献ep2303228b1公开了含有不同缓冲液的磷苯妥英钠液体制剂。该发明要求保护一种水性药物组合物,其包含磷苯妥英或其盐,和选自碳酸氢钠,磷酸钠,硼酸或甘氨酸的缓冲液,其中该组合物的ph小于8.3。该发明没有教导这些组合物是否稳定,也没有教导这些组合物是否可以冻干并获得室温下稳定的冻干组合物。
12、本发明人研究发现,使用专利文献ep2303228b1披露的处方所制得的磷苯妥英钠液体制剂,在25℃和40℃条件下存储不稳定,会产生杂质b。而将这些液体制剂冻干后,在25℃和40℃条件下存储仍不稳定,会产生杂质a。
13、专利文献us 6,133,248描述了一种具有延长的保质期的药物组合物,其包含磷苯妥英钠、环糊精和药学上可接受的载体。该专利文献表明,在37℃下放置10天,会新产生约10μg/ml的杂质c。杂质c在水性条件下不溶,该专利文献中环糊精的作用是增加杂质c的溶解度,但并不会影响该杂质的产生速率。此外,该专利文献没有提供有效减少杂质c及其他杂质产生的方法。
14、专利文献wo 9904798a1描述了冻干形式的磷苯妥英钠组合物,其可以通过添加药学上可接受的稀释剂(最好是水)来复溶。根据该专利文献的记载,在100mm氨丁三醇缓冲液中配制并冷冻干燥的磷苯妥英钠在复溶时达到大于140mg/ml的溶解度。但是,该专利没有教导磷苯妥英钠的冻干制剂是否稳定。本发明人研究发现,将含有缓冲液(包括氨丁三醇)的磷苯妥英钠组合物冻干后,在25℃和40℃放置14天,会生成杂质a。
15、常规的冷冻干燥过程包括:
16、1)制品的制备(前处理);
17、2)制品的冻结(预冻):将制品冻结成固态;
18、3)第一阶段干燥(升华干燥):将制品中的冰晶以升华方式除去;
19、4)第二阶段干燥(解析干燥):将残留于制品的水分在较高温度下蒸发一部分,使残余水分达到预定要求;
20、5)密封包装。
21、在第一阶段干燥中,物料需要吸收热量。如果不对药品进行加热或热量不足,则水分在升华时会吸收药品本身的热量而使药品的温度降低,致使药品的蒸气压降低,于是引起升华速度的降低,整个干燥的时间就会延长,生产率下降;如果对药品加热过多,药品的升华速率固然会提高,但在抵消了药品升华所吸收的热量之后,多余的热量会使冻结药品本身的温度上升,使药品出现局部甚至全部熔化,引起药品的干缩起泡现象,整个干燥就会失败。因此,第一阶段干燥中,热量的提供必需合适,冻干层必须控制在产品共熔点以下,才不致使冰晶熔化。
22、第二阶段干燥也称为解析干燥。在第一阶段干燥后,在干燥物质的毛细管壁和极性基团上还吸附有一部分水分,这些水分是未被冻结的。当他们达到一定含量时,就为微生物的生长繁殖和某些化学反应提供了条件。实验表明,即使是单分子层吸附的低含水量,也可能成为某些化合物的溶液,产生与水溶液相同的移动性和反应性。因此为了改善产品储存稳定性,延长其保存期,需要尽可能除去这些水分。
23、常规的的冻干工艺中,为了更好的除去产品中的水分,会选择延长冻干时间,从而使得产品的总冻干时间过长,导致冻干时间成本增加,冻干效率下降。目前没有关于磷苯妥英钠高效的冻干方法的研究报道。
技术实现思路
1、针对现有技术中存在的磷苯妥英钠制剂易降解,无法室温保存等技术问题,本发明旨在提供一种磷苯妥英钠固体组合物,以解决上述技术问题。本发明另一个目的在于提供一种高效的磷苯妥英钠冻干方法。
2、本发明提供一种磷苯妥英钠固体组合物,其特征在于,含有磷苯妥英钠和至少一种碳水化合物。
3、优选地,所述固体组合物可室温保存。
4、优选地,所述固体组合物是冻干组合物。
5、优选地,所述碳水化合物选自糖、寡糖的至少一种。
6、优选地,所述糖选自单糖、二糖、糖醇中的至少一种。
7、优选地,所述单糖选自葡萄糖、半乳糖、果糖中的至少一种。
8、优选地,所述二糖选自蔗糖、乳糖、海藻糖、麦芽糖、异麦芽糖中的至少一种。
9、优选地,所述糖醇选自山梨醇、甘露醇、木糖醇、麦芽糖醇中的至少一种。
10、优选地,所述寡糖选自棉籽糖、水苏糖、异麦芽低聚糖、低聚果糖、低聚甘露糖、大豆低聚糖中的至少一种。
11、优选地,在冻干前,所述碳水化合物在组合物中的重量体积比为1~20%,优选3~15%,更优选5~10%。
12、优选地,所述固体组合物还含有缓冲剂。
13、优选地,所述缓冲剂为选自磷酸盐缓冲剂、磷酸氢盐缓冲剂、磷酸二氢盐缓冲剂、碳酸氢盐缓冲剂、碳酸盐缓冲剂、硼酸缓冲剂、硼酸盐缓冲剂、氨基酸缓冲剂、三烷基胺缓冲剂、氨丁三醇缓冲剂、焦磷酸盐缓冲剂、甘氨酰甘氨酸(双甘氨肽)缓冲剂中的一种或多种;优选地,所述磷酸盐、磷酸氢盐、磷酸二氢盐、碳酸氢盐、碳酸盐、硼酸盐、焦磷酸盐各自独立地为钠盐、和/或钾盐;所述三烷基胺为三甲胺。
14、优选地,在冻干前中,所述缓冲剂的浓度为10~150mm,更优选20~100mm。
15、优选地,所述磷苯妥英钠固体组合物在冻干前、或复溶后的ph值为8~10,优选为8~9.3,更优选为8~9。
16、优选地,在冻干前,所述磷苯妥英钠的浓度为75mg/ml至150mg/ml,优选为75mg/ml至100mg/ml;更优选为75mg/ml或100mg/ml。
17、优选地,在复溶后,所述磷苯妥英钠的浓度为75mg/ml至150mg/ml,优选为75mg/ml至100mg/ml;更优选为75mg/ml。
18、优选地,所述磷苯妥英钠固体组合物在25℃和60%的相对湿度下14天没有杂质a、杂质b和杂质c产生。
19、优选地,所述磷苯妥英钠固体组合物在25℃和60%的相对湿度下3个月没有杂质a、杂质b和杂质c产生。
20、优选地,所述磷苯妥英钠固体组合物在40℃和75%相对湿度下放置14天没有杂质a、杂质b和杂质c产生。
21、优选地,所述磷苯妥英钠固体组合物在40℃和75%相对湿度下放置3个月没有杂质a、杂质b和杂质c产生。
22、优选地,所述固体组合物是冻干组合物,所述冻干组合物含有磷苯妥英钠、缓冲剂和至少一种碳水化合物;所述缓冲剂选自氨丁三醇;所述碳水化合物选自海藻糖、蔗糖、甘露醇或乳糖;所述冻干组合物在冻干前、或复溶后的ph值为8~9。
23、优选地,冻干前,所述磷苯妥英钠的浓度为75mg/ml或100mg/ml,所述缓冲剂的浓度为20~100mm,所述碳水化合物在组合物中的重量体积比为5~10%。
24、另一方面,本发明还提供一种磷苯妥英钠的冻干方法,其特征在于,所述冻干方法的总冻干时间比常规冻干方法的总冻干时间减少60%以上,优选减少70%以上。
25、优选地,所述方法包括:(1)配制磷苯妥英钠溶液;(2)将所述磷苯妥英钠溶液进行预冻;(3)不单独设置升华干燥步骤和解析干燥步骤,而以一定的升温速率将隔板温度直接升温至预定的温度进行干燥。
26、优选地,所述磷苯妥英钠溶液中含有磷苯妥英钠和至少一种碳水化合物;
27、优选地,所述碳水化合物选自糖、寡糖中的至少一种,所述糖选自单糖、二糖、糖醇中的至少一种;
28、优选地,所述单糖选自葡萄糖、半乳糖、果糖中的至少一种;
29、优选地,所述二糖选自蔗糖、乳糖、海藻糖、麦芽糖、异麦芽糖中的至少一种;
30、优选地,所述糖醇选自山梨醇、甘露醇、木糖醇、麦芽糖醇中的至少一种;
31、优选地,所述寡糖选自棉籽糖、水苏糖、异麦芽低聚糖、低聚果糖、低聚甘露糖、大豆低聚糖中的至少一种;
32、优选地,所述碳水化合物的重量体积比为1~20%,优选3~15%,更优选5~10%;
33、优选地,所述磷苯妥英钠溶液的ph值为8~10,优选为8~9.3,更优选为8~9;
34、优选地,所述磷苯妥英钠溶液还含有缓冲剂;
35、优选地,所述缓冲剂为选自磷酸盐缓冲剂、磷酸氢盐缓冲剂、磷酸二氢盐缓冲剂、碳酸氢盐缓冲剂、碳酸盐缓冲剂、硼酸缓冲剂、硼酸盐缓冲剂、氨基酸缓冲剂、三烷基胺缓冲剂、氨丁三醇缓冲剂、焦磷酸盐缓冲剂、甘氨酰甘氨酸(双甘氨肽)缓冲剂中的一种或多种;优选地,所述磷酸盐、磷酸氢盐、磷酸二氢盐、碳酸氢盐、碳酸盐、硼酸盐、焦磷酸盐各自独立地为钠盐、和/或钾盐;所述三烷基胺为三甲胺;
36、优选地,所述缓冲剂的浓度为10~150mm,更优选20~100mm;
37、优选地,所述磷苯妥英钠的浓度为75mg/ml至150mg/ml;更优选为75mg/ml至100mg/ml;进一步优选为75mg/ml或100mg/ml。
38、优选地,所述的冻干方法中,第(2)步骤中预冻温度为-40~-60℃,优选为-45~-55℃,更优选为-45~-50℃。
39、优选地,降温至所述预冻温度的降温速率为0.5~6℃/min,优选为1~5℃/min,更优选为1~1.5℃/min。
40、优选地,所述第(3)步骤中,所述升温速率为0.01~5℃/min,优选为0.025~3℃/min,更优选为0.05~1.5℃/min。
41、优选地,所述隔板温度直接升温至5~25℃,优选升温至10~25℃,更优选升温至20~25℃。
42、优选地,所述的磷苯妥英钠固体组合物用于治疗癫痫或其他惊厥状态。
43、另一方面,还提供所述的磷苯妥英钠固体组合物在制备治疗癫痫或其他惊厥状态的药物中的用途。
44、另一方面,还提供一种治疗癫痫或其他惊厥状态的方法,包括给予需要的患者治疗癫痫或其他惊厥状态有效量的上述磷苯妥英钠固体组合物。
45、本发明说明书和权利要求中,除非另有说明,否则本发明中使用的科学和技术名词具有本领域技术人员所通常理解的含义。然而,为了更好地理解本发明,下面提供部分相关术语的定义和解释。
46、本发明中碳水化合物的分类引自文献“carbohydrates in human nutrition:report of a joint fao/who expert consultation,rome,14-18april 1997”。其中糖是指聚合度为1~2的糖类总称,包括单糖、二糖及糖醇,如葡萄糖、半乳糖、果糖、蔗糖、乳糖、海藻糖、麦芽糖、异麦芽糖、山梨醇、甘露醇、木糖醇、麦芽糖醇。寡糖是指聚合度为3~9的糖类总称,如棉籽糖、水苏糖、异麦芽低聚糖、低聚果糖、低聚甘露糖、大豆低聚糖。
47、本发明中碳水化合物的百分比(%)指重量体积比,所述的“重量体积比”是指每100ml液体体系中含有所述成分的重量(单位g),即g/100ml。
48、本发明中缓冲剂的浓度单位mm指毫摩尔浓度,所述的“毫摩尔浓度”是指每1l液体体系中含有所述成分的毫摩尔数(单位mmol),即mmol/l。
49、本发明中所有稳定性研究中,25℃条件下,相对湿度为60%;40℃条件下,相对湿度为75%。
50、本发明中rp-hplc,是指反相高效液相色谱。
51、本发明中检测限是指样品中被测物能被检测到的最低量。其中,本发明中杂质a的检测限是11.0pg,杂质b的检测限为6.3pg,杂质c的检测限为4.5ng。
52、本发明中所述的“无杂质产生”、“没有杂质a、杂质b以及杂质c产生”、“没有检测到杂质a、杂质b、以及杂质c,也没有检测到其他杂质”、“没有杂质a、杂质b和杂质c以及其他杂质的产生”、“未出现杂质”等类似表述均指待测物中相应杂质低于检测限。
53、本发明中所述的“未检出”是指待测物中相应杂质低于检测限。
54、本发明中附图2、附图3中杂质含量为0,表示相应杂质未检出,也即杂质低于检测限。
55、本发明中所述的“n/a”表示不适用。
56、本发明中所述的“pes”表示聚醚砜。
57、本发明中水含量通过karl fischer滴定法测定。
58、本发明中采用fts lyo star ii冻干机中冻干。
59、本发明中的术语“复溶”表示用水性溶液(包括但不限于乙醇、水、缓冲液、氯化钠溶液、葡萄糖水溶液或其混合物,例如注射用水、生理盐水等)将冻干制剂的各组分溶解以获得复溶后的药物制剂。本发明中冻干制剂的复溶可以采用本领域技术人员通常所熟知的技术手段进行。因此,将冻干制剂复溶后可获得复溶制剂。
60、有益效果
61、本发明提供的磷苯妥英钠固体组合物,稳定性好,能够在室温下保存。而市售的磷苯妥英钠注射液必须在2-8℃储存,即使在如此低温下保存,市售产品仍不可避免会产生杂质。
62、作为本发明本发明中一方面的技术方案,所提供的磷苯妥英钠固体组合物,其在25℃和60%湿度条件、40℃和75%湿度条件下放置14天,没有杂质a、杂质b和杂质c产生。
63、作为本发明中另一方面的技术方案,所提供的磷苯妥英钠固体组合物,其在2-8℃、25℃和60%湿度条件、40℃和75%湿度条件下放置1个月、2个月和3个月,没有杂质a、杂质b和杂质c产生。
64、另外,本发明提供的磷苯妥英钠的冻干方法,所述冻干方法采用非常规冻干方法,没有设置独立的升华干燥和解析干燥阶段,而以一定升温速率将隔板温度直接升温至预定温度(例如20℃等)进行冻干,水分含量符合质量要求,冻干时间有了明显的缩短,而且冻干后的产品复溶性较好,在1分钟内可以完全复溶,方便临床上使用。
65、作为本发明中另一方面的技术方案,所提供的冻干工艺,冻干产品质量稳定,在25℃和60%湿度条件、40℃和75%湿度条件下放置14天,没有杂质a、杂质b和杂质c产生。
66、作为本发明中另一方面的技术方案,所提供的冻干工艺,冻干产品质量稳定,在2-8℃、25℃和60%湿度条件、40℃和75%湿度条件下放置1个月、2个月和3个月,没有杂质a、杂质b和杂质c产生。
本文地址:https://www.jishuxx.com/zhuanli/20240614/87451.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。