医用注射装置制造方法及由此制得的医用注射装置与流程
- 国知局
- 2024-06-20 12:57:17
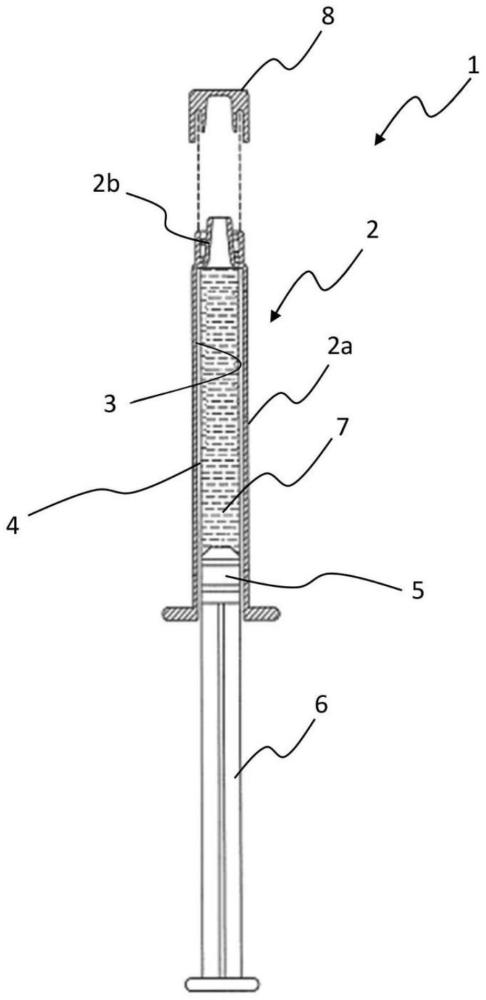
本发明涉及一种医用注射装置制造方法,该医用注射装置包括内表面涂覆涂层的玻璃筒体,该筒体配置为以滑动接合方式接纳柱塞;本发明还涉及一种通过上述方法获得的医用注射装置以及一种组装上述医用装置的套组。
背景技术:
1、众所周知,注射装置通常包括容器内滑动接合的密封柱塞,以便通过注射将药物分配给患者,这样的注射装置广泛应用于医疗领域。
2、这种注射装置包括注射针、药筒以及用于皮下和/或静脉注射药物的自助式注射器或自动式注射器。
3、此类装置中,首先需要满足的是,柱塞在注射装置筒体(例如注射器的筒体)内呈现最佳的滑动性能(在静摩擦及动摩擦方面)。为此,使用通常硅油基润滑物质来施涂注射器主体的内表面和柱塞。特别是,采用润滑物质的目的是优化柱塞的滑动性能,特别是降低克服静摩擦所需作用力(松脱力)和滑动柱塞时克服动摩擦所需作用力(平均滑动力)。
4、另一个亟需解决的问题是,尤其是在注射装置(例如预灌药式注射器)情况下,应尽量保持柱塞的滑动性能长期不变。
5、事实上,一方面若用预灌式注射装置来确保给药便捷及管理灵活,另一方面则意味着注射装置灌装后必然要储存相当长的时间,大约几周或几个月,有时甚至更久,例如在蛋白类药物或疫苗的情况下,还需要在极低温下储存,从而保证药物稳定性及延长保质期。
6、然而,人们相信存在硅基涂层正是生物技术药物、特别是重组蛋白不稳定的因素之一,这种不稳定性则与内在结构敏感性有关。实际上,硅油会分离到溶液中形成微粒,文义归类为内在微粒,在硅水界面上可能有蛋白吸附到微粒上,蛋白可能会发生结构变性和聚集,从而导致微粒本身出现团聚。聚集现象至关重要的原因是,可能导致治疗效果丧失,增加免疫原性风险。
7、因此,预灌式注射装置中出现的另一重要需求是,即不仅要长期保持涂层的最佳滑动性能,还要长期保持硅粒在药物配方中的低释放性。
技术实现思路
1、本技术人注意到,目前已有几种医用注射装置制造方法来尝试满足上述需求,但这些方法会引发管理或复杂性问题,因此也会产生成本问题,而这些问题迄今尚未得到解决。
2、某些情况下会使用不同类硅油的混合物,可能还添加了其他物质。就此,本技术人注意到,越是弃离纯硅(即,无混合或无添加),长期保持其性质和行为就越发困难。
3、人们还曾提议对沉积在注射器内表面上的有机硅层进行辐照,使硅至少部分交联,事实表明这有利于实现降低微粒释放值。这种辐照可以借助uv、ir、伽马射线、离子轰击,也可以借助真空或大气压下火炬型或电晕效应型等离子体处理。
4、某些情况下,人们提出了沉积几个连续的硅层,也可能经历辐照。
5、此类采用含添加剂的硅或混合硅还可能需要辐照处理的过程例如参阅专利文献us20020012741a1、ep3378514a1、us7648487b2、us9662450b2、us10066182b2、ep2387502b1、us7553529b2、us20110276005a1、ep2081615b1、us5338312a、us4844986a、us4822632a、us20080071228a1。
6、专利文献wo2013045571a1中还描述了旨在获得满足滑动佳且释放低这两项要求的注射器的方法,这两点均需长期保持恒定(还需长期保持厚度不变)。该文献公开了将运动粘度为900cst至1200cst的有机硅喷涂到注射器内表面上,随后进行等离子体处理使有机硅表现出高稳定性且低释放性。该文献指出了有机硅表面等离子处理中释放低的原因。
7、专利文献wo2009053947a2和wo2015136037a1提供了类似的技术方案。
8、所有这些文献都表明采用运动粘度相当低(大约1000cst)的有机硅,结合辐照处理,特别是等离子体处理,作为解决上述问题的最佳组合。
9、专利文献de 10000505还公开了一种空心筒体内部硅化方法,其中运动粘度优选为350cst~20000cst的硅油沉积在体腔内壁上。硅油特别是通过喷墨印刷中所用类型的喷头喷洒沉积,某一实施例中,可以加热喷头。
10、然而,本技术人观察到,上述现有技术公开的制造方法,除了意味着医用注射装置的制造时间延长并且方法本身的管理复杂度加剧外,还可能引发现有技术中尚未发现的问题,即灌装药物后,需要对医用注射装置进行目视检查,确定不存在缺陷以及可光学检测微粒形式的外来污染物。
11、这种检查早先必须借助人工,目前可派给基于光学采集系统图像分析技术的自动化设备。医用注射装置内含溶液的纯度要求不断提高,因此控制装置不仅要突出显示液体中存在的超小杂质,而且还要将杂质与容器外观不构成杂质的缺陷区分开来,因此,错误分类则会导致医用注射装置报废。
12、就此,本技术人观察到,施涂到医用注射装置的筒体内表面的硅油层部分交联,特别是通过等离子体辐照获得的部分交联,产生了更不规则却更稳定的表面结构,这可能会误导自动光学检测系统将表面的不规则错误归类为杂质,从而产生本不该存在的生产废料,造成经济损失。
13、有鉴于此,本技术人认识到,需要开发一种医用注射装置制造方法,该方法不仅能够满足上述需求,使柱塞在注射装置筒体内表现出最佳滑动性能(静摩擦及动摩擦方面)以及低微粒释放的最佳特性,这两种特性都能长期保持不变,而且还能减少医用注射装置的目视检查器件可能错误检测到虚假缺陷的相关问题。
14、本技术人了解到,与现有技术相比,通过改变涂料组合物流变特性以及涂料组合物用于涂覆医用注射装置筒体内表面的涂覆方法,可以实现所有这些预期特征。
15、特别是,本技术人经实验证实,通过使用涂料组合物来涂覆医用注射装置筒体内表面,该涂料组合物基本几乎全部由单一类型的硅油构成,该硅油在室温下的运动粘度远高于现有技术采用的硅油,将这种硅油热涂到筒体内表面上,施涂到该表面的涂层冷却后,能够同时获得:
16、所需的最佳滑动性和低微粒释放性,两者皆基本长期恒定;以及
17、最佳涂层表面规整性,从而医用注射装置的目视检查器件不会受到误导。
18、特别是,实验中,上述涂层表面规整性与现有技术中使用低运动粘度但高微粒释放率的硅油所得的非交联涂层表面规整性相当。尽管使用的硅油在室温下的运动粘度要高得多,尽管施涂的涂层平均厚度很薄,大约只有100-250纳米,
19、但实验中,相较于现有技术中使用低运动粘度硅油所得的部分交联涂层,上述涂层表面规整性得到改善。
20、另外,本技术人经实验证实,通过使用上述涂料组合物来涂覆医用注射装置筒体内表面,该涂料组合物基本几乎全部由单一类型的硅油构成,该硅油在室温下的运动粘度远高于现有技术采用的硅油,将这种硅油热涂到筒体内表面上,施涂到该表面的涂层冷却后,还能获得大规模工业生产所需的涂覆均匀性和高度工艺重现性。
21、因此,本发明第一方面涉及一种如权利要求1和2定义的医用注射装置制造方法,该医用注射装置包括内表面涂覆涂层的玻璃筒体,该筒体配置为以滑动接合方式接纳柱塞。
22、特别是,根据第一实施例,本发明医用注射装置制造方法包括如下步骤:
23、(a)提供涂料组合物,其包含等于或大于92wt.%的聚二甲基硅氧烷,其室温下运动粘度为11500cst(115cm2/s)至13500cst(135cm2/s);
24、(b)将涂料组合物加热到100℃至150℃的温度;
25、(c)将加热到所述温度的涂料组合物施涂到筒体内表面上,以在所述内表面上形成涂层,通过光学反射法测得其平均厚度s为100nm至250nm;
26、其中,筒体内表面涂层的厚度标准差等于或小于90nm。
27、此外,本发明第二实施例中,本发明医用注射装置制造方法包括如下步骤:
28、(a)提供涂料组合物,其包含等于或大于92wt.%的聚二甲基硅氧烷,其室温下运动粘度为11500cst(115cm2/s)至13500cst(135cm2/s);
29、(b)将涂料组合物加热到100℃至150℃的温度;
30、(c)将加热到所述温度的涂料组合物施涂到筒体内表面上,以在所述内表面上形成涂层,通过光学反射法测得其平均厚度为100nm至250nm;
31、其中,对于每批10个筒体,涂层厚度的批平均标准差sd的值等于或小于70nm;
32、其中,批平均标准差sd通过如下方式获得:
33、(i)在批次中第i筒体的平面展开轴向长度为1.0mm的每个任意部分ni的至少6个点处测量涂层厚度spi;
34、(ii)对于批次中第i筒体的每个所述部分ni以及对于每个第i筒体,通过下式计算平均厚度sni:
35、sni=(σp=1,6spi)/6
36、(iii)对于每个筒体部分n,通过下式计算该部分n的批平均厚度snl:
37、snl=(σi=1,10sni)/10
38、(iv)对于批次中10个注射器,计算关于部分n的批平均厚度snl的标准差sdn;及
39、(v)通过下式根据厚度标准差sdn的值来计算批平均标准差sd:
40、sd=(σi=1,n sdn)/n
41、其中n为批次中每个筒体的部分n的总数。
42、本技术人经实验发现,如下详述,通过室温下热涂上述基于聚二甲基硅氧烷的高粘度涂料组合物,在筒体内表面上形成的涂层可以在施涂和分布方面与低粘度硅油表现出相同的效果。
43、本技术人经实验还发现,涂层冷却后且粘度特性恢复到室温粘度特性后,与现有技术所述的低粘度涂层(无论是否经受部分交联处理)相比,实现了一系列有利的改进特性。
44、第一,本技术人经实验观察到,本发明方法形成的涂层有利地不仅能够具有制药和化妆品工业所需的低厚度值,而且还能在筒体内表面上沿着每段筒体分布得非常均匀。
45、特别是,本技术人经实验观察到,本发明方法在筒体内表面上施涂的涂层厚度值能够有利地完全与现有技术中采用低粘度硅油所得的厚度值相当。
46、本技术人经实验观察到,筒体内表面所施涂层的粘度一旦返回到其在室温下的粘度值,就会赋予涂层稳定特性,允许克服未经受部分交联的低粘度(如前所述,大约1000cst)硅油形成涂层的所有缺陷。
47、特别是,本发明方法形成的涂层能够有利地克服现有技术中非交联涂层的下列缺陷:
48、筒身在储存期间处于直立位时,硅在重力作用下朝筒身下部迁移,因此硅层随着时间推移趋于沿着医用注射装置(例如注射器)的筒体轴线形成不均匀的分布;
49、使用医用注射装置(例如注射器)时会导致柱塞滑动阻力不均匀;
50、药物就更有可能与医用注射装置(例如注射器)的筒体的制造材料(玻璃)直接相互作用,部分涂层也更有可能从表面脱落到溶液中;
51、特别是结合搅拌等机械应力的情况下,或者通过滑动柱塞分配筒体内含液体时,可能触发变性和蛋白聚集现象。
52、因此,本发明方法能够有利地形成具有厚度特性、均匀特性和稳定特性的涂层,使柱塞在筒体中实现最佳滑动特性,尽管形成该涂层的硅油粘度远高于上文现有技术文献提出的硅油。
53、第二,本技术人经实验观察到,本发明方法能够有利地形成高表面规整性和高覆盖均匀性的涂层,使得医用注射装置的目视检查器件、特别是自动化型目视检查器件不会受到误导。
54、特别是,本发明方法能够有利地在筒体内表面上获得厚度非常均匀的涂层,通过光学反射法(或取决于分辨率的光学干涉法)测得涂层的厚度标准差等于或小于90nm。
55、这样,涂层不会引发虚假缺陷问题,从而解决了现有技术中部分交联硅涂层存在的问题。
56、有利地,本发明方法还能在筒体内表面上获得平均厚度完全符合制药和化妆品工业要求的涂层,尽管这种涂层是由高运动粘度的硅材构成。
57、第三,本技术人经实验观察到,本发明方法形成的涂层因涂层室温粘度值相关的稳定特性而能够有利地表现出医用注射装置筒体内储存溶液中低微粒释放特性。
58、根据本技术人进行的测试,这些低微粒释放特性与现有技术中部分交联硅涂层特性完全相当或有所改进,而现有技术中部分交联硅涂层却会引发上述虚假缺陷问题。
59、第四,本技术人经实验观察到,在室温或高于室温储存情况下,上述最佳柱塞滑动特性和筒体内储存溶液中低微粒释放特性长期保持基本恒定,在低温储存情况下,满足制药和化妆品行业的另一点重要需求。
60、第五,本技术人经实验观察到,在医疗器械的不同生产批次内,能够高度重现性获得上述涂层平均厚度均匀特性,这正是制药和化妆品行业典型大规模生产中非常理想的特性。再者,尽管该涂层是由高运动粘度的硅材构成。
61、本发明另一方面涉及一种如权利要求25定义的制造医用注射装置的设备,该医用注射装置包括内表面涂覆涂层的玻璃筒体,该筒体配置为以滑动接合方式接纳柱塞。
62、特别是,本发明制造医用注射装置的设备包括:
63、涂料组合物的储罐,该储罐的至少一个加热元件配置为加热所储存的涂料组合物;
64、至少一个分配头,该分配头配置为分配经加热的涂料组合物并设置有至少一个分配喷嘴,分配头各自的加热元件配置为加热喷嘴所分配的涂料组合物;
65、布置于分配头上游的循环泵;
66、各医用注射装置的一个或多个筒体的支撑框架;
67、其中,所述至少一个分配头与支撑框架可彼此相对移动,以将所述至少一个分配头的喷嘴插入/拔出所述一个或多个筒体中的相应筒体。
68、本发明又一方面涉及一种如权利要求28和29定义的医用注射装置。
69、特别是,根据第一实施例,本发明医用注射装置包括内表面涂覆涂层的玻璃筒体,该筒体配置为以滑动接合方式接纳柱塞,
70、其中,所述筒体内表面涂层基本上由聚二甲基硅氧烷制成,其室温下运动粘度为11500cst(115cm2/s)至13500cst(135cm2/s),平均厚度为100nm至250nm;
71、其中,筒体内表面涂层的厚度标准差等于或小于90nm。
72、另外,根据第二实施例,本发明医用注射装置包括内表面涂覆涂层的玻璃筒体,该筒体配置为以滑动接合方式接纳柱塞,
73、其中,所述筒体内表面涂层基本上由聚二甲基硅氧烷制成,其室温下运动粘度为11500cst(115cm2/s)至13500cst(135cm2/s),平均厚度为100nm至250nm;
74、其中,对于每批10个筒体,涂层厚度的批平均标准差sd的值等于或小于70nm;
75、其中,批平均标准差sd通过如下方式获得:
76、(i)在批次中第i筒体的平面展开轴向长度为1.0mm的每个任意部分ni的至少6个点处测量涂层厚度spi;
77、(ii)对于批次中第i筒体的每个所述部分ni以及对于每个第i筒体,通过下式计算平均厚度sni:
78、sni=(σp=1,6spi)/6
79、(iii)对于每个筒体部分n,通过下式计算该部分n的批平均厚度snl:
80、snl=(σi=1,10sni)/10
81、(iv)对于批次中10个注射器,计算关于部分n的批平均厚度snl的标准差sdn;及
82、(v)通过下式根据厚度标准差sdn的值来计算批平均标准差sd:
83、sd=(σi=1,n sdn)/n
84、其中n为批次中每个筒体的部分n的总数。
85、有利地,上述注射装置实现了上文就其制造方法说明的有利技术特征以及有关筒体内表面涂层实现特性的有利技术特征。
86、本发明还一方面涉及一种如权利要求46和47定义的组装医用注射装置的零件套组。
87、特别是,根据第一实施例,本发明零件套组包括无菌包装中的下列单独部件:
88、内表面涂覆涂层的玻璃筒体,该筒体配置为以滑动接合方式接纳柱塞,
89、柱塞,该柱塞配置为滑动接合在所述筒体中,
90、其中,所述筒体内表面涂层基本上由聚二甲基硅氧烷制成,其室温下运动粘度为11500cst(115cm2/s)至13500cst(135cm2/s),平均厚度s为100nm至250nm;
91、其中,通过光学反射法测得筒体内表面涂层的厚度标准差等于或小于90nm。
92、另外,根据第二实施例,本发明零件套组包括无菌包装中的下列单独部件:
93、内表面涂覆涂层的玻璃筒体,该筒体配置为以滑动接合方式接纳柱塞,
94、柱塞,该柱塞配置为滑动接合在所述筒体中,
95、其中,所述筒体内表面涂层基本上由聚二甲基硅氧烷制成,其室温下运动粘度为11500cst(115cm2/s)至13500cst(135cm2/s),平均厚度为100nm至250nm;
96、其中,对于每批10个筒体,涂层厚度的批平均标准差sd的值等于或小于70nm;
97、其中,批平均标准差sd通过如下方式获得:
98、(i)在批次中第i筒体的平面展开轴向长度为1.0mm的每个任意部分ni的至少6个点处测量涂层厚度spi;
99、(ii)对于批次中第i筒体的每个所述部分ni以及对于每个第i筒体,通过下式计算平均厚度sni:
100、sni=(σp=1,6spi)/6
101、(iii)对于每个筒体部分n,通过下式计算该部分n的批平均厚度snl:
102、snl=(σi=1,10sni)/10
103、(iv)对于批次中10个注射器,计算关于部分n的批平均厚度snl的标准差sdn;及
104、(v)通过下式根据厚度标准差sdn的值来计算批平均标准差sd:
105、sd=(σi=1,n sdn)/n
106、其中n为批次中每个筒体的部分n的总数。
107、有利地,上述零件套组允许采取无菌方式储存、运输并随后组装本公开注射装置。
108、定义
109、本说明书及所要求保护技术方案的范畴内,术语“室温(room temperature,rt)”表示60%相对湿度下测得的25℃±2℃温度。
110、本说明书及所要求保护技术方案的范畴内,具体注明的所有百分比均理解为按重量百分比计。
111、本说明书及所要求保护技术方案的范畴内,术语“平均值(average value)”是指所考虑具体实体值的算术平均值。
112、本说明书及所要求保护技术方案的范畴内,所有压力值均应理解为相对压力值。换言之,本文注明的压力值不包括大气压,除非另作声明。
113、本说明书及所要求保护技术方案的范畴内,表示数量、参数、百分比等所有数值实体应理解为在任何情况下均前缀术语“约(about)”,除非另作声明。另外,除了下文具体注明之外,所有数值实体范围还包括最大数值和最小数值的所有可能组合以及所有可能中间范围。
114、本说明书及所要求保护技术方案的范畴内,通过tga和dsc热重分析技术测量聚二甲基硅氧烷的运动粘度。
115、热重分析(thermogravimetry,tg)或热重分析(thermogravimetric analysis,tga)是一种用于表征更广泛热分析系列材料的实验技术。该技术包括在受控气氛条件下,连续测量材料样品质量随时间变化(等温)或随温度变化(升温/降温)。
116、dsc技术可以确定何温度或温度范围内发生任何转变(例如熔化或结晶过程)并定量测量与之相关的能量。dsc分析实际上测定样品在受控式加热/冷却(动态条件)或保持恒温(等温条件)时出现的热流。
117、通过这两种技术的结合,可以将所获得的热曲线与已知粘度硅油的标准曲线相关联,从而确定硅材的运动粘度。
118、这样就能使用校准曲线来确定硅材的运动粘度,该校准曲线能够将粘度值(与聚合物链长度相关)与不同温度下观察到的热现象(重量损失)相关联。
119、用多份二氯甲烷萃取涂层中存在的聚二甲基硅氧烷,二氯甲烷会在分析前蒸发。
120、采用tga 4000型热重分析仪(perkinelmer)进行tga分析,而采用dsc 204f1型差示扫描量热计(netzsch)进行dsc分析。
121、tga分析遵循的热循环为:从30℃到500℃,升温速率为10℃/min。
122、dsc分析遵循的热循环为:从-80℃到30℃,升温速率为10℃/min。
123、本说明书及所要求保护技术方案的范畴内,施涂到注射装置的筒体内表面上的涂层厚度应理解为通过基于发射光辐照(白光或特定波长的激光)撞击分析样品的光学技术来测量。
124、光学反射计等仪器检测两束光的反射波长差异,一束光反射自注射装置的筒体材料(玻璃),另一束光反射自涂层。这种差异允许通过获知所分析样品的折射率和几何形状来确定层厚。如果分析过程中使用白光作为光源,仪器可以检测到最小厚度80nm。通过使用特定准直波长(激光),例如630~680nm准直波长,分辨率可提高到20nm,在此情况下能够使用干涉技术。
125、本说明书及所要求保护技术方案的范畴内,涂层的平均厚度s特别是优选地通过如下方式获得:
126、(i)在平面展开轴向长度为1.0mm的每个任意筒体部分n的至少6个点处测量涂层厚度sp;
127、(ii)计算各个上述n个筒体部分的平均厚度sn,其中sn=(σp=1,6sp)/6;
128、(iii)计算筒体涂层平均厚度s,其中s=(σn=1,n sn)/n,n为筒体部分n的总数。
129、一般而言,本说明书及所要求保护技术方案的范畴内,在n个统计单位组成的群体检测到实体“x”(例如施涂到注射装置的筒体内表面的涂层厚度)的术语“标准差(standarddeviation)”或“均方差(average square deviation)”定义为:
130、
131、其中,
132、
133、为实体“x”的算术平均值。
134、特别优选地,施涂到注射装置的筒体内表面的涂层厚度标准差的获得方式是根据上述三点(i)-(iii)确定涂层平均厚度s,以及
135、(iv)计算上述n个筒体部位的平均厚度sn相对于筒体涂层平均厚度s的标准差sd。
136、本发明实施例的范畴内,如上所述,可以获得施涂到一批预定个数筒体(例如10个筒体)中每个筒体的内表面涂层的平均厚度以及涂层的批标准差。
137、本发明实施例的范畴内,“涂层的批平均厚度标准差sd”是指如上所获厚度标准差sdn的算术平均值。如上所述,该参数表明不同生产批次之间的工艺重现性。
138、本发明各实施例的范畴内,注射装置筒体中平面展开轴向长度为1.0mm的n个部分的总数(由n表示)随筒体本身尺寸变化。
139、因此,例如,在注射器标称容积为0.5ml的情况下,注射装置的n个部分的总数n等于40,在注射器标称容积为1.0ml long的情况下,总数n等于45,在注射器标称容积为3.0ml情况下,总数n等于90。
140、本说明书及所要求保护技术方案的范畴内,注射器指定标称容积为0.5ml、1mllong或3ml符合标准iso 11040-4(2015)。
141、本说明书及所要求保护技术方案的范畴内,术语“轴向(axial)”及相应术语“轴向上(axially)”用于指代医用注射装置的纵向方向,对应于其筒体的纵向方向,而术语“径向(radial)”及相应术语“径向上(radially)”用于指代垂直于上述纵向方向的任何方向。
142、本说明书及所要求保护技术方案的范畴内,术语“周向(circumferential)”及相应术语“周向上(circumferentially)”用于指代医用注射装置的筒体内表面在该筒体本身纵向的垂直平面内的伸展方向。
143、本发明上述一个或多个方面可以具备下述一个或多个优选特征,这些优选特征可以根据应用要求相互组合。
144、某一优选实施例中,步骤(a)包括提供涂料组合物,其聚二甲基硅氧烷含量等于或大于95wt.%、优选等于或大于98wt.%,室温下运动粘度为11500cst(115cm2/s)至13500cst(135cm2/s)。
145、更优选,步骤(a)包括提供涂料组合物,其聚二甲基硅氧烷含量约等于100wt.%,室温下运动粘度为11500cst(115cm2/s)至13500cst(135cm2/s)。
146、这样提供的制造方法就能有利地采取特别简单的可重现方式实施,尽量减少或完全消除将不同密度和/或粘度的硅材混合后难以保持涂料组合物流变性质恒定的相关问题。
147、有利地,该制造方法还能在不向硅材中添加任何添加剂的情况下实施。
148、某一优选实施例中,步骤(a)提供涂料组合物包括将所述涂料组合物储存在储罐中。
149、这样就能有利地始终具备可用于实施该方法所需量的涂料组合物。
150、优选地,储罐由适合容纳有机硅涂料组合物的材料制成,例如不锈钢。
151、优选地,步骤(b)将涂料组合物加热到120℃至150℃的温度。
152、这样就能有利地优化后续步骤(c)将经加热的涂料组合物施涂到筒体内表面上,从而促进内表面上形成非常均匀的涂层。
153、某一优选实施例中,步骤(b)加热涂料组合物包括加热上述储罐以使涂料组合物达到100℃至150℃、优选120℃至150℃的所述温度。
154、为此,涂料组合物储罐所设的至少一个加热元件配置为加热所储存的涂料组合物。
155、出于本发明目的,储罐的加热元件可以是配置为释放热能并选择性放置成与储罐中储存的涂料组合物呈热交换关系的任何元件。
156、仅举例而言,加热元件可以是置于罐内的加热线圈(以及例如电阻器或内部循环合适加热流体的管道)或者是置于罐外的护套,该护套中装有一个或多个电阻器或循环有合适的加热流体。
157、某一优选实施例中,所述方法还可以包括步骤(d)将储存在储罐中经加热的涂料组合物保持5psi(0.34巴)至150psi(10.34巴)、优选10psi(0.69巴)至30psi(2.07巴)、更优选10psi(0.69巴)至15psi(1.03巴)的压力。
158、这样就能有利地优化后续步骤(c)将经加热的涂料组合物施涂到筒体内表面上,从而促进内表面上形成非常均匀的涂层。
159、某一优选实施例中,所述方法还包括步骤(e)将经加热的涂料组合物馈送到分配头,该分配头设有至少一个分配喷嘴。
160、这样就能有利地将经加热的涂料组合物施涂到筒体内表面上,从而内表面上形成非常均匀的涂层。
161、优选地,经加热涂料组合物的分配头设置有相应的加热元件,该加热元件配置为加热由喷嘴分配的涂料组合物。
162、出于本发明目的,喷嘴的加热元件可以是配置为释放热能且选择性放置成与喷嘴本身分配的涂料组合物呈热交换关系的任何元件。
163、仅举例而言,加热元件可以是与分配喷嘴呈热交换关系的电阻器,例如整合到分配喷嘴相关联的壳体(例如圆柱形壳体)中。
164、优选地,步骤(e)将经加热的涂料组合物馈送到分配头是通过布置于分配头上游的循环泵来实施。
165、这样就能有利地根据生产需要向分配头适当馈送涂料组合物。
166、某一优选实施例中,循环泵的相应加热元件配置为加热泵的输送压头。
167、出于本发明目的,泵输送头的元件可以是配置为释放热能且选择性放置成与输送头本身分配的涂料组合物呈热交换关系的任何元件。
168、仅举例而言,加热元件可包括与泵输送头呈热交换关系的一个或多个电阻器,例如整合到输送头相关联的相应壳体(例如圆柱形壳体)中。
169、某一优选实施例中,步骤(c)将经加热的涂料组合物施涂到筒体内表面上是通过经由分配头分配涂料组合物来实施。
170、这样就能有利地将经加热的涂料组合物非常均匀地施涂到筒体内表面上。
171、某一优选实施例中,步骤(b)加热涂料组合物包括加热分配头和/或泵,优选地加热泵输送头,以使涂料组合物达到或维持所述100℃至150℃的温度。
172、这样就能有利地减少泵的功率吸收和磨损,从而有利于泵的操作和维护成本。
173、某一优选实施例中,分配头和泵可以如上所述受到加热。
174、某一优选实施例中,所述制造方法提供了将泵输送头加热到50℃至60℃的温度。
175、某一优选实施例中,涂料组合物的储罐、循环泵和分配头经由管道彼此流体连通。
176、优选地,管道与相应的加热元件(例如电阻器)或管道(其中循环合适的加热流体)外套呈热交换关系。
177、优选地,上述管道由不锈钢等耐温材料制成而隔热或者由隔热的金属或塑料制成。
178、本技术人经实验观察到,通过对涂料组合物的储罐、循环泵、分配头和相应的连接管道中一者或多者进行加热,可以有利地均衡涂料组合物的粘度之后才将涂料组合物分配到筒体内表面上,从而有利地缩短分配时间,使涂料组合物在筒体内表面上的分布更加均匀。
179、本优选实施例的上下文中,步骤(b)加热涂料组合物优选地包括加热上述管道,以使涂料组合物处于或维持上述100℃至150℃的温度。
180、本技术人经实验观察到,将涂料组合物加热到超过150℃的温度可能导致硅材性质改变,这可能导致不理想的微粒释放加剧和/或释放低温下通常保留的物质。
181、某一优选实施例中,步骤(c)将经加热的涂料组合物施涂到筒体内表面上是通过在5psi(0.34巴)至150psi(10.34巴)、优选6psi(0.41巴)至10psi(0.69巴)的压力下分配经加热的涂料组合物来实施。
182、这样就能有利地将经加热的涂料组合物非常均匀地施涂到筒体内表面上。
183、某一优选实施例中,步骤(c)将经加热的涂料组合物施涂到筒体内表面上包括:向分配头馈送压力为5psi(0.34巴)至150psi(10.34巴)、优选为6psi(0.41巴)至10psi(0.69巴)的配气(例如空气)。
184、这样就能有利地采取非常均匀的方式分配经加热的涂料组合物,以便在筒体内表面上施涂同等均匀的涂层。
185、某一优选实施例中,所述方法包括将涂料组合物储罐的压力维持高于分配头的分配喷嘴的压力。
186、这样就能有利地采取非常均匀的方式分配经加热的涂料组合物,以便在筒体内表面上施涂同等均匀的涂层。
187、某一优选实施例中,步骤(c)将经加热的涂料组合物施涂到筒体内表面上包括在分配经加热的涂料组合物的同时,在分配头与筒体之间传递相对运动。
188、某一优选实施例中,步骤(c)将经加热的涂料组合物施涂到筒体内表面上包括在分配头插入筒体的相对运动期间,将经加热的涂料组合物分配到筒体内表面上。
189、优选实施例中,相应医用注射装置的一个或多个筒体可以由相对于经加热涂料组合物的一个或多个相应分配头可移动的支撑框架来支撑。
190、这样就能将分配头的喷嘴插入/拔出所述一个或多个筒体中的相应筒体。
191、优选地,分配头固定,并且所述一个或多个筒体的支撑框架可移向分配头和移离分配头,以便实现分配头与筒体之间的相对运动。
192、替代的优选实施例中,分配头可移动,并且所述一个或多个筒体的支撑框架可以固定,或者同样分配头和支撑框架皆可移动。
193、优选地,步骤(c)将经加热的涂料组合物施涂到筒体内表面上包括使筒体朝向相应分配头移动的同时通过分配头的喷嘴分配涂料组合物。
194、这样就能有利地在筒体内表面上施涂非常均匀的涂层。
195、某一优选实施例中,将经加热的涂料组合物分配到筒体内表面上的时间为0.3秒至1秒、优选0.4秒至0.7秒。
196、这样就能有利地将分配头插入和拔出筒体的时间之和给出的所谓“总循环时间”或“喷涂时间”限制为大约不到3秒,这视为与工业生产线的正常循环时间兼容。
197、就此,本技术人经实验观察到,通过实施上述一个或多个步骤来加热储罐、加热分配头、加热分配头上游的循环泵或所述泵的部件(例如,优选为泵输送头)、并且加热确保储罐、泵和分配头之间流体连通的连接管道,能够有利地便于实现经加热涂料组合物的上述分配时间。
198、某一特别优选实施例中,通过实施加热储罐、泵、分配头和相关连接管道的步骤有利地便于实现经加热涂料组合物的上述分配时间。
199、如上所述,本技术人实际上经实验观察到,这种方式操作允许均衡涂料组合物的粘度之后再将涂料组合物分配到筒体内表面上,从而有利地缩短分配时间,使涂层组合物在筒体内表面上的分布更加均匀。
200、某一优选实施例中,步骤(c)将经加热的涂料组合物施涂到筒体内表面上包括在0.1μl/s至5μl/s、优选约等于0.5μl/s的流速下分配经加热的涂料组合物。
201、这样就能有利地在筒体内表面上施涂非常薄的涂层。
202、某一优选实施例中,步骤(c)将经加热的涂料组合物施涂到筒体内表面上包括按0.2μg/mm2至0.4μg/mm2单位面积用量将经加热的涂料组合物施涂到筒体内表面上。
203、同样,这种情况下能够有利地在筒体内表面上施涂非常薄的涂层。
204、某一优选实施例中,步骤(c)将经加热的涂料组合物施涂到筒体内表面上,使得筒体内表面上形成的涂层通过光学反射法测得的平均厚度为100nm至200nm。
205、有利地,如上所述,筒体内表面上形成涂层的这种平均厚度完全符合制药和化妆品工业的要求,尽管事实上涂层是由高运动粘度的硅材构成。
206、某一优选实施例中,本发明方法能够在筒体内表面上获得厚度非常均匀的涂层,通过光学反射法(或取决于分辨率的光学干涉法)测得其厚度标准差等于或小于70nm、优选等于或小于50nm。
207、这样就能有利地获得最佳表面规整特性的涂层,从而医用注射装置的目视检查器件、特别是自动化型目视检查器件不会受到误导。
208、某一优选实施例中,本发明方法能够实现针对每批10个筒体在筒体内表面上形成厚度非常均匀的涂层,如上定义涂层的批平均厚度标准差sd的值等于或小于60nm、优选等于或小于50nm。
209、这样就能有利地按照大规模工业生产中的要求,采取可高度重现性的方式在一批多个筒体上获得具备最佳表面规整特性的涂层。
210、某一优选实施例中,本发明医用注射装置制造方法还可以包括:在步骤(c)将经加热的涂料组合物施涂到筒体内表面上之后,步骤(f)对筒体内表面上形成的涂层进行聚二甲基硅氧烷的部分交联处理。
211、优选地,通过辐照进行部分交联处理。
212、优选地,通过等离子体辐照对涂层进行辐照处理,优选地在大气压下利用等离子炬通过氩气流进行辐照处理,优选地氩气纯度超过99%(例如99.999%)。
213、这样可能有利的是,必要时视具体应用而定,可以进一步改进涂层的低微粒释放特性。
214、有利地,本技术人经实验发现,可以进行部分交联处理以使涂层润滑特性不会受到影响。
215、为此,优选实施例中,所述辐照处理的时间为0.2秒至1秒、优选为0.2至0.6秒、更优选为0.2至0.5秒(包含端值)、愈优选为约等于0.3秒。
216、本技术人经实验发现,如下详述,通过将辐照时间限制到这个取值区间内,获得的涂层能够有利地具备柱塞在注射装置筒体内的最佳滑动性能(静摩擦和动摩擦方面),同时具备最佳低微粒释放特性,两者皆长期保持恒定不变。
217、有利地,根据该优选实施例获得的部分交联涂层因其表面规整性而仍能显著减少医用注射装置的目视检查器件(特别是自动化型目视检查器件)可能误检虚假缺陷的相关问题。
218、不受任何解释性理论束缚,本技术人认为上述取值区间内的辐照时间有利于涂层固结,进一步减少微粒释放,却不会明显影响涂层表面规整性,也不会引起柱塞在筒体中的静摩擦力和动滑动摩擦力平均值发生明显变化。
219、特别是,本技术人经实验观察到,根据本发明优选实施例,通过辐照处理获得的微粒释放值远低于采用现有技术中非交联低粘度硅材的涂料,相当于经过辐照处理的涂层。
220、有利地,如下参照本技术人所做实验详述,无论是在室温或高于室温的条件下,还是在低温条件下,例如在-5℃至-40℃范围内的温度下,这种低颗粒释放特性也基本上长期保持不变。
221、这个特征在医用注射装置(例如注射器)经历长期储存和/或灌装有需低温保存的药物的情况下尤应受到重视。
222、另外,本技术人经实验发现,如下文详述,上述取值区间内的辐照时间不会对筒体内表面的涂层覆盖百分率产生不利影响,该百分率平均至少保持在90%左右。
223、某一优选实施例中,在步骤(c)将经加热的涂料组合物施涂到筒体内表面上之后,步骤(f)对筒体内表面上形成的涂层进行辐照处理的时间间隔为至少15分钟、优选为15至20分钟。
224、这样就能有利地允许分配到筒体内表面上的硅材液滴相互聚结,实现该表面至少90%的覆盖百分率。
225、就此,本技术人观察到,若等待时间不足15分钟,筒体内表面的覆盖百分率就会导致筒体中存储的注射液药物组合物与其玻璃内表面之间产生更多不必要的相互作用。
226、本技术人还指出,在生产时间大幅增加的情况下,等待时间超过20分钟也不会带来明显改善。
227、某一优选实施例中,本发明制造方法还可以包括:在步骤(c)将经加热的涂料组合物施涂到筒体内表面上之前,步骤(g)对筒体内表面进行预处理来提高涂层与内表面的粘附性。
228、某一特别优选实施例中,该预处理包括在筒体内表面上形成助粘剂层,优选包含[(双环庚烯)乙基]三甲氧基硅烷的助粘剂层。
229、优选地,上述预处理是通过如下步骤实施:
230、(g1)优选地通过超声波静态喷嘴将[(双环庚烯)乙基]三甲氧基硅烷异丙醇溶液、优选2.2wt.%的溶液雾化到筒体内表面上;
231、(g2)优选地在烘箱中加热经此处理的筒体,直到玻璃表面上存在的异丙醇蒸发,并提供用于在玻璃与助粘剂层之间形成化学键的热能。
232、某一替代优选实施例中,上述预处理可以通过如下步骤实施:
233、(g1')优选地在烘箱中将筒体加热到预定温度;
234、(g2')优选地通过超声波静态喷嘴将[(双环庚烯)乙基]三甲氧基硅烷异丙醇溶液、优选2.2wt.%的溶液雾化到经加热筒体的内表面上;
235、这种情况下,将筒体加热到的温度适合随后蒸发雾化溶液内异丙醇并提供足够的热能在玻璃与助粘剂层之间形成化学键。
236、优选地,步骤(g2)和(g1')加热筒体是在加热到优选120℃至145℃、更优选约等于140℃温度的烘箱中进行14至25分钟,优选地约等于20分钟。
237、优选地,喷射到筒体内表面上的[(双环庚烯)乙基]三甲氧基硅烷异丙醇溶液量为7μl至50μl,优选为7μl至22μl。
238、本发明优选实施例中,根据美国药典2021版44-nf39规定的美国usp 787标准,在-40℃温度下储存3个月后,筒体内表面涂层在测试溶液中释放微粒的平均粒径等于或大于10μm或者等于或大于25μm,通过光阻法测定的归一化微粒浓度平均值等于或小于上述标准规定限值的60%。
239、特别是,对于平均粒径等于或大于25μm的微粒,该平均值等于或小于上述标准规定限值的5%。
240、某一优选实施例中,根据美国药典2021版44-nf39规定的美国usp 787标准,在-40℃温度下储存3个月后,例如通过辐照处理,优选地通过等离子体辐照处理,筒体内表面上部分交联的涂层在测试溶液中释放微粒的平均粒径等于或大于10μm或者等于或大于25μm,通过光阻法测定的归一化微粒浓度平均值等于或小于上述标准规定限值的10%。
241、特别是,对于平均粒径等于或大于25μm的微粒,该平均值等于或小于上述标准规定限值的1%。
242、这两个优选实施例特别有利于包含温敏活性成分的可注射药物组合物的情况,例如包含重组蛋白或mrna疫苗的所谓生物技术药物。事实上,这些优选实施例实现了即使这类药物组合物按要求低温长期储存之后,也能够显著减少释放到医用注射装置的筒体中储存的药物组合物中的微粒量。
243、某一优选实施例中,根据美国药典2021版44-nf39规定的美国usp 789标准,在+5℃或+25℃或+40℃温度下储存3个月后,例如通过辐照处理,优选地通过等离子体辐照处理,筒体内表面上部分交联的涂层在测试溶液中释放微粒的平均粒径等于或大于10μm或者等于或大于25μm,通过光阻法测定的归一化微粒浓度平均值等于或低于上述标准规定限值。
244、上述优选实施例特别有利于眼科领域使用可注射药物组合物的情况,对于眼科领域,美国标准usp 789规定了非常严格的限制,即,即使这类药物组合物按要求的储存温度长期储存后,医用注射装置的筒体中所储存药物组合物中的最大可耐受微粒量。
245、关于上述内容,本说明书及所要求保护技术方案的范畴内,术语“归一化(normalised)”是指相对于所考虑标准的极限值或微粒计数最大值的归一化值。
246、某一优选实施例中,本发明方法还包括步骤(h)用注射液药物组合物灌装医用注射装置的筒体,所述步骤(h)是在筒体内表面上形成的涂层冷却到室温之后实施。
247、这样就能有利地获得预灌装一定剂量注射液药物组合物备用的医用装置,例如注射器。
248、本发明医用注射装置的优选实施例中,平面展开轴向长度为1.0mm的每个任意筒体部分中与该部分总面积相对应的覆盖率等于至少90%,该覆盖率定义为涂层覆盖面积与总测量面积之比。
249、这样就能有利地实现:
250、降低注射装置的筒体中储存的注射液药物组合物与筒体的玻璃内表面之间发生不理想接触的风险;
251、柱塞在注射装置筒体内的最佳滑动性能(静摩擦和动摩擦方面);
252、涂层的最佳表面规整特性,诸如显著减少医用注射装置的目视检查器件可能误检到虚假缺陷的相关问题。
253、本发明医用注射装置的优选实施例中,标称容积为1ml的空筒体用来在室温下测量柱塞在筒体中的静滑动摩擦力,至少30次测量平均值为2n至3n。
254、本发明医用注射装置的优选实施例中,标称容积为0.5ml的空筒体室温储存3个月后用来在室温下测量柱塞在筒体中的静滑动摩擦力,至少30次测量平均值为1n至3n。
255、本发明医用注射装置的优选实施例中,标称容积为1ml的空筒体-40℃储存7天后用来测量柱塞在筒体中的静滑动摩擦力,至少30次测量平均值为1.5n至3n。
256、本发明医用注射装置的优选实施例中,标称容积为1ml的空筒体用来在室温下测量柱塞在筒体中的动滑动摩擦力,至少30次测量平均值为1.5n至2.5n。
257、本发明医用注射装置的优选实施例中,标称容积为0.5ml的空筒体室温储存3个月后用来在室温下测量柱塞在筒体中的动滑动摩擦力,至少30次测量平均值为1n至2n。
258、本发明医用注射装置的优选实施例中,标称容积为1ml的空筒体-40℃储存7天后用来测量柱塞在筒体中的动滑动摩擦力,至少30次测量平均值为1.5n至2.5n。
259、有利地,上述柱塞在筒体内的静滑动摩擦力和动滑动摩擦力平均值完全符合制药和化妆品行业的要求,一般静滑动摩擦力为2n至6n,一般动滑动摩擦力为1n至3n。
260、优选地,通过如下测试法测量柱塞在筒体内的静滑动摩擦力和动滑动摩擦力平均值。
261、将柱塞安装到标称容积为1ml long或0.5ml的空筒体中,在其定位后24小时内,从零预压开始,对于标称容积1ml long的筒体,对柱塞施加的恒定滑动速度等于240mm/min,对于标称容积0.5ml的筒体,对柱塞施加的恒定滑动速度等于100mm/min,适于保持柱塞运动,并通过测力计首先测量静摩擦力,然后测量这个柱塞滑动期间的动摩擦力。
262、关于该测试方法的更多细节参阅下述实施例。
263、优选实施例中,如上关于制造方法所述,本发明医用注射装置包括筒体内表面上部分交联的涂层,如上所述,优选地通过辐照处理、更优选地通过等离子体辐照处理进行部分交联。
264、优选实施例中,如上就制造方法所述,本发明医用注射装置还可以包括施涂到筒体内表面的助粘剂层,优选为含[(双环庚烯)乙基]三甲氧基硅烷的助粘剂层。
265、优选实施例中,如上关于制造方法所述,本发明医用注射装置还包括安装在筒体中与筒体滑动接合的柱塞。
266、优选实施例中,如上关于制造方法所述,本发明医用注射装置还可以包括筒体内与其内表面相接触的注射液药物组合物。
267、优选实施例中,注射液药物组合物包含选自如下一种或多种适合注射形式的药物和/或活性成分:过敏原特异性免疫治疗组合物、寡核苷酸、特别是反义寡核苷酸和rnai反义寡核苷酸、生物反应调节剂、血液衍生物、酶、单克隆抗体、特别是缀合单克隆抗体和双特异性单克隆抗体、溶瘤病毒、肽、特别是重组肽和合成肽、多糖、蛋白、特别是重组蛋白和融合蛋白、疫苗、特别是结合疫苗、dna疫苗、灭活疫苗、mrna疫苗、重组载体疫苗、亚单位疫苗或上述组合,只要相容即可。
268、更优选地,所述适合注射形式的药物和/或活性成分选自:gen-3009、人胰类似物a21g+pramlintide、azd-5069+durvalumab、futuximab+modotuximab、[225ac]-fpi-1434、111in-cp04、14-f7、212pb-tcmc-trastuzumab、2141v-11、3bnc-117ls、3k3a-apc、8h-9、9mw-0211、a-166、a-319、aadvac-1、ab-002、ab-011、ab-022、ab-023、ab-154、ab-16b5、ab-729、abbv-011、abbv-0805、abbv-085、abbv-151、abbv-154、abbv-155、abbv-184、abbv-3373、abbv-368、abbv-927、abelacimab、abgn-107、abgn-168h、abl-001、abvac-40、aby-035、乙酰半胱氨酸+菠萝蛋白酶、aci-24、aci-35、acp-014、acp-015、act-101、actimab-a、actimab-m、ad-214、adavosertib+durvalumab、adct-602、adg-106、adg-116、adm-03820、advince、aex-6003、aflibercept生物类似物、afm-13、agen-1181、agen-2373、agle-177、agt-181、aic-649、aimab-7195、ak-101、ak-102、ak-104、ak-109、ak-111、ak-112、ak-119、ak-120、al-002、al-003、al-101、aldafermin、aldesleukin、alg-010133、alm-201、almb-0168、alnaat-02、alnagt-01、aln-hsd、alpn-101、alt-801、altp-1、altp-7、alx-0141、alx-148、alxn-1720、am-101、amatuximab、amc-303、amelimumab、amg-160、amg-199、amg-224、amg-256、amg-301、amg-330、amg-404、amg-420、amg-427、amg-509、amg-673、amg-701、amg-714、amg-757、amg-820、amrs-001、amv-564、amy-109、amz-002、analgecine、安克洛酶、andecaliximab、anetumab corixetan、anetumab ravtansine、ank-700、蛇毒抗体、炭疽抗体、2019冠状病毒病(covid-19)抗体、破伤风抗体、i型糖尿病抗体、实体瘤ox40激动剂抗体、(重组)抗嗜血因子、实体瘤和卵巢癌抑制epha2反义寡核苷酸rnai、anx-007、anx-009、ap-101、apitegromab、apl-501、apl-501、apn-01、aps-001+氟胞嘧啶、apsa-01、apt-102、apvac-1、apvac-2、apvo-436、apx-003、apx-005m、arct-810、argx-109、argx-117、aroang-3、aroapoc-3、arohif-2、aro-hsd、ascrinvacumab、aslan-004、asp-1235、asp-1650、asp-9801、ast-008、astegolimab、asunercept、at-1501、atacicept、ati-355、atl-101、ator-1015、ator-1017、atp-128、atrc-101、atrosab、atx-101、atxgd-59、atxms-1467、atyr-1923、au-011、(缀合)rituximabav-1、avb-500、avdoralimab、ave-1642、avi-3207、avid-100、avid-200、aviscumine、avizakimab、axatilimab、b-001、b-002、barusiban、bat-1306、bat-4306、bat-4406f、bat-5906、bat-8003、batroxobin、bay-1905254、bay-2315497、bay-2701439、bb-1701、bbt-015、bcd-096、bcd-131、bcd-217、bct-100、bemarituzumab、bepranemab、bermekimab、bertilimumab、betalutin、bevacizumab、bexmarilimab、bg-00010、bgba-445、bhq-880、bi-1206、bi-1361849、bi-456906、bi-655064、bi-655088、bi-754091、bi-754111、bi-836858、bi-836880、bi-905677、bi-905711、biib-059、biib-076、biib-101、bil-06v、bimagrumab、bio89-100、2019冠状病毒病(covid-19)、尿路感染、人工关节和不动杆菌感染生物反应调节剂、不明适应症生物反应调节剂、糖尿病黄斑水肿和湿性黄斑变性双特异性单克隆抗体i、hiv感染抑制hiv 1env双特异性单克隆抗体、检测肿瘤gd2和cd3双特异性单克隆抗体、检测胰管腺癌pd-l1和ctla4双特异性单克隆抗体、bivv-020、bleselumab、bm-32、bms-986012、bms-986148、bms-986156、bms-986178、bms-986179、bms-986207、bms-986218、bms-986226、bms-986253、bms-986258、bms-986258、bms-986263、bnc-101、bnt-111、bnt-112、bnt-113、bnt-114、bnt-121、bos-580、肉毒杆菌毒素、bp-1002、bpi-3016、brevarex mab-ar20.5、brivoligide、bromelain、bt-063、bt-1718、bt-200、bt-5528、bt-588、bt-8009、bti-322、btrc-4017a、budigalimab、bxq-350、(人)c1酯酶抑制剂、cabiralizumab、camidanlumab tesirine、canerpaturev、cavatak、cba-1205、cbp-201、cbp-501、cc-1、cc-90002、cc-90006、cc-93269、cc-99712、ccw-702、cdx-0159、cdx-301、cdx-527、celyvir、cemdisiran、cendakimab、cerc-002、cerc-007、cevostamab、cibisatamab、cigb-128、cigb-258、cigb-300、cigb-500、cigb-552、cigb-814、cigb-845、cinpanemab、cinrebafuspα、cis-43、civi-007、cjm-112、ckd-702、clustoidd.pteronyssinus、cm-310、cmk-389、cmp-001、cnto-6785、cnto-6785、cnv-nt、(重组)凝血因子viii、cobomarsen、codrituzumab、cofetuzumab pelidotin、cor-001、cosibelimab、cosibelimab、cotadutide、cpi-006、crx-100、csj-137、csl-311、csl-324、csl-346、csl-730、csl-889、ctb-006、cti-1601、ctp-27、ctx-471、cue-101、cusatuzumab、cv-301、cvbt-141、cx-2009、cx-2029、cyn-102、cypep-1、cyt-107、cyt-6091、(人)抗巨细胞病毒免疫球蛋白、达拉芬尼甲磺酸盐+帕尼单抗+曲美替尼二甲亚砜、dac-002、dalcinonacogα、dalotuzumab、danvatirsen+durvalumab、dapiglutide、daxdilimab、db-001、dcra-1at、decavil、depatuxizumab、desmopressin、df-1001、df-6002、diamyd、dilpacimab、diridavumab、dk-001、dkn-01、dm-101、dm-199、dmx-101、dnl-310、dnp-001、dnx-2440、domagrozumab、donanemab、donidalorsen钠盐、dp-303c、ds-1055a、ds-2741、ds-6157、ds-7300、ds-8273、durvalumab+monalizumab、durvalumab+oleclumab、durvalumab+oportuzumab monatox、durvalumab+selumetinib硫酸盐、dx-126262、dxp-593、dxp-604、dzif-10c、e-2814、e-3112、ebi-031、ebi-031、钇90标记埃多曲肽efavaleukinα、efpegsomatropin、eg-mirotin、elezanumab、elipovimab、emactuzumab、enadenotucirev、engedi-1000、ensituximab、eo-2401、epcoritamab、ery-974、etigilimab、etokimab、evitar、evx-02、exenatide、f-0002adc、f-520、f-598、f-652、faricimab、faz-053、fb-704a、fb-825、ff-21101、(人)浓缩纤维蛋白原、ficlatuzumab、flotetuzumab、flysyn、fmab-2、fns-007、fol-005、for-46、foralumab、foxy-5、fpp-003、fr-104、fresolimumab、fs-102、fs-118、fs-120、fs-1502、fsh-gex、过敏性哮喘融合蛋白、特发性血小板减少性紫癜拮抗血小板生成素受体融合蛋白、多形性胶质母细胞瘤和恶性胶质瘤拮抗表皮生长因子受体融合蛋白、肿瘤抑制cd25融合蛋白、肿瘤靶向间皮素融合蛋白、结肠炎、高血压和溃疡性结肠炎融合蛋白、fx-06、g-035201、g-207、g-3215、garetosmab、gatipotuzumab、gb-223、gbb-101、gc-1118a、gc-5131a、gem-103、gem-333、gem-3psca、gemibotulinumtoxin a、gen-0101、gen-1046、gensci-048、gentuximab、gevokizumab、glenzocimab、glofitamab、glucagon、gm-101、gma-102、gma-301、gnr-051、gnr-055、gnr-084、gnx-102、醋酸戈舍瑞林、gosuranemab、gp-asit、gr-007、gr-1401、gr-1405、gr-1501、grf-6019、grf-6021、gs-1423、gs-2872、gs-5423、gsk-1070806、gsk-2241658a、gsk-2330811、gsk-2831781、gsk-3174998、gsk-3511294、gsk-3537142、gt-02037-、gt-103、gtx-102、gw-003、gwn-323、gx-301、gxg-3、gxp-1、h-11b6、hab-21、halmpe-1、hb-0021、hbm-4003、hdit-101、her-902、hfb-30132a、hh-003、hl-06、hlx-06、hlx-07、hlx-20、hlx-22、hm-15211、hm-15912、hm-3、hpn-217、hpn-328、hpn-424、hpn-536、hpv-19、hrescap、hs-214、hs-628、hs-630、hs-636、hsv-1716、htd-4010、hti-1066、hu8f4、hub-1023、hvegf-26104、hx-009、(重组)透明质酸酶、ibi-101、ibi-110、ibi-112、ibi-188、ibi-302、ibi-318、ibi-322、ibi-939、ic-14、icon-1、ict-01、ieramilimab、ifabotuzumab、igem-f、igm-2323、igm-8444、ign-002、ima-950、ima-970a、imc-002、imcf-106c、imcy-0098、imgn-632、imgn-005、imm-01、imm-201、(人)免疫球蛋白、imsidolimab、ina-03、inbrx-101、inbrx-105、incagn-1876、incagn-1949、incagn-2385、inclacumab、indatuximab ravtansine、interferonα-2b、invac-1、io-102、io-103、io-112、io-202、ion-224、ion-251、ion-464、ion-537、ion-541、ion-859、ionis-agtlrx、ionisar-2.5rx、ionis-c9rx、ionis-fb-lrx、ionis-fxilrx、ionis-fxirx、ionis-gcgrrx、ionis-hbvlrx、ionis-hbvrx、ionis-maptrx、ionis-pkkrx、ionistmprss-6lrx、ipn-59011、ipp-204106、ir-cpi、irl-201104、irl-201805、isa-101、isb-1302、isb-1342、isb-830、iscalimab、isu-104、it-1208、itf-2984、ixtm-200、jbh-492、jk-07、jmt-101、jmt-103、jnj-0839、jnj-3657、jnj-3989、jnj-4500、jnj-67571244、jnj-75348780、jnj-9178、js-003、js-004、js-005、jsp-191、jtx-4014、jy-025、jzb-30、jzb-34、k-170、k-193、kan-101、kd-033、ker-050、kh-903、khk-4083、khk-6640、edv paediatric、kla-167、kla-167、klt-1101、kmrc-011、kn-026、kpl-404、ksi-301、ktn-0216、ktp-001、kur-113、ky-1005、ky-1044、labetuzumab govitecan、lacnotuzumab、lacutamab、ladiratuzumab vedotin、laronidase、lbl-007、ldos-47、letolizumab、醋酸亮丙瑞林、levi-04、lh-021、liatermine、lirilumab、lis-1、lka-651、llf-580、lmb-100、lna-043、load-703、lodapolimab、lorucafuspα、lp-002、lt-1001、lt-1001、lt-1001、lt-3001、lt-3001、lti-01、ltx-315、luaf-82422、luaf-87908、lulizumab pegol、lvgn-6051、ly-3016859、ly-3022855、ly-3041658、ly-3305677、ly-3372993、ly-3375880、ly-3434172、ly-3454738、ly-3561774、lzm-009、m-032、m-1095、m-254、m-6495、m-701、m-802、m-9241、mag-tn3、mau-868、mb-108、mbs-301、mcla-117、mcla-145、mcla-158、mdna-55、mdx-1097、medi-0457、medi-0618、medi-1191、medi-1341、medi-1814、medi-3506、medi-3617+tremelimumab、medi-5117、medi-5395、medi-570、medi-5752、medi-5884、medi-6012、medi-6570、medi-7352、medi-9090、men-1112、meplazumab、mezagitamab、mg-021、mg-1113a、mgc-018、mil-62、mil-77、mil-86、mitazalimab、mk-1654、mk-3655、mk-4166、mk-4280、mk-4621、mk-5890、molgramostim、肿瘤鉴定cd276缀合单克隆抗体、肿瘤鉴定cd45缀合单克隆抗体、非小细胞肺癌和转移性结直肠癌鉴定ceacam5缀合单克隆抗体、转移性结直肠癌鉴定mucin 1缀合单克隆抗体、前列腺癌靶向psma缀合单克隆抗体、登革热单克隆抗体、乳糜泻、肿瘤和热带痉挛性截瘫拮抗il-2rβ单克隆抗体、类风湿性关节炎拮抗白细胞介素6受体单克隆抗体、肿瘤拮抗pd1的单克隆抗体、实体瘤拮抗pd1的单克隆抗体、hiv-1抑制cd4的单克隆抗体、肿瘤抑制gd2的单克隆抗体、狂犬病抑制糖蛋白的单克隆抗体、自身免疫性疾病和肌肉骨骼疾病抑制il17的单克隆抗体、哮喘和慢性阻塞性肺病(copd)抑制il5的单克隆抗体、实体瘤抑制pd-l1的单克隆抗体、强直性脊柱炎、银屑病和类风湿性关节炎抑制tnf-α的单克隆抗体、杜普伊特伦挛缩症抑制tnf-α的单克隆抗体、糖尿病性黄斑水肿和湿性老年黄斑变性抑制vegf的单克隆抗体、肿瘤和眼科抑制vegf的单克隆抗体、转移性结直肠癌和非小细胞肺癌抑制vegfa的单克隆抗体、血癌和代谢紊乱靶向cd66b的单克隆抗体、hiv感染靶向gp41的单克隆抗体、morab-202、motrem、mp-0250、mp-0274、mp-0310、mp-0420、mrg-001、mrg-002、mrg-003、mrg-110、mrna-2416、mrna-2752、mrna-3927、msb-0254、msb-2311、msc-1、mt-1001、mt-1002、mt-2990、mt-3724、mt-3921、mtx-102、murlentamab、mvt-5873、mvxonco-1、mw-11、mw-33、na-704、namilumab、naratuximab emtansine、navicixizumab、nbe-002、nbf-006、nc-318、nc-410、nemvaleukinα、neopv-01、ng-348、ng-350a、ng-641、ngm-120、ngm-395、ngm-621、ni-006、ni-0801、nidanilimab、nimacimab、nis-793、niz-985、nja-730、njh-395、nktr-255、nktr-358、nmil-121、nn-9215、nn-9499、nn-9775、nn-9838、nn-9931、nnc-03850434、np-024、np-025、np-137、npc-21、npt-088、npt-189、nrp-2945、nstride aps、nvg-111、nxt-007、nzv-930、obi-888、obi-999、obt-076、oc-001、醋酸奥曲肽、醋酸奥曲肽cr、醋酸奥曲肽微球、odronextamab、odronextamab、oh-2、olamkicept、oleclumab、olinvacimab、olpasiran、olvimulogene nanivacirepvec、oms-906、onabotulinumtoxina、onc-392、oncase-peg、人乳头瘤病毒相关癌症、人乳头瘤病毒感染和2019冠状病毒病(covid-19)溶瘤病毒、转移性乳腺癌溶瘤病毒、肿瘤溶瘤病毒、实体瘤溶瘤病毒、复发性前列腺癌和转移性胰腺癌激活il-12的溶瘤病毒、肿瘤激活胸苷激酶的溶瘤病毒、实体瘤拮抗pd1的溶瘤病毒、实体瘤靶向cd155/necl5的溶瘤病毒、肿瘤靶向cd46和slc5a5的溶瘤病毒、人乳头状瘤病毒(hpv)相关实体瘤靶向e6和e7的溶瘤病毒、实体瘤靶向mage-a3的溶瘤病毒、oncos-102、oncr-177、ongericimab、ono-4685、onvatilimab、opk-88005、opt-302、orca-010、orienx-010、orilanolimab、oricumab、os-2966、ose-127、osocimab、otelixizumab、oto-413、otsa-101、oxs-1550、oxs-3550、p-28r、p-2g12、pacmilimab、panobacumab、parvoryx、pasireotide、pasotuxizumab、pc-mab、pd-01、pd-0360324、pd-1+antagonist ropeginterferonα-2b、pegbelfermin、peginterferonλ-1a、pelareorep、pelareorep、pemziviptadil、pen-221、戊聚硫钠、pepinemab、2019冠状病毒疾病(covid-19)多肽、实体瘤多肽、pertuzumab生物改良剂、pexastimogene devacirepvec、pf-04518600、pf-06480605、pf-06730512、pf-06755347、pf-06804103、pf-06817024、pf-06823859、pf-06835375、pf-06863135、pf-06940434、pf-07209326、pf-655、phn-013、phn-014、phn-015、pidilizumab、pin-2、plamotamab、(人)plasminogen 1、plexaris、pm-8001、pnt-001、pollinex quattro tree、polycab、poly-iclc、polypepi-1018、ponsegromab、pp-1420、pr-15、pr-200、prasinezumab、prexigebersen、prl3-zumab、糖尿病足溃疡和脑出血蛋白、骨关节炎和哮喘蛋白、传染病和肿瘤激活il12蛋白、prs-060、prtx-100、prv-300、prv-3279、prx-004、psb-205、pt-101、pt-320、ptr-01、ptx-35、ptx-9908、ptx-9908、ptz-329、ptz-522、pvx-108、qbeco-ssi、qbkpn-ssi、ql-1105、ql-1203、ql-1207、ql-1604、qpi-1007、qpi-1007、quavonlimab、quetmolimab、qx-002n、qx-005n、radspherin、ranibizumab、ranpirnase、ravagalimab、新代ravulizumab、rc-28、rc-402、rc-88、rd-001、rec-0438、甲氨蝶呤毒性重组羧肽酶g2、有机磷神经毒剂中毒重组酶、心血管、中枢神经系统、肌肉骨骼和代谢疾病激动ghrh重组肽、传染性疾病重组血浆凝胶酶原替代物、肠炎病、多发性硬化和银屑病重组蛋白、肿瘤重组蛋白、肿瘤激动ifnar1和ifnar2重组蛋白;化疗引发胃肠道粘膜炎和口腔粘膜炎激动kgfr重组蛋白、特发性血小板减少性紫癜激动血小板生成素受体重组蛋白、淋巴瘤和实体瘤抑制cd13重组蛋白、血友病a和血友病b抑制凝血因子xiv重组蛋白、急性高尿酸血症重组尿酸氧化酶替代物、三氟乙酸红酶肽、regn-19081909、regn-3048、regn-3051、regn-3500、regn-4018、regn-4461、regn-5093、regn-5458、regn-5459、regn-5678、regn-5713、regn-5714、regn-5715、regn-6569、regn-7075、regn-7257、remlarsen、renaparin、rep-2139、rep-2165、reteplase、rg-6139、rg-6147、rg-6173、rg-6290、rg-6292、rg-6346、rg-70240、rg-7826、rg-7835、rg-7861、rg-7880、rg-7992、rgls-4326、rigvir、rilimogene galvacirepvec、risuteganib、rituximab、rmc-035、ro-7121661、ro-7227166、ro-7284755、ro-7293583、ro-7297089、romilkimab、ropocamptide、rosibafuspα、rph-203、rpv-001、rqnestin-34.5v.2、rslv-132、rv-001、rxi-109、rz-358、sab-176、sab-185、sab-301、sait-301、sal-003、sal-015、sal-016、sanguinate、sar-439459、sar-440234、sar-440894、sar-441236、sar-441344、sar-442085、sar-442257、sb-11285、sbt-6050、scb-313、scib-1、sco-094、sct-200、scta-01、sd-101、sea-bcma、sea-cd40、selectate、selicrelumab、selk-2、semorinemab、serclutamab talirine、seribantumab、setrusumab、sevuparin钠盐、sfr-1882、sfr-9213、sfr-9216、sfr-9314、sg-001、sgnb-6a、sgncd-228a、sgn-tgt、shr-1209、shr-1222、shr-1501、shr-1603、shr-1701、shr-1702、shr-1802、shra-1201、shra-1811、sib-001、sib-003、simlukafuspα、siplizumab、sirukumab、skb-264、sl-172154、sl-279252、sl-701、soc-101、sojb、somatropin sr、sotatercept、sprifermin、srf-617、srp-5051、sss-06、sss-07、st-266、sta-551、sti-1499、sti-6129、stk-001、stp-705、str-324、stro-001、stro-002、stt-5058、subq-8、sulituzumab、suvratoxumab、svv-001、sy-005、syd-1875、sym-015、sym-021、sym-022、sym-023、syn-004、syn-125、乙型肝炎和ii型糖尿病抑制slc10a1合成肽、慢性肾病调节ghsr合成肽、甲状腺髓样癌靶向cckbr合成肽、神经内分泌胃肠胰肿瘤靶向体生长抑素受体合成肽、t-3011、t-3011、ta-46、tab-014、tab-014、tafoxiparin钠盐、tak-101、tak-169、tak-573、tak-611、tak-671、talquetamab、tasadenoturev、tbio-6517、tbx.oncv nsc、tebotelimab、teclistamab、telisotuzumab vedotin、telomelysin、temelimab、tenecteplase、tesidolumab、teverelix、tf-2、tg-1801、tg-4050、tg-6002、tg-6002、t-guard、thor-707、thr-149、thr-317、thrombosomes、thymalfasin、tilavonemab、tilt-123、tilvestamab、tinurilimab、tipapkinogene sovacivec、tiprelestat、tm-123、tmb-365、tnb-383b、tnm-002、tnx-1300、tomaralimab、tomuzotuximab、tonabacase、tralesinidaseα、trebananib、trevogrumab、trk-950、trph-222、trs-005、tst-001、tthx-1114、tti-621、tti-622、ttx-030、tvt-058、tx-250、ty-101、tyzivumab、u-31402、ub-221、ub-311、ub-421、ub-621、ubp-1213、uc-961、ucb-6114、ucht-1、ucpvax、ulocuplumab、unex-42、uni-epo-fc、urelumab、uv-1、v-938、急性淋巴细胞白血病疫苗、b细胞非霍奇金淋巴瘤疫苗、慢性淋巴细胞白血病疫苗、胶质瘤疫苗、荷尔蒙敏感性前列腺癌疫苗、黑色素瘤疫苗、非肌浸润性膀胱癌疫苗、卵巢癌疫苗、肿瘤靶向brachyury和her2疫苗、肿瘤靶向brachyury疫苗、b细胞非霍奇金淋巴瘤靶向ccl20疫苗、结直肠癌靶向cea疫苗、代谢紊乱、免疫、传染病和肌肉骨骼疾病靶向ifn-α疫苗、val-201、vantictumab、vanucizumab、varlilumab、vas-01、vax-014、vb-10neo、vcn-01、vibecotamab、vibostolimab、vir-2218、vir-2482、vir-3434、vis-410、vis-649、vixarelimab、vls-101、vofatamab、volagidemab、vopratelimab、voyager-v1、vrc-01、vrc-01ls、vrc-07523ls、vtp-800、vunakizumab、vupanorsen钠盐、vx-001、vx-006、w-0101、wbp-3425、xav-19、xentuzumab、xmab-20717、xmab-22841、xmab-23104、xmab-24306、xmt-1536、xoglo、xoma-213、xw-003、y-14、y-242、yh-003、yh-14618、ys-110、yyb-101、zagotenemab、zalifrelimab、zampilimab、zanidatamab、zanidatamab、zansecimab、zenocutuzumab、zg-001、zk-001、zl-1201、zofin或上述组合,只要相容即可。
269、某一优选实施例中,组装本发明医用注射装置的零件套组包括上述医用装置的任何适用优选特征。
本文地址:https://www.jishuxx.com/zhuanli/20240619/7166.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表