粒度分布保持稳定性得到改善的白蛋白结合型紫杉类纳米粒子的制备方法与流程
- 国知局
- 2024-07-12 10:21:25
本技术要求于2021年11月3日向韩国专利厅提交且申请号为第10-2021-0150107号的韩国专利申请的优先权,其全部内容通过引用结合在本技术中。本发明涉及粒度分布保持稳定性得到改善的白蛋白结合型紫杉类纳米粒子的制备方法。
背景技术:
1、难溶性药物是指由于化合物的结构上具有疏水性部位而不易溶于水的药物,因其难溶性而在大多数时候使其实用性受限。例如,在开发为新药的药物中,约有41%以上因难溶性而在中途放弃,美国药典(us pharmacopeia)中记载的药物中约1/3以上分类为难溶性药物。为了使用这些难溶性药物,应加入用于解决难溶性的附加物质,但却有许多因附加物质的毒性而受限的案例。例如,为了使难溶性物质变为水可溶性,通常使用利用乳化剂的乳化、利用脂质体的捕获等方法,但这些方法的使用因非人源性物质的混入以及物理不稳定性等原因而受到限制。
2、紫杉醇(paclitaxel,ptx)为包含从短叶红豆杉(taxus brevifolia)的树皮中提取的二萜类化合物(diterpenoid)衍生物的药物,基本上具有由紫杉烷环(taxane ring)与酯侧链(ester side chain)构成的生物碱(alkaloid)结构。已知紫杉醇具有促进微管蛋白(tubulin)组合体向稳定的微管(microtubules)转化的抗细胞分裂活性,已知对肺癌、乳腺癌等多种癌症具有功效。如上所述,紫杉醇作为抗癌药物表现出卓越的潜能,但由于对水的溶解度低,因此,在癌症的治疗领域中的广泛使用受到限制。为了解决紫杉醇的难溶性,以往将紫杉醇溶于乙醇中来使用,但近来为了提高输送效率,将紫杉醇与白蛋白结合来用作注射剂。并且,已知有使用作为聚氧乙烯蓖麻籽油(polyoxyethylated castor oil)与无水乙醇(absolute ethanol)的混合物的称为cremophor el的溶剂改善紫杉醇的水溶解度来在全身给药中使用的方法。以这样的形态商用化的制剂为taxoltm。但据报告,若在临床上过量给药这样的溶剂,则表现出心脏毒性、神经毒性、神经障碍及过敏症等副作用。
3、为了克服taxoltm的因上述溶剂表现出副作用等缺点,abraxanetm将与人血清白蛋白结合的紫杉醇配制为纳米粒子形态,通过人类及动物实验表现出提升的肿瘤反应,从而作为成功的抗癌治疗剂使用至今。然而,在与abraxanetm相关的现有专利文献1(pct/us1998/013272)中公开的制备方法中,说明应在使紫杉醇与白蛋白的混合液高压均质化后即刻迅速进行减压干燥,若在高压均质化后不即刻迅速连续地进行减压干燥,则包含紫杉醇及白蛋白的纳米粒子的粒度将随着时间的经过大幅增加。这样,若高压均质化后纳米粒子的粒度分布不保持均匀而迅速增加,则必须选择复杂的连续工序,这非常不利于规模化,而且还要迅速进行减压干燥,还要根据需要进行去除凝集为无法用作药物的纳米粒子的追加工序。不仅如此,在专利文献1中公开的工序中,以实施例5(example 5)为基准,作为起始物质的紫杉醇溶液与白蛋白溶液的浓度分别稀释为7.5%(w/v)、3%(w/v),若以这种方式来构成规模化设备,则混合槽等设备的容积要大,进而,为了减少最终分散液的体积,还需要进行浓缩工序,从而发生大幅减少纳米粒子生产量的问题。
4、在本说明书全文中,参考许多论文及专利文献的内容并标注其引用。引用的论文及专利文献的公开内容的全部作为参照插入本说明书中,以便于更为明确地说明本发明所属技术领域的水平及本发明的内容。
技术实现思路
1、技术问题
2、本发明人为了导出能够克服上述专利文献1的问题的白蛋白结合型紫杉类纳米粒子的制备方法而反复研究,结果,确认到本发明一实施方式的包含紫杉类及白蛋白的纳米粒子的制备方法能够解决专利文献1中公开的工序所受的限制,即,高压均质化之后,减压干燥之前和/或减压干燥工序中纳米粒子的大小迅速增大的问题。并且,从经济性及效率性层面证明本发明的制备方法能够提供适合规模化的环境,从而完成本发明。
3、因此,本发明的目的在于,提供粒度分布保持稳定性得到改善的包含紫杉类及白蛋白的纳米粒子的制备方法。
4、本发明的再一目的在于,提供通过上述制备方法制备的包含紫杉类及白蛋白的纳米粒子。
5、本发明的另一目的在于,提供保持包含紫杉类及白蛋白的纳米粒子的粒度分布的稳定化方法。
6、本发明的其他目的及优点将通过下述发明的详细说明、发明要求保护范围以及附图得以进一步明确。
7、技术方案
8、本说明书中使用的数值限定,例如,包括范围在内的在温度、时间、压力、量、浓度等中使用的术语“约(about)”是指(+)或(-)10%、5%、4%、3%、2%、1%或它们之间的范围或特定数值。
9、本说明书中使用的术语“纳米粒子”是指具有小于1μm的粒度大小(尺寸(dimension))的粒子。在本发明的纳米粒子用于静脉内注射的情况下,优选地,上述纳米粒子具有500nm以下的大小。具体地,上述纳米粒子以具有50-500nm、50-400nm、50-300nm、50-200nm、50-190nm、50-180nm、50-170nm、50-160nm、50-150nm、80-500nm、80-400nm、80-300nm、80-200nm、80-190nm、80-180nm、80-170nm、80-160nm、80-150nm、100-500nm、100-400nm、100-300nm、100-200nm、100-190nm、100-180nm、100-170nm、100-160nm、100-150nm、110-500nm、110-400nm、110-300nm、110-200nm、110-190nm、110-180nm、110-170nm、110-160nm或110-150nm的大小为优选。
10、在粒子的集团中,形成集团的粒子的大小可以通过平均数和/或百分数来表示。例如,d10表示粒子的10%为比该值小的大小,d50表示粒子的50%为比该值小的大小,d90表示粒子的90%为比该值小的大小。粒子的平均大小能够以d50来表示。
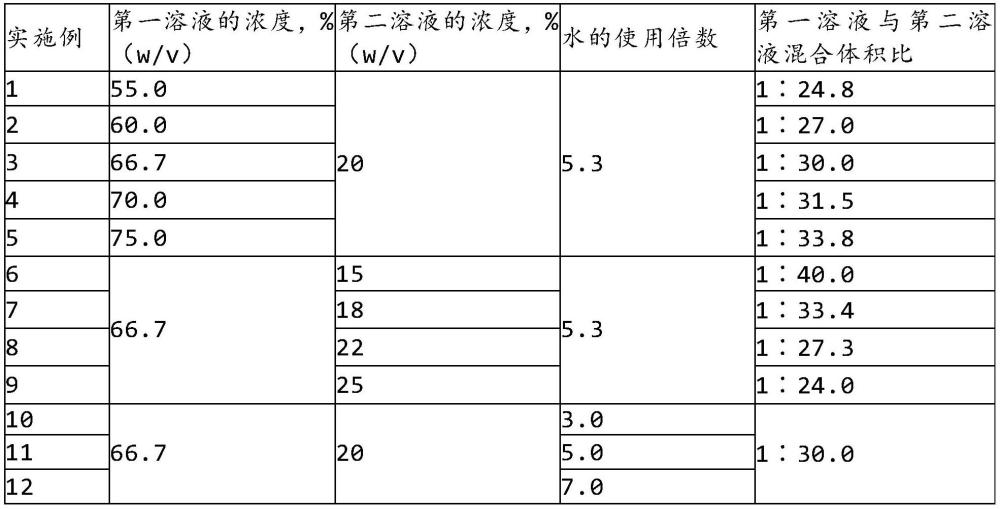
11、在本发明的一实例中,上述第一溶液的紫杉类的浓度可以为55~75%(w/v)、60~75%(w/v)、65~75%(w/v)、70~75%(w/v)、55~70%(w/v)、55~65%(w/v)、55~60%(w/v)、60~70%(w/v)、64~68%(w/v)或65~67%(w/v)。
12、在本发明的一实例中,上述第一溶液的溶剂选自由乙醇、甲醇、异丙醇、丁醇、二甲基亚砜(dmso)、n,n二甲基甲酰胺(dmf)、四氢呋喃(thf)、乙腈、二氯甲烷、乙酸乙酯、己烷、乙醚、苯、三氯甲烷、丙酮及它们的组合组成的组中,但不限定于此。
13、在本发明的具体实例中,上述第一溶液的溶剂为乙醇及三氯甲烷的混合溶剂。上述乙醇∶三氯甲烷的体积比可以为1∶5至1∶20、1∶6至1∶20、1∶7至1∶20、1∶8至1∶20、1∶9至1∶20、1∶10至1∶20、1∶12至1∶20、1∶14至1∶20、1∶15至1∶20、1∶5至1∶18、1∶6至1∶18、1∶7至1∶18、1∶8至1∶18、1∶9至1∶18、1∶10至1∶18、1∶12至1∶18、1∶14至1∶18、1∶15至1∶18、1∶5至1∶16、1∶6至1∶16、1∶7至1∶16、1∶8至1∶16、1∶9至1∶16、1∶10至1∶16、1∶12至1∶16、1∶14至1∶16、1∶15至1∶16、1∶5至1∶15、1∶6至1∶15、1∶7至1∶15、1∶8至1∶15、1∶9至1∶15、1∶10至1∶15、1∶12至1∶15或1∶14至1∶15,但不限定于此。
14、在本发明的一实例中,若上述第一溶液的紫杉类的浓度小于本发明中定义的55~75%(w/v)范围的下限值,则即使进行水稀释步骤,也会发生粒子大小在减压干燥之前迅速上升为无法用作注射剂型的有效成分的200nm以上的问题。
15、并且,若第一溶液的紫杉类的浓度大于本发明中定义的55~75%(w/v)范围的上限值,则在纳米粒子的制备过程中因紫杉醇的析出而使高压匀质机无法正常运行,纳米粒子的粒度也增加,因此,超过75%(w/v)的浓度会发生无法生产均匀粒度的纳米粒子的问题。
16、在本发明的一实例中,上述紫杉类可以为紫杉醇、多烯紫杉醇或它们的组合,但不限定于此。
17、在本发明的一实例中,上述第二溶液的白蛋白的浓度可以为15~25%(w/v)、18~25%(w/v)、22~25%(w/v)、15~22%(w/v)、15~18%(w/v)、18~22%(w/v)、19~21%(w/v)。
18、在本发明的一实例中,上述第二溶液的溶剂为选自由水、蒸馏水、灭菌水、磷酸盐缓冲溶液(pbs)、甲醇、纯水、乙醇、1-丙醇、2-丙醇、1-戊醇、乙二醇-丁醚、乙二醇、丙酮、2-丁酮、4-甲基-2-丙酮、三氯甲烷及它们的组合组成的组中的水性溶剂,但不限定于此。
19、若上述第二溶液的白蛋白浓度小于本发明中定义的15~25%(w/v)范围的下限值,则为了使组中制备的纳米粒子中紫杉醇∶白蛋白的重量比为与abraxanetm相同的1∶9,只能过度增加分散液的体积,结果超过通常填充体积范围,需要追加浓缩工序,从而发生现实中难以在规模化生产中使用的问题。并且,若第二溶液的白蛋白浓度大于本发明中定义的15~25%(w/v)范围的上限值,则即使进行水稀释步骤,也会发生粒子大小在减压干燥之前迅速上升为无法用作注射剂型的有效成分的200nm以上的问题。
20、在本发明的一实例中,上述白蛋白可以为人血清白蛋白(human serum albumin,hsa)、牛血清白蛋白(bovine serum albumin,bsa)、卵白蛋白(ovalbumin,ova)或它们的组合。
21、在本发明的一实例中,上述步骤(c)中第一溶液与第二溶液的混合体积比为1∶20至1∶45,但不限定于此。例如,第一溶液与第二溶液的混合体积比可以为1∶20至1∶43、1∶20至1∶41、1∶20至1∶39、1∶20至1∶37、1∶20至1∶35、1∶20至1∶33、1∶20至1∶31、1∶20至1∶29、1∶20至1∶27、1∶20至1∶25、1∶20至1∶23、1∶20至1∶21、1∶22至1∶45、1∶24至1∶45、1∶26至1∶45、1∶28至1∶45、1∶30至1∶45、1∶32至1∶45、1∶34至1∶45、1∶36至1∶45、1∶38至1∶45、1∶40至1∶45、1∶42至1∶45、1∶44至1∶45、1∶22至1∶40、1∶25至1∶40、1∶25至1∶35、1∶25至1∶30、1∶30至1∶40或1∶30至1∶35。
22、为了使最终制备的纳米粒子中紫杉醇∶白蛋白的重量比为与abraxanetm相同的约1∶9,本发明所属技术领域的普通技术人员并且/或者可以考虑反应性选择适当的比例来进行。上述紫杉醇∶白蛋白的重量比不必限定于1∶9,重量比可以为1∶7至11的范围、1∶8至10或1∶8.5至9.5的范围。
23、在本发明的一实例中,上述步骤(c)中悬混液的制备通过高压均质化(homogenization)来实现。
24、在本发明的一实例中,上述高压均质化在10℃至40℃、15℃至40℃、20℃至40℃、30℃至40℃或35℃至40℃的温度条件下进行,但不限定于此。
25、在本发明的一实例中,上述高压均质化在10000psi至30000psi、12000psi至30000psi、15000psi至30000psi、16000psi至30000psi、17000psi至30000psi、18000psi至30000psi、10000psi至25000psi、12000psi至25000psi、15000psi至25000psi、16000psi至25000psi、17000psi至25000psi、18000psi至25000psi、10000psi至20000psi、12000psi至20000psi、15000psi至20000psi、16000psi至20000psi、17000psi至20000psi或18000psi至20000ps的条件下进行,但不限定于此。
26、上述高压均质化进行一次以上,更具体地,进行1次至5次、1次至4次或1次至3次,但不限定于此。
27、在本发明的一实例中,上述步骤(d)的稀释以悬混液的体积为基准,可以稀释3倍至12倍、5倍至12倍、7倍至12倍、10倍至12倍、3倍至10倍、3倍至7倍、3倍至5倍、5倍至10倍或5倍至7倍,但不限定于此。
28、若稀释中使用的水性溶剂的使用倍数小于本发明中定义的3倍至12倍范围的下限值,则即使进行水稀释步骤,也会发生粒子大小在减压干燥之前迅速上升为无法用作注射剂型的有效成分的200nm以上的问题。上述粒子大小的增加可以由纳米粒子间的凝集(agglomeration)引起。在静脉内注射用纳米粒子的情况下,若纳米粒子凝集,则会堵塞血管,因此,纳米粒子的凝集及纳米粒子的稳定性会给包含纳米粒子的药物组合物的功效及安全性带来影响。
29、并且,若水性溶剂的使用倍数大于本发明中定义的3倍至12倍范围的上限值,不仅增加紫杉醇的游离部分(free fraction),即,增加未封入率(5.3倍水稀释时未封入率为0.72%→13倍水稀释时未封入率为6.24%),还在纳米粒子粒度稳定化中使用所需以上的水,从而在规模化工序层面发生效率及经济不佳的问题。
30、在本发明的一实例中,上述步骤(d)的稀释液中的纳米粒子的平均粒度为100nm至200nm或110nm至190nm,但不限定于此。
31、在本发明的一实例中,上述制备方法还可以包括步骤(e),通过干燥所稀释的上述溶液来获得纳米粒子。
32、在本发明的一实例中,上述干燥可以为减压干燥、冷冻干燥或加热干燥,但不限定于此。
33、在本发明的一实例的上述干燥为减压干燥的情况下,可以选择使用旋转蒸发器(rotary evaporator)等通常的减压干燥方法来进行,不限定于特定减压干燥条件。
34、在本发明的具体实例中,上述减压干燥可以在10℃至70℃、20℃至70℃、30℃至70℃、40℃至70℃、10℃至60℃、10℃至50℃、10℃至40℃、20℃至60℃、30℃至50℃、35℃至45℃、38℃至42℃或39℃至41℃范围的温度条件下进行,但不限定于此。
35、在本发明的具体实例中,上述减压干燥可以在10hpa至110hpa、20hpa至110hpa、30hpa至110hpa、40hpa至110hpa、50hpa至110hpa、10hpa至100hpa、10hpa至90hpa、10hpa至80hpa、10hpa至70hpa、20hpa至100hpa、30hpa至90hpa、40hpa至80hpa、50hpa至70hpa或55hpa至65hpa范围的压力条件下进行,但不限定于此。
36、从进行干燥之前到结束干燥为止,存在于所稀释的上述溶液中的纳米粒子的平均粒度可以保持100nm至200nm,优选地,可以保持110nm至190nm。
37、本发明的一实施方式提供的包含紫杉类及白蛋白的纳米粒子的制备方法不进行用水稀释的步骤,与高压均质化后迅速进行减压干燥的以往工序相比,减压干燥之前水稀释液内纳米粒子的平均大小即使时间流逝也保持均匀,表现出结构稳定性和粒度分布非常优秀的显著效果,本发明的这些效果将通过后述的实施例、比较例、实验例得到验证。
38、根据本发明的另一实施方式,提供通过上述本发明一实施方式的制备方法制备的包含紫杉类及白蛋白的纳米粒子。
39、在本发明的一实例中,通过本发明一实施方式的制备方法制备的上述包含紫杉类及白蛋白的纳米粒子在使干燥的纳米粒子在水性溶剂(包括生物体内(in vivo)及生物体外(in vitro))中再组成(reconstitution)时,具有与干燥之前的纳米粒子(例如,上述步骤(d)的稀释液内的纳米粒子)的特性实质上相同的治疗活性及粒子特性。
40、将上述干燥的纳米粒子在水性溶剂中再组成时,平均粒子的大小、粒子的大小分布与干燥前的纳米粒子实质上相同。上述实质上相同的含义是指与冷冻干燥前的有关纳米粒子的参数相比,冷冻干燥结束后的纳米粒子相关的参数包括在±10%的范围,更具体地,包括在±7%范围、±5%范围、±4%范围或±3.5%范围。
41、在本发明的一实例中,上述干燥的纳米粒子在室温下稳定至少3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月、12个月或以上的时间,即使在室温下保管上述时间后,在水性溶剂中再组成时,仍表现出干燥前纳米粒子的治疗活性及粒子特性。
42、在本发明的具体实例中,上述干燥为冷冻干燥。
43、在本发明的一实例中,上述冷冻干燥是指冷冻作为干燥对象的纳米粒子,然后在真空环境中通过升华来去除冷冻的溶剂的过程。在上述冷冻干燥中,为了强化冷冻干燥的产品的保管稳定性,选择性地包含赋形剂或冷冻保护剂。
44、上述赋形剂或冷冻保护剂包括:聚合物,例如葡聚糖及聚乙二醇;糖类,例如,蔗糖、葡萄糖、海藻糖及乳糖;表面活性剂,例如,聚山梨酯;以及氨基酸,例如,甘氨酸、精氨酸及丝氨酸,但不限定于此。
45、在本发明的一实例中,除本发明的紫杉类以外,上述纳米粒子还可以包含一种以上治疗剂。
46、在本发明的一实例中,为了向患者给药,上述纳米粒子可以进行药剂学配制。可以使用本发明所属技术领域中的多种剂型及药物传递系统。例如,可以参照gennaro,a.r.,ed.(1995)remington's pharmaceutical sciences,18th ed.,mack publishing co.。
47、在本发明的一实例中,本发明的纳米粒子可以作为药物组合物通过如下途径中的一种来给药:口服;以及胃肠外,例如,经皮、鼻腔内(intranasal)、肌肉内、静脉内、皮下、皮内、肿瘤内等。
48、在本发明的一实例中,本发明的纳米粒子可以包含如下固体、液体、半固体或气体赋形剂。
49、上述固体药剂学赋形剂包括淀粉、纤维素、滑石粉(talc)、葡萄糖、乳糖、蔗糖、明胶、麦芽、大米、面粉(flour)、硅胶、硬脂酸镁、硬质酸钠、单硬脂酸甘油酯、氯化钠、干燥脱脂牛奶(dried skim milk)等。
50、上述液体及半固体赋形剂可以在甘油、丙二醇、水、乙醇以及包括源自石油、动物、植物及合成的油在内的多种油,例如,花生油(peanut oil)、大豆油、矿物油(mineraloil)、芝麻油等中选择。优选的液体载体,尤其是注射溶液用载体包括水、生理盐水、葡萄糖水溶液(aqueous dextrose)及乙二醇。其他适当的药剂学赋形剂及其剂型记载在由e.w.martin编辑的remington's pharmaceutical sciences(mack publishing company,18th ed.,1990)中。
51、在本发明的具体实例中,上述纳米粒子为静脉内注射来配制。在本发明的其他具体实例中,上述纳米粒子为向肿瘤直接注射或灌流来配制。
52、根据本发明的一实施方式,本发明提供包括如下步骤的纳米粒子的粒度分布保持稳定化方法:
53、步骤(a),准备紫杉类以55~75%(w/v)的浓度溶解的第一溶液;
54、步骤(b),准备白蛋白以15~25%(w/v)的浓度溶解的第二溶液;
55、步骤(c),混合第一溶液与第二溶液来制备悬混液;以及
56、步骤(d),以上述悬混液的体积为基准,使用3倍至12倍的水性溶剂稀释。
57、上述本发明一实施方式的纳米粒子的粒度分布保持稳定化方法包括与上述本发明一实施方式的纳米粒子的制备方法相同的步骤(a)至步骤(d),为避免两发明之间相同内容的重复记载,本说明书中将省略其记载。
58、发明的效果
59、与通过现有工序制备的纳米粒子相比,本发明的包含紫杉类及白蛋白的纳米粒子的制备方法即使时间流逝,也均匀保持纳米粒子的平均大小,结构稳定性和粒度分布非常优秀,可以有效用作改善的制备包含紫杉类及白蛋白的纳米粒子的方法。
本文地址:https://www.jishuxx.com/zhuanli/20240614/86412.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表