一种基于振荡流的微流控大分子药物输送装置
- 国知局
- 2024-06-20 11:13:19
本发明属于微流控,涉及一种基于振荡流,利用挤压力和剪切力使周围介质的大分子药物可以直接扩散到细胞质中的微流控装置,具体为一种基于振荡流的微流控大分子药物输送装置。
背景技术:
1、大分子药物(即蛋白质和肽、抗体、激素、核酸、疫苗等)由于其生物多样性、高效能、耐受性好、免疫原性低、位点特异性活性大等优点,被广泛用作各种疾病的诊断、预防和治疗。将生物大分子输送到活细胞中,可以实现对细胞功能的调节和疾病的治疗,例如:通过细胞内递送核酸酶进行基因编辑、转运抗体进行治疗、或输送mrna调节基因表达。尽管利用生物大分子进行疾病治疗具有许多优点,但由于其固有的物理化学性质,如大分子尺寸、结构复杂性、亲水性、化学不稳定等,大分子药物的递送仍然面临挑战。因此,亟需建立一种输送效率高、低成本、且集成化的大分子药物输送装置。
2、目前,基于微流控的大分子药物输送方法主要依赖于膜穿孔,膜穿孔主要分为以下几类,第一种为电穿孔方法,事实上,电穿孔已经证明了它在许多dna和rna传递应用程序中的有效性,用于以前难以转染的原代细胞,例如:基于单细胞阵列的纳米电穿孔装置及其应用(专利号:cn202011093674.2)。然而,这种方法可能会导致细胞死亡,并已被证明会造成损害。第二种为微注射方法,它可能是将物质输送到细胞质的最直接的方法,无论细胞类型或传递材料,例如:基于微流控芯片的超微注射法及其在高通量筛选中的应用(专利号:cn202011630458.7)。尽管对某些应用有效,如生产转基因生物,但该方法的低通量在许多治疗和研究应用中是一个劣势。第三种为通道收缩方法,通道收缩进行细胞挤压的递送方法由于其结构简单、操作便捷等优势,在体外细胞递送中具有很大的发展潜力。这种方法将细胞通过一系列小于自身尺寸的狭窄收缩通道,从而产生瞬时的膜破坏或孔洞的形成,实现大分子的扩散性递送。然而,现有通道收缩方法中狭窄通道尺寸远小于细胞(收缩率<50%)会导致通道极易堵塞,且通过狭窄通道时高流速造成的高剪切力,会降低细胞活性,影响后续评估。
技术实现思路
1、为解决上述问题,本发明提出了结合振荡流与弱狭窄通道(收缩率75-90%)的大分子药物跨细胞膜输送策略,具体为一种高度集成、便捷高效输送生物大分子的微流控装置。弱狭窄通道可保证细胞通过时不易堵塞且所受剪切力微弱,振荡流驱动则可保证细胞可在“无限长”通道内经历足够时长的弱剪切力刺激以改变细胞膜通透性,进而实现生物大分子的跨细胞膜递送,同时可通过多个主通道并行以提高通量。同时,将黄原胶应用于大分子药物跨细胞膜输送,具有独特的优势,一方面,相比于其他粘弹性流体,黄原胶具有独特的流变性:黄原胶在水溶液中表现出非牛顿流体的特性。另一方面,黄原胶具有良好的水溶性。这使得黄原胶可以在水溶液中形成均匀、透明的胶体,易于与其他成分混合。通过黄原胶产生的振荡流带动细胞在充满生物大分子的低强度的狭窄通道中间歇运动,快速的机械变形会导致瞬时膜破裂或孔洞的形成,使周围介质中的大分子扩散到细胞质中,实现大分子药物的高效输送。同时,将无阀微泵集成在芯片上,泵膜驱动信号由单片机产生,使系统高度集成化,便于推广。
2、本发明的技术方案:
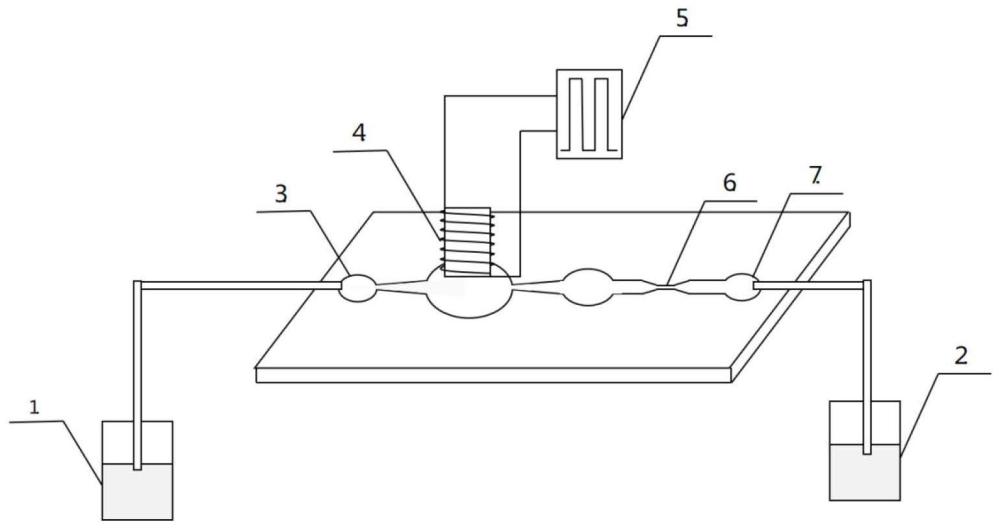
3、一种基于振荡流的微流控大分子药物输送装置,主要由微流控芯片、泵膜控制系统、储液池及导管组成。
4、所述的储液池包括样品池和收集池,样品池用于盛放生物大分子药物和细胞样品,收集池用于盛放大分子药物已输送至细胞内的样品。
5、所述的微流控芯片包括一个微流控芯片入口和一个微流控芯片出口,还包括、无阀微泵和压缩通道。所述的无阀微泵由泵体与泵膜组成,泵体包括微泵入口、扩张锥管、泵腔、收缩锥管和液体暂存腔;所述的泵体、压缩通道以及微流控芯片出口是在微流控芯片基底上刻蚀形成的内部通道;微泵入口作为微流控芯片入口,其一端连接导管,导管与样品池连接,用于将样品池中的样品送入微流控芯片中;所述的扩张锥管,其入口端与微泵入口的另一端连接,其出口端与泵腔的入口端连接;所述的收缩锥管,其入口端与泵腔的出口端连接,其出口端与液体暂存腔的入口端连接;所述的液体暂存腔,其出口端与压缩通道的入口端连接,压缩通道的出口端与微流控芯片出口连接;微流控芯片出口连接导管,导管与收集池连接,用于将震荡后的样品送入收集池中;所述的泵腔,其顶端为开口结构,开口上覆盖有泵膜。
6、所述的扩张锥管和收缩锥管的入口端尺寸小于出口端尺寸。
7、所述的压缩通道包括窄直通道、宽直通道和过渡段,其中间部分为截面较小的窄直通道,其前后两段为截面较大的宽直通道,其中,窄直通道的两端通过过渡段与宽直通道连接,靠近压缩通道的入口端的过渡段的截面由大变小,靠近压缩通道的出口端的的截面由小变大;宽直通道的入口端作为压缩通道的入口端,与液体暂存腔连接,宽直通道的出口端作为压缩通道的出口端,与微流控芯片出口连接。
8、所述的压缩通道的整体长度为微米级,其中,窄通道的长度为百纳米量级;宽直通道的截面宽度为百纳米量级,宽直通道的宽高比为1:1,窄通道的截面宽度与高度均为十纳米级。
9、所述的泵膜控制系统由电磁铁与单片机组成,通过电磁感应方式驱动泵膜;其中,电磁铁主要由铁芯与线圈组成,铁心固定在微流控芯片上表面,铁芯下端的中心点与泵腔圆心的位置一致,线圈缠绕在铁芯上;单片机与线圈相连,通过发出方波信号使电磁铁产生周期性变化的磁场,泵膜在磁场的作用下振动,驱动泵腔中的流体。
10、所述的泵膜为各向同性磁流变弹性材料,材料以pdms为基底,混入体积分数为1%-5%的铁磁颗粒(fe3o4),经过混合、匀胶、烘干制备而成。
11、所述的微流控芯片基底的材料为pdms。
12、所述的生物大分子药物和细胞,加入到水中,然后加入黄原胶,获得混合液后再加入到样品池中;所述的黄原胶在混合液中浓度为1000ppm。
13、本发明的有益效果:
14、(1)本发明提供的利用振荡流的微流控大分子药物输送装置,集成度高、设计巧妙、操作简单,利用振荡流设计实现短通道的“无限长”,实现大分子药物的高效输送。同时,利用无阀微泵生成振荡流,使设备的结构简单,集成度高,易于推广,可用于生物、环境、化学领域微粒的富集。
15、(2)相较于传统的通道收缩方法,本发明使用的通道为“两边宽中间窄”,并在窄通道和宽通道之间加入了过渡段,这使得细胞可以很丝滑的从宽通道进入窄通道。而本发明中窄通道的截面更大,使细胞受到的挤压力与剪切力强度更低,细胞的活性更好、不易堵塞。当细胞通过窄通道后会进入过渡段和宽通道,解决了细胞堵塞问题。
16、(3)相较于传统的溶液,本发明应用了黄原胶悬浮液,使输送效率更高效,且黄原胶具有独特的流变性和良好的水溶性,能够提供更高的挤压力与剪切力且具有良好的润滑作用,可以有效改善细胞堵塞,使系统更高效的实现大分子药物输送。
技术特征:1.一种基于振荡流的微流控大分子药物输送装置,其特征在于,所述的基于振荡流的微流控大分子药物输送装置主要由微流控芯片、泵膜控制系统、储液池及导管组成;
2.根据权利要求1所述的一种基于振荡流的微流控大分子药物输送装置,其特征在于,所述的泵膜为各向同性磁流变弹性材料,材料以pdms为基底,混入体积分数为1%-5%的铁磁颗粒,经过混合、匀胶、烘干制备而成。
3.根据权利要求1或2所述的一种基于振荡流的微流控大分子药物输送装置,其特征在于,所述的微流控芯片基底的材料为pdms。
4.根据权利要求1或2所述的一种基于振荡流的微流控大分子药物输送装置,其特征在于,所述的生物大分子药物和细胞,加入到水中,然后加入黄原胶,获得混合液后再加入到样品池中。
5.根据权利要求4所述的一种基于振荡流的微流控大分子药物输送装置,其特征在于,所述的黄原胶在混合液中浓度为1000ppm。
技术总结本发明属于微流控技术领域,涉及一种基于振荡流的微流控大分子药物输送装置。本发明装置集成度高、设计巧妙、操作简单,利用振荡流设计实现短通道的“无限长”,实现大分子药物的高效输送。同时,利用无阀微泵生成振荡流,使设备的结构简单,集成度高,易于推广,可用于生物、环境、化学领域微粒的富集。本发明使用的压缩通道的截面更大,这样会使细胞受到的挤压力与剪切力强度更低,细胞的活性更好、不易堵塞。相较于传统的粘弹性流体,本发明应用了黄原胶,是输送效率更高效,且黄原胶具有独特的流变性和良好的水溶性,能够提供更高的挤压力与剪切力且具有良好的润滑作用,可以有效改善细胞堵塞,使系统更高效的实现大分子药物输送。技术研发人员:薛春东,于新琪,徐潇宇,李珊珊,覃开蓉,刘书馨,李泳江,那景童,郑周义受保护的技术使用者:大连理工大学技术研发日:技术公布日:2024/6/18本文地址:https://www.jishuxx.com/zhuanli/20240619/1238.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。