电化学构建C(sp3)-C(sp3)键的方法及其制备的化合物
- 国知局
- 2024-07-27 11:48:55
本发明涉及电化学构建c(sp3)-c(sp3)键的,进一步地说,是涉及电化学构建c(sp3)-c(sp3)键的方法及其制备的化合物。
背景技术:
1、c(sp3)-c(sp3)键广泛存在于生物活性物质,功能性聚合物和材料等各种有机分子中。因此,开发创新和高效的合成c(sp3)-c(sp3)键的方法将具有很大的科学价值和实用价值。现有的构建c(sp3)-c(sp3)键通常涉及烷基卤化物与sp3杂化碳亲核试剂(如格氏试剂、有机锌和有机硼等有机金属试剂)之间的反应,通过过渡金属催化的杂交偶联或直接亲核取代反应进行。然而,由于有机金属试剂的制备、处理、稳定性和对官能团的耐受性等问题,它们的实际应用非常受限。值得注意的是,这些有机金属亲核试剂通常是通过有机卤化物制备,使用常见易得的烷基卤化物亲电交叉偶联构筑c(sp3)-c(sp3)键不仅可以减少反应步骤,简化反应操作,提高经济效益,还可以显著提高官能团兼容性,但是化学计量还原剂和脱卤试剂的使用限制了其被广泛应用的可能。
2、有机电合成通过单电子转移(set)过程生成活性自由基物种的能力创造了广泛的合成机会,并且它能利用可再生和易得的电能来取代传统的氧化还原试剂,从而避免使用化学计量的化学品和减少化学废物。如使用两个简单的不同未活化烷基卤化物的交叉偶联构建c(sp3)-c(sp3)仍然充满挑战,需要克服以下科学问题(a)如何避免自偶联反应(视所需的产物需要),并从催化剂与两种结构、电子甚至空间相似的未活化烷基卤化物的反应中选择性地获得交叉偶联产物;(b)如何在不影响任何敏感官能团的情况下达到烷基卤化物的还原电位,以及如何避免还原脱卤和其他副反应的发生;(c)如何通过在生物相关化合物的所需碳(sp3)原子上顺利实现安装目标烷基来实现后期转化。
3、因此,需要开发一种新的效果更好的c(sp3)-c(sp3)键的构筑方法。
技术实现思路
1、为解决现有技术中出现的问题,本发明提出了电化学构建c(sp3)-c(sp3)键的方法及其制备的化合物。本发明通过电化学的方法构建c(sp3)-c(sp3)键,该方法是一种更高效、高选择性、绿色的烷基卤化物交叉偶联构建c(sp3)-c(sp3)键的方法。
2、为实现上述目的,本发明采用以下技术方案:
3、本发明的目的之一是提供一种电化学构建c(sp3)-c(sp3)键的方法,包括以下步骤:在保护性气氛中,催化剂的作用下,未活化的卤化物、配体、支持电解质在溶剂中进行电化学反应,实现c(sp3)-c(sp3)键的偶联。
4、作为进一步优选的实施方式:所述未活化的卤化物选自一级卤化物、二级卤化物或三级卤化物中的至少一种;
5、优选地,所述一级卤化物对应的结构式为:r1-r2-x;
6、所述二级卤化物对应的结构式为:;
7、
8、所述三级卤化物对应的结构式为:
9、
10、其中,所述未活化的卤化物中的x各自独立地选自卤素;
11、r1选自取代或未取代的芳基(优选选自取代或未取代的苯基)、取代或未取代的酯基、取代或未取代的酰胺基、羧基、卤素、羟基、氰基、烯基、取代或未取代的炔基、bpin基(联硼酸频那醇酯基)、nhboc基、h、醚基;
12、r2选自直链的亚烷基;
13、r3选自c1-c8的烷基;
14、r4选自c1-c8的烷基、r9-r10,其中,r9选自取代或未取代的芳基;r10选自c1-c10的亚烷基;
15、r5选自取代或未取代的环烷基、取得或未取代的杂环基;
16、r6、r7、r8各自独立地选自c1-c8的烷基。
17、作为进一步优选的实施方式:
18、所述未活化的卤化物中的x各自独立地选自br或i;
19、r2选自直链的c1-c8的亚烷基;优选选自直链的c1-c6的亚烷基;
20、r3选自c1-c5的直链烷基;优选选自c1-c3的直链烷基;
21、r4选自c1-c5的直链烷基、r9-r10,其中,r9选自取代或未取代的苯基;r10选自c1-c6的直链亚烷基;优选地,r4选自为c1-c3的直链烷基;
22、r5选自取代或未取代的c4-c20的环烷基、取代或未取代的含n杂环基、取代或未取代的含氧杂环基;优选地,r5选自c4-c15的环烷基、取代或未取代的含n六元杂环基、取代或未取代的含氧六元杂环基或取代或未取代的含氧五元杂环基;
23、r6、r7、r8各自独立地选自c1-c5的直链烷基;优选地,r6、r7、r8各自独立地选自c1-c3的直链烷基。
24、作为进一步优选的实施方式,所述未活化的卤化物选自以下化合物中的至少一种:
25、
26、
27、作为进一步优选的实施方式:
28、所述催化剂选自镍催化剂,优选所述催化剂选自卤化镍、高氯酸镍或乙二醇二甲醚溴化镍中的至少一种;进一步优选所述卤化镍选自溴化镍、氯化镍或碘化镍中的至少一种;和/或,
29、所述配体选自吡啶类配体或1,4-双(二苯基膦)丁烷中的至少一种;进一步优选所述吡啶类配体选自三联吡啶、2,6-二(1-吡唑基)吡啶、4,4′,4″-三叔丁基-2,2′:6′,2″-三联吡啶、4,4'-二叔丁基-2,2'-二吡啶、4,4'-二甲基-2,2'-联吡啶中的至少一种;和/或,
30、所述支持电解质选自卤化盐或四丁基四氟硼酸胺中的至少一种;进一步优选所述卤化盐选自溴化钠、四丁基碘化铵、四丁基溴化铵、四丁基氯化铵、碘化钾、碘化铵中的至少一种;和/或,
31、所述溶剂为有机溶剂,优选所述有机溶剂选自n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、乙腈或n-甲基吡咯烷酮中的至少一种。
32、作为进一步优选的实施方式,在本发明中,通过电化学反应进行构建c(sp3)-c(sp3)键,其中的卤化物可以相同也可以不同,优选所述卤化物选自两种不同的卤化物,记为卤化物一和卤化物二;上述卤化物一、卤化物二仅是为了说明选自不同的卤化物,卤化物一、卤化物二的配比也没有特殊要求,能实现上述反应即可,优选所述卤化物一和卤化物二的摩尔比为1:1—4;优选为1:1.5—3;或者,所述卤化物二和卤化物一的摩尔比为1:1—4;优选为1:1.5—3。
33、作为进一步优选的实施方式:以加入的所述卤化物总量计,所述催化剂与所述卤化物的摩尔比为1:10—100;优选为1:30—60,进一步优选为1:35—45;
34、所述配体与所述卤化物的摩尔比为1:5—40;优选为1:10—30,进一步优选为1:15—25;
35、所述支持电解质与所述卤化物的摩尔比为1:1—20;优选为1:3—15,进一步优选为1:7—15;
36、所述溶剂与所述卤化物的体积摩尔比为1-10ml:1;优选为3-6ml:1。
37、作为进一步优选的实施方式:所述电化学反应时,通入恒定电流,优选地,
38、所述恒定电流为5-50ma;优选为5-30ma;和/或,
39、通电反应时间为5-24h;优选为8-14h;和/或,
40、通电反应温度为-10-30℃;优选为20-25℃;和/或,
41、电氧化羰基化反应时,采用的电极中,阴极材料选自镍片、铁片、泡沫镍、石墨毡、铂片;阳极材料选自镁片、锌片、铝片、铁片。
42、本发明的目的之二是提供本发明的目的之一所述的电化学构建c(sp3)-c(sp3)键的方法制备的化合物,所述化合物具有以下结构通式:
43、
44、所述化合物中的r11、r12各自独立地选自权利要求1-8中所述的
45、
46、作为进一步优选的实施方式,所述化合物选自以下化合物:
47、
48、
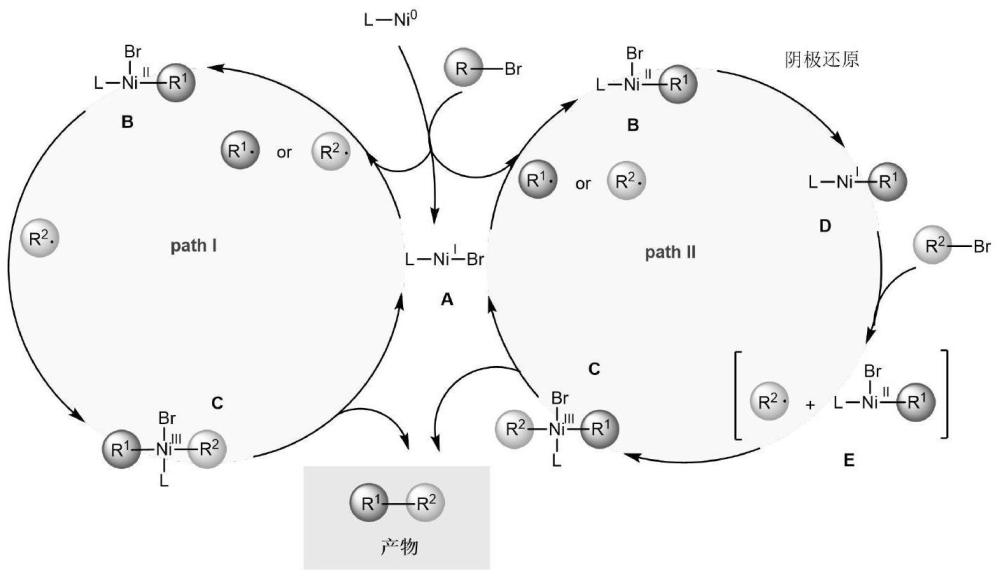
49、本发明反应机理如图1所示。从图1中,可以看出:在路径i中,电还原二价镍生成零价镍物种,之后零价镍还原烷基卤化物生成物种a和烷基自由基,由于两种烷基卤化物的浓度和电化学特性的差异,物种a参与一系列识别和连续的自由基添加和还原消除过程,最终产生交叉偶联产物。此外,在路径ii中,研究表明一价镍物种d具有与另一分子卤化物反应的能力,从而形成三价镍物种c,随后的反应通过还原消除步骤得到所需产物。
50、可见,本发明采用电化学催化方法,可通过不同配体去调控不同烷基卤化物的交叉偶联,适用于一级、二级、三级卤化物。同时该反应具有广泛的底物耐受性和官能团兼容性,并且适用于广泛的后修饰天然产物分子。作者通过一系列的机理试验和dft计算,证明了交叉偶联的高选择性是由不同底物的还原电势差异、位阻效应及所添加底物的浓度差共同决定的。该电化学合成方法实现的烷基卤化物交叉偶联构建c(sp3)-c(sp3)键反应,具有反应条件温和,选择性高、清洁绿色,反应操作简单的特点。
51、与现有技术相比,本发明具有以下优点:
52、本发明提供了一种的电化学构建c(sp3)-c(sp3)键的方法,该方法是一种更高效、高选择性、绿色的烷基卤化物交叉偶联构建c(sp3)-c(sp3)键的方法。
53、本发明的方案反应条件简单温和、选择性高、底物范围广(适用于一级、二级、三级卤化物)、官能团耐受性强(基本任何敏感官能团在反应过程中都不受影响,都不会发生副反应),所用原料廉价易得,具有良好的工业应用前景。
本文地址:https://www.jishuxx.com/zhuanli/20240726/119699.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表