一种新颖的GLV-酚酰胺:生物合成及在保护植物免受食草动物攻击中的功能的制作方法
- 国知局
- 2024-08-05 12:15:41
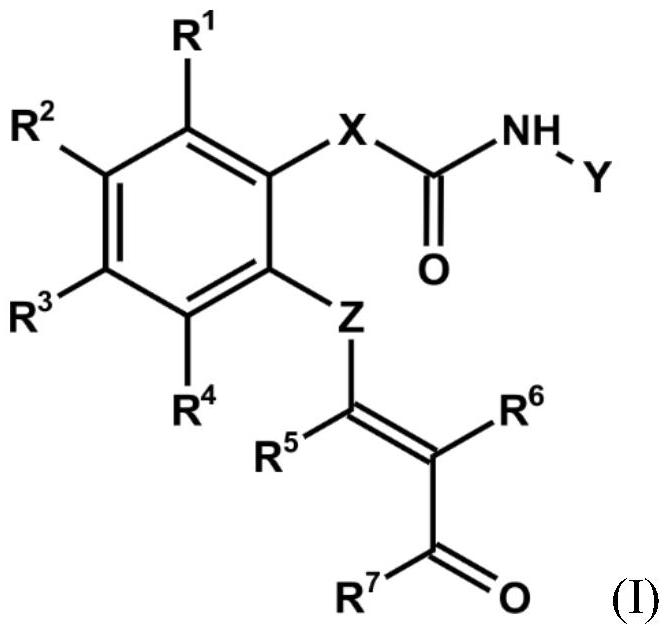
本发明涉及介导对叶蝉和飞虱害虫的抗性的通式(i)的化合物或对映异构体、非对映异构体、立体异构体。本发明进一步涉及制备所述化合物的方法,使用至少bbl2多肽以及ppo、at1、odc、hpl、pal、c4h、4cl、hct和/或c3h活性的酶促制备所述化合物的方法。进一步考虑了制备所述化合物的遗传修饰的生物体、用于异源表达活性的表达盒、相应多肽和多核苷酸用于制备所述化合物的用途、包含所述化合物的组合物、以及所述化合物用于植物保护的用途。
背景技术:
1、植物处于大多数陆地食物链的底端,不断受到食草动物和病原体的攻击(kessler和kalske,annual review of ecology,evolution,and systematics 49,115-138(2018),bednarek和osbourn,science 324,746-748(2009))。植物为大多数植食性昆虫物种提供各种资源,诸如食物、交配和产卵地点以及庇护所。昆虫对宿主植物的选择涉及对宿主植物的各种物理和化学特征的复杂行为应答,所述应答在不同的空间尺度上起作用,并且包括长距离嗅觉(例如,气味受体感知的植物衍生挥发物)和视觉(例如,植物形状、大小和颜色)线索以及短距离趋化性和味觉(例如,化学感受器感知的表面代谢物)线索(thorsteinson,ann.rev.entomol.5,193-218(1960))。昆虫用于宿主选择的植物的物理和化学特征取决于昆虫物种的进食集团(feeding guild)和饮食行为(例如多食性或寡食性)(prokopy和owens,entomol exp appl 24(3):609-62(1978))。
2、昆虫也可以感知植物激素。例如,谷实夜蛾(helicoverpa zea)(鳞翅目)幼虫可以感知茉莉酸(ja)(li等人,nature 419:712-715(2002)),茉莉酸在受到攻击过程中在食用植物中积聚,并诱导植物防御代谢物的从头合成(dicke和baldwin,trends plant sci,15:167-175,(2010))。因此,昆虫可能根据植物产生某些植物激素的能力来选择植物进食。
3、在某些情况下,昆虫可以抑制植物防御代谢物的积累作为食用植物选择的一种机制(howe和jander,annu rev植物biol 59:41-66(2008))。这些抑制机制经常与植物激素生物合成或信号传递途径的改变相关,并且可能涉及昆虫(musser等人,nature,416:599-600(2002))或载体微生物(mayer等人.j chem ecol,34:1045-1049(2008))所产生的特定酶(例如,葡萄糖氧化酶)。
4、对于半翅目的昆虫来说,对宿主植物特征的行为应答涉及一系列步骤,包括用唇轻拍和用它们刺穿式口器探测。这些最初的探测和进食尝试也会引发植物激素(诸如ja)及其介导的诱导的防御代谢物的快速积累。例如,当通过沉默ja生物合成途径的初始关键步骤而使渐狭叶烟草(nicotiana attenuata)植物缺乏ja时,它们在自然界中会受到小绿叶蝉属(empoasca)的半翅类叶蝉的严重攻击。
5、对提供生物因子(诸如小绿叶蝉属叶蝉)抗性的植物特性的研究主要集中于对病原体的非宿主抗性(fan等人,science 331,1185-1188(2011);peart等人,proc natl acadsci u s a 99,10865-10869(2002);sohn等人,new phytol 193,58-66(2012))和对食草动物的宿主抗性(agrawal,science 279,1201-1202(1998);karban和baldwin,universityof chicago press,104-166(2007))。这种侧重点差异可能反映了食草动物的更大生理自主性,它们会选择性地选取植物进行攻击,同时还面临着发现食草动物拒绝攻击的宿主抗性特性的挑战。在实验室的无选择测定中,由于防御途径被废除而变得“失去防御能力”的植物可能受到非宿主食草动物的攻击(muller等人,j chem ecol 36,905-913(2010);barth and jander,植物j 46,549-562(2006))。
6、但是,这些测定并未捕捉到昆虫在自然界中选择其宿主植物的选择性程序,从而限制了从这些实验室研究中可以得出关于非宿主抗性的推论。由于实地研究不足,非宿主抵抗食草动物的机制和代谢特性仍然在很大程度上未知。
7、尽管对植物在抵抗病原体的非宿主抗性方面起作用的特性了解很多,但对抵抗食草动物的非宿主抗性却知之甚少,尽管其在农业上具有重要意义。例如,小绿叶蝉属叶蝉通过窃听茉莉酸(ja)介导的信号传递的未知输出来识别宿主植物。
8、因此需要能够改善植物保护以对抗食草动物诸如叶蝉或飞虱的手段和方法。
技术实现思路
1、本发明解决了该需求并提供了通式(i)的化合物
2、
3、其中:
4、r1、r2、r3和r4彼此独立地各自是h、oh、(c1-c6)-烷基或(c1-c6)-烷氧基;
5、r5、r6和r7彼此独立地各自是h或(c1-c6)-烷基;
6、x是直链或支链(c1-c8)-烷基或直链或支链(c2-c8)-烯基,
7、y选自-(ch2)m-nh2、-(ch2)n-nh-(ch2)o-nh2、-(ch2)p-nh-(ch2)q-nh-(ch2)r-nh2、nh-(ch2)m-nh2、nh-(ch2)n-nh-(ch2)o-nh2和nh-(ch2)p-nh-(ch2)q-nh-(ch2)r-nh2,其中m、n、o、p、q和r各自是1至10之间的整数,或酪胺酯;且
8、z是直链或支链(c1-c8)-烷基或直链或支链(c2-c8)-烯基,
9、或其对映异构体、非对映异构体、立体异构体或盐。
10、发明人意外地发现,所述化合物赋予叶蝉抗性,并且可能提供对所有以刺吸方式进食或将其卵产在叶片中的昆虫的抗性。
11、在所述化合物的一个优选实施方案中,r1、r2、r3和r4中的两个是oh;r5、r6和r7各自是h;且x是直链(c2-c8)-烯基。
12、在所述化合物的一个优选实施方案中,r1和r4是h,r2和r3是oh,且x是-ch=ch-。
13、在一个进一步优选的实施方案中,所述化合物具有下式(ii):
14、
15、其中r5、r6、r7和z如上面所定义;
16、或是其对映异构体、非对映异构体、立体异构体或盐。
17、在另一个优选的实施方案中,所述化合物具有式(iii)
18、
19、或是其对映异构体、非对映异构体、立体异构体或盐。
20、在其它方面,本发明涉及制备根据本发明的化合物的方法。
21、在一个优选的实施方案中,所述方法是使用至少bbl2(小檗碱桥酶2)多肽的酶促制备方法。
22、在所述方法的一个进一步优选的实施方案中,所述bbl2(小檗碱桥酶2)多肽是:
23、(a)由具有seq id no:1的核苷酸序列的多核苷酸编码;
24、(b)由作为seq id no:1的变体的多核苷酸编码;
25、(c)由作为seq id no:1的等位基因变体的多核苷酸编码;
26、(d)由作为seq id no:1的物种同源物的多核苷酸编码;
27、(e)由与如在(a)至(d)中的任一项中所定义的多核苷酸具有至少75%、80%、90%、95%、97%、98%或99%同一性的多核苷酸编码;
28、(f)由能够在严谨条件下与在(a)至(d)中指定的多核苷酸中的任一种杂交的多核苷酸编码;
29、(g)由具有seq id no:2的多肽代表;
30、(h)由具有bbl2(小檗碱桥酶2)功能的seq id no:2的多肽片段代表;
31、(i)由具有bbl2(小檗碱桥酶2)功能的seq id no:2的多肽结构域代表;
32、(j)由包含与seq id no:2的氨基酸序列具有至少75%、80%、90%、95%、97%、98%或99%同一性的氨基酸序列并且具有bbl2(小檗碱桥酶2)功能的多肽代表;或
33、(k)由在(a)至(f)中指定的多核苷酸中的任一种编码的多肽代表。
34、在所述方法的一个进一步优选的实施方案中,所述酶促制备方法另外使用ppo(多酚氧化酶)活性或多肽,其中优选地所述ppo(多酚氧化酶)活性或多肽是:
35、(a)由具有seq id no:3或5的核苷酸序列的多核苷酸编码;
36、(b)由作为seq id no:3或5的变体的多核苷酸编码;
37、(c)由作为seq id no:3或5的等位基因变体的多核苷酸编码;
38、(d)由作为seq id no:3或5的物种同源物的多核苷酸编码;
39、(e)由与如在(a)至(d)中的任一项中所定义的多核苷酸具有至少75%、80%、90%、95%、97%、98%或99%同一性的多核苷酸编码;
40、(f)由能够在严谨条件下与在(a)至(d)中指定的多核苷酸中的任一种杂交的多核苷酸编码;
41、(g)由具有seq id no:4或6的多肽代表;
42、(h)由具有ppo(多酚氧化酶)活性的seq id no:4或6的多肽片段代表;
43、(i)由具有ppo(多酚氧化酶)活性的seq id no:4或6的多肽结构域代表;
44、(j)由包含与seq id no:4或6的氨基酸序列具有至少75%、80%、90%、95%、97%、98%或99%同一性的氨基酸序列并且具有ppo(多酚氧化酶)活性的多肽代表;或
45、(k)由在(a)至(f)中指定的多核苷酸中的任一种编码的多肽代表。
46、在一个优选的实施方案中,所述酶促制备方法另外使用ppo(多酚氧化酶)活性或多肽,其中优选地所述ppo(多酚氧化酶)活性或多肽是:
47、(a)由具有seq id no:3或5的核苷酸序列的多核苷酸编码;
48、(b)由作为seq id no:3或5的变体的多核苷酸编码;
49、(c)由作为seq id no:3或5的等位基因变体的多核苷酸编码;
50、(d)由作为seq id no:3或5的物种同源物的多核苷酸编码;
51、(e)由与如在(a)至(d)中的任一项中所定义的多核苷酸至少75%、80%、90%、95%、97%、98%或99%同一性的多核苷酸编码;
52、(f)由能够在严谨条件下与在(a)至(d)中指定的多核苷酸中的任一种杂交的多核苷酸编码;
53、(g)由具有seq id no:4或6的多肽代表;
54、(h)由具有ppo(多酚氧化酶)活性的seq id no:4或6的多肽片段代表;
55、(i)由具有ppo(多酚氧化酶)活性的seq id no:4或6的多肽结构域代表;
56、(j)由包含与seq id no:4或6的氨基酸序列具有至少75%、80%、90%、95%、97%、98%或99%同一性的氨基酸序列并且具有ppo(多酚氧化酶)活性的多肽代表;或
57、(k)由在(a)至(f)中指定的多核苷酸中的任一种编码的多肽代表。
58、在所述方法的一个进一步优选的实施方案中,所述酶促制备方法另外使用at1(多胺羟基肉桂酰基转移酶1)活性或多肽,其中优选地所述at1(多胺羟基肉桂酰基转移酶1)活性或多肽是:
59、(a)由具有seq id no:7的核苷酸序列的多核苷酸编码;
60、(b)由作为seq id no:7的变体的多核苷酸编码;
61、(c)由作为seq id no:7的等位基因变体的多核苷酸编码;
62、(d)由作为seq id no:7的物种同源物的多核苷酸编码;
63、(e)由与如在(a)至(d)中的任一项中所定义的多核苷酸具有至少75%、80%、90%、95%、97%、98%或99%同一性的多核苷酸编码;
64、(f)由能够在严谨条件下与在(a)至(d)中指定的多核苷酸中的任一种杂交的多核苷酸编码;
65、(g)由具有seq id no:8的多肽代表;
66、(h)由具有at1(多胺羟基肉桂酰基转移酶1)活性的seq id no:8的多肽片段代表;
67、(i)由具有at1(多胺羟基肉桂酰基转移酶1)活性的seq id no:8的多肽结构域代表;
68、(j)由包含与seq id no:8的氨基酸序列具有至少75%、80%、90%、95%、97%、98%或99%同一性的氨基酸序列并且具有at1(多胺羟基肉桂酰基转移酶1)活性的多肽代表;或
69、(k)由在(a)至(f)中指定的多核苷酸中的任一种编码的多肽代表。
70、在所述方法的一个进一步优选的实施方案中,所述酶促制备方法另外使用odc(鸟氨酸脱羧酶)活性或多肽和/或hpl(氢过氧化物裂解酶)活性或多肽,其中优选地
71、(a)所述odc(鸟氨酸脱羧酶)活性或多肽是:
72、(a)由具有seq id no:9或11的核苷酸序列的多核苷酸编码;
73、(b)由作为seq id no:9或11的变体的多核苷酸编码;
74、(c)由作为seq id no:9或11的等位基因变体的多核苷酸编码;
75、(d)由作为seq id no:9或11的物种同源物的多核苷酸编码;
76、(e)由与如在(a)至(d)中的任一项中所定义的多核苷酸具有至少75%、80%、90%、95%、97%、98%或99%同一性的多核苷酸编码;
77、(f)由能够在严谨条件下与在(a)至(d)中指定的多核苷酸中的任一种杂交的多核苷酸编码;
78、(g)由具有seq id no:10或12的多肽代表;
79、(h)由具有odc(鸟氨酸脱羧酶)活性的seq id no:10或12的多肽片段代表;
80、(i)由具有odc(鸟氨酸脱羧酶)活性的seq id no:10或12的多肽结构域代表;
81、(j)由包含与seq id no:10或12的氨基酸序列具有至少75%、80%、90%、95%、97%、98%或99%同一性的氨基酸序列并且具有odc(鸟氨酸脱羧酶)活性的多肽代表;或
82、(k)由在(a)(a)至(f)中指定的多核苷酸中的任一种编码的多肽代表;且
83、(b)所述hpl(氢过氧化物裂解酶)活性或多肽是:
84、(a)由具有seq id no:13、15或17的核苷酸序列的多核苷酸编码;
85、(b)由作为seq id no:13、15或17的变体的多核苷酸编码;
86、(c)由作为seq id no:13、15或17的等位基因变体的多核苷酸编码;
87、(d)由作为seq id no:13、15或17的物种同源物的多核苷酸编码;
88、(e)由与如在(a)至(d)中的任一项中所定义的多核苷酸具有至少75%、80%、90%、95%、97%、98%或99%同一性性的多核苷酸编码;
89、(f)由能够在严谨条件下与在(b)(a)至(d)中指定的多核苷酸中的任一种杂交的多核苷酸编码;
90、(g)由具有seq id no:14、16或18的多肽代表;
91、(h)由具有hpl(氢过氧化物裂解酶)活性的seq id no:14、16或18的多肽片段代表;
92、(i)由具有hpl(氢过氧化物裂解酶)活性的seq id no:14、16或18的多肽结构域代表;
93、(j)由包含与seq id no:14、16或18的氨基酸序列具有至少75%、80%、90%、95%、97%、98%或99%同一性的氨基酸序列并且具有hpl(氢过氧化物裂解酶)活性多肽代表;或
94、(k)由在(b)(a)至(f)中指定的多核苷酸中的任一种编码的多肽代表。
95、在所述方法的一个进一步优选的实施方案中,所述酶促制备方法另外使用pal(l-苯丙氨酸氨裂解酶)活性或多肽和/或c4h(反式-肉桂酸4-羟化酶)活性或多肽和/或4cl(4-香豆酸:辅酶a连接酶)活性或多肽和/或hct(羟基肉桂酰基-转移酶)活性或多肽和/或c3h(香豆酸3-羟化酶)活性或多肽,其中优选地:
96、(a)所述pal(l-苯丙氨酸氨裂解酶)活性或多肽是:
97、(a)由具有seq id no:19、21、23或25的核苷酸序列的多核苷酸编码;
98、(b)由作为seq id no:19、21、23或25的变体的多核苷酸编码;
99、(c)由作为seq id no:19、21、23或25的等位基因变体的多核苷酸编码;
100、(d)由作为seq id no:19、21、23或25的物种同源物的多核苷酸编码;
101、(e)由与如在a(a)至(d)中的任一项中所定义的多核苷酸具有至少75%、80%、90%、95%、97%、98%或99%同一性的多核苷酸编码;
102、(f)由能够在严谨条件下与在a(a)至(d)中指定的多核苷酸中的任一种杂交的多核苷酸编码;
103、(g)由具有seq id no:20、22、24或26的多肽代表;
104、(h)由具有pal(l-苯丙氨酸氨裂解酶)活性的seq id no:20、22、24或26的多肽片段代表;
105、(i)由具有pal(l-苯丙氨酸氨裂解酶)活性的seq id no:20、22、24或26的多肽结构域代表;
106、(j)由包含与seq id no:20、22、24或26的氨基酸序列具有至少75%、80%、90%、95%、97%、98%或99%同一性的氨基酸序列并且具有pal(l-苯丙氨酸氨裂解酶)活性的多肽代表;或
107、(k)由在a(a)至(f)中指定的多核苷酸中的任一种编码的多肽代表;且
108、(b)所述c4h(反式-肉桂酸4-羟化酶)活性或多肽是:
109、(a)由具有seq id no:27的核苷酸序列的多核苷酸编码;
110、(b)由作为seq id no:27的变体的多核苷酸编码;
111、(c)由作为seq id no:27的等位基因变体的多核苷酸编码;
112、(d)由作为seq id no:27的物种同源物的多核苷酸编码;
113、(e)由与如在b(a)至(d)中的任一项中所定义的多核苷酸具有至少75%、80%、90%、95%、97%、98%或99%同一性的多核苷酸编码;
114、(f)由多核苷酸能够在严谨条件下与在b(a)至(d)中指定的多核苷酸中的任一种杂交的多核苷酸编码;
115、(g)由具有seq id no:28的多肽代表;
116、(h)由具有c4h(肉桂酸4-羟化酶)活性的seq id no:28的多肽片段代表;
117、(i)由具有c4h(肉桂酸4-羟化酶)活性的seq id no:28的多肽结构域代表;
118、(j)由包含与seq id no:28的氨基酸序列具有至少75%、80%、90%、95%、97%、98%或99%同一性的氨基酸序列并且具有c4h(肉桂酸4-羟化酶)活性的多肽代表;或
119、(k)由在b(a)至(f)中指定的多核苷酸中的任一种编码的多肽代表;且
120、(c)所述4cl(4-香豆酸:辅酶a连接酶)活性或多肽是:
121、(a)由具有seq id no:29、105、107、109、111、113、115、117、119、121、123、125、127、129或131的核苷酸序列的多核苷酸编码;
122、(b)由作为seq id no:29、105、107、109、111、113、115、117、119、121、123、125、127、129或131的变体的多核苷酸编码;
123、(c)由作为seq id no:29、105、107、109、111、113、115、117、119、121、123、125、127、129或131的等位基因变体的多核苷酸编码;
124、(d)由作为seq id no:29、105、107、109、111、113、115、117、119、121、123、125、127、129或131的物种同源物的多核苷酸编码;
125、(e)由与如在c(a)至(d)中的任一项中所定义的多核苷酸具有至少75%、80%、90%、95%、97%、98%或99%同一性的多核苷酸编码;
126、(f)由能够在严谨条件下与在c(a)至(d)中指定的多核苷酸中的任一种杂交的多核苷酸编码;
127、(g)由具有seq id no:30、106、108、110、112、114、116、118、120、122、124、126、128、130或132的多肽代表;
128、(h)由具有4cl(4-香豆酸:辅酶a连接酶)活性的seq id no:30、106、108、110、112、114、116、118、120、122、124、126、128、130或132的多肽片段代表;
129、(i)由具有4cl(4-香豆酸:辅酶a连接酶)活性的seq id no:30、106、108、110、112、114、116、118、120、122、124、126、128、130或132的多肽结构域代表;
130、(j)由包含与seq id no:30、106、108、110、112、114、116、118、120、122、124、126、128、130或132的氨基酸序列具有至少75%、80%、90%、95%、97%、98%或99%同一性的氨基酸序列并且具有4cl(4-香豆酸:辅酶a连接酶)活性的多肽代表;或
131、(k)由在c(a)至(f)中指定的多核苷酸中的任一种编码的多肽代表;且
132、(d)所述hct(羟基肉桂酰基-转移酶)活性或多肽是:
133、(a)由具有seq id no:31、33、35、37、39、41或43的核苷酸序列的多核苷酸编码;
134、(b)由作为seq id no:31、33、35、37、39、41或43的变体的多核苷酸编码;
135、(c)由作为seq id no:31、33、35、37、39、41或43的等位基因变体的多核苷酸编码;
136、(d)由作为seq id no:31、33、35、37、39、41或43的物种同源物的多核苷酸编码;
137、(e)由与如在d(a)至(d)中的任一项中所定义的多核苷酸具有至少75%、80%、90%、95%、97%、98%或99%同一性的多核苷酸编码;
138、(f)由能够在严谨条件下与在d(a)至(d)中指定的多核苷酸中的任一种杂交的多核苷酸编码;
139、(g)由具有seq id no:32、34、36、38、40、42或44的多肽代表;
140、(h)由具有hct(羟基肉桂酰基-转移酶)活性的seq id no:32、34、36、38、40、42或44的多肽片段代表;
141、(i)由具有hct(羟基肉桂酰基-转移酶)活性的seq id no:32、34、36、38、40、42或44的多肽结构域代表;
142、(j)由包含与seq id no:32、34、36、38、40、42或44的氨基酸序列具有至少75%、80%、90%、95%、97%、98%或99%相似性的氨基酸序列并且具有hct(羟基肉桂酰基-转移酶)活性的多肽代表;或
143、(k)由在d(a)至(f)中指定的多核苷酸中的任一种编码的多肽代表;且
144、(e)所述c3h(香豆酸3-羟化酶)活性或多肽是:
145、(a)由具有seq id no:45的核苷酸序列的多核苷酸编码;
146、(b)由作为seq id no:45的变体的多核苷酸编码;
147、(c)由作为seq id no:45的等位基因变体的多核苷酸编码;
148、(d)由作为seq id no:45的物种同源物的多核苷酸编码;
149、(e)由与如在e(a)至(d)中的任一项中所定义的多核苷酸具有至少75%、80%、90%、95%、97%、98%或99%同一性的多核苷酸编码;
150、(f)由能够在严谨条件下与在e(a)至(d)中指定的多核苷酸中的任一种杂交的多核苷酸编码;
151、(g)由具有seq id no:46的多肽代表;
152、(h)由具有c3h(香豆酸3-羟化酶)活性的seq id no:46的多肽片段代表;
153、(i)由具有c3h(香豆酸3-羟化酶)活性的seq id no:46的多肽结构域代表;
154、(j)由包含与seq id no:46的氨基酸序列具有至少75%、80%、90%、95%、97%、98%或99%同一性的氨基酸序列并且具有c3h(香豆酸3-羟化酶)活性的多肽代表;或
155、(k)由在e(a)至(f)中指定的多核苷酸中的任一种编码的多肽代表。
156、在一个进一步优选的实施方案中,所述酶促制备通过体外提供的活性或多肽进行。特别优选的是,在ph值4.8或更低的ph值实行所述方法,更优选地通过使用氩气流固相萃取实行所述方法。
157、在一个进一步优选的实施方案中,所述酶促制备通过在活细胞、组织或生物体中提供的活性或多肽进执。
158、在一个进一步优选的实施方案中,所述酶促制备通过遗传修饰的细胞、组织或生物体和在遗传修饰的细胞、组织或生物体中进行,其中所述遗传修饰允许如上文定义的一种或多种活性或多肽的异源表达。
159、在另一个方面,本发明涉及一种用于制备根据本发明的化合物的生物体、组织或细胞,其被遗传修饰,其中所述遗传修饰允许如本文中定义的一种或多种活性或多肽的异源表达。
160、在所述方法、生物体、组织或细胞的一个优选的实施方案中,所述遗传修饰至少导致如本文中定义的bbl2(小檗碱桥酶2)多肽的表达。
161、在所述方法、生物体、组织或细胞的一个优选的实施方案中,所述遗传修饰至少导致如本文中定义的ppo(多酚氧化酶)活性或多肽的表达。
162、在所述方法、生物体、组织或细胞的一个进一步优选的实施方案中,所述遗传修饰至少导致如本文中定义的at1(多胺羟基肉桂酰基转移酶1)活性或多肽的表达。
163、在所述方法、生物体、组织或细胞的一个进一步优选的实施方案中,所述遗传修饰至少导致如本文中定义的odc(鸟氨酸脱羧酶)活性或多肽和/或hpl(氢过氧化物裂解酶)活性或多肽的表达。
164、在所述方法、生物体、组织或细胞的另一个优选的实施方案中,所述遗传修饰至少导致如本文中定义的pal(l-苯丙氨酸氨裂解酶)活性或多肽和/或c4h(反式-肉桂酸4-羟化酶)活性或多肽和/或4cl(4-香豆酸:辅酶a连接酶)活性或多肽或hct(羟基肉桂酰基-转移酶)活性或多肽和/或c3h(香豆酸3-羟化酶)活性或多肽的表达。
165、在所述方法、生物体、组织或细胞的另一个优选的实施方案中,所述表达由天然的、受调控的、组织特异性的或组成型的启动子传递。
166、特别优选的是,所述启动子允许(i)如本文中定义的活性或多肽的多顺反子表达,(ii)如本文中定义的活性或多肽的单独表达;或(iii)至少两种选自如本文中定义的活性的活性的组的成组表达。
167、进一步特别优选的是,所述表达是过表达。
168、在一个进一步优选的实施方案中,所述过表达由强调控的或强组成型启动子传递,和/或通过提供编码所述活性或多肽的遗传元件的至少第二个拷贝来传递。
169、在本发明的另一个具体实施方案中,所述酶活性或多肽来自属于烟草属的生物体。特别优选的是,所述酶活性或多肽来自渐狭叶烟草种类。
170、进一步优选的是,所述多核苷酸被包含在一个或多个染色体外载体或质粒中,和/或整合在所述生物体的基因组中。
171、在一个进一步优选的实施方案中,所述遗传修饰的生物体、组织或细胞是真核的。特别优选的是,所述遗传修饰的生物体是植物,或其中所述组织是植物组织,或其中所述细胞是植物细胞。
172、在进一步优选的实施方案中,所述遗传修饰的生物体属于、或所述组织或细胞衍生自被昆虫食草动物攻击的高等植物,优选受以撕裂和冲刷和/或刺吸方式进食的昆虫攻击的高等植物,更优选烟草属、茄属、稻属、玉米属、菜豆属或山茶属的高等植物。
173、在另一个方面,本发明涉及用于在真核宿主细胞中异源表达的表达盒,其中所述表达盒包含如本文中定义的多核苷酸。优选的是,所述宿主细胞是植物细胞。
174、在另一个方面,本发明涉及载体或插入构建体,其包含如本文中定义的多核苷酸或如本文中定义的表达盒。
175、在又另一个方面,本发明涉及如本文中定义的多肽或多核苷酸、如本文中定义的表达盒或如本文中定义的载体或插入构建体用于制备本发明的化合物的用途。
176、在另一个方面,本发明涉及如本文中定义的生物体、组织或细胞、或包含如本文中定义的表达盒或载体或插入构建体的生物体、组织或细胞用于制备本发明的化合物的用途。
177、在另一个方面,本发明涉及组合物,其包含根据本发明的化合物或用本发明的方法制备的化合物或由如本文中定义的生物体、组织或细胞制备的化合物。任选地,所述组合物另外包含可接受的载体、稳定剂和/或铺展剂。
178、在又另一个方面,本发明涉及本发明的化合物或用根据本发明的方法制备的化合物或由如本文中定义的生物体、组织或细胞制备的化合物用于植物保护以免受食草动物攻击的用途,或如本文中定义的组合物用于植物保护以免受抗食草动物攻击的用途。
179、在一个优选的实施方案中,所述食草动物是昆虫。
180、在另一个优选的实施方案中,所述昆虫是以撕裂和冲刷和/或刺吸方式进食的昆虫。
181、在一个进一步优选的实施方案中,所述昆虫是叶蝉或飞虱。特别优选的是,所述昆虫属于脊冠叶蝉(aphrodinae)、bathymatopohorinae、大叶蝉(cicadellinae)、离脉叶蝉(coelidiinae)、角顶叶蝉(deltocephalinae)、errhomeninae、尖颊叶蝉亚科(euacanthelinae)、宽头叶蝉(eurymelinae)、横脊叶蝉(evacantinae)、杆叶蝉(hylicinae)、叶蝉亚科(iassinae)、jascopinae、耳叶蝉(ledrinae)、迈叶蝉(megophthalminae)、窗翅叶蝉(mileewinae)、nastlopinae、多彩叶蝉(neobaliane)、新离脉叶蝉(neocoelidinae)、聂叶蝉(nioniinae)、凸缘叶蝉(phereurhinina)、portaninae、长胸叶蝉(signoretiinae)、锥胸叶蝉(tartesinee)、小叶蝉(typhlory bina)或窄颊叶蝉(ulopinae)科,更优选小绿叶蝉属(empoasca)、circulifer属、褐飞虱属(nilaparvata)、白背飞虱属(sogatella)、黑尾叶蝉属(nepotettix)或cicadulina属。
182、在另一个方面,本发明涉及本发明的化合物或用本发明的方法制备的化合物或由如本文中定义的生物体、组织或细胞制备的化合物或如本文中定义的组合物作为杀昆虫剂的用途。优选的是,所述杀昆虫剂是针对如上面所定义的昆虫。
183、在另一个优选的实施方案中,本发明涉及植物保护方法,其包括使植物或植物的一部分与如上面所定义的本发明的化合物或组合物接触。
本文地址:https://www.jishuxx.com/zhuanli/20240802/261837.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表