一种多壁碳纳米管-金属-PDA复合纳米材料及其制备方法及基于其的双响应载药系统
- 国知局
- 2024-08-22 14:48:22
本发明属于肿瘤治疗,涉及一种多壁碳纳米管-金属-pda复合纳米材料及其制备方法及基于其的双响应载药系统。
背景技术:
1、胰腺癌是一种高度恶性肿瘤,死亡率高,被称为“癌中之王”。其中80%的患者在首次确诊时已无手术机会,只能采取药物和介入治疗。不同于肝癌、结直肠癌和胃癌等其他消化道肿瘤,胰腺癌由于其“乏血供”特殊病生理特点,无论是化疗药物还是靶向药物只有极少部分药物可到达肿瘤区域发挥作用,胰腺癌的死亡率长期居高不下。因此,开发出对胰腺癌具有疗效好、副作用小的新治疗方法是非常重要且具有现实意义的。肿瘤介入消融治疗是继手术切除、放、化疗治疗之后的第四大肿瘤治疗方法,因具有疗效好、精准度高、创伤小和可局部、重复实施等优点,近年来在肿瘤精准治疗领域受到极大关注。不可逆电穿孔(irreversible electroporation,ire)消融治疗是一种新兴的介入消融方法,通过纳秒或微秒级的高电压电脉冲在肿瘤细胞膜上制造纳米级的孔洞,诱导肿瘤细胞凋亡和坏死,从而达到杀伤肿瘤的目的。与传统的肿瘤热消融、化学消融相比,ire消融治疗的最大优势在于在杀伤肿瘤的同时,不破坏周边正常的细胞、组织、神经和血管,因而特别适合胰腺肿瘤的治疗,但同样地,ire消融治疗也存在一定的局限性。由于肿瘤细胞具有异质性,不同肿瘤细胞内和细胞间的导电性能存在差异,因而作用于肿瘤细胞的电流强度难以保证,导致单次ire消融的效果和范围存在差异,因此与传统的热消融和化学消融相比存在一定的劣势。
技术实现思路
1、本发明针对现有技术中出现的不足,提供一种多壁碳纳米管-金属-pda复合纳米材料及其制备方法及基于其的双响应载药系统。
2、本发明的一个目的通过以下技术方案来实现:
3、一种多壁碳纳米管-金属-pda复合纳米材料,所述多壁碳纳米管-金属-pda复合纳米材料包括多壁碳纳米管(mwcnt)、金属纳米粒子和聚多巴胺(pda),所述多壁碳纳米管表面负载金属纳米粒子,聚多巴胺连接在多壁碳纳米管和/或金属纳米粒子上;所述多壁碳纳米管-金属-pda复合纳米材料具备超声显像功能。
4、优选地,所述多壁碳纳米管-金属-pda复合纳米材料的导电率为≥70μs/cm。
5、进一步优选,所述多壁碳纳米管-金属-pda复合纳米材料的导电率为80~500μs/cm。例如可以为80、100、120、150、180、200、250、300、350、400、450或500μs/cm,但不限于所列举的数值,数值范围内其它未列举的数值同样适用。
6、优选地,所述金属为金、银、铂、铜、铁中的一种或多种。
7、进一步优选,所述金属为金。
8、优选地,所述金属纳米粒子的平均粒径为1~300nm。进一步优选,所述金属纳米粒子的平均粒径为1~200nm;再进一步优选为1~50nm。
9、本发明的第二个目的通过以下技术方案来实现:
10、一种多壁碳纳米管-金属-pda复合纳米材料的制备方法,所述金属为金,包括以下步骤:
11、s1、在多壁碳纳米管水分散液中搅拌加入氯金酸溶液,加热反应,然后加入柠檬酸钠溶液,继续加热反应,固液分离后,获得多壁碳纳米管-au;
12、s2、在多壁碳纳米管-au悬浮液中加入氨水,再加入盐酸多巴胺溶液反应,固液分离后,获得多壁碳纳米管-au-pda复合纳米材料。
13、优选地,步骤s1中,加入氯金酸溶液之前,先将多壁碳纳米管水分散液进行超声处理。
14、优选地,超声处理的功率为10~800w,超声处理的时间为0.5~500min。进一步地,超声处理的频率为10~100khz。进一步优选,超声处理的功率为50~500w,例如可以为50、80、100、120、150、180、200、250、300、350、400、450或500w,但不限于所列举的数值;超声处理的时间为2~100min,例如可以为2、5、8、10、15、20、25、30、35、50、70、90或100min,但不限于所列举的数值。
15、步骤s1中,氯金酸溶液为氯金酸溶于水中形成,作为列举,氯金酸溶液的浓度为0.1~1000mg/ml;优选地,所述氯金酸溶液的浓度为0.5~200mg/ml。
16、步骤s1中,柠檬酸钠溶液为柠檬酸钠溶于水中形成,作为列举,柠檬酸钠溶液的浓度为0.1~1000mg/ml;优选地,所述柠檬酸钠溶液的浓度为0.5~200mg/ml。
17、优选地,多壁碳纳米管与氯金酸的质量比为1:0.01~100;进一步优选,多壁碳纳米管与氯金酸的质量比为1:0.1~10,例如可以为1:0.1、1:0.5、1:1、1:2、1:5、1:8或1:10,但不限于所列举的数值。
18、优选地,氯金酸与柠檬酸钠的质量比为1:0.01~100;进一步优选,氯金酸与柠檬酸钠的质量比为1:1~20,例如可以为1:1、1:2、1:4、1:6、1:8、1:10、1:12、1:15、1:18或1:20,但不限于所列举的数值。
19、优选地,步骤s1的加热反应温度为80~200℃,时间为1~30min;进一步优选,步骤s1的加热反应温度为120~180℃,时间为2~15min。优选地,步骤s1的继续加热反应温度为80~200℃,时间为2~60min;进一步优选,步骤s1的继续加热反应温度为120~180℃,时间为5~50min。
20、步骤s2的多壁碳纳米管-au悬浮液为步骤s1的多壁碳纳米管-au分散于溶剂中形成,溶剂可以为水、甲醇、乙醇、丙酮中的一种或多种。
21、优选地,步骤s2中加入的氨水浓度为5~30%(w/w)。
22、优选地,步骤s2中,多壁碳纳米管-au的质量与氨水的体积比为1:0.05~10(mg/ml);进一步优选为1:0.1~5(mg/ml)。
23、步骤s2中,盐酸多巴胺溶液为盐酸多巴胺溶于水中形成,作为列举,盐酸多巴胺溶液浓度为0.1~2000mg/ml;优选地,盐酸多巴胺溶液浓度为0.5~200mg/ml。
24、优选地,步骤s2中,多壁碳纳米管-au与盐酸多巴胺的质量比为1:0.01~100;进一步优选为1:0.1~50;再进一步优选为1:1~30。
25、优选地,步骤s2加入盐酸多巴胺溶液的反应温度为10~40℃,反应时间为0.1~10小时。进一步优选为在室温下反应0.5~5小时。
26、制备得到的多壁碳纳米管-金属-pda复合纳米材料具备超声显像功能。
27、优选地,制备得到的多壁碳纳米管-金属-pda复合纳米材料的导电率≥70μs/cm。
28、本发明的第三个目的通过以下技术方案来实现:
29、一种多壁碳纳米管-金属-pda复合纳米材料的制备方法,所述金属为银,包括以下步骤:
30、s1、将硝酸银溶液加入多壁碳纳米管水分散液中,进行超声处理,固液分离后,获得多壁碳纳米管-ag;
31、s2、在多壁碳纳米管-ag悬浮液中加入氨水,再加入盐酸多巴胺溶液反应,固液分离后,获得多壁碳纳米管-ag-pda复合纳米材料。
32、优选地,步骤s1中,硝酸银溶液为硝酸银溶于有机溶剂中形成,有机溶剂可列举为甲醇、乙醇、丙酮等。作为列举,硝酸银溶液的浓度为0.1~1000mg/ml;优选地,所述硝酸银溶液的浓度为0.5~200mg/ml。
33、优选地,步骤s1中,多壁碳纳米管与硝酸银的质量比为1:0.01~100;进一步优选,多壁碳纳米管与硝酸银的质量比为1:0.1~10,例如可以为1:0.1、1:0.5、1:1、1:2、1:5、1:8或1:10,但不限于所列举的数值。
34、优选地,所述超声处理的功率为10~800w,超声处理的时间为5~500min,超声处理的频率为10~100khz。进一步优选,超声处理10~50min。
35、步骤s2的优选同本发明第二个目的的多壁碳纳米管-金属-pda复合纳米材料的制备方法。
36、制备得到的多壁碳纳米管-金属-pda复合纳米材料具备超声显像功能。
37、优选地,制备得到的多壁碳纳米管-金属-pda复合纳米材料的导电率≥70μs/cm。
38、本发明的第四个目的通过以下技术方案来实现:
39、一种基于多壁碳纳米管-金属-pda复合纳米材料的双响应载药系统,所述双响应载药系统由多壁碳纳米管-金属-pda复合纳米材料包封治疗药物构成。
40、优选地,所述治疗药物为抗肿瘤药物,进一步地,所述治疗药物为抗胰腺肿瘤药物,包括但不限于盐酸阿霉素(dox)、吉西他滨、卡培他滨、顺铂、表柔比星等中的一种或多种。
41、优选地,所述双响应载药系统在酸刺激和/或电刺激下释放治疗药物。进一步优选,所述双响应载药系统在在酸刺激或电刺激下释放10h时治疗药物的释放率>8%;进一步优选,所述双响应载药系统在在酸刺激和电刺激下释放10h时治疗药物的释放率>20%。
42、本发明的第五个目的通过以下技术方案来实现:
43、一种基于多壁碳纳米管-金属-pda复合纳米材料的双响应载药系统的制备方法,包括以下步骤:将多壁碳纳米管-金属-pda复合纳米材料分散于水中,然后加入治疗药物,搅拌得到双响应载药系统。
44、优选地,多壁碳纳米管-金属-pda复合纳米材料与加入的治疗药物的质量比为1:0.01~100,进一步优选为1:0.05~10,可以列举为1:10、1:5、1:2、1:1、1:0.5、1:0.25、1:0.1或1:0.05,但不限于所列举的数值。
45、优选地,搅拌1~70h得到双响应载药系统。进一步优选,搅拌2~50h,再进一步优选,搅拌5~40h。
46、与现有技术相比,本发明具有以下有益效果:
47、1、本发明通过原位生长法,从而成功在mwcnt上负载金属,制备获得了具备导电性能的mwcnt-金属;
48、2、本发明利用持续超声的方法,提升了一步法合成mwcnt-金属中金属纳米颗粒的负载量;
49、3、本发明进一步在mwcnt-金属上连接聚多巴胺,聚多巴胺有利于提高复合纳米材料的分散性,且最重要的是,聚多巴胺连接在mwcnt-金属上,获得的mwcnt-金属-pda具有优异的导电性和稳定性;
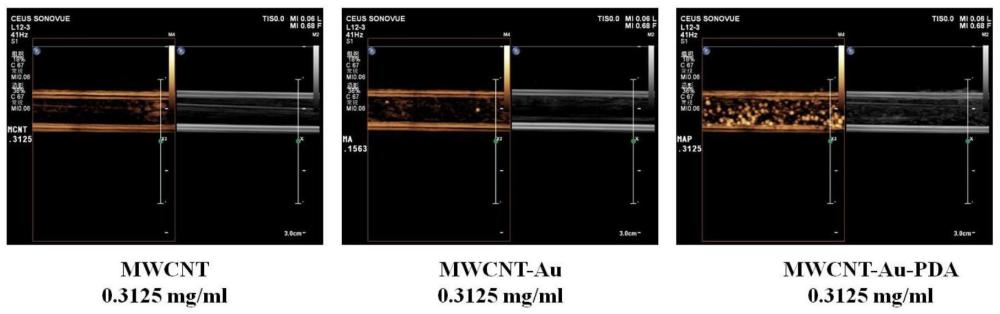
50、4、本发明提供的mwcnt-金属-pda具有优异的超声显像能力,更有利于显示mwcnt-金属-pda纳米药物荷载体系在癌细胞体内外实验中摄取和代谢情况;
51、5、本发明提供的基于多壁碳纳米管-金属-pda复合纳米材料的双响应载药系统具备双重响应释放功能(电响应性和酸响应性),即在酸性环境中和电刺激时均可有效释放治疗药物,可对局部肿瘤进行有效杀伤;
52、6、本发明提供的双响应载药系统可以与ire电消融治疗进行有机结合,ire消融在细胞膜上产生的纳米级孔洞也有助于双响应载药系统缓释出的抗肿瘤药物进入细胞内发挥作用,提高肿瘤细胞凋亡和坏死的比率和数量,进一步提升单次ire电消融治疗肿瘤的效果和范围,预防肿瘤的局部复发和转移。
本文地址:https://www.jishuxx.com/zhuanli/20240822/279950.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表