一种抗原表位在制备治疗肿瘤的产品中的应用
- 国知局
- 2024-09-14 14:24:46
本发明属于生物,具体涉及一种抗原表位在制备治疗肿瘤的产品中的应用。
背景技术:
1、恶性肿瘤是现代人类健康的巨大威胁。20世纪以来人们开始利用免疫系统特异性消除肿瘤的发生。伴随着基因的改变,主要包括了同义突变、非同义突变、插入或缺失突变等,这些基因改变都可能产生新抗原。带有新抗原的肿瘤细胞在死亡后被附近的抗原递呈细胞捕获,经吞噬加工后递呈出新抗原,激活附近引流淋巴结里的t细胞,后者通过循环系统到达肿瘤微环境,识别肿瘤细胞表面的新抗原,进而杀伤肿瘤。
2、目前针对新抗原开发免疫疗法,包括个性化新抗原疫苗、免疫检查点阻断疗法(immune checkpoint inhibitors,icb)和抗原特异性t细胞的过继细胞转移疗法(adoptive cell therapy,act)。2015年肿瘤新抗原疫苗的文章首次发表于science杂志,证实了新抗原dc疫苗可以有效的激活抗原特异性的t细胞。2017年靶向黑色素瘤新抗原的多肽疫苗与rna疫苗研究发表于nature杂志,在接种了多表位rna疫苗的13名患者中都检测到了针对部分疫苗新表位的t细胞反应,来自2名患者的活检报告证实了疫苗诱导的新抗原特异性t细胞的浸润和自体黑色素瘤细胞的特异性杀伤。除了针对新抗原开发的肿瘤疫苗,靶向新抗原的过继性免疫治疗(adoptive cell transfer therapy,act)也受到了关注,2021年,宾夕法尼亚大学医学院的研究人员开发的tcr-t细胞免疫疗法,靶向kras g12v新抗原,用于治疗kras突变驱动的难以治疗的癌症,包括肺癌、结肠直肠癌、和胰腺肺癌。该疗法的首个临床试验预计在2022年启动,证明了新抗原是一种非常有前景的基于免疫疗法的临床靶点。
3、然而,患者的肿瘤差异和个体差异也导致了肿瘤新抗原的产生极具个性化,新抗原很难共享使用。“免疫编辑”也在很大程度上影响了新抗原可用性,nature报导了关于胰腺导管腺癌(pdac)的跟踪研究结果,揭示了在人类肿瘤中存在免疫编辑的现象。且有证据表明,免疫编辑可能会使一些肿瘤的反应性降低,因此免疫编辑很有可能会降低新抗原特异性的免疫反应。新抗原预测过程需要的全基因组测序、rna测序,另外个性化疫苗的生产也造成新抗原疗法成本昂贵,限制了它的推广。新抗原预测的不准确性造成了这种治疗方案的发展局限。2020年,由25个新抗原预测团队组成的肿瘤新抗原选择联盟(tumorneoantigen selection alliance,tesla),他们同时对6名肿瘤患者样本进行新抗原预测,将所有团队预测出的抗原肽进行排序后,选择了前608个进行免疫原性的检测,结果发现仅有37个具有免疫原性,免疫原性预测的平均准确度只有6%。
4、综上所述,新抗原预测技术的缺陷、在部分患者中表达比例低、个性化生产成本高昂,以及免疫编辑造成肿瘤携带的天然新抗原的免疫原性低等都限制了其广泛应用的潜力。
技术实现思路
1、本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明提出一种抗原表位的应用。
2、本发明还提出一种含有上述抗原表位的生物材料。
3、本发明还提出一种抗肿瘤组合产品。
4、根据本发明的一个方面,提出了一种抗原表位在以下(1)~(5)任一项中的应用;
5、(1)制备治疗和/或预防肿瘤的产品;
6、(2)制备car-t靶点治疗产品;
7、(3)制备tcr-t靶点治疗产品;
8、(4)制备肿瘤免疫产品;
9、(5)制备肿瘤相关的疫苗;
10、所述抗原表位为利用rna编辑对肿瘤抗原进行定点突变得到新的抗原表位。
11、在本发明的一些实施方式中,所述定点突变通过将肿瘤抗原rna的核酸序列中的a突变到i和/或c突变到u来达成。
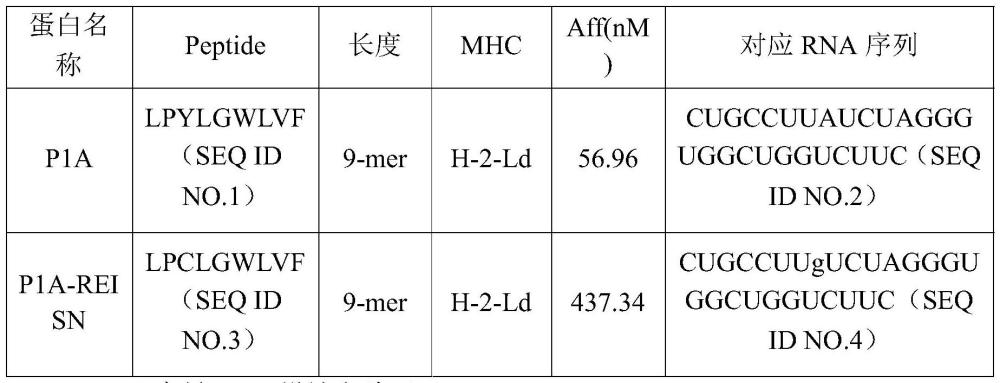
12、在本发明的一些实施方式中,所述肿瘤抗原包括p1a、afp和spag9-2。
13、在本发明的一些实施方式中,所述抗原表位的氨基酸序列如seq id no.3、seq idno.11、seq id no.16、seq id no.17或seq id no.18所示。
14、在本发明的一些实施方式中,所述肿瘤抗原包括肿瘤特异性抗原和肿瘤相关抗原。
15、在本发明的一些实施方式中,所述肿瘤相关抗原包括胚胎抗原、分化抗原、癌睾抗原和病毒抗原中的至少一种。
16、在本发明的一些实施方式中,所述肿瘤特异性抗原包括化学物质诱发的肿瘤特异性抗原、病毒诱发的肿瘤特异性抗原和自发肿瘤的抗原性中的至少一种。
17、在本发明的一些实施方式中,所述肿瘤包括睾丸癌、直肠癌、结直肠癌、小肠癌、大肠癌、胃癌、食管癌、下咽癌、喉癌、口腔癌、鼻腔癌、胰腺癌、肝癌、肺癌、乳腺癌、卵巢癌、宫颈癌、子宫内膜癌、阴道癌、输卵管癌、肾癌、黑色素瘤、脑瘤、甲状腺癌、甲状旁腺癌、白血病、淋巴瘤、骨髓瘤、肉瘤、前列腺癌、膀胱癌、胆管癌、胆囊癌中的至少一种。
18、在本发明的一些实施方式中,所述rna编辑技术采用的编辑系统包括leaper、λn-boxb或ms2-mcp2。
19、在本发明的一些实施方式中,还包括对制备得到的抗原表位进行检测的步骤,所述检测包括对抗原表位进行序列分析。
20、在本发明的一些实施方式中,所述序列分析的方法为测序。
21、在本发明的一些实施方式中,还包括对新的肿瘤相关抗原表位进行计算机辅助设计分析亲和力的步骤。
22、在本发明的一些实施方式中,计算机辅助设计分析亲和力采用的设计软件为netmhcpan-4.1及其他计算mhc与短肽亲和力的辅助软件。
23、在本发明的第二方面,提出了一种生物材料,所述生物材料能够诱导rna编辑生成上述的抗原表位。
24、在本发明的一些实施方式中,所述生物材料包括重组表达载体、表达盒、重组菌、宿主细胞或rna。
25、在本发明的一些实施方式中,所述表达载体包括病毒载体。
26、在本发明的一些实施方式中,所述rna包括经修饰的rna或环状rna。
27、在本发明的一些实施方式中,所述重组表达载体包括编辑靶标rna的腺苷脱氨酶向导rna或编码所述向导rna的构建体。
28、在本发明的一些实施方式中,所述构建体表达的向导rna的序列不小于16bp,与靶位点mrna的序列反向互补,同源性不小于85%。
29、在本发明的一些实施方式中,所述向导rna的序列如seq id no.5、seq id no.6、seq id no.7、seq id no.12、seq id no.19、seq id no.20、seq id no.21所示。
30、在本发明的第三方面,提出了一种抗肿瘤组合产品,所述抗肿瘤组合产品包括上述抗原表位和/或生物材料。
31、在本发明的一些实施方式中,所述抗肿瘤组合产品还包括免疫检查点抑制剂(icb)。
32、在本发明的一些实施方式中,所述免疫检查点抑制剂包括ctla-4单抗、pd-1/pd-l1单抗。
33、在本发明的一些实施方式中,所述抗肿瘤组合产品为药品、疫苗、保健品或食品。
34、在本发明的一些实施方式中,所述药品还包括药物载体和/或药用辅料。
35、在本发明的一些实施方式中,所述药用载体包括核酸载体。
36、在本发明的一些实施方式中,所述核酸载体包括dna载体、rna载体和腺相关病毒载体中的至少一种。
37、在本发明的一些实施方式中,所述疫苗包括多肽类疫苗、病毒疫苗、dna疫苗、rna疫苗、细胞类疫苗中的至少一种。
38、根据本发明的一些的实施方式,至少具有以下有益效果:本发明方案针对目前已有的肿瘤抗原表位进行编辑,避免的新抗原预测的不准确性,且降低预测的时间和经济成本;选择在肿瘤细胞共享表达,但在正常组织不表达的肿瘤相关性抗原表位,人为引入的新抗原具备肿瘤特异性和共享性;使用较比dna编辑更为安全可控的rna编辑系统,编辑针对mrna而非基因组dna,编辑结果可逆且可控;同时,目前针对共享抗原表位的研究受限于该类型抗原的高反应性t细胞阴性筛选,本发明针对该类抗原引入点突变,突变后的抗原表位不被阴性筛选所限制;免疫编辑可能会使目前的新抗原治疗反应性降低,而本发明的方案可以在肿瘤发生发展的过程中随时灵活的引入新抗原,增强免疫治疗的反应性。
本文地址:https://www.jishuxx.com/zhuanli/20240914/293928.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表