一种半自动密闭化制备肿瘤特异性T细胞制剂的方法
- 国知局
- 2024-10-21 15:10:16
本发明属于细胞培养,具体涉及一种半自动密闭化制备肿瘤特异性t细胞制剂的方法。
背景技术:
1、肿瘤特异t细胞可有效抑制肿瘤细胞生长,而且肿瘤特异t细胞的抗肿瘤效应对集体免疫系统功能不产生危害,在当前对肿瘤特异性抗原了解相对较少的情况下,应用肿瘤特异t细胞作为肿瘤放化疗和手术后的辅助治疗有重要的临床意义。
2、目前,在细胞疗法的细胞制剂生产上,外周血成分分离以及细胞培养过程一般是依靠人工操作的方法进行的,在进行实验时中,常需要使用移液管或者吸管将血液转移到离心管中,通过多步离心及进行组分转移而实现各成分分离,在培养过程中,液体试剂或细胞培养液的转移也多会暴露于空气中,这种开放式方法容易造成制备过程污染,过程繁琐,费时费力,且手动分离会造成转移过程中材料的浪费。因此,希望提供一种半自动、密闭生产肿瘤特异性t细胞制剂的方法。
技术实现思路
1、本发明的目的在于提供提供一种半自动、密闭生产肿瘤特异性t细胞制剂的方法,简化肿瘤特异性t细胞的培养过程,提高安全性,降低污染。
2、为了实现上述发明目的,本发明提供以下技术方案:
3、本发明提供了一种半自动密闭化制备肿瘤特异性t细胞制剂的方法,包括以下步骤:
4、(1)利用外周血单采机分离血细胞,并收集于采集套件上的储液袋中,然后利用无菌接管机将装有血细胞的储液袋连接到一次性细胞处理套件上的样品袋管路上,使其与pbmc分离机连通;
5、(2)准备培养基、分离液、洗涤液连接无菌接管机的一次性转液管,在自动补液机的驱动下分别转入一次性细胞处理套件上配套的储液袋中,并将一次性细胞处理套件上配套的储液袋与pbmc分离机上的凹槽连接,打开pbmc分离机对步骤(1)的血细胞进行自动化分离、洗涤、浓缩和收集,得到含有pbmc的储液袋;
6、(3)准备cd14磁珠重悬液连接无菌接管机的一次性转液管,在自动补液机的驱动下转入一次性细胞处理套件上配套的储液袋,然后与pbmc分离机上的凹槽连接,打开pbmc分离机将cd14磁珠重悬液与步骤(2)收集的pbmc导入pbmc分离机的离心杯中,进行磁珠孵育,得到含有cd14磁珠孵育好的pbmc的储液袋;
7、(4)准备培养基和macs buffer,与含有cd14磁珠孵育好的pbmc的储液袋分别连接无菌接管机的一次性转液管,在自动补液机的驱动下分别转入一次性细胞处理套件上配套的储液袋,并将一次性细胞处理套件上配套的储液袋与pbmc分离机上的凹槽连接,打开pbmc分离机进行自动化分选、洗涤和收集,得到cd14+细胞和cd14-细胞;
8、(5)利用步骤(4)得到的cd14+细胞培养得到dc细胞,利用cd14-细胞培养得到cik细胞;
9、(6)将步骤(5)得到的dc细胞和cik细胞混合共培养,纯化,即可得到肿瘤特异性t细胞制剂。
10、优选地,步骤(1)所述外周血单采机的单采参数为3~5次循环,每次循环450~550ml,采集时间1.5~2.5h。
11、优选地,步骤(2)和步骤(4)中所述培养基为x-vivo无血清培养基,步骤(2)中所述分离液为人淋巴分离液,所述洗涤液为含0.8~1.0%nacl的生理盐水;步骤(3)中所述cd14磁珠重悬液为含有0.08~0.12%cd14磁珠的macs buffer。
12、优选地,在步骤(5)培养dc细胞的过程中,依次添加dc细胞培养试剂a、dc细胞培养试剂b和dc细胞培养试剂c进行培养。
13、所述dc细胞培养试剂a为含有il-4和gm-csf的无血清培养基x-vivo,添加量为0.15~0.25ml,培养时间为4~5d;
14、所述dc细胞培养试剂b为含有gm-csf的无血清培养基x-vivo,添加量为0.15~0.25ml,培养时间为20~24h;
15、所述dc细胞培养试剂c为含ifn-γ和lps的无血清培养基x-vivo,添加量为0.15~0.25ml,培养时间为18~22h;
16、优选地,所述il-4的质量浓度为45~55ng/ml,gm-csf的质量浓度为90~110ng/ml,ifn-γ的浓度为900~1100iu/ml,lps的质量浓度为8~12ng/ml;
17、优选地,在步骤(5)cik细胞培养的过程中,依次添加cik细胞培养试剂a和cik细胞培养试剂b进行培养;
18、所述cik细胞培养试剂a为含90~110ng/ml ifn-γ和45~55ng/ml cd3单克隆抗体(okt-3)以及40ng~60ng/ml cd3/cd28单克隆抗体的无血清培养基x-vivo,添加量为0.05~0.15ml,培养时间为20~28h;
19、所述cik细胞培养试剂b为400~700iu/ml il-2的无血清培养基x-vivo,添加量为0.05~0.15ml,培养时间为5~6d。
20、优选地,准备dc细胞培养试剂a、b、c和cik细胞培养试剂a、b连接无菌接管机的一次性转液管,在自动补液机的驱动下分别转入一次性细胞处理套件上配套的储液袋中。
21、优选地,在步骤(6)dc-cik细胞共培养过程中,使用的共培养试剂为含有450~550iu/ml il-2和4~6%(体积比)自体血浆的无血清培养基x-vivo;
22、所述dc细胞、cik细胞和共培养试剂的的体积比为4~6:45~55:1;
23、dc-cik细胞共培养的培养时间为1~7d。
24、优选地,dc细胞培养、cik细胞培养和共培养过程均在35~39℃、4~6%(体积比)co2的培养箱中进行。
25、优选地,在所述磁珠孵育的程序中,离心腔转速5g~242g、温度0~8.3℃、时间10min~30min。
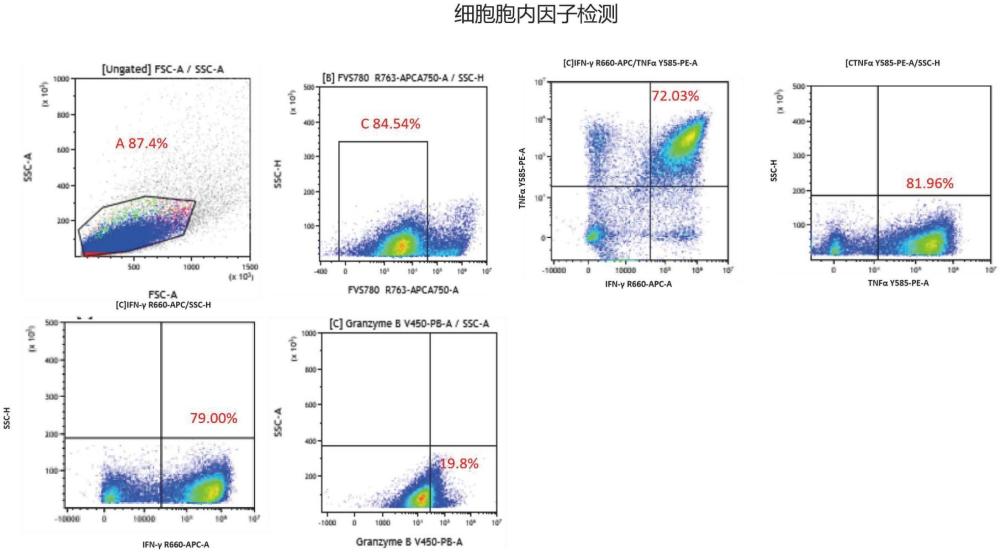
26、本发明针对肿瘤患者外周血,利用外周血单采机器采集血细胞,利用pbmc分离机分离pbmc,通过磁珠分选机进行细胞分选,设置自动补液机补充细胞培养过程中用到的液体试剂,通过无菌接管机将不同的设备和试剂进行连接,得到一种半自动密闭化制备肿瘤特异性t细胞制剂的方法。可在非gmp环境下自动进行细胞洗涤浓缩、细胞制剂制备、细胞因子和试剂的添加,保证了pbmc分离和dc-t细胞培养过程的安全性,提高了产能、减少人力和厂房建设成本,还能够在同比gmp环境下完成相同类型细胞培养产出,保证高抗肿瘤特异性t细胞cd3表面pd-1的表达,以及inf-γ,tnf-α和granzb等胞内因子的表达量。
技术特征:1.一种半自动密闭化制备肿瘤特异性t细胞制剂的方法,其特征在于,包括以下步骤:
2.如权利要求1所述制备肿瘤特异性t细胞制剂的方法,其特征在于,步骤(1)所述外周血单采机的单采参数为3~5次循环,每次循环450~550ml,采集时间1.5~2.5h。
3.如权利要求2所述制备肿瘤特异性t细胞制剂的方法,其特征在于,步骤(2)和步骤(4)中所述培养基为x-vivo无血清培养基,步骤(2)中所述分离液为人淋巴分离液,所述洗涤液为含0.8~1.0%nacl的生理盐水;步骤(3)中所述cd14磁珠重悬液为含有0.08~0.12%cd14磁珠的macs buffer。
4.如权利要求3所述制备肿瘤特异性t细胞制剂的方法,其特征在于,在步骤(5)培养dc细胞的过程中,依次添加dc细胞培养试剂a、dc细胞培养试剂b和dc细胞培养试剂c进行培养;
5.如权利要求4所述制备肿瘤特异性t细胞制剂的方法,其特征在于,所述il-4的质量浓度为45~55ng/ml,gm-csf的质量浓度为90~110ng/ml,ifn-γ的浓度为900~1100iu/ml,lps的质量浓度为8~12ng/ml。
6.如权利要求5所述制备肿瘤特异性t细胞制剂的方法,其特征在于,在步骤(5)cik细胞培养的过程中,依次添加cik细胞培养试剂a和cik细胞培养试剂b进行培养;
7.如权利要求6所述制备肿瘤特异性t细胞制剂的方法,其特征在于,准备dc细胞培养试剂a、b、c和cik细胞培养试剂a、b连接无菌接管机的一次性转液管,在自动补液机的驱动下分别转入一次性细胞处理套件上配套的储液袋中。
8.如权利要求7所述制备肿瘤特异性t细胞制剂的方法,其特征在于,在步骤(6)dc-cik细胞共培养过程中,使用的共培养试剂为含有450~550iu/ml il-2和4~6%(体积比)自体血浆的无血清培养基x-vivo;
9.如权利要求8所述制备肿瘤特异性t细胞制剂的方法,其特征在于,dc细胞培养、cik细胞培养和共培养过程均在35~39℃、4~6%(体积比)co2的培养箱中进行。
10.如权利要求9所述制备肿瘤特异性t细胞制剂的方法,其特征在于,在所述磁珠孵育的程序中,离心腔转速5g~242g、温度0~8.3℃、时间10min~30min。
技术总结本发明提供了一种半自动密闭化制备肿瘤特异性T细胞制剂的方法,属于细胞培养技术领域。包括以下步骤:利用外周血单采机分离血细胞置于储液袋中,然后将装有血细胞的储液袋连接到一次性细胞处理套件样品袋管路上;准备相应试剂连接无菌接管机的一次性转液管,在自动补液机的驱动下分别转入一次性细胞处理套件上配套的储液袋中,将其与PBMC分离机连接,对血细胞进行自动化分离、洗涤、浓缩、收集、磁珠孵育以及自动化分选等步骤,得到CD14+细胞和CD14‑细胞后进行DC‑T细胞培养,得到肿瘤特异性T细胞制剂。本发明可在非GMP环境下完成PBMC分离和DC‑T细胞培养过程,保证了培养过程的安全性,提高了产能、减少人力成本。技术研发人员:向橦,夏建川,叶茂受保护的技术使用者:中山大学肿瘤防治中心(中山大学附属肿瘤医院、中山大学肿瘤研究所)技术研发日:技术公布日:2024/10/17本文地址:https://www.jishuxx.com/zhuanli/20241021/320721.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表