一种基于色相变化的免疫层析试纸条双重分析方法
- 国知局
- 2024-10-21 15:12:11
本发明属于食品安全与品质检测领域,具体涉及一种基于色相变化的免疫层析试纸条双重分析方法。
背景技术:
1、食源性疾病是世界范围内的一个重要公共卫生问题,大约一半以上的食源性疾病是由细菌污染引起的。沙门氏菌属、弯曲杆菌属、单核细胞增生李斯特菌、金黄色葡萄球菌和致病性大肠杆菌是导致食品相关问题数量最多的主要病原体。
2、核酸检测在临床诊断、基因编辑、大流行疾病预防以及各种生物医学研究中至关重要。聚合酶链反应(polymerase chain reaction)是最早的,也是目前最流行的扩增和检测低丰度核酸的扩增技术。虽然pcr已广泛应用于各个领域,但它需要精密且昂贵的热循环仪,这在很大程度上限制了pcr在资源有限的环境和即时检测(poc)分析中的应用。为了满足在条件受限的环境下信号放大的需求,已经开发了多种等温核酸扩增方法,如重组酶聚合酶扩增(rpa)、滚环扩增(rca)、环介导等温扩增(lamp)、以及链置换扩增(sda)等。这些等温扩增方法因操作简单、具有较快扩增速度、高灵敏度和选择性、并且能在低温和恒定温度下操作而引起广泛关注。但是,在扩增过程中,二聚体与非靶扩增子的形成等非特异性现象会造成假阳性结果,因而寻找一种高特异性识别靶序列的分析方法是非常有必要的。
3、基于聚类规则间隔短回文重复序列(clustered regularly interspaced shortpalindromic repeats,crispr)相关核酸酶(cas)检测是一种很有前景的核酸检测新方法。已有很多工作报道,cas效应蛋白被用作高度特异性的序列识别元件,与等温扩增技术相联用,结合不同的信号读取方式进行现场检测,极大提高了核酸检测的特异性和准确度。目前,基于crispr/cas9结合等温扩增、侧流层析技术主要是通过在crispr/cas9体系中修饰信号分子,cas9与扩增产物结合形成复合物,该复合物可被测试线捕获,最终在侧流层析试纸条上测试线和质控线实现肉眼可读取的显色变化。
4、但是,目前基于crispr/cas9的侧流免疫层析试纸条只能实现单靶标检测,且通过肉眼判读胶体金试纸条测试线颜色的强弱时,只能得出“是”或“否”的定性结果,难以实现裸眼半定量或定量。
技术实现思路
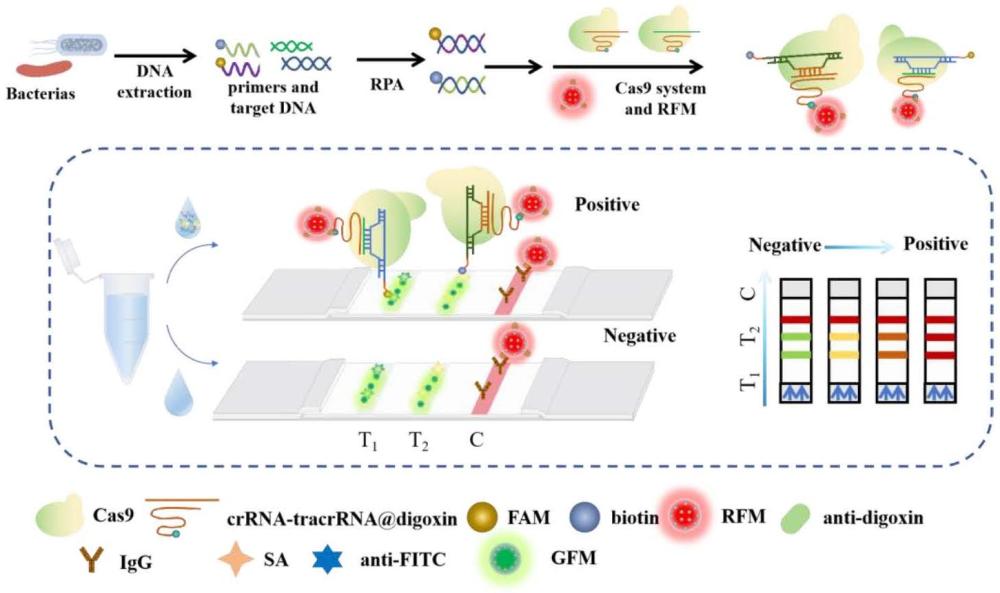
1、本发明提供了一种基于色相变化的免疫层析试纸条双重分析方法,免疫层析试纸条的测试线ⅰ上固定绿色荧光微球和抗体1,测试线ⅱ上固定绿色荧光微球和抗体2,结合垫喷涂抗体3修饰的红色荧光微球,通过在tracrrna上修饰抗原3使得dgrna1和dgrna2上同时修饰有同一种抗原;检测原理为:两种待测病原菌特征基因经核酸扩增后分别生成抗原1和抗原2标记的特异产物,随后分别被抗原3修饰的cas9/dgrna1和cas9/dgrna2结合并形成复合物,在层析作用下先与抗体3修饰的红色荧光微球耦联,再流经试纸条测试线ⅰ和测试线ⅱ时分别被相应的抗体捕获并导致紫外激发下相应测试线颜色由绿向红变化;无目标病原菌的样品相应测试线呈绿色;待测目标物浓度升高会导致相应测试线颜色由绿向黄绿、橙、或红发生变化,分别根据测试线呈现的颜色,可同时肉眼判别两种目标病原菌的大致含量,实现半定量检测。
2、本发明具体包括以下步骤:
3、1)免疫层析试纸条的组装;
4、2)提取待测样品的基因组dna;
5、3)对待测样本进行核酸扩增;
6、4)利用crispr/cas9对核酸扩增产物进行识别、结合;
7、5)采用免疫层析试纸条进行检测;
8、6)对免疫层析试纸条检测结果进行定性及半定量判读。
9、所述步骤1)中用于检测食源性致病菌核酸的免疫层析试纸条,其长为6~8cm,宽为3~4mm,其结构包括ps底板、样品垫、结合垫、硝酸纤维素膜、吸水垫(图1)。
10、所述ps底板作为侧向流动试纸条的骨架,用于粘贴并固定样品垫、结合垫、硝酸纤维素膜和吸水垫。
11、所述样品垫为玻璃纤维膜构成,固定在试纸条的起始端,作为试纸条与样品直接交流的窗口,用于样品的滴加。
12、所述结合垫固定在样品垫和硝酸纤维素膜之间,结合垫两侧分别与样品垫1和硝酸纤维素膜有2-3mm的重叠。所述结合垫表面喷涂了抗体3标记的红色荧光微球。
13、所述硝酸纤维素膜是检测结果的呈现窗口,划了质控线(c线)和测试线i、测试线ii。所述质控线靠近吸水垫一端,固定了抗体3对应的二抗;所述测试线i靠近结合垫一端,固定了抗体1和绿色荧光微球;所述测试线ii在测试线i和质控线中间,固定了抗体2和绿色荧光微球。所述测试线ⅰ与测试线ⅱ之间的距离为4-6mm,测试线ⅱ与质控线之间的距离为4-6mm。
14、在硝酸纤维素膜上设置测试线ⅰ、测试线ⅱ和质控线的方法为:取绿色荧光微球gsqs离心并重悬在含1%w/v tween-20的pbs缓冲溶液中,加入抗体1溶液并超声混匀,得到gsqs-抗体1混合溶液,即为测试线ⅰ溶液;用同样的方法制备gsqs-抗体2混合溶液;将测试线ⅰ溶液、测试线ⅱ溶液和质控线溶液(即抗体3对应的二抗溶液,浓度为1mg/ml,10mm pbs,ph 7.4)分别以1μl/cm的速度,用三维平面点膜喷金仪在硝酸纤维素膜上划线,烘干后即可。测试线ⅰ、测试线ⅱ和质控线的宽度约为3~4mm。
15、所述吸水垫为待测液流动提供动力,在试纸条的最末端。
16、所述抗体1为链霉亲和素、抗fitc、抗地高辛及其他常用抗原标签中的一种,所述抗体2为链霉亲和素、抗fitc、抗地高辛等抗体中的一种,所述抗体3为链霉亲和素、抗fitc、抗地高辛等抗体中的一种,且抗体1、抗体2、抗体3为不同种类的抗体。所述抗原1、抗原2、抗原3为三种不同的抗原,所述抗原1、抗原2、抗原3分别对应抗体1、抗体2、抗体3,抗原1、抗原2、抗原3为生物素、fitc、地高辛及其他常用抗原标签中的一种。
17、所述绿色荧光微球优选但不限于dsio2@gqds@sio2(gsqs),所述红色荧光微球优选但不限于dsio2@aunps@sio2@rqds(saq)。所述红色荧光微球的吸收光谱与所述绿色荧光微球的发射光谱存在较大重叠,所述绿色荧光微球发射的荧光能被所述红色荧光微球吸收(内滤效应),导致所述绿色荧光微球发光难以被观察到,颜色变化更明显。所述红色荧光微球以树状sio2(dsio2)为模板、aunps和rqds逐层自组装和包封的复合纳米材料。所述测试线上的内滤效应主要是由红色荧光微球saq中aunps的最大吸收(533nm)和gsqs的发射(525nm)有较好重叠而实现的。
18、所述步骤2)中样品基因组dna的提取方法包括但不限于柱层析法、酚抽提法、碱裂解法、ctab裂解法、磁珠提取法等。
19、所述步骤3)中对样本进行核酸扩增的方法包括但不限于重组酶聚合酶等温扩增(rpa)、滚环扩增(rca)、环介导等温扩增(lamp)、以及链置换扩增(sda)等。
20、所述步骤4)中利用crispr/cas9识别核酸扩增产物进行结合的条件优选为:100~500nm cas9、150~550nm dgrna1(crrna1-tracrrna)、150~550nm dgrna2(crrna2-tracrrna)、2~6μl扩增产物、检测缓冲液。所述crispr/cas9对核酸扩增产物进行检测的缓冲液包含tris-hcl缓冲液(5~50mm,ph 7.9)、mgcl2(5~15mm)、nacl(5~100mm)等。反应温度包括但不限于30~40℃,反应时间包括但不限于5~30分钟。
21、所述步骤4)中,dgrna1由crrna1和tracrrna骨架组成,dgrna2由crrna2和tracrrna骨架组成;
22、其中,crrna1的寡核苷酸链优选为:
23、5’-atgagttgatagcctcgtttguuuaagagcuaugcu-3’;
24、其中,crrna2的寡核苷酸链优选为:
25、5’-gaatatcgtactggcgatatguuuaagagcuaugcu-3’;
26、其中,tracrrna骨架为3’端修饰的寡核苷酸链,tracrrna序列优选为:5’-agcauagcaaguuuaaauaaggcuaguccguuaucaacuugaaaaaguggcacc gagucggugcuuu-3’;
27、所述副溶血弧菌正向引物和反向引物中的一条修饰有抗原1,所述沙门氏菌正向引物和反向引物中的一条修饰有抗原2,所述tracrrna骨架修饰有抗原3,使得dgrna1和dgrna2上同时修饰有同一种抗原;
28、所述抗原1、抗原2、抗原3为生物素、fitc、地高辛及其他常用抗原标签中的一种,所述抗原1、抗原2、抗原3为三种不同的抗原,所述抗原1、抗原2、抗原3分别对应抗体1、抗体2、抗体3。
29、所述cas9与dgrna1(由crrna1和tracrrna骨架组成)在所述检测缓冲液中形成复合后可识别并结合所述副溶血弧菌的扩增产物。
30、所述cas9与dgrna2(由crrna2和tracrrna骨架组成)在所述检测缓冲液中形成复合后可识别并结合所述沙门氏菌的扩增产物。
31、所述检测缓冲液包含10~50mm tris-hcl、ph 7.5~8.5、20~100mm nacl、5~20mm mgcl2、40~300μg/ml bsa。
32、所述步骤5)中采用免疫层析试纸条进行检测原理为:当待测样品中存在待测病原菌中的一种时,其特征基因经核酸扩增后产生大量的带有抗原1或抗原2修饰的扩增产物。所述扩增产物与cas9、抗原3修饰的dgrna1和dgrna2、检测缓冲液混合后被相应的cas9/dgrna结合,形成扩增产物1-cas9/dgrna1复合物1和扩增产物2-cas9/dgrna2复合物2。当带有抗原1或抗原2修饰的扩增产物-cas9/dgrna复合物流经结合垫时,复合物1和复合物2分别通过抗原3与抗体3修饰的红色荧光微球结合,随后在流经测试线i和测试线ii时抗体1或抗体2会分别捕捉抗原1、抗原2,使得扩增产物1-cas9/dgrna1复合物1在测试线i固定,扩增产物2-cas9/dgrna2复合物2在测试线ii固定,测试线i呈黄绿、橙或红色,测试线ii呈黄绿、橙或红色。相反的,当样品中不含相应的待测病原菌时,核酸扩增时无法形成相应扩增产物,抗体3修饰的红色荧光微球无法被测试线捕捉,测试线呈现绿色。随着待测病原菌浓度的增加,测试线信号呈现出绿色—黄绿色—橙色—红色的色相变化趋势,根据测试线颜色的不同能够读出特定的浓度,从而实现待测病原菌的半定量检测。
33、所述步骤5)中采用免疫层析试纸条进行检测的方法为:在所述步骤4)crispr/cas9识别后的反应产物中加入稀释缓冲液(0.2mmol/l edta,4mmol/l tris-hcl,10mmol/lmgcl2,ph=7.4)稀释,其中crispr反应产物与稀释缓冲液的最终体积比为1∶2~1∶5,之后将稀释产物滴加在试纸条样品垫上,层析10~15分钟。用波长为350nm的紫外激发光对划线区域进行照射,观察颜色变化情况。
34、所述步骤6)中对免疫层析试纸条检测结果进行半定量分析的方法为:采用一系列已知浓度的样品按照从所述步骤2)到步骤5)的方法进行检测,用波长为365nm的紫外激光对测试线和质控线进行照射,并用手机软件读取测试线上的色相值、制作标准比色卡。采用从步骤2)到步骤5)的方法对待测样品进行检测,并将侧向流动试纸条检测的结果与所述比色卡进行肉眼比对,实现待测样品的半定量检测。
35、所述步骤6)中对免疫层析试纸条检测结果定性判读的方法为:
36、当样品中存在一种待测致病菌时,肉眼观察到对应的测试线ⅰ或测试线ⅱ呈现红色、橙色或黄绿色,r/g值大于1.0;
37、当样品中存在两种待测致病菌时,肉眼观察到测试线ⅰ呈现红色、橙色或黄绿色,r/g值大于1.0;测试线ⅱ呈现红色、橙色或黄绿色,r/g值大于1.0;
38、当样品中不存在待测致病菌时,肉眼观察到测试线ⅰ和测试线ⅱ均为明显的绿色,r/g值小于1.0;
39、所述步骤6)中对免疫层析试纸条检测结果进行半定量分析的方法为:
40、将检测结果的颜色和色相值与标准比色卡上的颜色和色相值进行目测比对,标准比色卡上与检测结果最接近的颜色或色相值所对应的浓度作为样品中食源性致病菌的浓度,实现待测样品的半定量检测。
41、本发明的有益效果
42、(1)本发明提供一种将免疫层析试纸条与核酸扩增、crispr/cas9结合实现病原菌检测的方法,相比于常规核酸扩增与免疫层析试纸条结合的方法,本方法通过引入crispr/cas9能够提高检测结果的特异性。
43、(2)本发明提供的色相变化试纸条与常规胶体金试纸条相比,其结果的呈现是测试线从一种颜色向另一种颜色过渡,通过人眼对色相变化的敏感性强于对色度变化的敏感性,结合标准比色卡,无需借助仪器即可读出样本中目标病原菌的含量,实现半定量检测。
44、(3)本发明的色相变化的原理是通过不同荧光发射的纳米粒子的颜色叠加和内滤效应实现,相比于普通的颜色叠加的原理具有更为明显的颜色变化。
45、(4)本发明提供的方法在试纸条的硝酸纤维素膜上设计了两条测试线,分别针对不同的待测致病菌,并针对两种病原菌检测分别制作了两套标准比色卡,可实现两种病原菌同时肉眼半定量检测。
本文地址:https://www.jishuxx.com/zhuanli/20241021/320844.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表