吉西他滨的口服活性前药的制作方法
- 国知局
- 2024-11-06 15:08:32
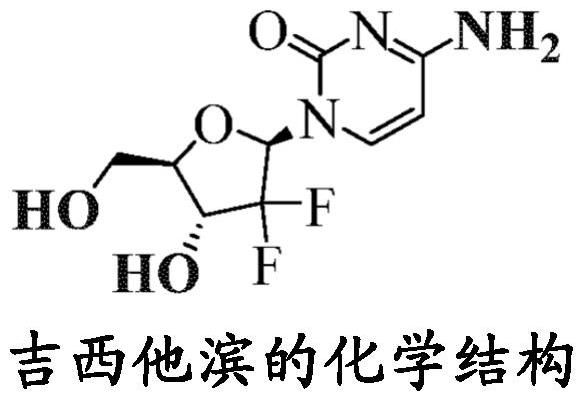
背景技术:
1、下面描述的吉西他滨是嘧啶核苷类似物,其显示对几种实体瘤类型具有活性。在1996年fda批准后,吉西他滨已成为治疗胰腺癌的护理标准。最近,该化合物还获得了用于治疗非小细胞肺癌、卵巢癌、膀胱癌和乳腺癌的批准。
2、
3、吉西他滨通过静脉内输注以约1000至1250mg/m2的剂量在30分钟内施用,每周一次,长达7周,然后从治疗起算停止一周。吉西他滨通过口服方式的使用受到其差的口服生物利用度的限制,这是首过代谢的结果。shipley la.等人“metabolism and dispositionof gemcitabine,and oncolytic deoxycytidine analog,in mice,rats,and dogs”.drugmetabolism&disposition.20(6):849-55,1992。此外,当口服给药时,在给予167、333或500mg/kg的单次口服(管饲)吉西他滨剂量的小鼠中,吉西他滨涉及引起不良的剂量限制性肠损伤,其特征在于在整个肠道长度上粘膜上皮中度至显著损失(萎缩性肠病)。horton nd等人,“toxicity of single-dose oral gemcitabine in mice”,american associationfor cancer research,poster presentation,orlando,fl,2004年3月27-31日。在先前的小鼠研究中,通过静脉内给药的可比较的暴露不会导致死亡或胃肠道毒性。
4、2009年,bender等人报道了吉西他滨的口服活性前药;ly2334737由于在4-(n)-位的丙戊酸键而显著不易于被cda降解。基于hct-116人结肠异种移植物中的体内数据,ly2334737进入i期临床研究,但在2013年日本患者的研究中观察到意外的肝毒性后,该开发终止。
5、如上述吉西他滨化学结构所示,吉西他滨具有适于化学前药衍生化的三个官能团(即-oh、-oh、-nh2)。wo2020/107013中描述了三取代的药物,其中所有三个可用部分都被取代。然而,三取代的前药化合物在室温下不稳定。该活性成分的不稳定性在制剂开发中提出了显著的问题,并且药物产品不稳定。因此,三取代的化合物不适合于进展为用于治疗用途的口服活性前药。
6、在该领域中一直在寻找吉西他滨的口服活性前药,用于开发和/或提供适合于癌症治疗的药物产品治疗,特别是用于治疗胰腺癌、卵巢癌和乳腺癌。
技术实现思路
0、发明概述
1、本发明涉及一类新的吉西他滨口服活性前药,其包含口服活性取代的前药,其中用前部分(用于修饰母体药物结构以改善物理化学、生物药学或药代动力学性质的化学官能团)衍生化特定官能团的组合。前部分通常是无活性的和生物学上安全的。然而,这些基团中的一个通常总是h,特别是r3处的基团,如下所示。
2、因此,本发明提供了式(i)化合物或其n-氧化物,或者所述式(i)化合物或其n-氧化物的药学上可接受的盐、溶剂合物、多晶型物、互变异构体、立体异构体、同位素形式或前药:
3、
4、其中:
5、r1选自2-丙基戊酸、2-(叔丁氧基羰基)-氨基-3-甲基丁酸和2-氨基-3-甲基丁酸;
6、r2是h;和
7、r3选自h、2-丙基戊酸、2-(叔丁氧基羰基)-氨基-3-甲基丁酸和2-甲基丙酸。
8、这种取代的化合物具有一个游离的伯醇位置(没有异丁酸部分),并且它是有利的,因为它对于适合于治疗用途的药物的制剂显示出增加的稳定性。
9、在其他实施方案中,r1和r3在以下相应组合中选择,以产生具体命名的化合物:
10、丙戊酸(2-丙基戊酸)(r1)和丙戊酸(r3),该实施方案的化合物为:2-丙基戊酸(2r,3r,5r)-4,4-二氟-2(羟基甲基)-5-(2-氧代4-(2丙基戊酰氨基)-1,2-二氢嘧啶-1-基)氧杂环戊烷-3-基酯;或
11、丙戊酸和h,该实施方案的化合物为:n-(1-((2r,4r,5r)-3,3-二氟-4-羟基-5-(羟基甲基)氧杂环戊烷-2-基)-2-氧代-1,2-二氢嘧啶-4-基)-2-丙基戊酰胺;或
12、boc缬氨酸(2-(叔丁氧基羰基)-氨基-3-甲基丁酸)和h,该实施方案的化合物为:(1-((1-((2r,4r,5r)-3,3-二氟-4-羟基-5-(羟基甲基)氧杂环戊烷-2-基)-2-氧代-1,2-二氢嘧啶-4-基)氨基)-3-甲基-1-氧代丁-2-基)氨基甲酸叔丁酯;或
13、缬氨酸(2-氨基-3-甲基丁酸)和h,该实施方案的化合物为:2-氨基-n-(1-((2r,4r,5r)-3,3-二氟-4-羟基-5-(羟基甲基)氧杂环戊烷-2-基)-2-氧代-1,2-二氢嘧啶-4-基)-3-甲基丁酰胺盐酸盐;或
14、boc缬氨酸和boc缬氨酸,该实施方案的化合物为:(2s)-2-(叔丁氧基羰基)氨基-3-甲基丁酸(2r,3r,5r)-5-(4-(2-((叔丁氧基羰基)氨基)-3-甲基丁酰氨基)-2-氧代-1,2-二氢嘧啶-1-基)-4,4-二氟-2-(羟基甲基)氧杂环戊烷-3-基酯;
15、缬氨酸和缬氨酸,该实施方案的化合物为:(2s)-2-氨基-3-甲基丁酸(2r,3r,5r)-5-(4-(2-氨基-3-甲基丁酰氨基)-2-氧代-1,2-二氢嘧啶-1-基)-4,4-二氟-2-(羟基甲基)氧杂环戊烷-3-基酯二盐酸盐;或
16、boc缬氨酸和异丁酸(2-甲基丙酸),该实施方案的化合物为:异丁酸(2r,3r,5r)-5-(4-(2-((叔丁氧基羰基)氨基)-3-甲基丁酰氨基)-2-氧代-1,2-二氢嘧啶-1-基)-4,4-二氟-2-(羟基甲基)氧杂环戊烷-3-基酯;或
17、缬氨酸和异丁酸,该实施方案的化合物为:异丁酸(2r,3r,5r)-5-(4-(2-氨基-3-甲基丁酰氨基)-2-氧代-1,2-二氢嘧啶-1-基)-4,4-二氟-2-(羟基甲基)氧杂环戊烷-3-基酯盐酸盐;或
18、丙戊酸和异丁酸,该实施方案的化合物为:异丁酸(2r,3r,5r)-4,4-二氟-2-(羟基甲基)-5-(2-氧代-4-(2-丙基戊酰氨基)-1,2-二氢嘧啶-1-基)氧杂环戊烷-3-基酯。
19、在实施方案中,在r3处的前药部分不是h。
20、在进一步的实施方案中,所述化合物由式(ii)表示:
21、
22、和/或名为(2s)-2-氨基-3-甲基丁酸(2r,3r,5r)-4,4-二氟-2-(羟基甲基)-5-(2-氧代-4-(2-丙基戊酰氨基)-1,2-二氢嘧啶-1-基)氧杂环戊烷-3-基酯盐酸盐的化合物。
23、双取代的化合物在室温下具有改善的稳定性。此外,本发明的化合物在2℃至8℃下具有稳定性。与三取代化合物相比,本发明具有基本特征和优点。本发明的化合物足够稳定以用作活性成分,特别是作为制剂中的api,使得能够稳定储存和运输,这是提供商业上合适的药物产品的关键因素。
24、本发明延伸至药物组合物,其包含含有本文公开的化合物的制剂。
25、在实施方案中,所述制剂包含粉末。本发明进一步延伸至包含该制剂的胶囊。
26、本发明的化合物可含有一个或多个不对称碳原子。因此,化合物可以作为非对映异构体、对映异构体或其混合物存在。每个不对称碳原子可以是r或s构型,并且这两种构型都在本发明的范围内。
27、还考虑了任何一种这样的化合物的修饰的化合物,其包括与未修饰的化合物相比具有改善的(例如,增强的、更大的)药物溶解度、稳定性、生物利用度和/或治疗指数的修饰。示例性修饰包括(但不限于)适用的前药衍生物和富含氘的化合物。
28、应当认识到,本发明的化合物可以以盐或溶剂合物的形式存在并任选地施用。本发明包括任何一种上述化合物及其修饰物的任何药学上可接受的盐和溶剂合物。在实施方案中,优选的盐是盐酸盐。
29、此外,在本发明的范围内的是化合物和/或含有一种或多种所述化合物和/或其盐的药物组合物,其用于治疗肿瘤疾病,包括pim过表达的肿瘤疾病,其中包括但不限于白血病、淋巴瘤、多发性骨髓瘤、前列腺癌、胰腺癌、胃癌、结肠癌或肝癌。
30、本发明进一步延伸至所述化合物在制备用于治疗所述疾病的药物中的用途。本发明还涉及治疗pim过表达的肿瘤疾病的方法,所述肿瘤疾病包括但不限于白血病、淋巴瘤、多发性骨髓瘤、前列腺癌、胰腺癌、胃癌、结肠癌或肝癌,所述方法通过向有需要的受试者施用有效量的一种或多种上述化合物、其修饰物和/或盐及其组合物来进行。
31、本发明进一步延伸至制备如式(i)或(ii)或本文公开的任何实施例中提供的本发明化合物的方法,其包括4步方法,所述4步方法包括:
32、在r2位选择性保护吉西他滨的伯醇以产生第一中间体(1);
33、在r1位置处肽偶联中间体1以产生第二中间体(2);
34、在r3位酯化第二中间体(2)以产生第三中间体(3);和
35、优选在室温下将第三中间体(3)脱保护。
36、在实施方案中,可以用甲硅烷基化反应物(tbdmscl)进行伯醇(r2-基团)的保护。此外,可以使用edci.hcl/hobt,优选地在不存在另外的碱的情况下,进行在氨基(r1-基团)上的肽偶联步骤。不存在的另外的碱可以是例如dipea或tea。可以使用edci.hcl/hobt作为偶联剂,任选地使用dmap作为催化剂进行仲醇(r3-基团)上的肽样酯化。最后,可以用4mhcl/二噁烷或accl/etoh进行脱保护步骤。
37、在实施方案中,所述方法还包括分离步骤,并且可以通过使用反溶剂从反应混合物中进行沉淀来进行。优选地,tbme用作反溶剂。
38、本发明的这种所得方法/途径产生了一种新的化合物,出乎意料地使得能够以更少的合成步骤进行这种生产。特别地,至少避免了先前假定和相关联的必要的色谱步骤,即产生现有技术的三取代化合物和相关化合物所需的那些,并且这免除使用大量溶剂和废物(环境改善)。此外,实现了预期的更好的最终api和制剂稳定性以及前药在体内的相同生物脱保护。
39、在下面的说明书中阐述本发明的一个或更多个实施方案的细节。根据说明书和权利要求,本发明的其他特征、目的和优点将是显而易见的。应当理解,除非不适用或明确放弃,否则本文所述的本发明的所有实施方案/特征(化合物、药物组合物、制备/使用方法等),包括实施例和原始权利要求中描述的任何具体特征,可以彼此组合。
本文地址:https://www.jishuxx.com/zhuanli/20241106/325520.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。