金属配体纳米T细胞调节药物及其制备方法和应用
- 国知局
- 2024-07-12 10:35:53
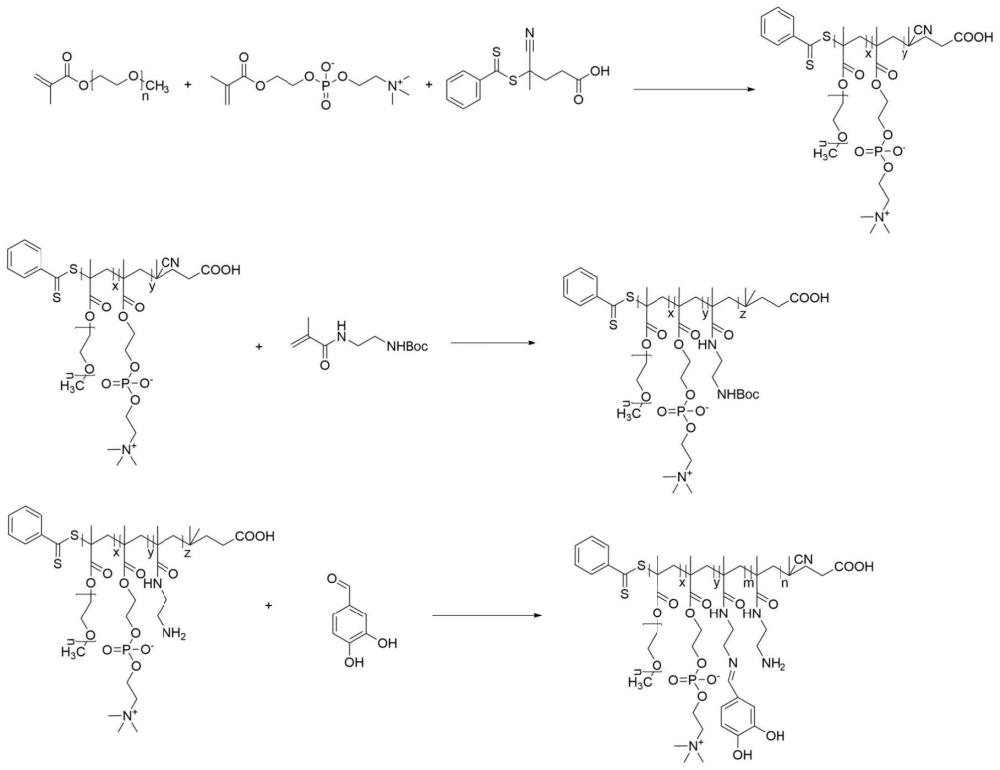
本发明属生物医用材料,具体涉及金属配体纳米t细胞调节药物及其制备方法和应用。
背景技术:
1、免疫是机体识别并清除抗原物质的保护性机制,分为固有免疫和获得性免疫。其中,细胞毒性t细胞(ctls,即激活的cd8 t细胞)作为获得性免疫的中流砥柱,属于免疫调控效应t细胞的类别,由抗原物质经树突状细胞(dc细胞)捕获并修饰整合为短肽抗原经主要组织相容性复合体i类分子(mhc-i)呈递给cd8 t细胞表面受体(tcr)来激活并分化原始cd8t细胞所得,是抵抗肿瘤生成、增殖、转移的最重要的执行性免疫组分。具体而言,细胞毒性t细胞膜表面高度表达cd8蛋白,用于特异性识别有核细胞表面的主要组织相容性复合体i类分子(mhc-i)所呈递的短肽抗原,从而开展特异性杀伤,即经抗原识别后细胞毒性t细胞释放穿孔素和脱粒酶并结合成超分子攻击粒子对靶细胞膜穿孔并递送脱粒酶进细胞内启动靶细胞多通路程序性死亡,与此同时,细胞毒性t细胞还可分泌干扰素-γ(ifn-γ)、白介素-2(il-2)等功能性免疫细胞因子来调控免疫应答,特别是影响自然杀伤细胞(nk细胞)和巨噬细胞的功能。
2、然而,尽管细胞毒性t细胞是抗肿瘤免疫反应中最重要的效应细胞之一,在肿瘤负荷机体中,其杀肿瘤功能却极大地受到肿瘤免疫微环境(tme)中多重免疫抑制途径的损害,包括对ctls的瘤内浸润和功能效价的抑制。据报道,初始的免疫肿瘤微环境存在多种免疫细胞类型,大多数为免疫抑制性细胞,如髓性抑制性细胞、m2型巨噬细胞、调节性t细胞等,这些免疫细胞可协调激活多重信号通路支持肿瘤生长、转移及免疫逃逸。其中,就恶性脑胶质瘤而言,其瘤内约35%的细胞均为免疫抑制性m2型巨噬细胞,该免疫细胞可通过释放il-10、tgf-β等免疫抑制性细胞因子来诱导招募免疫抑制性组分进入免疫微环境,同时抑制cd8 t细胞的激活和浸润,最终支持肿瘤生长与恶性侵袭。与此同时,少量浸润进免疫微环境的t细胞也仅展现出受限的糖酵解活性及功能效价。另外,一些金属离子如镁离子(mg2+)、锰离子(mn2+)、锌离子(zn2+)等都具有直接重塑并增强t细胞毒性的功能,可以大幅提高已浸润效应t细胞的杀肿瘤效价。
3、因此,研究一种针对改善恶性脑胶质瘤的细胞毒性t细胞瘤内浸润并增强其杀肿瘤效价最终全面激发抗肿瘤免疫反应的纳米药物具有极大的价值和临床应用转化潜力。基于此,如何设计并制备具有强效t细胞调控功能的纳米药物来实现免疫抑制微环境的逆转并激活强大的继发性抗肿瘤免疫反应是研发关键。与此同时,该纳米药物应具备肿瘤内高效递送特性,由此保障该纳米粒子的瘤内高效运作并最终抑制肿瘤进程。
4、鉴于此,特提出本发明。
技术实现思路
1、本发明旨在提出金属配体纳米t细胞调节药物的制备方法及其抗肿瘤应用。本发明实施例提供的金属多酚纳米t细胞调节药物通过重塑t细胞肿瘤浸润状态及杀肿瘤活性来改善免疫抑制微环境导致的效应t细胞功能受限,从而充分增强抗肿瘤免疫效应。
2、本发明第一方面的目的,在于提供一种金属配体纳米t细胞调节药物。
3、本发明第二方面的目的,在于提供本发明第一方面的金属配体纳米t细胞调节药物的制备方法。
4、本发明第三方面的目的,在于提供本发明第一方面的金属配体纳米t细胞调节药物的应用。
5、本发明第四方面的目的,在于提供一种产品。
6、为了实现上述目的,本发明所采取的技术方案是:
7、本发明的第一个方面,提供一种金属配体纳米t细胞调节药物,所述金属配体纳米t细胞调节药物包括金属配体网络和负载于所述金属配体网络的巨噬细胞极化药物,其中,所述金属配体网络由修饰有胆碱类似物和多酚的两亲性聚合物与金属离子形成。
8、在本发明一些实施方式中,所述多酚包括邻苯二酚基团。
9、在本发明一些实施方式中,所述胆碱类似物包括2-甲基丙烯酰氧乙基磷酸胆碱。
10、在本发明一些实施方式中,所述聚合物包括聚乙二醇。
11、在本发明一些实施方式中,所述聚合物上修饰的邻苯二酚基团来源于多巴胺结构。
12、在本发明一些实施方式中,所述金属配体网络由修饰有邻苯二酚基团和胆碱类似物的聚乙二醇和金属离子形成,其中,金属离子与胆碱类似物和邻苯二酚基团中的一种或两种共配位。
13、在本发明一些实施方式中,所述胆碱类似物用于血脑屏障穿透。
14、在本发明一些实施方式中,所述金属离子选自镁离子、锰离子和锌离子中的一种或至少两种的组合。
15、通过选择不同的金属离子,功能化的金属配体网络结构通过作用于不同的信号通路增强细胞毒性t细胞功能。例如,当金属离子为镁离子时,金属配体网络响应肿瘤细胞内酸性环境释放镁离子与t细胞受体结合引起白细胞功能相关抗原的构象变化,相继激发下游近端信号通路粘附斑激酶(fak)和远端信号通路细胞外信号调节蛋白激酶1/2(erk1/2),最终增强cd8 t细胞的细胞毒性;当金属离子为锰离子、锌离子时,可以直接活化cd8 t细胞内的cgas-sting通路从而增强其抗肿瘤免疫反应。
16、在本发明一些实施方式中,所述聚合物上修饰的多酚与共价连接的胆碱类似物的摩尔比为1~6:1。例如摩尔比为1:1、2:1、3:1、4:1、5:1以及6:1等1~6:1之间的任意数值以及任意数值之间的两个范围值。
17、在本发明一些优选实施方式中,所述聚合物上修饰的多酚与共价连接的胆碱类似物的摩尔比为1~4:1。
18、在本发明一些更优选实施方式中,所述聚合物上修饰的多酚与共价连接的胆碱类似物的摩尔比为4:1。
19、在本发明一些实施方式中,所述金属离子与所述修饰有胆碱类似物和多酚的两亲性聚合物的质量比为1:2~10。该比例取决于金属类别,例如为1:2、1:3、1:4、1:5、1:6、1:7、1:8、1:9以及1:10等1:2~10之间的任意数值以及任意数值之间的两个范围值。示例的,镁离子与修饰有邻苯二酚并共价偶联胆碱类似物的聚合物的质量比为1:2~10,优选为1:2。
20、在本发明一些实施方式中,所述巨噬细胞极化药物选自β位点淀粉样蛋白前体蛋白裂解酶1抑制剂、toll样受体激动剂、sting激动剂的至少一种。
21、在本发明一些实施方式中,所述巨噬细胞极化药物选自维罗司他(mk8931)、imidazoquinoline(咪唑喹啉)、瑞喹莫德(resiquimod)和循环二核苷酸(cyclicdinucleotides)中的至少一种。
22、在本发明一些实施方式中,所述金属配体网络与巨噬细胞极化药物的质量比为5~30:3。例如5:3、10:3、20:3以及30:3等5~30:3之间的任意数值以及任意数值之间的两个范围值。
23、在本发明一些优选实施方式中,所述金属配体网络与巨噬细胞极化药物的质量比为10~30:3。
24、在本发明一些更优选实施方式中,所述金属配体网络与巨噬细胞极化药物的质量比为20:3。
25、在本发明一些实施方式中,所述金属配体纳米t细胞调节药物的直径为50~70nm。
26、在本发明一些实施方式中,所述金属配体纳米t细胞调节药物的水合粒径为60~90nm。
27、本发明提供的金属配体纳米t细胞调节药物可以通过静脉给药从两个维度调控t细胞功能,用于恶性脑胶质瘤治疗。具体地,金属配体纳米t细胞调节药物由表面修饰的胆碱类似物mpc介导主动靶向穿过血脑屏障到达恶性脑胶质瘤病灶部位,在酸性肿瘤环境中响应性降解,释放巨噬细胞极化剂诱导生成大量的m1型巨噬细胞用于肿瘤细胞吞噬和免疫炎性因子生成,从而激活并促进cd8 t细胞的肿瘤局部浸润;同时,释放的金属离子作用于浸润性细胞毒性t细胞的表面受体通过激活其下游信号通路重塑t细胞的细胞毒性,增强抗肿瘤免疫效果。
28、本发明的第二个方面,提供本发明第一方面的金属配体纳米t细胞调节药物的制备方法,包括以下步骤:将修饰有胆碱类似物和多酚的两亲性聚合物与巨噬细胞极化药物共混,再与金属离子混合,超声,即得到金属配体纳米t细胞调节药物。
29、在本发明一些实施方式中,所述超声的条件为40~60hz超声15~30分钟。
30、在本发明一些优选实施方式中,所述超声的条件为40~50hz超声15~20分钟。
31、在本发明一些实施方式中,所述制备方法包括将巨噬细胞极化药物与修饰有胆碱类似物和多酚的两亲性聚合物分别溶于甲醇溶液,混合后一并加入金属盐溶液进行超声自组装处理。具体来说,将巨噬细胞极化药物与修饰有胆碱类似物和多酚的两亲性聚合物分别溶于甲醇溶液中,随后按比例混合,在超声(50hz,35%强度)下加入金属盐溶液后持续超声20分钟,旋蒸移除甲醇有机溶剂初步得到金属配体纳米t细胞调节药物混合溶液,之后通过超滤及冷冻干燥进行程序性纯化和浓缩,-80℃冰箱保存待用。
32、本发明的第三个方面,提供本发明第一方面的金属配体纳米t细胞调节药物在(1)~(10)中任一种中的应用:
33、(1)制备抗肿瘤药物;
34、(2)促进巨噬细胞向m1型极化;
35、(3)制备促进巨噬细胞向m1型极化的产品;
36、(4)增强巨噬细胞的吞噬作用;
37、(5)制备增强巨噬细胞的吞噬作用的产品;
38、(6)制备促进t细胞浸润的产品;
39、(7)增强t细胞对肿瘤细胞的杀伤力;
40、(8)制备增强t细胞对肿瘤细胞的杀伤力的产品;
41、(9)提高ctls对癌细胞的细胞毒性;
42、(10)制备提高ctls对癌细胞的细胞毒性的产品。
43、在本发明一些实施方式中,所述产品包括试剂和药物。
44、在本发明一些实施方式中,所述试剂包括体外试剂。
45、本发明的第四个方面,提供一种产品,包括本发明第一方面的金属配体纳米t细胞调节药物。
46、在本发明一些实施方式中,所述产品具有以下任一项的功能:
47、(a)抑制肿瘤;
48、(b)促进巨噬细胞向m1型极化;
49、(c)增强巨噬细胞的吞噬作用;
50、(d)促进t细胞浸润;
51、(e)增强t细胞对肿瘤细胞的杀伤力;
52、(f)提高ctls对癌细胞的细胞毒性。
53、在本发明一些实施方式中,所述产品包括试剂和药物。
54、在本发明一些实施方式中,所述产品还包括药学上可接受的辅料。
55、在本发明一些实施方式中,所述药学可接受的辅料包括填充剂、崩解剂、稀释剂、润滑剂、粘合剂、湿润剂、矫味剂、助悬剂、溶剂、缓释剂、乳化剂、吸收促进剂、表面活性剂、防腐剂、色素、香精和溶剂中的至少一种。
56、在本发明一些实施方式中,所述填充剂选自淀粉、蔗糖、乳糖、甘露醇、山梨醇、木糖醇、微晶纤维素或葡萄糖等;所述粘合剂选自纤维素衍生物、藻酸盐、淀粉、水、糊精、明胶或聚乙烯吡咯烷酮等;所述崩解剂选自微晶纤维素、羚甲基淀粉钠、交联聚乙烯吡咯烷酮、低取代羟丙基纤维素或交联羚甲基纤维素钠;所述润滑剂选自硬脂酸、聚乙二醇、碳酸钙、碳酸氢钠、微粉硅胶、滑石粉或硬脂酸镁:所述助悬剂选自微粉硅胶、蜂蜡、纤维素、固态聚乙二醇:所述润湿剂选自甘油、吐温-80、氢化蓖麻油或卵磷脂:所述溶剂选自乙醇、液态聚乙二醇、异丙醇、吐温-80、甘油、丙二醇或植物油,所述植物油选自大豆油、蓖麻油、花生油、调和油等:所述表面活性剂选自十二烷基苯磺酸钠、硬脂酸、聚氧乙烯-聚氧丙烯共聚物、脂肪酸山梨坦或聚山梨(吐温)等:所述矫味剂选自阿斯巴甜、蔗糖素、香精、甜菊素、安赛蜜、柠檬酸或糖精钠;所述防腐剂选自对羟苯甲酸甲酯或对羟苯甲酸丙酯中的至少一种。
57、本发明的有益效果是:
58、本发明提供的金属配体纳米t细胞调节药物经胆碱类似物2-甲基丙烯酰氧乙基磷酸胆碱(mpc)介导的血脑屏障穿透作用后到达恶性脑胶质瘤病灶部位,在酸性肿瘤微环境中响应性降解,释放功能性金属离子及巨噬细胞极化剂,m1型巨噬细胞的生成一方面识别并吞噬肿瘤细胞,产生免疫炎性因子并呈递相关抗原激活幼稚cd8 t细胞并促进其向肿瘤局部区域浸润;另一方面,金属离子作用于浸润性细胞毒性t细胞的表明受体通过激活其下游代谢通路重塑t细胞的细胞毒性,增强抗肿瘤免疫效果。不同于已发表的作用于肿瘤细胞的金属多酚药物(如中国发明专利cn116672449a),本发明提供的金属配体纳米t细胞调节药物主要以脑瘤局部数量稀少且功能失调的t细胞为治疗切入点,经特定材料设计直接引入靶向穿透血脑屏障的性能,并在脑瘤局部通过巨噬细胞极化药物及金属离子免疫佐剂的协同作用响应性促进cd8 t细胞浸润并增强其肿瘤杀伤作用;其中,该纳米t细胞调节药物突出强调了t细胞浸润数量及肿瘤杀伤质量在脑瘤治疗中同等重要,且金属离子如镁离子是首次作为免疫佐剂用于纳米药物介导的脑瘤t细胞调节治疗;同时,经验证该金属配体纳米t细胞调节药物具有安全可靠、性能优良的特点。由此,这种针对脑瘤内部t细胞数量及质量调控的金属配体纳米药物为改善抑制性恶性脑胶质瘤免疫微环境,增强胶质瘤疗效提供了一种新方法。
59、本发明提供的制备方法利用疏水作用和金属配位作用原理进行分子自组装,操作简单、稳定可靠,通过一步合成法快速制备金属配体纳米t细胞调节药物。
本文地址:https://www.jishuxx.com/zhuanli/20240614/87930.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表