不对称双分支Lacto-N-neo-hexaose(LNnH)人乳寡糖链的合成方法
- 国知局
- 2024-06-20 10:27:56
本发明涉及糖类物质的合成,具体涉及不对称双分支lacto-n-neo-hexaose(lnnh)人乳寡糖链的合成方法。
背景技术:
1、研究发现,人乳与其它动物的母乳有很大不同,其中最大的不同之一在于人乳中的寡糖即人乳寡糖(human milk oligosaccharides,hmos),作为继乳糖和脂质的第三大营养成分,不仅种类多,且含量高。特别是在分娩后的初乳中,有着牛乳所无法比拟的寡糖含量,可达20g/l。
2、通过色谱法和质谱法,已在母乳中鉴定出超过200种hmos结构。hmos总体可以分为两类:以galβ1-3glcnac构型的重复二糖单元连接到乳糖上的ⅰ型结构和以galβ1-4glcnac构型的重复二糖单元连接到乳糖上的ⅱ型结构。除可以形成单分支hmos外,还可以形成双分支、三分支、四分支等更复杂的核心结构;在乳糖或者延伸链所形成的核心结构上可以进行更加复杂的岩藻糖基化和唾液酸化修饰。这些结构复杂的hmos由五个核心组成:半乳糖、葡萄糖、n-乙酰氨基葡萄糖、岩藻糖和n-乙酰神经氨酸。
3、lnnh(lacto-n-neo-hexaose)是支链hmos的核心单元之一,其还原端半乳糖的3位和6位分别含有一个n-乙酰-d-乳糖胺(lacnac,galβ1-4glcnac)单元。它们可以分别被岩藻糖基化和/或唾液酸化修饰,形成丰富的不对称双分支hmos结构。此外,它还可以进一步延伸和/或继续引入分支形成其他核心单元,如lnno(lacto-n-neo-octaose)等。
4、但对于lnnh的制备,面临着β1,6-糖苷键的引入和分支的不对称性修饰等多重困难,lnnh和其岩藻糖基化和/或唾液酸化的糖链结构尚未被大量合成研究。代谢工程促进了少数简单hmos的高效生物合成,但对于目前大多数复杂的lnnh相关糖链的形成仍无法实现。广泛的化学合成策略,如汇聚式合成、固相合成和一锅合成等,已被开发用于制备分支hmos。然而,这些化学方法需要多步合成和纯化过程,试剂和溶剂消耗高,收率损失大,导致生产成本高,总收率低。
技术实现思路
1、为了克服上述问题,本发明提供了不对称双分支lacto-n-neo-hexaose(lnnh)人乳寡糖链的合成方法。本发明中利用化学法高效制备了式(i)所示的分支对称的四糖,式(i)所示的分支对称的四糖在酶法组装模块一的催化下分别合成式(ii)所示的分支不对称的五糖和式(iii)所示的分支对称的六糖;式(ii)所示的分支不对称的五糖在酶法组装模块二的催化下合成式(iv)所示的分支不对称的六糖,式(iv)所示的分支不对称的六糖在酶法组装模块一的催化下合成式(vi)所示的分支不对称的七糖;式(iii)所示的分支对称的六糖在酶法组装模块三的催化下合成式(v)所示的分支对称的八糖。
2、
3、本发明所采用的不同的酶法组装模块中,含有糖激酶和/或糖核苷生成酶和糖基转移酶,并且均发挥各自重要的催化作用,而且酶之间协同作用,构成一个有机的酶反应体系,前一种酶的催化效果会直接影响后一种酶的作用效果。本发明在试验过程中对上述酶均进行了多次的优化和筛选,结果发现:escherichia coli galactokinase(galk),bifidobacterium longum udp-sugar pyrophosphorylase(blusp)和neisseriameningitidesβ1,4-galactosyltransferase(nmlgtb);bacteroides fragilisbifunctional l-fucokinase/gdp-fucose pyrophosphorylase(fkp)和helicobacterpyloriα1,3-fucosyltransferase(hpα1,3fuct);neisseria meningitides cmp-sialicacid synthetase(nmcss)和photobacterium damselaeα2,6-sialyltransferase(pd2,6st)作为本发明的酶法模块所采用的酶,其催化效果最为优异,,特别适用于分支人乳寡糖的酶催化合成,合成效率高。而且上述酶均为细菌来源,均可在常规的大肠杆菌表达系统中方便的表达纯化。
4、本发明的第一方面,提供不对称双分支lacto-n-neo-hexaose(lnnh)人乳寡糖链的合成方法,包括:
5、以式(i)所示的分支对称的四糖为糖基受体,以半乳糖为糖基供体,经酶法组装模块一催化反应生成式(ii)所示的分支不对称的五糖和式(iii)所示的分支对称六糖;以式(iv)所示的分支不对称的六糖为糖基受体,以半乳糖为糖基供体,经酶法组装模块一催化反应生成式(vi)所示的分支不对称的七糖;
6、以式(ii)所示的分支不对称的五糖为糖基受体,以岩藻糖为糖基供体,经酶法组装模块二催化反应生成式(iv)所示的分支不对称的六糖;
7、以式(iii)所示的分支对称的六糖为糖基受体,以唾液酸为糖基供体,经酶法组装模块三催化反应生成式(v)所示的分支对称的八糖;
8、式(i)~式(vi)所示的化合物的结构式为:
9、
10、式(i)~式(vi)所示的化合物中r1为羟基、叠氮取代烷基、炔基取代烷基、巯基取代烷基、α-或β-构型取代烷基、α-或β-构型丝氨酸残基、α-或β-构型苏氨酸残基。
11、本发明的有益效果在于:
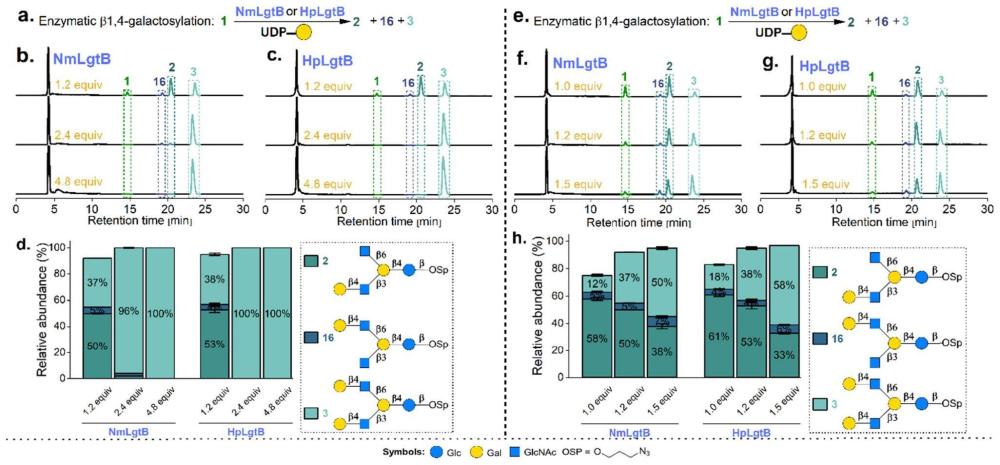
12、(1)糖链合成中广泛应用的两种细菌来源的β1,4-半乳糖基转移酶,包括neisseria meningitidis来源的nmlgtb和helicobacter pylori来源的hplgtb,均可在大肠杆菌体系中高水平表达,具有显著的催化活性。本发明通过运用这两种细菌来源的β1,,4半乳糖基转移酶实现了对称分支人乳四糖式(i)的区域选择性半乳糖基化,成功制备了不对称分支五糖式(ii),为后续lnnh分支糖链的不对称修饰提供了可能。通过酶的表达量和反应中催化效率的筛选,最终选用nmlgtb构建酶法组装模块。为了合成不对称分支lnnh相关人乳寡糖,需要设计多个酶法组装模块。酶法模块设计时,首先需要对设计的目标糖链中单糖的组成、顺序以及糖苷键构型进行分析,确定合成所需要的关键酶;然后对关键酶进行优化筛选,根据酶的催化活性、酶对底物的区域选择性、空间选择性等角度进行考察,分别建立了针对五糖、六糖、七糖和八糖合成的不同的酶法组装模块,实现了不对称分支lnnh相关人乳寡糖抗原的高效、快速合成。
13、(2)本发明通过酶法模块化组装策略,巧妙地结合了细菌来源的糖核苷生成酶和糖基转移酶,实现了具有重要生物学活性的不对称分支lnnh相关人乳寡糖的合成。本发明所利用的糖基转移酶、糖核苷生成酶以及糖激酶均为原核生物来源,具有蛋白表达量高、底物适应性广泛、催化效率高等优点,因而以其为基础的酶法模块化组装效率高,且适于大量制备;利用糖核苷酸生成酶可以从价廉、易得的单糖出发高效的转化为昂贵的核苷活化的糖基供体,大大降低了生产成本;相对于步骤繁琐、产率较低的化学合成法,酶法合成在空间和立体化学特异性方面具有明显的优势,大大简化了反应步骤,提高反应的总体收率。
本文地址:https://www.jishuxx.com/zhuanli/20240619/57.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。