抗CLDN18.2的纳米抗体、嵌合抗原受体及其应用的制作方法
- 国知局
- 2024-06-20 10:59:22
本公开涉及生物医药,具体地,本发明涉及特异性结合cldn18.2的纳米抗体或其抗原结合片段、基于特异性结合cldn18.2的纳米抗体或其抗原结合片段的嵌合抗原受体以及上述相关的应用。
背景技术:
1、claudin18.2(cldn18.2)是紧密连接蛋白家族成员claudin18的剪切变体2。cldn18.2是一种高选择性标志物蛋白,其只在分化的胃黏膜上皮细胞中表达,在正常健康组织中表达非常有限,且在未分化的胃干细胞中不表达。研究表明,cldn18.2在多种肿瘤,例如胃癌、胃食管癌、乳腺癌、结肠癌、肝癌、头颈癌、支气管癌、非小细胞肺癌、胰腺癌、食道癌、卵巢癌等的发生和发展中表达异常。这使得cldn18.2成为了肿瘤靶向免疫疗法领域令人关注的标志物。已有临床研究覆盖靶向cldn18.2的单克隆抗体、双特异性抗体、其衍生的嵌合抗原受体-t(car-t)和抗体药物缀合物(adc)。与传统抗体相比,纳米抗体具有尺寸小、稳定性高、易通过微生物系统生产、易改性、人源化简单、可以到达更多作用位点等优势,目前还存在开发抗cldn18.2纳米抗体的需求。
2、claudin18的剪切变体1,claudin 18.1(cldn18.1),与cldn18.2结构相似,仅在细胞外结构域ecl1序列上有7个氨基酸残基的差异。要开发特异性靶向cldn18.2而不靶向cldn18.1的抗体成为了一个难点。
3、近些年来,免疫学领域中对于转化医学的研究越来越多,尤其是肿瘤免疫。肿瘤免疫治疗中应用较为广泛的是car-t细胞免疫治疗策略。在90年代早期,这种免疫治疗策略在转化医学中就获得了较好的效果。正常机体内的t细胞被有效刺激并发挥免疫学功能需要多重信号的调控,主要包括t细胞受体与mhc-抗原肽复合物的识别作为第一信号、t细胞表面的共刺激分子识别活化作为第二信号,甚至还需要细胞因子参与形成第三信号。这种嵌合抗原受体主要是将t细胞刺激和活化的过程所需的蛋白分子进行人工串联整合,从而促进t细胞的活化和特异性杀伤。car-t细胞的特异性杀伤主要依赖于前端的抗体分子部分的识别和结合。目前使用较为广泛的是基于人或其它种属的单克隆抗体单链可变区(singlechain fv,scfv)对靶蛋白的特异性识别。但存在如下缺陷:在scfv与纳米抗体亲和力相当的基础上,scfv相对于纳米抗体而言分子量较大,在分子表达和功能发挥上均存在一定的局限性;scfv由其亲本单克隆抗体衍生而来,在活性和稳定性等方面都可能存在一定的不足。
4、鉴于此,有必要提供新型有效的抗cldn18.2的纳米抗体,以及新的嵌合抗原受体和/或融合蛋白,以解决现有技术存在的不足。
技术实现思路
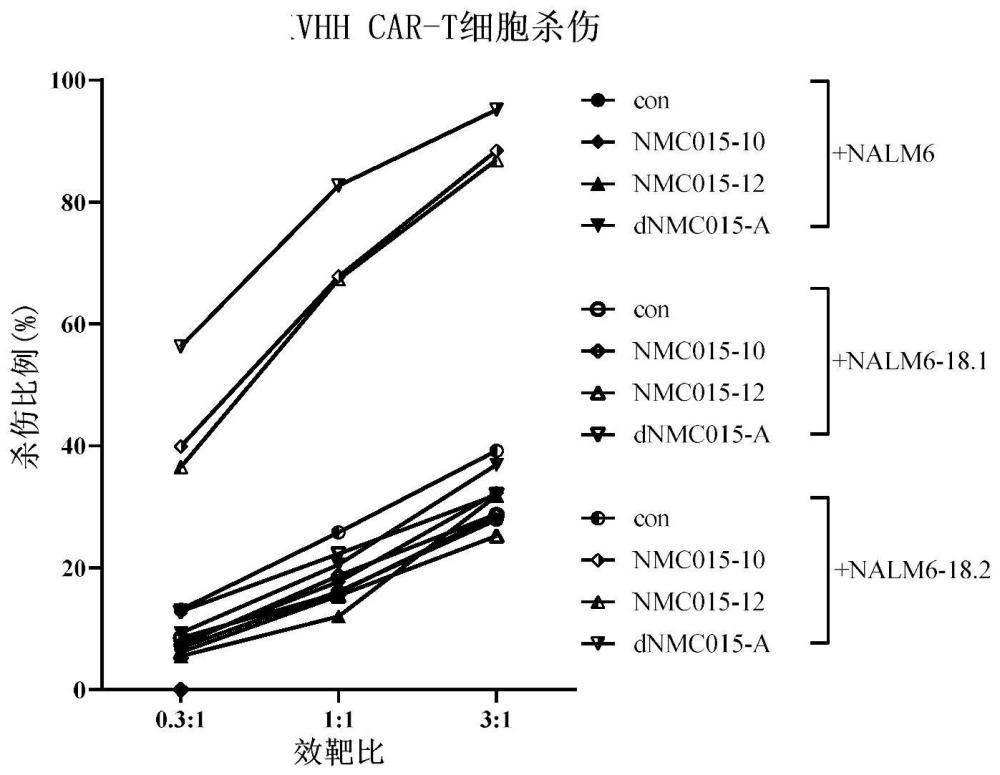
1、为了解决上述技术问题,本公开提供了新型且特异性结合cldn18.2的单和双纳米抗体。本公开还提供了基于纳米抗体的嵌合抗原受体以及嵌合抗原受体免疫细胞。本公开提供的单和双纳米抗体car-t细胞对cldn18.2表达阳性的细胞系产生了特异性的杀伤。
2、在一个方面,本公开提供了特异性结合cldn18.2的纳米抗体或其抗原结合片段,所述纳米抗体或其抗原结合片段包含以下(a)-(c)中至少一项:
3、(a)vhh10,所述vhh10包含cdr1、cdr2、cdr3,所述cdr1-3的氨基酸序列分别如seqid no:1、seq id no:2、seq id no:3所示或分别为与seq id no:1、seq id no:2、seq idno:3具有至少75%同一性的氨基酸序列;
4、(b)vhh12,所述vhh12包含cdr1、cdr2、cdr3,所述cdr1-3的氨基酸序列分别如seqid no:4、seq id no:5、seq id no:6所示或分别为与seq id no:4、seq id no:5、seq idno:6具有至少75%同一性的氨基酸序列;
5、(c)所述vhh10和vhh12。
6、在一个方面,本公开提供了特异性结合cldn18.2的纳米抗体或其抗原结合片段,所述纳米抗体或其抗原结合片段包含以下(a)-(c)中至少一项:
7、(a)vhh10,所述vhh10包含cdr1、cdr2、cdr3,所述cdr1-3的氨基酸序列分别如seqid no:1、seq id no:2、seq id no:3所示或分别为具有1、2、3或4个保守取代的seq id no:1、具有1、2、3或4个保守取代的seq id no:2、具有1、2、3或4个保守取代的seq id no:3;
8、(b)vhh12,所述vhh12包含cdr1、cdr2、cdr3,所述cdr1-3的氨基酸序列分别如seqid no:4、seq id no:5、seq id no:6所示或分别为具有1、2、3或4个保守取代的seq id no:4、具有1、2、3或4个保守取代的seq id no:5、具有1、2、3或4个保守取代的seq id no:6;
9、(c)所述vhh10和vhh12。
10、在一个方面,本公开提供了特异性结合cldn18.2的纳米抗体或其抗原结合片段所述纳米抗体或其抗原结合片段包含以下(a)-(c)中至少一项:
11、(a)vhh10,所述vhh10的重链可变区的氨基酸序列如seq id no:13所示或为与seqid no:13具有至少75%同一性的氨基酸序列;
12、(b)vhh12,所述vhh12的重链可变区的氨基酸序列如seq id no:14所示或为与seqid no:14具有至少75%同一性的氨基酸序列;
13、(c)所述vhh10和vhh12。
14、在另一个方面,本公开提供了基于特异性结合cldn18.2的纳米抗体或其抗原结合片段的嵌合抗原受体(car),所述嵌合抗原受体至少包含本文公开的纳米抗体或其抗原结合片段,优选地,所述嵌合抗原受体进一步包含以下的一项或多项:信号肽、铰链区、跨膜结构域、共刺激信号结构域、胞内信号传导结构域、自剪切肽、检测用标签、检测用标签信号肽;
15、优选地,所述信号肽包括下列分子的信号肽:t细胞受体的α链及β链、cd3ζ、cd3ε、cd4、cd5、cd8、cd9、cd28、cd16、cd22、cd64、cd80、cd86、cd134、cd137、cd154、gitr、icos、igg6;
16、优选地,所述铰链区包括下列分子的铰链区:cd8、cd28、igg1、igg4、4-1bb、pd-1、cd34、ox40、cd3ε、il-2受体、il-7受体、il-11受体;
17、优选地,所述跨膜结构域包括下列分子的跨膜结构域:cd8、cd28、igg1、igg4、4-1bb、pd-1、cd34、cd3ε、cd8α、il-2受体、il-7受体、il-11受体;
18、优选地,所述共刺激信号结构域包括下列分子的共刺激信号结构域:4-1bb、cd28、icos、cd27、cd19、cd4、cd8α、cd8β、hvem、light、cd40、ox40、dr3、gitr、cd30、tim1、cd2、cd226、cd278;
19、优选地,所述胞内信号传导结构域包括下列分子的胞内信号传导结构域:cd3ζ、fcrγ、fcrβ、cd3γ、cd3δ、cd3ε、tcrζ、cd4、cd5、cd8、cd21、cd22、cd79a、cd79b、cd278、fcεri、dap10、dap12、cd66d、fyn;
20、优选地,所述自剪切肽选自p2a、t2a、e2a、f2a;
21、优选地,所述检测用标签为tegfr;
22、优选地,所述检测用标签信号肽为tegfr信号肽;
23、最优选地,所述嵌合抗原受体为信号肽、本文公开的纳米抗体或其抗原结合片段、cd8铰链区、cd8跨膜结构域、4-1bb共刺激信号结构域、cd3ζ胞内信号传导结构域、t2a、tegfr信号肽、tegfr依次串联得到;
24、最优选地,所述cd8铰链区的氨基酸序列如seq id no:22所示或与seq id no:22具有至少75%的序列同一性;
25、最优选地,所述cd8跨膜结构域的氨基酸序列如seq id no:24所示或与seq idno:24具有至少75%的序列同一性;
26、最优选地,所述4-1bb共刺激信号结构域的氨基酸序列如seq id no:26所示或与seq id no:26具有至少75%的序列同一性;
27、最优选地,所述cd3ζ胞内信号传导结构域的氨基酸序列如seq id no:28所示或与seq id no:28具有至少75%的序列同一性;
28、最优选地,所述信号肽的氨基酸序列如seq id no:18所示或与seq id no:18具有至少75%的序列同一性;
29、最优选地,所述t2a的氨基酸序列如seq id no:30所示或与seq id no:30具有至少75%的序列同一性;
30、最优选地,所述tegfr信号肽的氨基酸序列如seq id no:18所示或与seq id no:18具有至少75%的序列同一性;
31、最优选地,所述tegfr的氨基酸序列如seq id no:32所示或与seq id no:32具有至少75%的序列同一性。
32、在另一个方面,本公开提供了编码本文公开的纳米抗体或其抗原结合片段、或本文公开的嵌合抗原受体的分离的核酸。
33、在一个方面,本公开提供了编码本文公开的纳米抗体或其抗原结合片段的分离的核酸,所述分离的核酸包含编码本文公开的vhh10的cdr1、cdr2、cdr3的核苷酸序列和/或编码本文公开的vhh12的cdr1、cdr2、cdr3的核苷酸序列,
34、优选地,编码所述vhh10的cdr1、cdr2、cdr3的核苷酸序列分别如seq id no:7、seqid no:8、seq id no:9所示或分别为与seq id no:7、seq id no:8、seq id no:9具有至少75%同一性的核苷酸序列;编码所述vhh12的cdr1、cdr2、cdr3的核苷酸序列分别如seq idno:10、seq id no:11、seq id no:12所示或分别为与seq id no:10、seq id no:11、seq idno:12具有至少75%同一性的核苷酸序列。
35、在一个方面,本公开提供了编码本文公开的纳米抗体或其抗原结合片段的分离的核酸,所述分离的核酸包含编码本文公开的vhh10的重链可变区的核苷酸序列和/或编码本文公开的vhh12的重链可变区的核苷酸序列,
36、优选地,编码所述vhh10的重链可变区的核苷酸序列如seq id no:15所示或为与seq id no:15具有至少75%同一性的核苷酸序列;编码所述vhh12的重链可变区的核苷酸序列如seq id no:16所示或为与seq id no:16具有至少75%同一性的核苷酸序列。
37、在一个方面,本公开提供了编码本文公开的嵌合抗原受体的分离的核酸,所述编码嵌合抗原受体的分离的核酸至少包含本文公开的编码纳米抗体或其抗原结合片段的分离的核酸,优选地,所述编码嵌合抗原受体的分离的核酸进一步包含以下的一项或多项:启动子核苷酸序列、信号肽编码序列、铰链区编码序列、跨膜结构域编码序列、共刺激结构域编码序列、胞内信号传导结构域编码序列、自剪切肽编码序列、检测用标签信号肽的编码序列、检测用标签编码序列;
38、优选地,所述启动子核苷酸序列为如seq id no:17所示的ef1α启动子序列;
39、优选地,所述信号肽编码序列为seq id no:19所示的信号肽编码序列;
40、优选地,所述铰链区编码序列为如seq id no:23所示的cd8α铰链区编码序列;
41、优选地,所述跨膜结构域编码序列为如seq id no:25所示的cd8α跨膜结构域编码序列;
42、优选地,所述共刺激结构域编码序列为如seq id no:27所示的4-1bb共刺激结构域编码序列;
43、优选地,所述胞内信号传导结构域编码序列为如seq id no:29所示的cd3ζ信号传导结构域编码序列;
44、优选地,所述自剪切肽编码序列为如seq id no:31所示的t2a编码序列;
45、优选地,所述检测用标签信号肽的编码序列为如seq id no:34所示的tegfr信号肽编码序列;
46、优选地,所述检测用标签编码序列为如seq id no:33所示的tegfr编码序列;
47、更优选地,所述编码嵌合抗原受体的分离的核酸为启动子核苷酸序列、信号肽编码序列、编码纳米抗体或其抗原结合片段的分离的核酸、铰链区编码序列、跨膜结构域编码序列、共刺激结构域编码序列、胞内信号传导结构域编码序列、自剪切肽编码序列、检测用标签信号肽的编码序列、检测用标签编码序列依次串联得到。
48、在一个方面,本公开提供了分离的多核苷酸,所述分离的多核苷酸的序列为本文公开的编码嵌合抗原受体的分离的核酸序列、或其互补序列。
49、在又一个方面,本公开提供了载体,所述载体包含本文公开的分离的核酸或分离的多核苷酸。在一个实施方式中,所述载体包括克隆载体、表达载体。优选地,所述载体包括dna载体、rna载体、质粒、转座子载体、crispr/cas9载体、病毒来源的载体,更优选地,所述病毒来源的载体包括慢病毒载体、逆转录病毒载体、腺病毒载体、腺相关病毒载体、痘病毒载体、疱疹病毒载体。
50、在又另一个方面,本公开提供了工程改造的宿主细胞,所述经工程改造的宿主细胞表达含有本文提供的分离的核酸、本文提供的分离的多核苷酸或本文提供的载体。在一个实施方式中,所述宿主细胞包括真核细胞、原核细胞。在一个实施方式中,所述宿主细胞为包括t细胞、b细胞、nk细胞、inkt细胞、ctl细胞、树突状细胞、髓样细胞、单核细胞、巨噬细胞或其任意组合的免疫细胞。在一个优选的实施方式中,所述宿主细胞为t细胞。
51、在又另一个方面,本公开提供了衍生物,所述衍生物包括可检测标记的本文公开的嵌合抗原受体、分离的核酸、或分离的多核苷酸,赋予抗生素抗性的本文公开的嵌合抗原受体、分离的核酸、或分离的多核苷酸,与治疗剂偶联或缀合的本文公开的嵌合抗原受体、分离的核酸、或分离的多核苷酸。在一个实施方式中,所述可检测标记包括荧光染料、化学发光标记物、胶体金、化学发光催化剂。在一个实施方式中,所述化学发光标记物包括鲁米诺及其衍生物、吖啶酯或其衍生物、金刚烷、异鲁米诺及其衍生物、稀土元素、联吡啶钌配合物;所述化学发光催化剂包括辣根过氧化物酶、碱性磷酸酶。在一个实施方式中,所述抗生素抗性的基因包括青霉素抗性基因、四环素抗性基因、氯霉素抗性基因、卡那霉素抗性基因。在一个实施方式中,所述治疗剂包括放射性核素、细胞因子、金纳米颗粒、病毒颗粒、脂质体、纳米磁粒、前药激活酶、化疗剂。在一个实施方式中,所述细胞因子包括il-2、il-3、il-4、il-5、il-6、il-9、il-10、il-12、il-13、il-14、ifn-γ、tnf-β、tnf-α、g-csf、m-csf;所述化疗剂包括顺铂、紫杉醇、长春新碱、门冬酰胺酶、奥沙利铂、草酸铂、乐沙定。
52、在一个方面,本公开提供了纳米抗体-药物偶联物或缀合物或组合物,所述纳米抗体-药物偶联物或缀合物或组合物包含本文公开的纳米抗体或其抗原结合片段和治疗剂。
53、在又一个方面,本公开提供了药物组合物,所述药物组合物包含本文公开的纳米抗体或其抗原结合片段、嵌合抗原受体、分离的核酸、分离的多核苷酸、载体、宿主细胞或、衍生物或纳米抗体-药物偶联物或缀合物或组合物,以及药学上可接受的载体。
54、在一个方面,本公开提供了用于检测cldn18.2蛋白的检测产品,所述检测产品包含本公开提供的纳米抗体或其抗原结合片段。
55、在另一个方面,本公开提供了试剂盒,所述试剂盒包含本文公开的分离的核酸、分离的多核苷酸或载体。在一个实施方式中,所述试剂盒还包括将所述分离的核酸、分离的多核苷酸或载体引入到宿主细胞中的试剂。在一个实施方式中,所述试剂盒还包括将所述分离的核酸、分离的多核苷酸或载体引入到宿主细胞中的说明书。
56、在又另一个方面,本公开提供了如下任一种方法,所述方法包括:
57、(a)制备本文公开的经工程改造的宿主细胞的方法,所述方法包括如下步骤:将本文提供的分离的核酸、分离的多核苷酸或载体引入到宿主细胞中;优选地,所述引入的方法包括脂质转染法、微注射、电穿孔、dna载体、rna载体、逆转录病毒载体、慢病毒载体、痘病毒载体、单纯疱疹病毒载体、腺病毒载体、腺相关病毒载体;
58、(b)刺激受试者靶细胞群或组织产生免疫应答的方法,所述方法包括如下步骤:给受试者施用本文公开的经工程改造的宿主细胞;
59、(c)生产本文公开的纳米抗体或其抗原结合片段的方法,所述方法包括如下步骤:培养本文公开的经工程改造的宿主细胞,从培养物中分离出本文公开的纳米抗体或其抗原结合片段;
60、(d)非诊断和非治疗目的地检测待测样品中cldn18.2的方法,所述方法包括如下步骤:将待测样品与本文公开的纳米抗体或其抗原结合片段接触,检测所述纳米抗体或其抗原结合片段与cldn18.2的复合物的形成;
61、优选地,所述纳米抗体或其抗原结合片段是被可用于检测的标记物标记的纳米抗体或其抗原结合片段;
62、更优选地,所述可用于检测的标记物包括荧光色素、亲和素、顺磁原子、放射性同位素;
63、最优选地,所述荧光色素为荧光素、罗丹明、texas红、藻红蛋白、藻蓝蛋白、别藻蓝蛋白、多甲藻黄素-叶绿素蛋白;
64、最优选地,所述亲和素为生物素、卵白亲和素、链亲和素、卵黄亲和素、类亲和素;
65、最优选地,所述放射性同位素为放射性碘、放射性铯、放射性铱、放射性钴;
66、(e)用于预防或治疗与cldn18.2表达异常相关疾病的方法,所述方法包括向有需要的受试者施用治疗有效量的本文公开的嵌合抗原受体、分离的核酸、分离的多核苷酸、载体、宿主细胞、衍生物、纳米抗体-药物偶联物或缀合物或组合物或药物组合物;
67、优选地,其中所述与cldn18.2表达异常相关疾病包括实体瘤,优选胃癌、胃食管癌、乳腺癌、结肠癌、肝癌、头颈癌、支气管癌、非小细胞肺癌、胰腺癌、食道癌、卵巢癌。
68、在另一个方面,本文公开了如下任一方面的应用,所述应用包括:
69、(a)本文公开的纳米抗体或其抗原结合片段在制备用于检测cldn18.2蛋白的检测产品中的应用;
70、(b)本文公开的纳米抗体或其抗原结合片段、嵌合抗原受体、分离的核酸、分离的多核苷酸、载体、经工程改造的宿主细胞、衍生物、纳米抗体-药物偶联物或缀合物或组合物、或药物组合物在制备用于预防或治疗与cldn18.2表达异常相关疾病的药物中的应用;
71、(c)本文公开的嵌合抗原受体、分离的核酸、分离的多核苷酸、载体、经工程改造的宿主细胞、衍生物在制备用于制备预防或治疗与cldn18.2表达异常相关疾病的免疫细胞的试剂盒中的应用;
72、(d)本文公开的试剂盒在制备用于预防或治疗与cldn18.2表达异常相关疾病的免疫细胞中的应用;
73、优选地,所述与cldn18.2表达异常相关疾病包括实体瘤,优选胃癌、胃食管癌、乳腺癌、结肠癌、肝癌、头颈癌、支气管癌、非小细胞肺癌、胰腺癌、食道癌、卵巢癌。
本文地址:https://www.jishuxx.com/zhuanli/20240619/831.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。