制备β-氨基吡嗪乙酸酯的方法与流程
- 国知局
- 2024-11-19 09:34:28
本公开属于医药领域,涉及制备β-氨基吡嗪乙酸酯的方法。
背景技术:
1、瑞格列汀是一类dpp-iv抑制剂,用于2型糖尿病的治疗。同类药物西他列汀于2006年10月获美国fda批准上市。
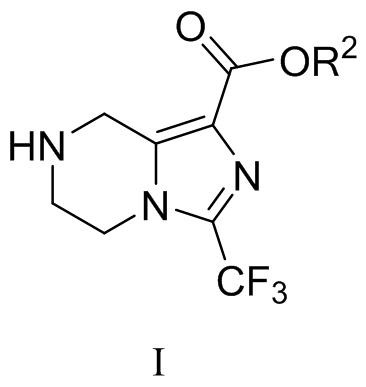
2、3-(三氟甲基)-5,6,7,8-四氢咪唑并[1,5-a]吡嗪-1-羧酸甲酯为制备瑞格列汀重要中间体,
3、。
4、wo2009082881公开了以2-氰基吡嗪为起始物,经氰基还原、酰胺化、关环等步骤获得3-(三氟甲基)-5,6,7,8-四氢咪唑并[1,5-a]吡嗪,然而与( r)-3-叔丁氧羰基氨基-4-(2,4,5-三氟苯基)-丁酸反应,随后再构造羧酸酯基。整体工艺收率偏低,同时价格昂贵的催化剂,如八羰基二钴,生产成本高,不利于放大生产。
5、。
6、cn106892926b则公开了一种3-(三氟甲基)-5,6,7,8-四氢咪唑并[1,5-a]吡嗪-1-羧酸甲酯的制备方法,并借此合成瑞格列汀,其包括2-(吡嗪-2-基)-2-(2,2,2-三氟乙酰胺)乙酸甲酯在脱水剂如pocl3条件下成环,以及还原步骤,
7、其中2-(吡嗪-2-基)-2-(2,2,2-三氟乙酰胺)乙酸甲酯由市售的n-(二苯基亚甲基)甘氨酸乙酯在碳酸钾、四正丁基溴化铵条件下与2-氯吡嗪反应,再水解、酰胺化获得,(参见 j. med. chem.1994,37, 4567-4571)。
技术实现思路
1、一方面,本公开提供了制备式i化合物或其盐的方法,,包括式d化合物在亚硝酸钠条件下转化为式e化合物,随后式e化合物在还原剂条件下形成式f化合物的步骤,其中,r2选自c1-6烷基或苄基,例如甲基、乙基或苄基。
2、在一些实施方案中,式d化合物与亚硝酸钠的摩尔比为1:1~1:6,包括但不限于1:1.1、1:1.2、1:1.3、1:1.4、1:1.5、1:1.6、1:1.7、1:1.8、1:1.9、1:2、1:2.5、1:3、1:3.5、1:4、1:4.5、1:5、1:5.5或1:6。
3、在一些实施方案中,式d化合物与亚硝酸钠反应还含有醋酸。
4、在一些实施方案中,式d化合物在亚硝酸钠和醋酸条件下反应生成式e化合物,其中式d化合物与亚硝酸钠摩尔比为1:1~1:6。
5、在一些实施方案中,式e化合物还原反应条件为锌粉/酸或h2/金属钯。在一些实施方案中,式e化合物在锌粉/酸条件下发生还原反应。在一些实施方案中,式e化合物在锌粉/醋酸条件下发生还原反应。在另一些实施方案中,式e化合物在h2/钯炭条件下发生还原反应。
6、在一些实施方案中,所述方法还包括式c化合物转化为式d化合物的步骤,其中,r1选自c1-6烷基或苄基,例如甲基、乙基或苄基;r2选自c1-6烷基或苄基,例如甲基、乙基或苄基。
7、在一些实施方案中,所述方法包括式c化合物在碱性条件下形成式d-1化合物,以及式d-1化合物转化式d化合物的步骤,其中反应所用碱(2)选自不限于氢氧化钠或氢氧化钾,,其中,r1选自c1-6烷基或苄基,例如甲基、乙基或苄基;r2选自c1-6烷基或苄基,例如甲基、乙基或苄基。
8、在一些实施方案中,反应所用碱(2)与式c化合物摩尔比为1:1~4:1,包括但不限于1:1、2:1、3:1或4:1。
9、在一些实施方案中,式c化合物脱羧反应温度为20~100℃,优选30~80℃,更优选40~60℃。
10、在一些实施方案中,式d-1化合物在二氯亚砜条件下与醇反应形成式d化合物,所述醇为c1-6烷基醇或苄基醇。
11、在一些实施方案中,式d-1化合物在二氯亚砜条件下与甲醇反应形成相应甲酯化合物。在一些实施方案中,式d-1化合物在二氯亚砜条件下与乙醇反应形成相应乙酯化合物。
12、另一方面,本公开方法还包括式a化合物与式b化合物在碱性条件下反应形成式c化合物的步骤,反应所用碱(1)选自但不限于碳酸铯,其中,r1选自c1-6烷基或苄基,例如甲基、乙基或苄基;x为卤素,例如氯。
13、在一些实施方案中,式a化合物与式b化合物摩尔比为1:1~6:1,优选1:1~3:1,更优选1:1~2:1。
14、在一些实施方案中,反应所用碱(1)与式b化合物摩尔比为1:1~4:1,包括但不限于1:1、2:1、3:1或4:1。
15、在一些实施方案中,式a化合物与式b化合物反应温度为60~100℃,包括但不限于60℃、70℃、80℃、90℃或100℃。
16、在一些实施方案中,式a化合物与式b化合物反应溶剂选自但不限于n,n-二甲基甲酰胺(dmf)或二甲亚砜(dmso)。
17、在一些实施方案中,式a化合物与式b化合物反应还可添加相转移催化剂,相转移催化剂选自但不限于四丁基溴化铵。
18、在一些实施方案中,四丁基溴化铵添加为催化量的,为式b化合物摩尔量的0.1~0.5eq(当量),包括但不限于0.1eq、0.2eq、0.3eq、0.4eq或0.5eq。
19、在一些实施方案中,本公开方案包括:a) 式a化合物与式b化合物在碳酸铯条件下反应形成式c化合物,b) 式c化合物转化为式d化合物,c) 式d化合物在亚硝酸钠条件下转化为式e化合物,随后式e化合物在还原剂条件下形成式f化合物,其中,r1选自c1-6烷基或苄基,例如甲基、乙基或苄基;r2选自c1-6烷基或苄基,例如甲基、乙基或苄基;x为卤素,例如氯。
20、另一方面,在一些实施方案中,式i化合物为所述方法包括化合物d在亚硝酸钠条件下反应生成化合物e,随后化合物e物在还原剂条件下形成化合物f的步骤,。
21、在另一些实施方案中,所述方法还包括式f化合物与三氟乙酰氯或三氟乙酰酐反应形成式g化合物,式g化合物在三氟乙酸酐条件下形成式h化合物,再经催化氢化形成式i化合物的步骤,催化氢化所用试剂为pd/c或氢氧化钯,其中,r2选自c1-6烷基或苄基,例如甲基、乙基或苄基。相关实验操作可参见cn114478536中所述,并将相关内容引入本文本以示说明。
22、在一些实施方案中,所述方法包括a) 化合物a与化合物b在碳酸铯条件下反应形成化合物c,b) 化合物c在氢氧化钠或氢氧化钾条件下反应形成式d-1化合物,c) 式d-1化合物与甲醇在二氯亚砜条件下反应形成化合物d,d) 化合物d在亚硝酸钠条件下形成化合物e,随后化合物e在h2/钯炭下反应形成化合物f,。
23、在一些实施方案中,步骤a)中化合物a与化合物b以1:1~2:1摩尔比投料,在碳酸铯条件下反应形成化合物c。
24、在一些实施方案中,步骤b)化合物c在氢氧化钠或氢氧化钾条件下脱羧形成式d-1化合物。
25、另一方面,本公开还提供制备化合物aa或其可药用盐的方法,,包括前述制备式i化合物的步骤,以及式i化合物与式ii化合物反应以形成式a-1化合物,式a-1化合物脱保护基形成化合物aa的步骤,其中,r2选自c1-6烷基或苄基,例如甲基、乙基或苄基;p为氨基保护基,例如叔丁氧羰基(boc)。
26、在一些实施方案中,式i化合物与式ii化合物在n, n-羰基二咪唑/咪唑盐酸盐条件下反应形成式a-1化合物。
27、在一些实施方案中,在盐酸条件下脱氨基保护基。相关实验操作可参见cn114478536中所述,并将相关内容引入本文本以示说明。
28、本公开化合物aa可药用盐包括但不限于磷酸盐。另一方面,本公开其他化合物或以盐形式存在,如以盐酸盐或硫酸盐。例如化合物f以盐酸形式存在。
29、另一方面,本公开所述制备方法还包括过滤、浓缩、经柱层析纯化和干燥中一步或多步操作。
30、“以形成”和“转化为”并不特指两个底物间的转化反应为单步骤的,可为两个底物间的单步骤或多步骤的反应。如中间体含有保护基,所述中间体经过一步脱除保护剂,随后再与相应底物反应以获得相应目标产物。
31、本公开中数值为仪器测量值,存在一定程度的误差,一般而言,正负10%均属于合理误差范围内。当然需要考虑该数值所用之处的上下文,例如,活性成分的粒径,该数值为测量后误差变化不超过正负10%,可以为正负9%、正负8%、正负7%、正负6%、正负5%、正负4%、正负3%、正负2%或正负1%,优选正负5%。
32、“烷基”指饱和的脂族烃基团,包括有1至6个碳原子的烷基。非限制性实施例包括甲基、乙基、正丙基、异丙基。
33、“保护基”是本领域已知的适当的用于氨基保护的基团,参见文献(《protectivegroups in organic synthesis》,5thed. t. w. greene&p. g. m. wuts)中的氨基保护基团。
本文地址:https://www.jishuxx.com/zhuanli/20241118/329355.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。