通过重组微生物生物技术生产胶原蛋白和细菌胶原蛋白样蛋白的制作方法
- 国知局
- 2024-11-21 11:53:18
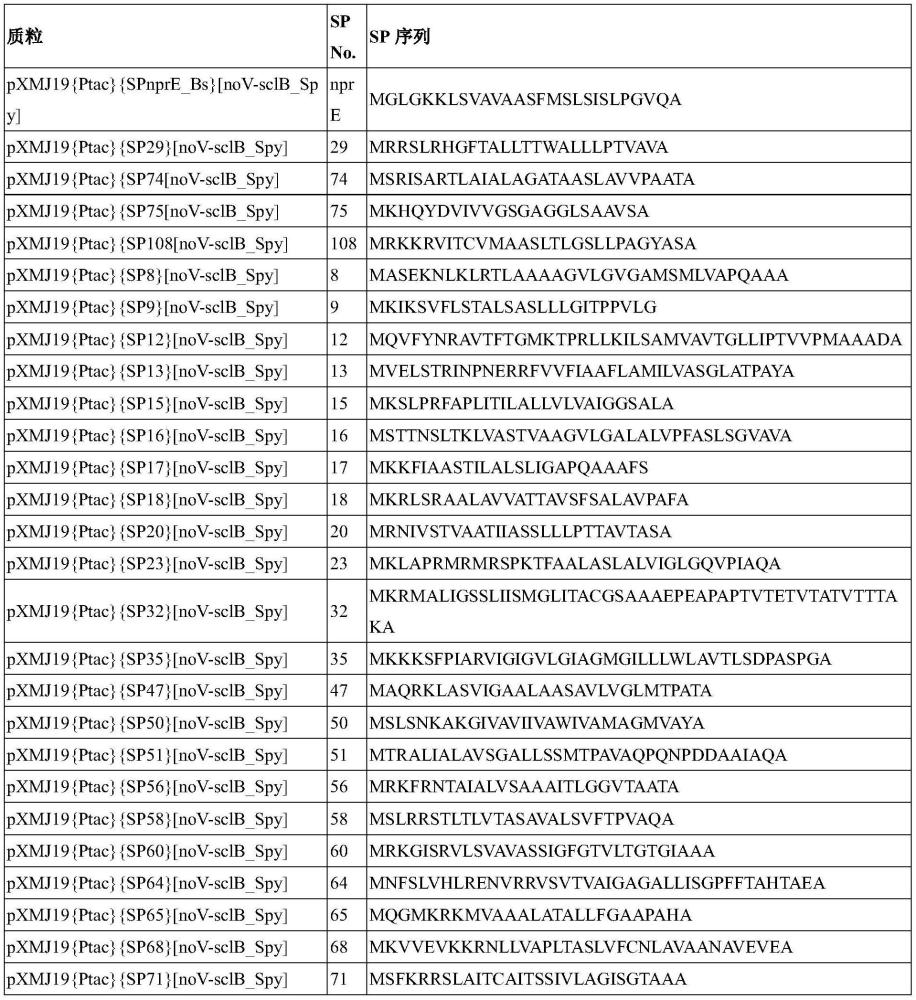
本发明涉及多核苷酸,其编码氨基酸序列,所述氨基酸序列编码胶原蛋白或细菌胶原蛋白样蛋白,其包含n末端信号序列,并且涉及由宿主将胶原蛋白和细菌胶原蛋白样蛋白分泌到发酵培养液中进行的发酵方法。
背景技术:
1、细菌来源的(工业上最相关的为酿脓链球菌(streptomyces pyogenes)的产物)胶原蛋白样蛋白(clp)具有明显令人感兴趣的机械性质,类似于高等的真核细胞的胶原蛋白,无需真核对应物所需的复杂成熟步骤。clp呈现出一种共同的结构:两个相互稳定的α螺旋构成“v结构域”,随后是棒样的结构胶原蛋白结构域。在胶原结构域之后,通常在蛋白的c末端存在膜锚(gpi样)。
2、已经在若干系统中尝试了胶原蛋白样蛋白的表达,包括大肠杆菌(escherichiacoli)和酿酒酵母(saccharomyces cerevisiae)。对于scl2在大肠杆菌(e.coli)中的表达(j.biol.chem.277,27312–27318),这样的制备的选择的构建体带有特定和必须的修饰,以有效地去除潜在免疫原性的v结构域:这样的修饰由通常插在v结构域和胶原蛋白结构域之间的蛋白酶切割位点组成。由于这种修饰,细菌宿主产生的蛋白必须从细胞内部分提取并用特定的蛋白酶加工以去除v结构域。仅由胶原蛋白样结构域组成的成熟蛋白必须对切割的v结构域、全细胞内蛋白内容物以及加入以加工未成熟clp的蛋白酶加以纯化。这样的工作流程极大地阻碍了整个方法的成本效益,因为1)所选产物必须与表达宿主细胞的全部内容物分离,2)蛋白酶通常是昂贵的酶。
3、因此,本发明的一个目的是提供一种制备胶原蛋白和clp的改进方法,其是有成本效益的且无需添加切割结构域的特定蛋白酶就可用。
4、在过去的许多情况下已经使用了谷氨酸棒杆菌(corynebacterium glutamicum(c.glutamicum))以通过分泌到上清中来制备异源蛋白。由于以下原因,其特别适合于这项任务:
5、i)高容量的分泌装置(apparatus)以将蛋白分泌到上清中,
6、ii)几乎完全没有会与异源蛋白竞争非常相同的分泌装置的内源蛋白分泌到上清中,
7、iii)大量遗传操作的工具的可用性,
8、iv)其生理和系统生物学的知识丰富,包括基因组序列、基因表达、蛋白和代谢丰度等,
9、v)超过50年的关于这种生物的工业应用和放大生产的经验,
10、vi)谷氨酸棒杆菌为安全的宿主(gras通知),因此没有关于工业使用的环境或健康问题。
11、然而,给定异源蛋白的有效分泌取决于许多因素,这些因素至少部分尚不清楚。这包括但不限于:
12、i.基因表达效率,即转录
13、ii.翻译效率
14、iii.新生多肽链的折叠动力学
15、iv.折叠的多肽的三维结构
16、v.多肽的翻译后修饰,例如糖基化或二硫键
17、vi.折叠的多肽通过分子伴侣的解折叠动力学
18、vii.细胞内、膜结合或细胞外蛋白的存在导致蛋白降解
19、viii.信号肽(sp)的选择
20、ix.sp与信号识别颗粒(spr)的相互作用
21、x.spr结合的多肽链与sec分泌装置的相互作用
22、xi.信号肽切割位点由信号肽酶切割
23、因此,很难合理地设计用于高效分泌生产给定异源蛋白的生产菌株。因此,个体因素通常通过随机方法进行调节,以创造各自因素的多样性,然后进行筛选活动,对这种多样性进行抽样。
24、例如,通过审视http://dx.doi.org/10.1016/j.jbiotec.2017.02.023的表1,这一点变得显而易见。发酵液中的蛋白浓度作为描述异源蛋白分泌到上清中的效率的一个参数,范围为每升发酵液0.5mg-5g,因此跨越了4个数量级。
25、因此,我们使用某些信号肽,用谷氨酸棒杆菌能够实现高水平的分泌是不可预测的,也是相当出人意料的。因此,我们要求保护这些信号肽用于通过谷氨酸棒杆菌和其他菌株高效产生胶原蛋白和细菌胶原蛋白样蛋白的用途。
26、更出人意料的是,信号肽的选择不仅会影响给定多肽的分泌效率,还会影响细胞信号肽酶切割信号肽酶切割位点的选择性。这一点非常重要,因为给定蛋白的氨基基础序列的真实性(authenticity)对于许多应用非常重要,最重要的是在医药或制药应用中。由于细胞信号肽酶对信号肽酶切割位点的不精确切割,这种蛋白的变体在n端存在额外或缺失的氨基酸残基,这是非常有问题的,因为这些在n端具有额外或缺失氨基酸残基的变体需要通过费力的纯化步骤去除,导致更高的制造成本,或者需要确认它们在制剂中的存在对蛋白的性能或接受蛋白制剂所属治疗的患者的健康没有负面影响。后者甚至更耗时、更昂贵,有时甚至无法确认。因此,本发明的目的是提供一种胶原蛋白的表达系统,包括细菌胶原蛋白样蛋白,其具有增强的胶原蛋白分泌,以及细胞信号肽酶对信号肽酶切割位点的选择性切割。
技术实现思路
1、因此,本发明提供一种用于分泌胶原蛋白或细菌胶原蛋白样蛋白的发酵方法,所述胶原蛋白或细菌胶原蛋白样蛋白包含n末端信号序列。
2、本发明涉及一种多核苷酸,其编码氨基酸序列,所述氨基酸序列编码胶原蛋白或细菌胶原蛋白样蛋白,其包含n末端信号序列,所述n末端信号序列与选自seq id no:6–66的氨基酸序列中的一个至少≥90%相同。
3、出人意料地发现,胶原蛋白样蛋白与各种n末端信号肽的特定融合产物导致增加的胶原蛋白样蛋白产生和分泌入发酵培养基中。
4、优选地,n末端信号序列与选自seq id no:6–66的氨基酸序列至少≥92%、≥94%、≥96%、≥97%、≥98%、≥99%或100%相同。
5、在一实施方案中,本发明的多核苷酸可以是可复制核苷酸序列,其编码来自酿脓链球菌(streptococcus pyogenes)、副猪嗜血杆菌(glaesserella parasuis)、玫瑰链孢囊菌(streptosporangium roseum)、易变噬几丁质菌(chitinophaga varians)、哈森氏菌(hazenellasp.)、幼虫类芽孢杆菌(paenibacillus larvae)、短杆菌(brevibacteriumsp.)、lacrimispora algidixylanolytica、aquimarina sediminis、或来自罗伊氏短芽孢杆菌(brevibacillus reuszeri),优选来自酿脓链球菌、副猪嗜血杆菌或来自玫瑰链孢囊菌的胶原蛋白或细菌胶原蛋白样蛋白。
6、在一实施方案中,本发明的多核苷酸可以为可复制核苷酸序列,其编码来自酿脓链球菌的胶原蛋白样蛋白。
7、更具体地,多核苷酸可以为可复制核苷酸序列,其编码来自的酿脓链球菌的胶原蛋白样蛋白的胶原蛋白样结构域。这指的是胶原蛋白样蛋白,其没有n末端v结构域,并且没有c末端膜锚。
8、因此,优选地,其中氨基酸序列编码细菌胶原蛋白样蛋白,其包含n末端信号序列,其中所述氨基酸序列与选自seq id no:67-127的氨基酸序列中的一个至少≥90%相同。
9、相应地,本发明还涉及多核苷酸和核酸分子,其包含这样的序列并且编码seqidno:67-127的多肽变体,所述多肽变体包含一个或多个插入或缺失。优选地,多肽包含最大5个、最大4个、最大3个或最大2个氨基酸的插入或缺失。
10、在另一优选实施方案中,氨基酸序列编码细菌胶原蛋白样蛋白,其包含n末端信号序列,其中所述氨基酸序列与选自seq id no:90、seq id no:101、seq id no:104或seq idno:106的氨基酸序列中的一个至少≥90%相同。
11、本发明还涉及多肽,其包含本发明的核苷酸序列编码的氨基酸序列。
12、本发明还涉及质粒和载体,其包含本发明的核苷酸序列,并且任选地在以下属的微生物中复制:毕赤酵母(pichia)属、棒杆菌(corynebacterium)属、假单胞菌(pseudomonas)属或埃希氏杆菌(escherichia)属,或者适合于在其中复制。在一优选的方式中,包含本发明的核苷酸序列的载体适合于在巴斯德毕赤酵母(pichia pastoris)的酵母中复制。
13、本发明还涉及毕赤酵母属、棒杆菌属、假单胞菌属或埃希氏杆菌属的微生物,其包含本发明的多核苷酸、载体和多肽。优选的微生物为巴斯德毕赤酵母、桥石短芽孢杆菌(brevibacillus choshinensis)或谷氨酸棒杆菌。
14、本发明还涉及本发明的微生物,其特征在于本发明的多肽整合在染色体中。通过使用本发明的载体,同源重组允许将染色体上的dna区段交换为通过所述载体运输到细胞中的本发明的多核苷酸。为了载体的环形dna分子与染色体上的靶dna的有效重组,在要交换的含有本发明的多核苷酸的dna区域的末端提供与靶位点同源的核苷酸序列,这确定载体整合和dna交换的位点。
15、本发明提供巴斯德毕赤酵母(p.pastoris)、大肠杆菌、p.putida或谷氨酸棒杆菌物种的微生物,其包含所要求保护的任何核苷酸序列,或者所要求保护的任何多肽,或者所要求保护的任何载体。
16、微生物可以是其中核苷酸以过表达形式存在的微生物。
17、微生物的特征可以在于,所述微生物具有产生和分泌精细化学品(finechemical)的能力。所述精细化学品优选为胶原蛋白或细菌胶原蛋白样蛋白。
18、过表达通常表示,与起始菌株(亲本菌株)或野生型菌株(如果这是起始菌株)相比,核糖核酸、蛋白(多肽)或酶的细胞内浓度或活性增加。起始菌株(亲本菌株)是指在其上进行导致过表达的措施的菌株。
19、在过表达中,优选重组过表达的方法。这些包括使用体外提供的dna分子生产微生物的所有方法。这样的dna分子包括,例如,启动子、表达盒、基因、等位基因、编码区等。这些通过转化、接合、转导等方法转化为期望的微生物。
20、表达或过表达的程度可以通过测量基因转录的mrna的量、确定多肽的量和确定酶活性来确定。
21、本发明公开用于制备精细化学品的发酵方法,其包括以下步骤:
22、a)在培养基中发酵本发明的微生物,
23、b)在所述培养基中积累胶原蛋白或细菌胶原蛋白样蛋白,其中获得发酵培养液。
24、如实施例所示,本发明的这样的方法的使用导致与各自的起始菌株相比,细菌胶原蛋白样蛋白的产物浓度和分泌的显著增加。
25、要使用的培养基或发酵培养基必须适当地满足各自菌株的需求。各种微生物的培养基的描述参见american society for bacteriology(washington d.c.,usa,1981)的手册"manual of methods for general bacteriology"。术语培养基(culture medium)和发酵培养基或培养基(medium)可以相互交换。
26、在优选的实施方案中,胶原蛋白或细菌胶原蛋白样蛋白的含量为至少100mg/l、或至少500mg/l、或至少1g/l、或至少5g/l。
27、在另一优选实施方案中,胶原蛋白或细菌胶原蛋白样蛋白的纯度为至少30%、或至少50%、或至少60%、或至少70%、或至少80%、或至少90%、或至少95%。
28、根据本发明,纯度定义为具有如上所定义的正确氨基酸序列的胶原蛋白样蛋白的量相对于发酵培养液的上清中总蛋白的量。
29、作为碳源,可以使用糖和碳水化合物,例如葡萄糖、蔗糖、乳糖、果糖、麦芽糖、糖蜜、来自甜菜糖或甘蔗加工的含蔗糖溶液、淀粉、淀粉水解产物和纤维素,油和脂肪,例如大豆油、葵花油、花生油和椰子脂肪,脂肪酸,例如棕榈酸、硬脂酸和亚油酸,醇类,例如甘油、甲醇和乙醇,以及有机酸,例如乙酸或乳酸。
30、作为氮源,可以使用有机氮化合物,如蛋白胨、酵母提取物、肉提取物、麦芽提取物、玉米浆、豆粕和尿素,或无机化合物,如硫酸铵、氯化铵、磷酸铵、碳酸铵和硝酸铵。氮源可以单独使用或作为混合物使用。
31、作为磷源,可以使用磷酸、磷酸二氢钾或磷酸氢二钾或相应的含钠盐。
32、此外,培养基必须含有生长所必需的盐,例如金属(如钠、钾、镁、钙和铁)的氯化物或硫酸盐的形式,如硫酸镁或硫酸铁。最后,除了上述物质外,还可以使用必需的生长物质,如氨基酸,如高丝氨酸,和维生素,如硫胺素、生物素或泛酸。
33、所述起始材料可以以单批形式添加到培养物中,或者在培养过程中以适当的方式供应。
34、碱性化合物如氢氧化钠、氢氧化钾、氨或氨水,或酸性化合物如磷酸或硫酸,以适当的方式用于培养物的ph控制。ph通常调节至6.0-8.5,优选6.5-8。为了控制泡沫的形成,可以使用消泡剂,例如脂肪酸的聚乙二醇酯。为了保持质粒的稳定性,可以向培养基中加入合适的选择性作用物质,例如抗生素。发酵优选在有氧条件下进行。为了维持所述有氧条件,将氧气或含氧气体混合物如空气引入培养物中。同样可以使用富含过氧化氢的液体。任选地,发酵在超大气压(superatmospheric pressure)下进行,例如在0.03-0.2mpa的超大气压下。培养的温度通常为20℃-45℃,优选25℃-40℃,特别优选30℃-37℃。在分批或补料分批工艺的情况下,优选连续培养,直到形成足以获得所需有机化合物的量。这个目标通常在10小时-160小时内达到。在连续方法中,可能需要更长的培养时间。由于微生物的活性,精细化学品在发酵培养基和/或微生物细胞中富集(积累)。
35、发酵培养基的实例可以在专利文献us 5,770,409、us 5,990,350、us 5,275,940、wo 2007/012078、us 5,827,698、wo 2009/043803、us 5,756,345或us 7,138,266中找到,可以任选地进行修饰以满足所用菌株的要求。
36、所述方法的特征在于,它是选自分批方法、补料分批方法、重复补料分批方法和连续方法的方法。
37、所述方法的进一步特征在于,从含精细化学品的发酵培养液中获得精细化学品或液体或固体的含精细化学品的产物。
38、基于其中存在本发明启动子变体的微生物的方法或发酵方法,本发明的方法或发酵方法相对于选自以下的一个或多个参数或其他方法参数及其组合的性能提高至少0.5%、至少1%、至少1.5%或至少2%:浓度(每体积形成的化合物)、产率(每消耗的碳源形成的化合物)、体积生产率(每体积和时间形成的化合物)和生物质比生产率(每细胞干质量或生物干质量和时间形成的化合物或者或每细胞蛋白和时间形成的化合物)。
39、由于发酵的措施,获得含有期望精细化学品,优选氨基酸或有机酸的发酵培养液。
40、然后,提供或产生或获得含有精细化学品的液体或固体形式的产物。
41、在优选的实施方案中,发酵培养液是指,微生物在一定温度下培养一定时间的发酵培养基或营养培养基。发酵培养基或发酵过程中使用的培养基包含确保产生期望化合物并通常确保生长和/或成活的所有物质或成分。
42、发酵完成后,所得发酵液相应地含有:
43、a)微生物细胞生长产生的微生物生物量(细胞质量),
44、b)发酵过程中形成的期望的精细化学品,
45、c)发酵过程中可能形成的有机副产物,
46、d)所用发酵培养基或起始材料中未被发酵消耗的成分,例如维生素,如生物素,或盐,如硫酸镁。
47、有机副产物包括除发酵中使用的微生物产生的相应期望化合物外,可能分泌的物质。
48、从培养容器或发酵容器中取出发酵培养液,任选地收集,并用于提供含有精细化学品的液体或固体形式的产物。表述“获得含精细化学品的产物”也用于此。在最简单的情况下,从发酵容器中取出的含精细化学品的发酵培养液本身就是获得的产物。
49、通过选自以下组的一种或多种措施去除在发酵过程中形成的有机副产物:
50、a)去除部分(>0%至<80%)至全部(100%)或基本上全部(≥80%、≥90%、≥95%、≥96%、≥97%、≥98%、≥99%)的水;
51、b)去除部分(>0%至<80%)至完全(100%)或基本上全部(≥80%、≥90%、≥95%、≥96%、≥97%、≥98%、≥99%)的生物质量,其中这在去除前任选地失活;
52、c)去除部分(>0%至<80%)至完全(100%)或基本上全部(≥80%、≥90%、≥95%、≥96%、≥97%、≥98%、≥99%、≥99.3%、≥99.7%)的在发酵过程中形成的有机副产物;以及
53、d)去除部分(>0%)至完全(100%)或基本上全部(≥80%、≥90%、≥95%、≥96%、≥97%、≥98%、≥99%、≥99.3%、≥99.7%)的所用的发酵培养基的组分或者未被发酵消耗的起始材料;
54、从发酵培养液获得期望的有机化合物的浓度或纯度。以这种方式,分离具有期望含量的化合物的产物。
55、去除部分(>0%至<80%)至全部(100%)或基本上全部(≥80%至<100%)的水(措施a))又称为干燥。
56、在所述方法的变型中,通过全部或几乎全部去除所用的发酵培养基中的水、生物质量、有机副产物和未消耗的组分,成功获得期望的有机化合物的纯的(≥80重量%、≥90重量%)或高纯度的(≥95重量%、≥97重量%、≥99重量%)产品形式,优选细菌胶原蛋白样蛋白。对于a)、b)、c)或d)的措施,现有技术中有大量的技术介绍可用。
57、在产生细菌胶原蛋白样蛋白的方法中,这样的方法是优选的,其中获得的产物不含任何发酵培养液的组分。这些产物特别地用于人类医药、制药工业和食品工业。
58、本发明的方法用于发酵生产和分泌胶原蛋白和细菌胶原蛋白样蛋白。
59、本发明最后涉及本发明的微生物用于发酵生产和分泌胶原蛋白和细菌胶原蛋白样蛋白的用途。
本文地址:https://www.jishuxx.com/zhuanli/20241120/333205.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。