一种用于检测水产品中食源性致病菌的四重TaqmanqPCR试剂的制作方法
- 国知局
- 2024-12-26 14:52:52
本发明属于分子生物学检测食源性细菌领域,具体涉及一种用于检测水产品中食源性致病菌的四重taqman qpcr试剂。
背景技术:
1、近年来,国内外食品安全状况不佳,因致病菌污染而导致的食物中毒事件频频出现。食源性致病菌已成为影响食品安全的最主要因素之一。随着渔业经济的发展及食品加工技术的进步,我国水产品供应日益丰富,消费也不断增长。然而,水产品在养殖、捕捞、储藏、加工、运输、销售等环节极易受到病原微生物污染,且我国各地居民普遍有吃鲜活水产品如生鱼片、生蚝、生虾的习惯。因此,检测水产品及其加工品中的食源性致病菌是确保其食用安全的重要举措,这直接关系到消费者的健康和生命安全。根据现行国家食品安全监管体系,金黄色葡萄球菌(staphylococcus aureus,sau)、副溶血性弧菌(vibrioparahaemolyticus,vp)、创伤弧菌(vibrio vulnificus,vv)和志贺氏菌(shigellacastellani,sc)均属于水产品中重点关注的食源性致病菌;这4种病原菌对食物污染引起的中毒事件常表现为急性肠胃炎,并伴有恶心、头痛、低热等症状,严重时可造成死亡。因此,建立针对水产品及其加工制品中副溶血性弧菌、创伤弧菌、志贺氏菌和金黄色葡萄球菌4种食源性致病菌的快速检测方法,对于保障我国水产品食用安全具有重要意义。
2、食源性致病菌传统的基于选择性培养基和生化分析的鉴定方法存在检测周期长、操作繁琐、检测单一等缺陷,很难满足现代化食品安全快速检测的需要。分子生物学检测技术,如聚合酶链式反应(polymerase chain reaction,pcr),因具有高效、灵敏、准确等优点,已广泛应用于食源性致病菌的检测。其中,相较于常规pcr,实时荧光定量pcr(real-time quantitative pcr,qpcr),尤其是多重qpcr,因其更为简化的流程、实时的样本定量分析、无需更多步骤的样品转移和扩增条带可视化、更优异的特异性和灵敏度及多靶标同时检测等显著性优势获得了更为广泛的关注和应用。至今,国内外已报道了不少分别针对这4种病原菌,或者将其中几种与其它常见食源性致病菌(如大肠杆菌、单增李斯特菌等)一齐进行检测的qpcr试剂盒和检测方法,例如,蔡先全发明的多重qpcr试剂盒靶向检测副溶血性弧菌、金黄色葡萄球菌和单增李斯特菌三种致病菌;何培彦发明的五重qpcr试剂盒靶向检测金黄色葡萄球菌、单增李斯特菌、沙门氏菌、副溶血性弧菌和志贺氏菌;上海测博生物发明的七重qpcr试剂盒靶向沙门氏菌、金黄色葡萄球菌、志贺氏菌、大肠杆菌、副溶血性弧菌、单增李斯特菌和蜡样芽胞杆菌,但未见研究和产品致力于水产品中副溶血性弧菌、创伤弧菌、志贺氏菌和金黄色葡萄球菌这4种重要食源性病原菌的同时检测。因而,从应用角度来看,开发快速、准确、操作简单、特异性强的四重qpcr诊断方法以实现副溶血性弧菌、创伤弧菌、志贺氏菌及金黄色葡萄球菌的同时鉴定及检测具有重要意义。
3、该四重qpcr检测方法可以同时在水产品中检测副溶血性弧菌、创伤弧菌、志贺氏菌(属)和金黄色葡萄球菌四种病原,但考虑到四重qpcr需要在一个体系中加入四对引物及四条探针,为了保证引物和探针间互不影响,引物及探针需要高度的特异性,避免引物、探针间发生结合或产生非特异性扩增。此外,考虑到模板中核酸的情况更为复杂,且不同引物所要求的退火温度可能不同。因此,建立一种四重taqman探针法qpcr检测方法具有很高的研究和实际应用价值,但实现起来颇具难度。
技术实现思路
1、本发明的目的在于克服现有技术的至少一个不足,提供一种用于检测水产品中食源性致病菌的四重taqman qpcr试剂。
2、本发明所采取的技术方案是:
3、第一个方面,本发明提供一种用于检测水产品中食源性致病菌的四重taqmanqpcr试剂,所述食源性致病菌为副溶血性弧菌、创伤弧菌、志贺氏菌和金黄色葡萄球菌;所述试剂包括四种食源性致病菌对应的特异性引物和taqman探针;
4、所述用于检测副溶血性弧菌的引物序列及taqman探针序列为:上游引物vp-f、下游引物vp-r、taqman探针vp-p;
5、所述vp-f具有如seq id no.1所示的序列;
6、所述vp-r具有如seq id no.2所示的序列;
7、所述vp-p具有如seq id no.3所示的序列;
8、所述用于检测创伤弧菌的引物序列及taqman探针序列为:上游引物vv-f、下游引物vv-r、taqman探针vv-p;
9、所述vv-f具有如seq id no.4所示的序列;
10、所述vv-r具有如seq id no.5所示的序列;
11、所述vv-p具有如seq id no.6所示的序列;
12、所述用于检测志贺氏菌的引物序列及taqman探针序列为:上游引物sc-f、下游引物sc-r、taqman探针sc-p;
13、所述sc-f具有如seq id no.7所示的序列;
14、所述sc-r具有如seq id no.8所示的序列;
15、所述sc-p具有如seq id no.9所示的序列;
16、所述用于检测金黄色葡萄球菌的引物序列及taqman探针序列为:上游引物sau-f、下游引物sau-r、taqman探针sau-p、上游引物sau-f1、下游引物sau-r1、taqman探针sau-p1;
17、所述sau-f具有如seq id no.10所示的序列;
18、所述sau-r具有如seq id no.11所示的序列;
19、所述sau-p具有如seq id no.12所示的序列;
20、所述sau-f1具有如seq id no.13所示的序列;
21、所述sau-r1具有如seq id no.14所示的序列;
22、所述sau-p1具有如seq id no.15所示的序列。
23、在一些实例中,不同菌株的探针标记有不同的荧光-淬灭基团。
24、在一些实例中,所述探针vp-p的5’端标记荧光报告染料为fam,3’端标记荧光淬灭基团为bhq1;
25、所述探针vv-p的5’端标记荧光报告染料为cy5,3’端标记荧光淬灭基团为bhq2;
26、所述探针sc-p的5’端标记荧光报告染料为vic,3’端标记荧光淬灭基团为bhq1;
27、所述探针sau-p的5’端标记荧光报告染料为rox,3’端标记荧光淬灭基团为bhq2。
28、第二个方面,本发明提供一种用于检测水产品中食源性致病菌的四重taqmanqpcr试剂盒,所述四重taqman qpcr试剂盒包含第一个方面所述的四重taqman qpcr检测试剂。
29、在一些实例中,所述食源性致病菌为副溶血性弧菌、创伤弧菌、志贺氏菌和金黄色葡萄球菌。
30、在一些实例中,所述试剂盒还包括阴性对照品,阳性对照品和裂解液。
31、在一些实例中,所述阳性对照品为副溶血性弧菌、创伤弧菌、志贺氏菌和金黄色葡萄球菌对应的基因组dna混合物。
32、在一些实例中,所述阴性对照品为depc水。
33、在一些实例中,所述裂解液组成为4.9~5.1mmol/l三(羟甲基氨基甲烷)和0.019~0.121%的十二烷基硫酸钠溶液。
34、第三个方面,本发明提供一种检测水产品中副溶血性弧菌、创伤弧菌、志贺氏菌和金黄色葡萄球菌的四重taqman qpcr检测试剂的检测方法,包括以下步骤:
35、1)提待测样本的基因组dna备用;
36、2)将待测样本的基因组dna作为模板加入到四重qpcr反应体系中进行扩增,反应体系包括第二个方面所述的四重taqman qpcr试剂盒;
37、3)设定qpcr程序并收集扩增过程中的荧光信号,并进行结果判定。
38、本发明的有益效果是:
39、1.由于目前缺乏行之有效的同时检测水产品中食源性致病菌的方法,本发明根据水产品重要食源性致病菌的特点,结合多重qpcr技术,设计了多重qpcr检测水产品中四种食源性致病菌的引物和探针组,包括副溶血性弧菌上下游引物及探针、创伤弧菌上下游引物及探针、志贺氏菌上下游引物及探针和金黄色葡萄球菌上下游引物及探针,分别对应于序列表中seq id no 1、2和3、seq id no 4、5和6、seq id no 7、8和9及seq id no 10、11和12。这种多重检测方式提高了检测效率,减少了实验成本。
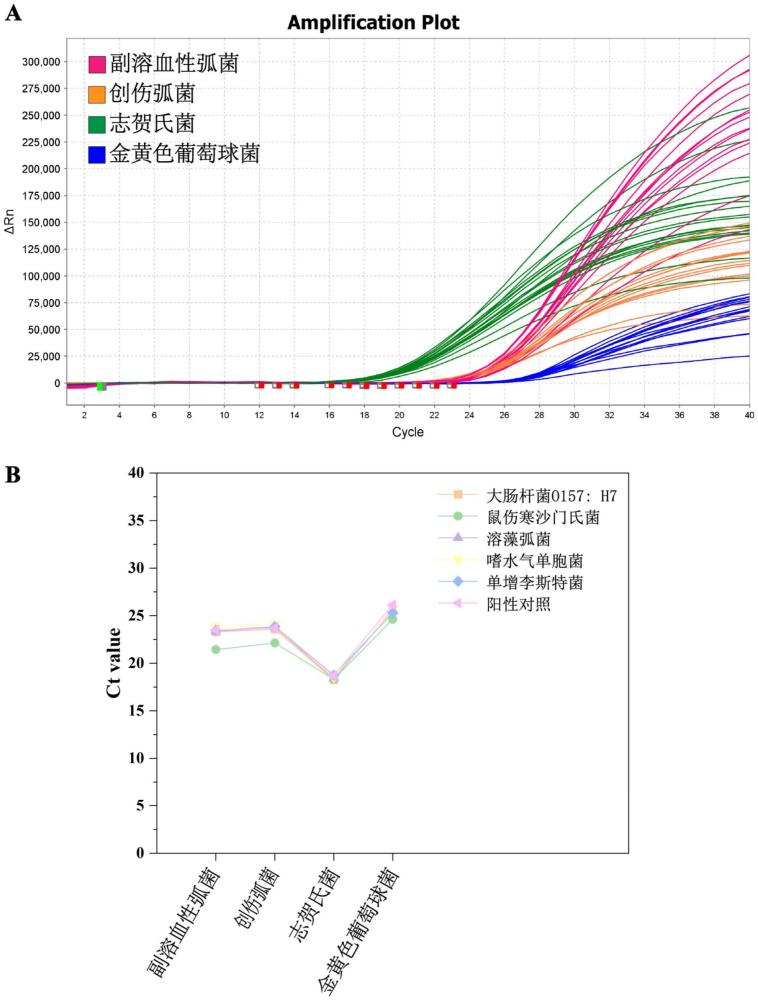
40、2.本发明提供的靶向副溶血性弧菌、创伤弧菌、志贺氏菌和金黄色葡萄球菌的引物-探针组合具有极高的特异性,仅在待测样本中含有目标菌时,才可在对应的荧光检测通道中观测到荧光信号,有效避免了假阳性或假阴性事件的发生,检测结果更加准确。
41、3.本发明建立的四重taqman探针法qpcr检测方法具有较高的灵敏度,针对副溶血性弧菌、创伤弧菌、志贺氏菌和金黄色葡萄球菌的检测灵敏度均可达到2.0×102cfu/ml,且结果具有极佳的可重复性。此外,相较于传统的依托于纯培养物的生化鉴定,本检测方法能够在8~11h内完成样本检测的全过程(包括样品的预增菌过程),其中qpcr反应时长为1h,人工操作时间1h。
42、4.综上所述,本发明提供了一种四重taqman qpcr试剂盒及其检测方法,该试剂盒具有高效、准确、灵敏、快速等特点,为水产品及其加工制品质量安全检测工作中对上述4种食源性致病菌的检测提供一种准确快速、高效经济的手段,对保障我国水产品食用安全具有重要意义。
本文地址:https://www.jishuxx.com/zhuanli/20241226/343744.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。