一种引物探针组合物、试剂盒和检测方法与流程
- 国知局
- 2024-06-20 11:07:08
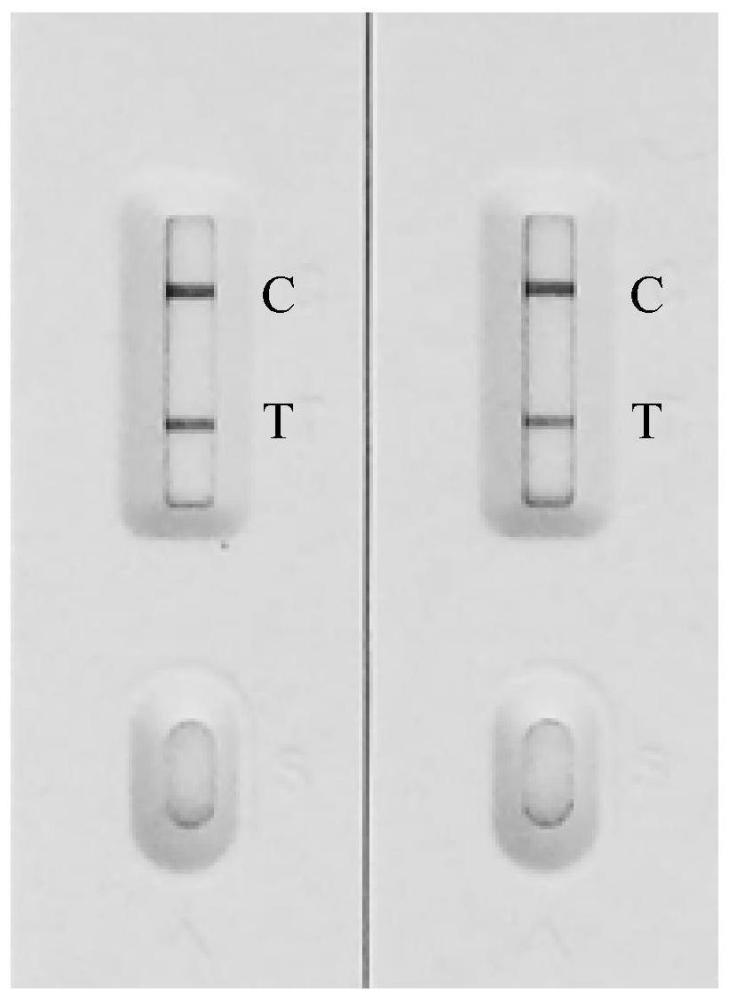
本发明属于突变位点检,尤其涉及一种引物探针组合物、试剂盒和检测方法。
背景技术:
1、表皮生长因子受体(egfr)基因突变是东亚人群中非小细胞肺癌(nsclc)最常见的驱动基因突变,突变率为30%-40%。以往多项研究支持egfr-酪氨酸激酶抑制剂(tki)治疗是egfr基因突变局部晚期或转移nsclc患者的标准治疗方案,但几乎所有服用egfr-tki的患者最终都会出现耐药,其中egfr基因第20号外显子发生错义突变(t790m突变)是耐药突变中最主要的类型。
2、目前已报道的egfr-tki耐药后组织样本的t790m突变阳性率基本在60%左右,血浆样本t790m突变阳性率基于不同方法差别较大,在23%-63%。目前,美国国立综合癌症网络(nccn)、欧洲临床肿瘤协会(esmo)指南、中国临床肿瘤学会(csco)原发性肺癌诊疗指南均推荐奥希替尼为局部晚期或转移nsclc egfr-tki耐药后t790m突变阳性患者的标准治疗。因此,egfr基因t790m突变检测对egfr-tki耐药的晚期nsclc患者后续治疗具有重要的临床指导意义。
3、目前,针对egfr t790m突变检测技术主要有以下几种:
4、sanger法利用一种dna聚合酶来延伸结合在待定序列模板上的引物,直到掺入一种链终止核苷酸为止,每一次序列测定由一套4个单独的反应构成,每个反应含有所有4种脱氧核苷酸三磷酸(dntp),并混入限量的一种不同的双脱氧核苷酸三磷酸(ddntp)。由于ddntp缺乏延伸所需要的3-oh基团,使延长的寡聚核苷酸选择性地在g、a、t或c处终止。sanger法对取材要求比较高,同时由于测序方法本身的限制,其灵敏度也不高,通常只能检测到15%-20%的突变基因,这种技术在组织样本中会出现大量的假阳性,而且无法应用到液态活检中。
5、数字pcr(digital pcr)作为dna定量的新技术,是将一个标准的pcr反应分配到大量微小的反应器中,在每个反应器中包含或不包含一个或多个拷贝的目标分子(dna模板),实现单分子模板pcr扩增,扩增结束后,通过阳性反应器的数目“数出”目标序列的拷贝数,这种方法的优点是可以对ctdna进行绝对定量,灵敏度可达到单个核酸分子,检测限低至0.001%,但同时也存在只能检测已知的突变位点、通量低且成本高的缺点。
6、arms法是利用pcr引物的3’端末位碱基必须与其模板dna互补才能有效扩增的原理,设计等位基因特异性pcr扩增引物,在严格的条件下,只有在引物3’末端碱基与模板配对时才能出现pcr扩增,从而检测出突变。arms方法检测灵敏度明显高于直接测序法等其他方法,利用qpcr的△ct值可检测出样品中含量低至1%的突变基因。现已成为国际上肿瘤个体化分子检测最重要的技术之一,其在临床应用中的优势已被业内专家广泛认可。但是引物3’末端碱基与模板不配对时也会出现扩增,不同的突变碱基变化其扩增效率具有一定的随机性(部分和完全配对引物相比扩增效率差别比较大,即qpcr中的△ct值大;部分和完全配对引物相比扩增效率差别比较小,即qpcr中的△ct值小,甚至为0),部分1%突变频率基因位点在在检测应用中的准确度无法满足要求。
7、二代测序进行egfr t790m snp检测,显而易见操作流程比较繁琐,实验周期比较长并且价格较为昂贵,因此该技术不适合作为初筛的检测手段。
8、总之,现有的针对于egfr t790m突变检测技术中,存在易出现假阳性、检测条件高、检测特异性和灵敏度无法完全保证的问题,严重影响检测结果的准确性。
技术实现思路
1、为解决上述问题,一种引物探针组合物,应用于检测肿瘤耐药基因snp突变位点,包括:错配引物和反向探针;
2、所述错配引物的核酸序列如seq id no.1所示;
3、其中,所述错配引物的核酸序列中第26-27号位置设有通配符nn;所述通配符nn选自ag、cg、at、tt、gt、ac、tc、gc和tg中的任意一种;
4、所述反向探针的核酸序列如seq id no.2所示;
5、优选地,所述肿瘤耐药基因为人表皮生长因子受体egfr基因;
6、优选地,所述snp突变位点为egfr基因第20号外显子的错义突变。
7、优选地,所述错配引物的5’端标记有荧光素;
8、优选地,所述荧光素选自6-fam、hex、tet、joe、cy3、cy5、rox、texas red中的任意一种;
9、优选地,所述荧光素为6-fam。
10、优选地,所述反向探针中标记有四氢呋喃,并且5’端标记有生物素,3’端标记有间臂基团;
11、优选地,所述四氢呋喃标记在距探针5’端的第33个碱基处;
12、优选地,所述间臂基团为c3 spacer。
13、此外,为解决上述问题,本发明还提供一种试剂盒,包括核酸检测试纸和包含有如上述所述引物探针组合物的扩增试剂。
14、优选地,还包括等温扩增试剂;
15、所述等温扩增试剂包括nfo酶、重组酶和扩增酶中的任意一种或几种。
16、优选地,所述核酸检测试纸包括底板,以及设于所述底板上的样品垫、标记物结合垫和层析反应膜;
17、优选地,所述标记物结合垫吸附有特异性复合物;所述特异性复合物是通过将胶乳微球与sa、鸡igy、叶酸、甘胆酸中的任意一种或者多种偶联得到的;
18、优选地,所述胶乳微球包括红色、蓝色和紫色;
19、优选地,所述层析反应膜上设置有检测线;所述检测线含有与所述引物探针组合物中的错配引物的5’端标记的荧光素对应的抗体;
20、优选地,在所述荧光素为6-fam时,所述检测线含有的抗体为抗fam抗体;
21、优选地,所述检测线中的抗体浓度均为0.25mg/ml-0.5mg/ml;
22、优选地,所述层析反应膜上还设置有质控线,所述质控线含有抗biotin抗体;
23、优选地,所述质控线中的抗体浓度0.25mg/ml-0.5mg/ml。
24、优选地,所述扩增试剂中的错配引物和反向探针的浓度比为1:0.6。
25、优选地,所述扩增试剂中的错配引物和反向探针的摩尔比为2:1。
26、优选地,所述扩增试剂中还包括缓冲液和醋酸镁溶液。
27、此外,为解决上述问题,本发明还提供一种检测方法,包括:
28、将含有样本的混合液加入如上述所述试剂盒的扩增试剂中进行扩增反应,扩增反应结束后,得到扩增溶液;
29、将所述扩增溶液稀释,加入至核酸检测试纸的样品垫上,并读取结果;
30、优选地,所述扩增反应的反应时间为15分钟,反应温度为40℃;
31、优选地,所述扩增溶液的稀释倍数为16倍;
32、优选地,所述检测方法的检测时间为15分钟;
33、优选地,所述加入至所述核酸检测试纸的样品垫上的稀释后的所述扩增溶液的体积为75μl;
34、优选地,所述扩增反应的反应体系为:
35、醋酸镁溶液2.5μl;
36、10μm错配引物2μl;
37、5μm反向探针1.2μl;
38、模板2μl;
39、无核酸酶水补至50μl。
40、本发明所提供一种引物探针组合物、试剂盒和检测方法,其中,所述引物探针组合物,应用于检测肿瘤耐药基因snp突变位点,包括:错配引物和反向探针;所述错配引物的核酸序列如seq id no.1所示;gcctcacctccaccgtgcagctcatnnt;其中,所述错配引物的核酸序列中5’端的第26-27号位置设有通配符nn;所述通配符nn选自ag、cg、at、tt、gt、ac、tc、gc和tg中的任意一种;所述反向探针的核酸序列如seq id no.2所示。本发明提供的引物探针组合物,首次将rpa技术应用于egfr的snp突变检测,基于引物探针组合物的技术和方法能够实现准确、快速、简便检测egfr的t790m突变,仅需通过对临床样品进行核酸提取并进行rpa等温扩增,结果可在核酸层析试纸条上清晰显示,不必在pcr仪中进行扩增,也不必通过测序获取结果,具有灵敏度高、特异性强、操作程序简单、检测时间短等优点,适用于非实验室环境下临床现场快速检测,具有广泛的应用前景。
本文地址:https://www.jishuxx.com/zhuanli/20240619/1085.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。