一种化妆品原料体外舒缓功效评估组合方法与流程
- 国知局
- 2024-08-08 16:53:20
本发明涉及一种化妆品原料体外舒缓功效评估组合方法,属于化妆品。
背景技术:
1、随着环境污染加重、生活压力激增、医美与化妆品的滥用,过敏性疾病发病率逐年上升,相应的敏感性皮肤在世界各地均有较高的发生率。敏感性皮肤是一种皮肤在生理或病理条件下的高度敏感状态,在受到内外源性刺激后具体表现为瘙痒、泛红、刺痛、灼热且极易反复发作,而当皮肤处于敏感状态时皮肤炎症发生率也会升高,伴随的一系列皮肤问题令人困扰。
2、针对此研发的舒缓类功效性护肤品,主要通过改善皮肤刺激后的敏感性相关反应、炎症反应等问题来达到舒缓效果。传统的原料评价方法主要通过动物模型实现,包括大小鼠耳肿胀及局部淋巴结试验,基于上述试验周期长、成本高及尊重动物福利及动物保护等多种因素,化妆品行业内正积极推进动物实验“3r”原则,进一步开展适合化妆品行业特点和实际需求的相关替代方法的研究。目前单一的体外评价模型缺陷在于相关通路不够全面,易出现错筛、漏筛的情况,构建体外舒缓功效评估组合方案有助于在高效的前提下更全面地实现舒缓类化妆品原料的开发和筛选。
3、巨噬细胞主要分布于人体真皮层中,是皮肤免疫应答过程的关键位点之一,内毒素诱导的raw264.7小鼠巨噬细胞模型被广泛用于研究炎症反应,巨噬细胞在外部受到细菌毒素如脂多糖(lps)等刺激时,可促使炎症介质如no、tnf-α、il-6、il-1β等的分泌;thp-1细胞是一种人白血病单核细胞系来源于骨髓的免疫活性细胞,是具有呈递、修饰抗原,启动免疫反应的作用,在这个过程中,lc活化成熟,表现为ii型组织相容性复合物(mhc ii)、共刺激分子cd86和cd54表达上调,同时该细胞系表型较为稳定,在人体的防御系统中起着极为重要的作用;肥大细胞是一种高度特异的分泌细胞,非免疫性刺激(如c48/80)可以直接激活三聚体g蛋白,通过进一步传递信号触发细胞脱颗粒,产生超敏反应,脱颗粒释放的介质会引起平滑肌收缩和微血管通透性升高,引起组织损伤,出现红斑、水肿、糜烂、渗出和瘙痒等表现,因此,敏感性皮肤研究中肥大细胞的效应地位不可取代。
4、现虽有一些化妆品及其原料舒缓功效的评价方法,但是在体实验中人体实验的志愿者招募、管理难度较大,测试周期长,开展的难度较高(湖北省麦诗特生物科技有限公司.一种具有保湿舒缓功效的精华乳组合物及其制备方法和应用:cn202111127654.7[p].2021-09-26.);而动物实验所需成本高,且与“3r”原则理念有所冲突,不适用于大量原料的筛选(广州远想生物科技股份有限公司.具有舒缓功效的护肤品组合物及制备方法:cn202110996084.9[p].2021-08-27);体外实验检测只选择了no验证作为指标,评估手段较为单一,可能出现错漏的情况(广东悠质检测技术有限公司.一种化妆品及其原料的舒缓功效测试方法:cn202111557320.3[p].2021-12-18.)。
5、综上所述,现有的化妆品原料舒缓功效的评价方法皆有一定的技术缺陷或成本限制,尚未有适用于化妆品原料的低成本、多维度、高通量的成体系检测筛选方案,故发明一种多评价维度的化妆品原料体外舒缓功效评估组合方法意义重大。
技术实现思路
1、本发明的目的是克服现有技术的缺陷,提供一种化妆品原料体外舒缓功效评估组合方法,包含急性单核细胞、巨噬细胞、肥大细胞三种细胞模型,组合了分子及表型的评价维度,使得化妆品舒缓原料的体外初步快筛覆盖了多类型免疫细胞,多维度评价手段,构建化妆品原料的舒缓功效综合评价方法,属于系统型评估方法,具快速、高效、全面的优势。
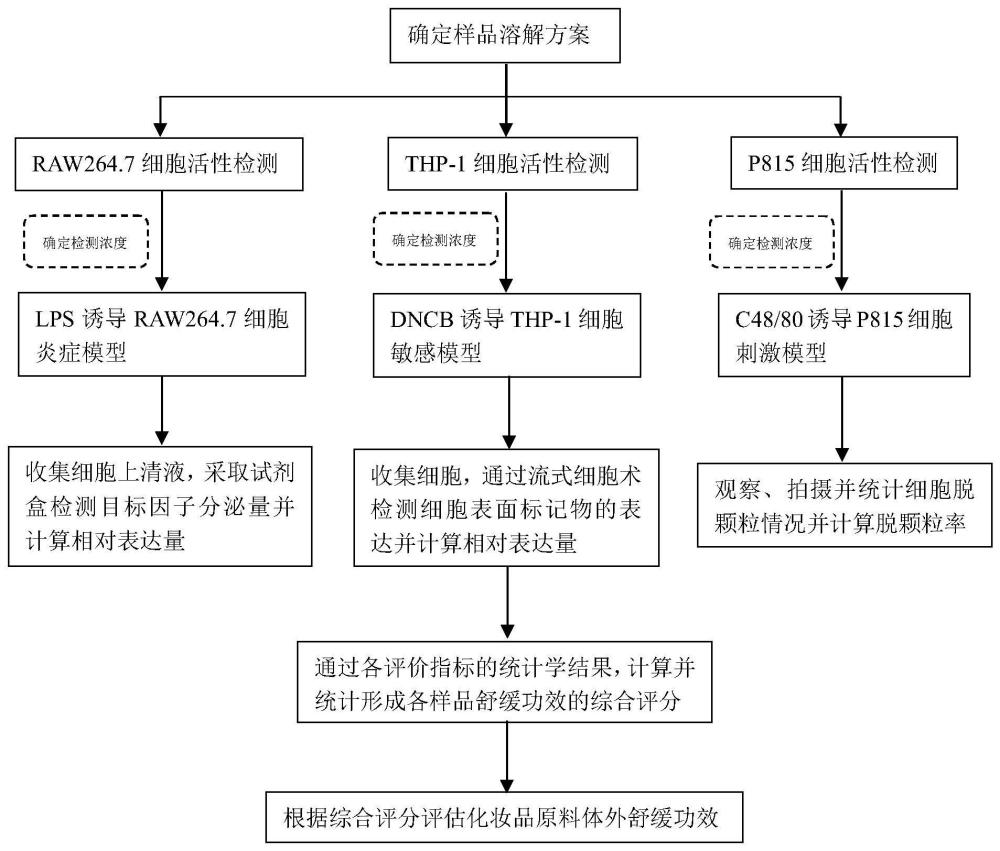
2、实现上述目的的技术方案是:一种化妆品原料体外舒缓功效评估组合方法,结合三种细胞模型检测结果对目标原料的舒缓功效进行评分筛选,包括以下步骤:
3、s1,raw264.7小鼠巨噬细胞培养,thp-1细胞培养,p815小鼠肥大细胞培养;
4、s2,评估原料样品的溶解性,确定溶解方案,通过细胞活性检测确定原料样品检测浓度,包括以下工序:
5、s21,取s1中对数生长raw264.7细胞接种在96孔板培养20h~24h,加入包含若干个不同浓度梯度的原料样品,对照为不添加任何原料样品的培养基溶液,培养18h~24h,mtt法检测细胞活性,计算细胞存活率,筛选得到raw264.7巨噬细胞模型细胞存活率为90%(cv90)时对应的原料样品给药浓度;
6、s22,取s1中对数生长thp-1细胞接种在24孔板中培养20h~24h,加入包含若干个不同浓度梯度的原料样品,对照为不添加任何原料样品的培养基溶液,培养18h~24h后离心收集细胞,先使用含有0.1%fbs的pbs缓冲液清洗,离心收集细胞后加入100μl 7-aad染色液,常温避光孵育10-15min,通过流式细胞仪进行活力分析,筛选得到thp-1细胞存活率为75%(cv75)时对应的原料样品给药浓度;
7、s23,取s1中对数生长p815细胞接种在96孔板培养20h~24h,加入包含若干个不同浓度梯度的原料样品,对照为不添加任何原料样品的培养基溶液,培养18h~24h,mtt法检测细胞活性,计算细胞存活率筛选得到p815肥大细胞模型细胞存活率为90%(cv90)时对应的原料样品给药浓度;
8、s3,取s1中对数生长的raw264.7细胞接种培养16h~24h,设置空白对照组、诱导对照组、阳性对照组及样品组,其中空白对照组及诱导对照组加入完全培养基,阳性对照组加入完全培养基配置的地塞米松(dex)溶液,样品组加入完全培养基配置的s21中选取的raw264.7巨噬细胞模型细胞存活率为90%时对应的给药浓度的原料样品,培养1h~4h后诱导对照组及样品组加入诱导药品脂多糖(lps)溶液,培养16h~24h后分别检测细胞上清液分泌炎症因子no、tnf-α、il-6、il-1β的含量;
9、s4,将s1中对数生长的thp-1细胞接种至24孔细胞培养板,设置空白对照组、诱导对照组、阳性对照组及样品组,空白对照组加入完全培养基,诱导对照组加入完全培养基配置的二硝基氯苯(dncb)溶液诱发敏感模型,阳性对照组加入含相同终浓度dncb配置的dex溶液,样品组加入含相同终浓度dncb配置的s22中选取的thp-1细胞存活率为75%时对应的给药浓度的原料样品,培养18-24h后经由细胞收集、cd86、cd54、7-aad抗体及同型对照染色处理后,通过流式细胞仪检测空白对照组、诱导对照组、阳性对照组及样品组cd86与cd54的表达量;
10、s5,将s1中对数生长的p815细胞接种至24孔细胞培养板培养16~24h,设置空白对照组、诱导对照组、阳性对照组及样品组,空白对照加入无血清培养基,诱导对照组加入由无血清培养基配置的compound 48/80(c48/80),阳性对照加入含相同终浓度c48/80配置的色苷酸钠溶液,样品组加入含相同终浓度c48/80配置的s23中选取的p815肥大细胞模型细胞存活率为90%时对应的给药浓度的原料样品,给药完毕后将孔板放置培养箱中每隔10min观察一次细胞的脱颗粒状态,与空白对照相比诱导对照组40~60%范围内的细胞出现脱颗粒现象时,将孔板放置0℃冰水浴中静置10min终止刺激,显微镜下观察p815肥大细胞并每组选择铺板率相似的5个区域,每个区域拍摄1张照片,统计细胞脱颗粒情况计算脱颗粒率;
11、s6,汇总s3中各组别炎症相关因子测定结果,计算检测样品组分泌量与诱导组分泌量比值得到相对表达量,应用graphpad prism作图,结果表示为mean±sd;各组间比较采用one-way anova统计分析;所有的统计分析均为双尾;
12、p<0.05认为具有显著差异,用“*”表示,说明该受试物具有一定抑制作用,评分为0.3;
13、p<0.01认为具有非常显著差异,用“**”表示,说明该受试物具有显著抑制作用,评分为0.7;
14、p<0.001认为具有极其显著差异,用“***”表示,说明该受试物具有极其显著抑制作用,评分为1.0;
15、s7,汇总s4中各组别目标分子的荧光强度,以诱导对照组的目标分子表达量为基准,计算得到各组cd86与cd54的相对表达量与抑制率,应用graphpad prism作图,结果表示为mean±sd;各组间比较采用one-way anova统计分析;所有的统计分析均为双尾;
16、p<0.05认为具有显著差异,用“*”表示,说明该受试物具有一定抑制作用,评分为0.3;
17、p<0.01认为具有非常显著差异,用“**”表示,说明该受试物具有显著抑制作用,评分为0.7;
18、p<0.001认为具有极其显著差异,用“***”表示,说明该受试物具有极其显著抑制作用,评分为1.0;
19、s8,汇总s5中各组别细胞脱颗粒率,计算检测原料样品组脱颗粒率与诱导组脱颗粒率比值,得到相对脱颗粒率,应用graphpad prism作图,结果表示为mean±sd;各组间比较采用one-way anova统计分析;所有的统计分析均为双尾;
20、p<0.05认为具有显著差异,用“*”表示,说明该受试物具有一定抑制作用,评分为0.3;
21、p<0.01认为具有非常显著差异,用“**”表示,说明该受试物具有显著抑制作用,评分为0.7;
22、p<0.001认为具有极其显著差异,用“***”表示,说明该受试物具有极其显著抑制作用,评分为1.0;
23、根据上述评分标准汇总所有检测指标评分,由此综合评估出舒缓功效更优的化妆品原料。
24、上述的一种化妆品原料体外舒缓功效评估组合方法,其中,s2中所述原料样品为化妆品原料,所述化妆品原料包含化学品、生物制品和植物提取物。
25、上述的一种化妆品原料体外舒缓功效评估组合方法,其中,s3所检测炎症相关因子no、tnf-α、il-6、il-1β中至少有一种构成raw264.7细胞维度评价指标,s4中所述目标分子为细胞表面标记物cd86和细胞表面标记物cd54中至少有一种构成thp-1细胞舒缓评价指标,s5中观察统计的细胞脱颗粒情况构成p815细胞维度舒缓评价指标。
26、上述的一种化妆品原料体外舒缓功效评估组合方法,其中,s2中水中溶解度≥1000μg/ml的原料样品直接溶于培养基进行后续实验;水中溶解度<1000μg/ml的原料样品用二甲基亚砜或乙醇为溶剂溶解后进行后续实验。
27、上述的一种化妆品原料体外舒缓功效评估组合方法,其中,使用二甲基亚砜或乙醇作为溶剂时,溶剂的体积百分比浓度不得超过总体积的1%,且对照组和样品组中溶剂的体积比例相同。
28、上述的一种化妆品原料体外舒缓功效评估组合方法,其中,s1中raw264.7小鼠巨噬细胞采用dmem+10%fbs完全培养基培养,thp-1细胞采用1640+10%fbs完全培养基培养,p815肥大细胞采用dmem+10%fbs完全培养基培养;s5中p815肥大细胞采用无血清高糖dmem基本培养基培养,所有培养条件均为37±0.5℃,(5±1)%co2浓度,湿度95%。
29、上述的一种化妆品原料体外舒缓功效评估组合方法,其中,s21中raw264.7小鼠巨噬细胞以(0.5-2.0)x105个细胞/ml的密度接种于96孔板中,每孔培养基100ul,每种待测原料样品配置5~8个浓度梯度,每个浓度设3个及以上复孔;s3中,raw264.7小鼠巨噬细胞以(0.5-2.0)x105个细胞/ml的密度接种于24孔板中,每孔培养基1000ul,加入lps最终浓度为100ng/ml~10μg/ml,每种原料样品设3个及以上复孔。
30、上述的一种化妆品原料体外舒缓功效评估组合方法,其中,s22中,thp-1细胞以(1.5-2.5)x106个细胞/ml的密度接种于24孔板中,每孔培养基500ul,每种待测原料样品配置5~8个浓度梯度,每个浓度设3个及以上复孔;s4中,thp-1细胞以(1.5-2.5)x106个细胞/ml的密度接种于24孔板中,每孔培养基500ul,dncb最终浓度为5μg/ml,每种原料样品设3个及以上复孔。
31、上述的一种化妆品原料体外舒缓功效评估组合方法,其中,s23中,p815细胞以(0.5-2.0)x105个细胞/ml的密度接种于96孔板中,每孔培养基100ul,每种待测原料样品配置5~8个浓度梯度,每个浓度设3个及以上复孔;s5中,p815细胞以(6.5-7.5)x104个细胞/ml的密度接种于24孔板中,每孔培养基1000ul,加入c48/80最终浓度为40μg/ml,每种原料样品设3个及以上复孔。
32、上述的一种化妆品原料体外舒缓功效评估组合方法,其中,s3中,dex最终浓度为1μg/ml;s4中,dex最终浓度为1μg/ml,s5中,色苷酸钠最终浓度为1000μg/ml,所述缓冲液皆为pbs缓冲液。
33、上述的一种化妆品原料体外舒缓功效评估组合方法,其中,s3中,炎症因子no含量采用no检测试剂盒检测,炎症因子tnf-α、il-6、il-1β含量采用elisa试剂盒检测。
34、上述的一种化妆品原料体外舒缓功效评估组合方法,其中,s6中所分析评价指标为no、tnf-α、il-6、il-1β的相对表达量;s7中所分析评价指标为cd86、cd54的相对表达量;s8中所分析评价指标为的相对脱颗粒率;最终需通过上述7个指标得出所测样品的综合评分,对化妆品原料体外舒缓功效进行评估比较。
35、本发明的化妆品原料体外舒缓功效评估组合方法,包含三种细胞模型,使得化妆品舒缓原料的筛选覆盖了多类型免疫细胞,多维度评价标准,构建化妆品原料的舒缓功效体外评价方法,具有快速、高效、全面的优势。也为舒缓原料的复配方案提供参考依据,也为护肤品行业动物替代实验、皮肤护理产品开发和功效验证的进一步研究提供有效依据。
本文地址:https://www.jishuxx.com/zhuanli/20240808/271007.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表