表面修饰的植物来源细胞外囊泡以及利用其的靶向药物递送载体的制作方法
- 国知局
- 2024-09-05 14:40:45
本发明涉及一种用磷脂进行表面修饰的植物来源的细胞外囊泡、其制备方法以及利用其的药物递送载体或药物组合物。
背景技术:
1、细胞外囊泡(extracellular vesicle)是指包含凋亡小体、微囊泡、外泌体并由小脂质双层包裹的膜颗粒。细胞外囊泡不仅从人类及动物细胞中分泌,还从昆虫、植物、微生物的细胞中分泌。尤其,它们包含细胞所具有的蛋白质、核酸、脂质、碳水化合物等特定分子,由脂质双层包裹而稳定地保护这些分子,并具有分泌后能够将其递送到其他细胞的特性。除了如上所述的各种信号分子的迁移以外,还跨国细胞边界之外在微环境中充当功能分子。因此,近年来进行大量的将细胞外囊泡用作治疗疾病的药物递送平台的研究。但是,以往使用的动物来源的细胞外囊泡存在稳定性问题以及批量生产时的成本可能非常高的缺点。
2、作为替代方案,植物来源细胞外囊泡与哺乳类等动物来源细胞外囊泡相似地将包含蛋白质及rna的生物分子通过细胞外空间递送到受体细胞,从而在介导细胞间通讯中发挥重要作用,并且可以转化为用于mirna及药物等治疗剂的递送载体。但是,植物来源的细胞外囊泡中不存在用于识别人体内的靶标的标记因子。因此,需要研究对植物来源细胞外囊泡的表面进行修饰以具有这种标记因子或对其进行加工以包含可以靶向的成分的技术。
技术实现思路
1、发明目的
2、因此,为了提供植物来源细胞外囊泡作为可以替代以往用作药物递送载体的动物细胞来源细胞外囊泡,本发明人提供包含如马来酰亚胺等官能团的表面成分,以便可以用特定物质对上述植物来源的细胞外囊泡的表面进行修饰,使得可以在人体内靶向并递送药物或在特定部位进行识别,从而完成对于表面修饰的植物来源细胞外囊泡的本发明。
3、因此,本发明的目的在于,提供一种用包含官能团的磷脂进行表面修饰的植物来源细胞外囊泡。
4、本发明的再一目的在于,提供一种包含上述细胞外囊泡的药物递送载体。
5、本发明的另一目的在于,提供一种包含上述细胞外囊泡的药物组合物。
6、本发明的还有一目的在于,提供一种用包含官能团的磷脂对植物来源细胞外囊泡的表面进行修饰的方法。
7、技术方案
8、为了实现如上所述的目的,本发明提供一种用包含官能团的磷脂进行表面修饰的植物来源细胞外囊泡。
9、为了实现本发明的另一目的,本发明提供一种包含上述细胞外囊泡的药物递送载体。
10、为了实现本发明的再一目的,本发明提供一种包含上述细胞外囊泡的药物组合物。
11、为了实现本发明的还有一目的,本发明提供一种用包含官能团的磷脂对植物来源细胞外囊泡的表面进行修饰的方法。
12、以下,将详细说明本发明。
13、作为本发明的一方面,本发明涉及一种用包含官能团的磷脂进行表面修饰的植物来源细胞外囊泡。
14、在本说明书中,术语“细胞外囊泡(extracellular vesicle)”为从各种细胞分泌的膜结构的小囊泡,其直径在约30-1000nm的范围内,具有通过多囊泡体与细胞质膜的融合释放到细胞外环境的特征。细胞外囊泡可以为细胞膜来源囊泡、核外颗粒体(ectosome)、脱落囊泡(shedding vesicles)、微粒(microparticles)、外泌体(exosome)、微囊泡(microvesicle)、外膜囊泡(outer membrane vesicles)、凋亡小体(apoptotic bodies),尤其,本发明中的细胞外囊泡可以为外泌体(exosome)。
15、本发明的植物来源细胞外囊泡尤其可以来源于可食用植物,不仅包含植物的有用成分,并且作为天然来源的物质副作用少且可以通过口服用递送及应用于肠道内。
16、在本说明书中,上述细胞外囊泡是通过用包含官能团的磷脂进行表面修饰的。上述磷脂的种类没有限制,例如,可以为选自由二棕榈酰磷脂酰胆碱(dppc)、二硬脂酰磷脂酰胆碱(dspc)、磷酸胆碱(dopc)、二肉豆蔻酰磷脂酰胆碱(dmpc)、磷脂酰胆碱(plpc)、磷脂酰乙醇胺(pe)、蛋黄磷脂酰胆碱(epc)、二月桂酰磷脂酰胆碱(dlpc)、二肉豆蔻酰磷脂酰胆碱(dmpc)、1-肉豆蔻酰-2-棕榈酰-磷脂酰胆碱(mppc)、1-棕榈酰-2-肉豆蔻酰磷脂酰胆碱(pmpc)、1-棕榈酰-2-硬脂酰磷脂酰胆碱(pspc)、1-硬脂酰-2-棕榈酰磷脂酰胆碱(sppc)、1,2-二硬脂酰-sn-甘油-3-磷酸胆碱(dapc)、1,2-花生酰磷脂酰胆碱(dbpc)、1,2-二(二十碳烯酰基)-sn-甘油-3-磷酸胆碱(depc)、棕榈酰油酰磷脂酰胆碱(popc)、溶血磷脂酰胆碱、二亚油酰磷脂酰胆碱二硬脂酰磷脂酰乙醇胺(dspe)、二肉豆蔻酰磷脂酰乙醇胺(dmpe)、二棕榈酰磷脂酰乙醇胺(dppe)、棕榈酰基油酰基磷脂酰乙醇胺(pope)以及溶血磷脂酰乙醇胺组成的组中的磷脂。
17、并且,上述磷脂可以为包含peg衍生物的peg脂质。“脂质-聚乙二醇(polyethyleneglycol,peg)接合体”、“脂质-peg”、“peg-脂质”、“peg-lipid”或“lipid-peg”是指脂质与peg缀合的形式,是指一侧端部结合有作为亲水性聚合物的聚乙二醇(peg)聚合物的脂质。并且,上述peg可以为在未与脂质结合的一侧结合有官能团的功能化peg(functionalized peg)。在此情况下能够使用的官能团可以为选自由琥珀酰(succinyl)、羧酸(carboxylic acid)、马来酰亚胺(maleimide)、胺基、生物素、氰尿酸(cyanur)以及叶酸(folate)等组成的组中的一种以上。
18、在本发明一实施例中,通过使用将作为磷脂的dspe与作为官能团的peg2000-马来酰亚胺基团(maleimide group)结合的dspe-peg2000-马来酰亚胺(maleimide)(1,2-二硬脂酰-sn-甘油-3-磷脂酰乙醇胺-n-[马来酰亚胺(聚乙二醇)-2000](1,2-distearoyl-sn-glycero-3-phosphoethanolamine-n-[maleimide(polyethylene glycol)-2000]))来对细胞外囊泡的表面进行修饰。上述dspe-peg2000-马来酰亚胺(maleimide)可以如下述化学式所示。
19、化学式1
20、
21、并且,本发明的上述细胞外囊泡还可以包含用于靶向的靶向物质。上述靶向物质不限于肽、核酸、适体、化学配体等类型,并且可以通过点击化学(click chemistry)反应结合到表面。在本发明一实施例中,使用适体作为靶向物质。上述“适体(aptamer)”是指与特定靶标结合的寡核苷酸(通常为20~80nt的dna或rna)。
22、上述适体可以通过结合到与本发明的细胞外囊泡表面的磷脂结合的官能团来对膜结构进行修饰,并可以通过点击化学(click chemistry)反应进行结合,以进行稳定且有效的反应。例如,如本发明一实施例所述,适体包含硫醇基团(thiol group),可以通过细胞外囊泡表面的马来酰亚胺进行结合。
23、作为本发明的再一方面,本发明提供一种包含上述表面修饰的植物来源细胞外囊泡的药物递送载体或药物组合物。
24、在本说明书中,上述“药物递送载体”是指给药到如人类等哺乳动物的包含一种以上治疗药物或核酸分子的药物组合物。药物组合物为“药学上可接受的”,这是指在妥当的医学判断范畴内符合合理的收益/风险并适合与哺乳动物,尤其是人类的组织接触的化合物、物质、组合物和/或给药形式,而没有过度的毒性、刺激、过敏反应以及其他问题并发症。
25、在本发明中,细胞外囊泡可以用作能够携带并递送多肽、肽、蛋白质、膜受体、mrna、sirna、mirna、dna以及化合物等的药物递送载体。
26、并且,本发明涉及一种包含上述表面修饰的植物来源细胞外囊泡的药物组合物,上述药物组合物是指用于预防或治疗疾病的物质。
27、在本说明书中,上述术语“预防”是指可以通过给药本发明的上述药物组合物来抑制疾病或推迟发病的所有行为。
28、在本说明书中,术语“治疗”是指通过给药本发明的上述药物组合物使症状好转或有益地改善的所有行为。
29、本发明的上述药物组合物可以根据常规方法剂型化成散剂、颗粒剂、片剂、胶囊剂、混悬液、乳液、糖浆、气溶胶等口服型剂型;外用剂;栓剂以及无菌注射溶液的形式使用,还可以包含上述剂型化所需的载体或赋形剂等。可以进一步包含在上述有效成分中的药学上可接受的载体、赋形剂以及稀释剂包括乳糖、葡萄糖、蔗糖、山梨糖醇、甘露糖醇、木糖醇、赤藓糖醇、麦芽糖醇、淀粉、阿拉伯橡胶、海藻酸盐、明胶、磷酸钙、硅酸钙、纤维素、甲基纤维素、微晶纤维素、聚乙烯吡咯烷酮、水、羟基苯甲酸甲酯、羟基苯甲酸丙酯、硬脂酸镁以及矿物油等。当进行剂型化时,可以使用常用的填充剂、增量剂、粘合剂、润湿剂、崩解剂、表面活性剂等稀释剂或赋形剂来制备。
30、例如,用于口服给药的固体制剂包括片剂、丸剂、散剂、颗粒剂、胶囊剂等,这种固体制剂通过在上述提取物或化合物中混合一种以上如面、淀粉、碳酸钙(calciumcarbonate)、蔗糖(sucrose)或乳糖(lactose)、明胶等赋形剂来制备。并且,除了简单的赋形剂以外,还可以使用如硬脂酸镁、滑石粉等润滑剂。用于口服给药的液体制剂包括悬浮剂、内用液剂、乳剂、糖浆剂等,除了常用的水、液体石蜡等简单稀释剂以外,可以包含各种赋形剂,例如,润湿剂、甜味剂、芳香剂、保存剂等。
31、用于肠胃外给药的制剂包括无菌水溶液、非水溶性溶剂、悬浮剂、乳剂、冻干制剂、栓剂。可以使用丙二醇(propylene glycol)、聚乙二醇、如橄榄油等植物油、如油酸乙酯等可注射的酯作为非水溶性溶剂以及悬浮剂。可以使用半合成脂肪酸酯(witepsol)、聚乙二醇、吐温(tween)61、可可脂、月桂酸甘油酯、甘油明胶等作为栓剂的基质。
32、本发明的药物组合物可以根据所需方法由口服或肠胃外给药(静脉注射、皮下、腹腔内或局部应用),给药量根据患者的状态及体重、疾病的严重程度及药物形式、给药途径及时间而异,并且可以由本领域的普通技术人员选择合适的形式。
33、本发明的上述药物组合物可以以药学有效量给药。在本发明中,“药学有效量”是指适于医学治疗的合理的、足以治疗疾病的量,其标准可以取决于患者的疾病、严重程度、药物活性、对药物的敏感性、给药时间、给药途径以及排泄率、治疗时间、联合使用的成分以及其他事项。本发明的上述药物组合物可以以单独治疗剂给药或与其他治疗剂联合给药,可以与现有的治疗剂依次或同时给药。考虑到所有上述因素,可以将给药量确定在使副作用最小化的水平,并且这可以由本领域的普通技术人员容易地确定。具体地,上述药物组合物的给药量可以根据患者的年龄、体重、严重程度、性别等而异,通常,每1kg的体重以0.001mg至150mg,更优选地,可以每天或隔天以0.01mg至100mg的量给药,1天1次至3次。但是,这只是一个例子,上述给药量可以根据需要进行不同的设定。
34、作为本发明的另一方面,本发明涉及一种用包含官能团的磷脂对植物来源细胞外囊泡的表面进行修饰的方法,上述方法包括如下步骤。
35、步骤1)从植物中得到细胞外囊泡;
36、步骤2)用包含官能团的磷脂对所得的上述细胞外囊泡的表面进行修饰;以及
37、步骤3)通过点击化学反应结合靶向物质。
38、上述步骤1)可以通过已知的通过植物的粉碎物、提取物等得到囊泡的方法进行,例如,可以通过离心植物粉碎物、榨汁液或提取物以得到剩余颗粒(pellet)来进行。上述过程不限于方法,还可以使用超速离心机(ultracentrifuge)、体积排除色谱(sizeexclusion chromatography)或细胞外囊泡分离试剂盒。
39、上述步骤2)中对细胞外囊泡的表面进行修饰的步骤可以使用如上所述的各种类型的磷脂,优选地,可以利用dpse-peg(2000)-马来酰亚胺(maleimide)进行表面修饰。
40、上述步骤3)的靶向物质的类型可以根据携带的药物的靶标而异,只要是能够通过上述细胞外囊泡的表面修饰的官能团及点击化学反应结合的都可以包括而没有限制。
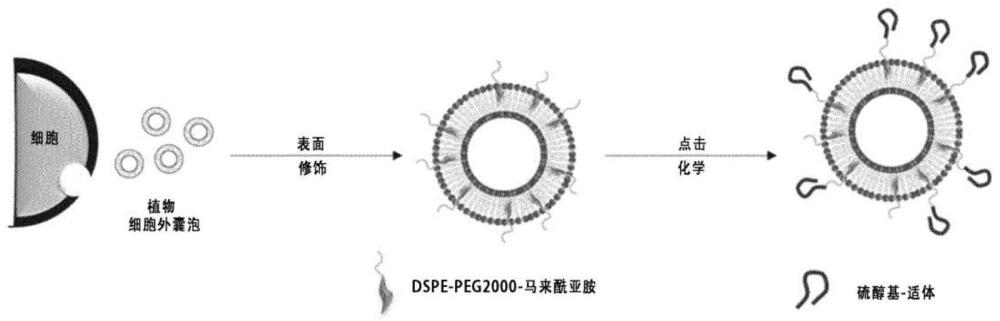
41、用磷脂进行表面修饰的细胞外囊泡的官能团暴露于囊泡外部。本发明一实施例的dpse-peg(2000)-马来酰亚胺(maleimide)的磷脂位于细胞外囊泡的表面膜上,在此情况下,dspe位于组成细胞外囊泡表面的磷脂之间,并且peg2000-马来酰亚胺(maleimide)部分暴露于细胞外囊泡的外部。当能够赋予特定靶标能力的靶向物质中包含硫醇基团(-sh基团,thiol group))时,在将其与包含暴露于外部的peg2000-马来酰亚胺基团(maleimidegroup)的表面修饰的细胞外囊泡一起进行培养的情况下,通过点击化学结合上述马来酰亚胺-硫醇(maleimide-thiol),使靶向物质结合到细胞外囊泡表面。
42、上述细胞外囊泡的表面修饰物以及靶向物质的结合不限于官能团的类型,只要是通过点击化学结合的官能团即可。
43、有益效果
44、本发明涉及一种用包含官能团的磷脂以及靶向物质进行表面修饰的植物来源的细胞外囊泡以及利用其的药物递送载体或药物组合物,来源于植物且经济实惠,有效制备稳定的细胞外囊泡,从而具有可以将其应用于各种药物递送的效果。
本文地址:https://www.jishuxx.com/zhuanli/20240905/287610.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
上一篇
RNA分子的制作方法
下一篇
返回列表