一种CHOHCD残留检测试剂盒及其检测方法与流程
- 国知局
- 2024-11-19 09:56:51
本发明涉及分析检测相关,具体为一种cho hcd残留检测试剂盒及其检测方法。
背景技术:
1、cho细胞即中国仓鼠卵巢细胞(chinese hamster ovary),该细胞具有不死性,可以传代百代以上,是目前生物工程上广泛使用的细胞。全世界批准正式应用于人类疾病治疗或疾病预防的基因工程产品约有三十多种,其中cho表达系统能准确的转录后修饰表达的蛋白在分子结构、理化特性和生物学功能,使它最接近于天然蛋白分子;其次,cho细胞既可贴壁生长,又可以悬浮培养,有较高的耐受剪切力和渗透压能力,培养体积能达到1000l以上;再次,cho细胞具有重组基因的高效扩增和表达能力;而且cho具有产物胞外分泌功能,并且很少分泌自身的内源蛋白,便于下游产物分离纯化。因此cho成为表达复杂生物大分子的理想宿主。
2、其中hcd是一种质谱技术,常用与蛋白质的鉴定和分析,虽然,cho分泌的内源蛋白很少但是依然会有少量蛋白残留在生物制品的半成品或成品中,因此需要进行进行蛋白检测,其中外源蛋白,其潜在的免疫原性有可能诱导机体产生相应抗体;其潜在的“佐剂效应”也可能会引起机体对药物产生抗体,进而影响药物的疗效。灵敏度高、重复性好的宿主蛋白检测方法不仅是保证生物制品安全有效的关键,也是生产过程控制和工艺优化的重要参数。由于hcd可能会引起不可预测的免疫反应,因此相关法规要求对hcd进行鉴定和定量,以保障患者使用安全。hcp残留检测是生物药能否成功获批的重要因素之一。
3、传统的高效液相色谱法的前处理过程复杂,需要经过繁琐的衍生标记,费时费力且衍生试剂毒性大,培养物基质干扰严重,单个样品分析测试时间长导致单位时间内检测分析样品量少,效率低下,检测通量与自动化程度低。
技术实现思路
1、为解决现有技术存在cho的残留检测的方法主要是高效液相色谱法。传统的高效液相色谱法的前处理过程复杂,需要经过繁琐的衍生标记,费时费力且衍生试剂毒性大,培养物基质干扰严重,单个样品分析测试时间长导致单位时间内检测分析样品量少,效率低下,检测通量与自动化程度低的缺陷,本发明提供一种cho hcd残留检测试剂盒及其检测方法。
2、为了解决上述技术问题,本发明提供了如下的技术方案:
3、本发明一种cho hcd残留检测试剂盒,包括溶剂、滤纸、缓冲剂;
4、溶剂为乙醇;
5、缓冲剂为50~200mmol/l的磷酸盐溶液;
6、作为本发明的一种优选技术方案,一种cho hcd残留检测试剂盒的检测方法,其特征在于,所述的方法包括以下步骤:
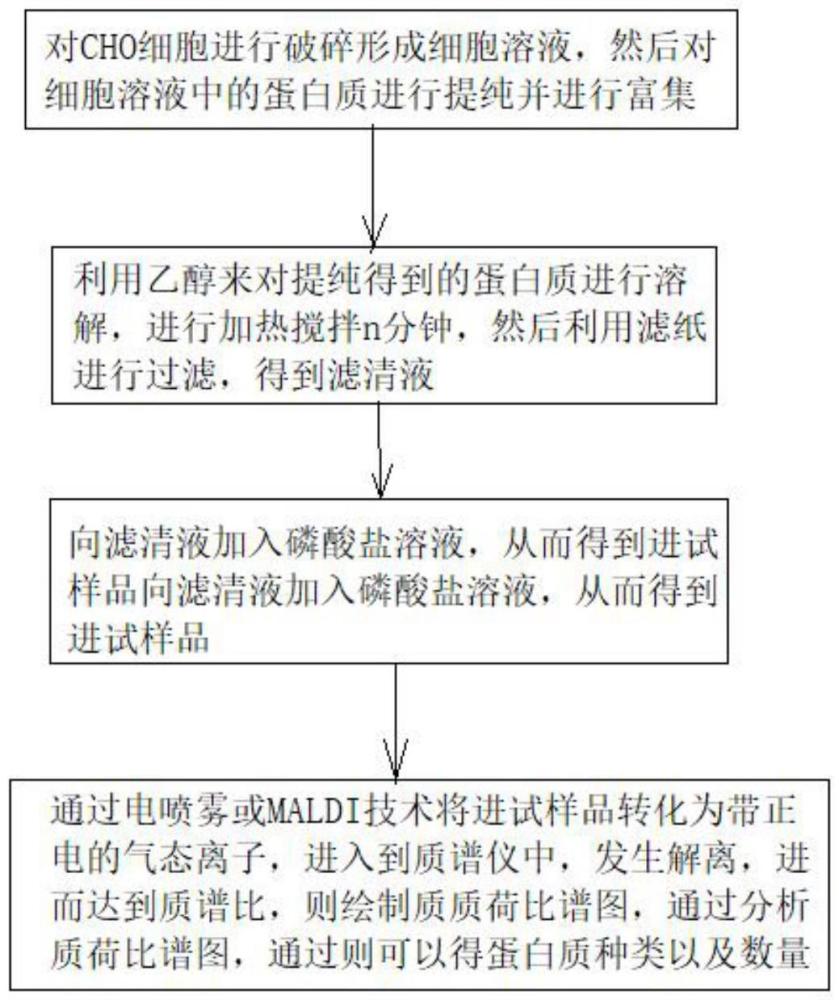
7、步骤1、对cho细胞进行破碎形成细胞溶液,然后对细胞溶液中的蛋白质进行提纯并进行富集;
8、步骤2、利用乙醇来对提纯得到的蛋白质进行溶解,进行加热搅拌n分钟,然后利用滤纸进行过滤,得到滤清液;
9、步骤3、向滤清液加入磷酸盐溶液,从而得到进试样品;
10、步骤4、通过电喷雾或maldi技术将进试样品转化为带正电的气态离子,进入到质谱仪中,发生解离,进而达到质谱比,则绘制质质荷比谱图,通过分析质荷比谱图,通过则可以得蛋白质种类以及数量。
11、作为本发明的一种优选技术方案,所述的步骤1中对细胞溶液中的蛋白质进行提纯并进行富集的方法是,包括以下步骤:
12、步骤1、取待分离纯化细胞溶液的样品,用无机盐水溶液溶解或稀释,混匀得到混合溶液;
13、步骤2:将低共熔溶剂和步骤1中的混合溶液混合均匀,然后离心得到液-液两相体系,收集下相萃取液;
14、步骤3、将步骤4中的下相萃取液用水稀释,混合均匀后离心得到液-固两相体系;
15、步骤4、将步骤3中的固相用水溶解,并进行超滤离心,除去残留的低共熔溶剂组分和无机盐,得到蛋白质溶液;
16、步骤5、将步骤4中的蛋白质溶液冷冻干燥,即得蛋白质纯品。
17、作为本发明的一种优选技术方案,所述步骤1中,当待分离纯化蛋白质的样品为蛋白质标准品时,混合溶液中蛋白质的浓度为2.5-15mg/ml,当待分离纯化蛋白质的样品为含蛋白质的生物样品时,生物样品与无机盐水溶液的体积比范围为1:10-100。
18、作为本发明的一种优选技术方案,所述步骤1中,无机盐为硫酸钠、磷酸氢二钾中的至少一种,无机盐水溶液的ph为7-10,所述步骤a2中,液-液两相体系中,无机盐的质量百分比为0.8%-6.04%。
19、作为本发明的一种优选技术方案,所述的低共熔溶剂由季铵盐和六氟异丙醇配制而成,液-液两相体系中,低共熔溶剂的-质量百分比为19.53%-54.82。
20、作为本发明的一种优选技术方案,所述季铵盐为氯化胆碱和/或四甲基氯化铵。
21、作为本发明的一种优选技术方案,所述的步骤2中采用振荡或者涡旋将低共熔溶剂和混合溶液混匀,其中,振荡速率为500-1500rpm,振荡时间为0-30min,振荡温度为15-55℃;涡旋功率为60w,涡旋时间为0-30min;离心转速为2000-6000rpm,离心时间为3-15min,所述步骤b1中,采用涡旋将下相萃取液和水混匀,其中,涡旋功率为60w,涡旋时间为1-15min;离心转速为2000-6000rpm,离心时间为3-15min。
22、本发明的有益效果是:
23、该种宿cho hcd残留检测试剂盒的检测方法在对cho细胞进行破碎形成细胞溶液,然后对细胞溶液中的蛋白质进行提纯并进行富集,利用乙醇来对提纯得到的蛋白质进行溶解,进行加热搅拌n分钟,然后利用滤纸进行过滤,得到滤清液;向滤清液加入磷酸盐溶液,从而得到进试样品;通过电喷雾或maldi技术将进试样品转化为带正电的气态离子,进入到质谱仪中,发生解离,进而达到质谱比,则绘制质质荷比谱图,通过分析质荷比谱图,通过则可以得蛋白质种类以及数量,这样将各个蛋白质通过质谱离子源电离用于质谱分析,能够有效降低样本需求量,降低样本前处理难度,增加蛋白质的在线分离度,准确鉴定出宿主细胞的数量和种类,而方便对cho细胞进行蛋白质残留鉴定。
技术特征:1.一种cho hcd残留检测试剂盒,其特征在于,包括溶剂、滤纸、缓冲剂;
2.根据权利要求1所述的一种cho hcd残留检测试剂盒的检测方法,其特征在于,所述的方法包括以下步骤:
3.根据权利要求2所述的一种cho hcd残留检测试剂盒的检测方法,其特征在于,所述的步骤1中对细胞溶液中的蛋白质进行提纯并进行富集的方法是,包括以下步骤:
4.根据权利要求3所述的一种cho hcd残留检测试剂盒的检测方法,其特征在于,所述步骤1中,当待分离纯化蛋白质的样品为蛋白质标准品时,混合溶液中蛋白质的浓度为2.5-15mg/ml,当待分离纯化蛋白质的样品为含蛋白质的生物样品时,生物样品与无机盐水溶液的体积比范围为1:10-100。
5.根据权利要求3所述的一种cho hcd残留检测试剂盒的检测方法,其特征在于,所述步骤1中,无机盐为硫酸钠、磷酸氢二钾中的至少一种,无机盐水溶液的ph为7-10,所述步骤a2中,液-液两相体系中,无机盐的质量百分比为0.8%-6.04%。
6.根据权利要求3所述的一种cho hcd残留检测试剂盒的检测方法,其特征在于,所述的低共熔溶剂由季铵盐和六氟异丙醇配制而成,液-液两相体系中,低共熔溶剂的-质量百分比为19.53%-54.82%。
7.根据权利要求3所述的一种cho hcd残留检测试剂盒的检测方法,其特征在于,所述季铵盐为氯化胆碱和/或四甲基氯化铵。
8.根据权利要求3所述的一种cho hcd残留检测试剂盒的检测方法,其特征在于,所述的步骤2中采用振荡或者涡旋将低共熔溶剂和混合溶液混匀,其中,振荡速率为500-1500rpm,振荡时间为0-30min,振荡温度为15-55℃;涡旋功率为60w,涡旋时间为0-30min;
技术总结本发明公开了一种CHO HCD残留检测试剂盒及其检测方法,包括溶剂、滤纸、缓冲剂;溶剂为乙醇;缓冲剂为50~200mmol/L的磷酸盐溶液;对CHO细胞进行破碎形成细胞溶液,然后对细胞溶液中的蛋白质进行提纯并进行富集;步骤2、利用乙醇来对提纯得到的蛋白质进行溶解,进行加热搅拌n分钟,然后利用滤纸进行过滤,得到滤清液;步骤3、向滤清液加入磷酸盐溶液,从而得到进试样品;步骤4、通过电喷雾或MALDI技术将进试样品转化为带正电的气态离子,进入到质谱仪中,发生解离,进而达到质谱比,则绘制质质荷比谱图,通过分析质荷比谱图,通过则可以得蛋白质种类以及数量;本发明采用的样本前处理方法过程简易,成本低,样本需求量少。技术研发人员:师要辉,马艳,沈治峰受保护的技术使用者:上海蓝析生物技术有限公司技术研发日:技术公布日:2024/11/14本文地址:https://www.jishuxx.com/zhuanli/20241118/330799.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。