生物补片及其制备方法和在软组织修复方面的应用与流程
- 国知局
- 2024-07-12 10:34:46
本发明涉及生物医用材料,特别涉及生物医用修复材料,具体涉及生物补片及其制备方法和在软组织修复方面的应用。
背景技术:
1、交通事故、工伤事故、运动意外及临床手术等事件经常会造成软组织损伤,然而软组织缺损的修复与再生始终是临床上的难题。目前,临床上一般使用生物补片作为替代和修复软组织的材料。
2、生物补片通常指取自同种或异种组织,具有经脱细胞处理去除组织中细胞成分而完整保留细胞外基质的三维框架结构,并能用于修复软组织的材料。生物补片具有良好的组织兼容性,可通过空间诱导和组织替代作用修复受损组织。近年来,生物补片被广泛应用于硬脑脊膜缺损修复、运动肌腱撕裂修复、疝及腹壁缺损的修复、烧伤整形、口腔膜缺损修复等多个方面。
3、适用于临床应用的理想的生物补片通常需要满足如下的综合性能:良好的组织兼容性、低毒性、低免疫排斥性、低病毒感染风险、适合的机械强度、与组织再生相匹配的降解速率等。
4、在生物补片的多种性能中,适合的机械强度起到关键支撑作用。然而,传统的生物补片机械强度较低,容易引发术后并发症,难以满足临床理想需求。对此,在制备生物补片的过程中,通常采用物理或/和化学方法来增强补片的力学性能,以期达到韧性好、拉伸强度高等方面的力学性能要求。比如,已有文献报道采用交联剂对生物补片进行交联处理以增强力学性能,然而,交联程度很难稳定控制,而且残留的交联剂具有潜在的细胞毒性,此外,还存在降解速率与组织再生不能同步匹配的问题。
5、此外,生物补片主要以异体和异种组织为主,因此存在免疫排斥和病毒感染等风险。对此,往往需要通过脱细胞过程和病毒灭活过程去除组织中的抗原,以降低病毒感染风险。但是,一方面,传统工艺脱细胞过程容易破坏组织补片结构完整性,导致力学性能严重下降,不利于生物补片在临床修复中的应用;另一方面,目前针对生物补片的脱细胞方法非常复杂,还会增加产品转化难度,而且一般需要使用强交联剂增强补片力学性能,而残留试剂容易导致材料严重的细胞毒性,还易加剧组织炎症反应。
技术实现思路
1、基于此,本发明的目的包括提供生物补片的制备方法,工艺简单,并可以兼顾生物补片的力学性能,本发明的方法可制备得到单层或多层生物补片,制备得到的生物补片可以用于软组织修复。
2、在本发明的第一方面,提供一种单层生物补片的制备方法,其包括如下步骤:
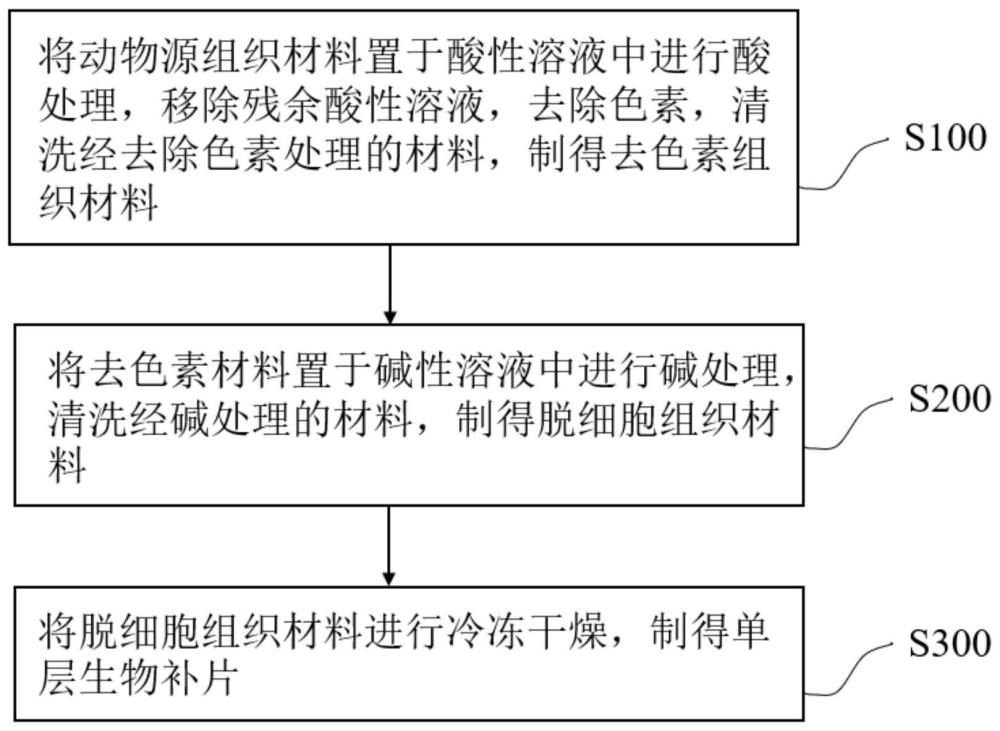
3、将动物源组织材料于酸性溶液中对进行酸处理,移除残余酸性溶液,去除色素,清洗经去除色素处理的材料,制得去色素组织材料;其中,所述动物源组织材料经过去除血液和去脂处理;所述酸性溶液为含有酸性试剂的水溶液;
4、将所述去色素组织材料于碱性溶液中进行碱处理,清洗经碱处理的材料,制得脱细胞组织材料;其中,所述碱性溶液为含有碱性试剂的水溶液;
5、将所述脱细胞组织材料进行预冻,在真空条件下冷冻干燥,制得所述单层生物补片。
6、在一些实施方式中,所述单层生物补片的制备方法满足如下特征中的一个或多个:
7、所述动物源组织材料为鱼皮;
8、所述动物源组织材料为片状,厚度为0.5mm~2mm;
9、所述单层生物补片的厚度为0.1mm~1mm。
10、在一些实施方式中,所述单层生物补片的制备方法满足如下特征中的一个或多个:
11、所述酸性试剂选自醋酸、柠檬酸、盐酸、甲酸、硫酸和硝酸中的一种或多种;
12、所述酸性试剂在所述酸性溶液中的浓度为1mm~500mm;
13、所述酸性溶液的ph值为1~5;
14、所述酸处理的时间为1min~60min;
15、所述去除色素采用刮除、搅拌和振荡中一种或多种方式;
16、采用水对所述经去除色素处理的材料进行振荡清洗;其中相对于所述经去除色素处理的每1g材料,用水体积为10ml~30ml;清洗次数为1次或多次,每次清洗5min~15min。
17、在一些实施方式中,所述单层生物补片的制备方法满足如下特征中的一个或多个:
18、所述碱性试剂选自碳酸钠、碳酸氢钠、磷酸三钠、磷酸一氢钠、磷酸氢二钠、氢氧化钠、碳酸钾、碳酸氢钾、磷酸三钾、磷酸一氢钾、磷酸氢二钾和氢氧化钾中的一种或多种;
19、所述碱性试剂在所述碱性溶液中的浓度为0.01mol/l~2mol/l;
20、所述碱性溶液的ph值为9~13;
21、所述碱处理于20℃~30℃在振荡条件下进行;其中,振荡频率为100rpm~200rpm;
22、所述碱处理的时间为6h~30h;
23、采用水对所述经碱处理的材料进行振荡清洗;其中相对于所述经碱处理的每1g材料,用水体积为10ml~50ml;清洗次数为1次或多次,每次清洗1min~12min。
24、在一些实施方式中,所述单层生物补片的制备方法满足如下特征中的一个或多个:
25、所述预冻于-80℃至-76℃进行;
26、所述预冻冷的时间为20h~24h;
27、所述冷冻干燥于20℃~30℃进行;
28、所述冷冻干燥于38pa~42pa进行;
29、所述冷冻干燥的时间为45h~50h。
30、在本发明的第二方面,提供一种多层生物补片的制备方法,其包括如下步骤:将多个单层生物补片经粘合、压合、干燥制成多层生物补片,或者经缝合制成多层生物补片;其中,所述单层生物补片采用本发明第一方面所述的制备方法制备得到。
31、在一些实施方式中,将多个所述单层生物补片经粘合、压合、干燥制成多层生物补片包括如下步骤:
32、采用胶粘液将所述多个单层生物补片粘合成多层材料;其中,相邻的任两个所述单层生物补片之间均填充有所述胶粘液;其中,所述胶粘液为含有胶粘剂的水溶液;
33、将所述多层材料进行压合处理;
34、将经压合处理的所述多层材料进行真空干燥。
35、在一些实施方式中,所述多层生物补片的制备方法满足特征中的一个或多个:
36、所述多层材料包括2、3或4个所述单层生物补片;
37、任意相邻的两个所述单层生物补片的相邻面之间,每平方厘米的粘合面之间的所述胶粘液的体积独立地为0.05ml~0.5ml;
38、所述胶粘剂选自丝素蛋白、明胶、羟乙基纤维素、羟甲基纤维素、聚乳酸、聚己内酯和聚乙醇酸中的一种或多种材质;
39、所述胶粘剂在所述胶粘液中的质量体积浓度为10%~30%(w/v);
40、所述压合处理的温度条件为35℃~37℃;
41、所述压合处理的压力条件为0.1mpa~0.5mpa;
42、所述压合处理的时间为0.5h~3h;
43、所述真空干燥的压力条件为0.9pa~1.1pa;
44、所述真空干燥的温度条件为25℃~37℃;
45、所述真空干燥的时间为1h~3h;
46、所述多层生物补片的厚度为0.5mm~2mm。
47、在一些实施方式中,将多个所述单层生物补片经缝合制成多层生物补片包括如下步骤:
48、将多个所述单层生物补片层叠成多层叠片;
49、将所述多层叠片采用缝合线于预设位置进行缝合。
50、在一些实施方式中,所述多层生物补片的制备方法满足特征中的一个或多个:
51、所述多层叠片包括2、3或4个所述单层生物补片;
52、所述缝合线选自聚乳酸缝合线、聚乙醇酸缝合线、聚酯缝合线和蚕丝缝合线中的一种或多种;
53、每平方厘米的层叠面积所需的缝合长度为0.5cm~2cm;其中,所述层叠面积指多个所述单层生物补片在所述多层叠片中的横向重叠部分;
54、所述多层叠片的缝合面上任一点距离最近缝合轨迹的最短距离≤1.6cm;
55、所述多层生物补片的厚度为0.5mm~2mm。
56、在本发明的第三方面,提供一种生物补片,其采用本发明第一方面或第二方面所述的制备方法制备得到。
57、在本发明的第四方面,提供本发明第三方面所述生物补片在制备软组织修复植入材料中的应用。
58、在一些实施方式中,所述的应用包括硬脑脊膜缺损修复、运动肌腱撕裂修复、疝及腹壁缺损的修复、烧伤整形修复和口腔膜缺损修复中的一种或多种。
59、本发明提供了单层生物补片的制备方法以及采用单层生物补片制备多层补片的方法。在单层补片的制备方法中,采用酸碱联合处理的方法脱细胞,工艺简单,处理试剂残余基本为无,细胞毒性低,还能保持良好的力学性能,易于转化为适于临床使用的产品。该方法利用酸碱中和简单有效地脱除细胞后,还使得酸碱联合处理后的残余试剂基本为无,细胞毒性低;而且酸碱联合处理的脱细胞方法对生物补片结构影响较小,有利于保持良好的力学性能。此外,原材料来源广泛且成本低廉,而且工艺过程绿色环保。在多层生物补片的制备方法中,基于制备得到的单层补片,还联合叠层技术,采用简单有效的多层复合工艺(可使用粘合剂或缝合技术)进一步提高生物补片的力学性能。进一步地,前述方法制备得到的生物补片(包括单层生物补片和多层生物补片)可用于软组织修复,可针对不同的损伤部位大小进行相适应的裁剪,方便临床使用,还能满足多种不同组织损伤修复中对生物补片生物相容性、力学性能、尺寸等方面的多重要求。
本文地址:https://www.jishuxx.com/zhuanli/20240614/87833.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表