使用间充质干细胞进行分层细胞片的工程化的制作方法
- 国知局
- 2024-08-08 17:05:37
背景技术:
1、已有关于细胞片(cell sheets)的研究报告。例如,欧洲专利号2266500讨论了能够经受植入手术的假体组织或片,以及用来源于除心肌以外的部分的细胞生产该假体组织或片。
2、据称,欧洲专利号1857126提供了“一种用于生产根据权利要求1所述的培养的细胞片的方法,其包含在细胞培养支持物上培养至少一种类型的细胞的步骤,所述细胞选软骨细胞、软骨祖细胞、滑膜来源细胞、滑膜来源干细胞、成骨细胞、间充质干细胞、脂肪来源细胞和脂肪来源干细胞,细胞培养支持物的支持物表面涂覆有温度响应性聚合物,该温度响应性聚合物在水中具有0℃至80℃的上限或下限临界溶解温度,此后,包含以下步骤:(1)将培养基的温度调节至高于上限临界溶解温度或低于下限临界溶解温度的温度;(2)使培养的细胞片与载体紧密接触;以及(3)将培养的细胞片与载体一起脱离。”第[0013]段。
3、据称,sato等人在regenerative medicine(2019)4中陈述“目前的软骨再生疗法在治疗膝骨关节炎(oak)方面并非完全有效。我们已经开发了用于自体移植的软骨细胞片,并在体外和体内临床前研究中进行了测试,并且报道了软骨细胞片的移植促进大鼠、兔和小型猪模型中的透明软骨修复。然而,软骨细胞片的自体移植在人类中还未见报道。这里,我们报告了我们的联合疗法,在传统手术治疗oak后,进行自体软骨细胞片移植进行软骨修复。”摘要。
4、据称,thorp等人在cells 2021,10,643中陈述了以下内容:“关节软骨缺陷代表了未来骨关节炎(oa)和退行性关节疾病进展的诱发因素。尽管多种临床可用的疗法成功地减轻了短期疼痛并恢复了有限活动能力,但目前的治疗方法无法可靠地再生天然透明软骨或阻止这些缺损部位的软骨退化。旨在解决当前临床软骨再生疗法局限性的新疗法越来越多地关注同种异体细胞,特别是间充质干细胞(msc),作为表达软骨形成谱系定向能力的有效、分段且可用的细胞来源。采用同种异体间充质干细胞的创新组织工程化方法旨在开发三维(3d)软骨分化结构,用于直接和即时替代透明软骨,改善局部组织整合并优化治疗效果。在新兴的组织工程化技术中,基于可控的3d细胞相互作用和保留的细胞粘附分子,细胞片组织工程化的进步为实现体外透明样分化和有效移植提供了前景广阔的能力。”摘要。
5、尽管已有各种报道,但本领域仍需要与细胞片生产相关的新型工程化技术。
技术实现思路
1、在方法方面,本发明提供了一种使用脂肪基质细胞、骨髓干细胞或脐带干细胞来生产细胞片的方法。在一个实施方案中,该方法包含以下步骤:a)将细胞培养表面与细胞外基质接触,以使细胞附着于该表面;b)在细胞外基质接触的细胞培养表面上接种细胞;c)向细胞中加入化学限定培养基;d)在标准大气下在预定温度下培养细胞;e)监测来自细胞的细胞片的生长,直至获得预定的监测值;f)使用机械或细胞片处理对细胞片进行工程化,从而生产细胞片。
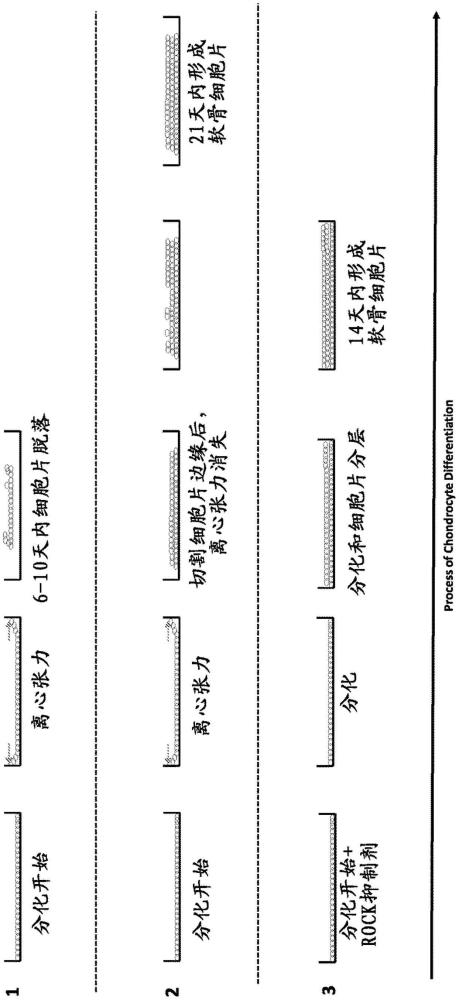
2、在另一个实施方案中,本发明提供了一种制备细胞片的方法,包含:在培养基中在容器的细胞培养表面上培养多个干细胞,向容器中加入分化培养基和rho激酶(rock)抑制剂,其中分化培养基和rock抑制剂在2天内相继加入,以及从细胞培养表面脱离由干细胞分化的细胞形成的细胞片。
3、在另一个实施方案中,提供了一种生产细胞片的方法,包含:在培养基中在容器的细胞培养表面上培养多个干细胞,在分化培养基中分化干细胞,去除生长至与容器的壁接触的细胞,以及从细胞培养表面脱离由干细胞分化的细胞形成的细胞片。
4、在一些实施方案中,干细胞是脂肪基质细胞、骨髓干细胞、间充质干细胞或脐带干细胞。在一些实施方案中,由干细胞分化的细胞是软骨细胞或成骨细胞。
5、在一些实施方案中,分化培养基和rock抑制剂在2天内相继加入。在一些实施方案中,在加入分化培养基后24小时内加入rock抑制剂。在一些实施方案中,rock抑制剂选自y-27632、y-33075和h-1152。在一些实施方案中,加入rock抑制剂以达到1μm至20μm的浓度。
6、另一个实施方案提供了一种修复患者的软骨的方法,该患者具有受损或不健康软骨,包含将通过本文公开的方法制备的细胞片的一部分植入患者体内存在受损或不健康软骨的部位。
7、另一个实施方案提供了一种治疗患有骨关节炎的患者的骨关节炎或骨软骨缺损的方法,包含将通过本文公开的方法制备的细胞片的一部分植入患者体内存在与骨关节炎相关的受损或不健康组织或存在骨软骨缺损的部位。
技术特征:1.一种制备细胞片的方法,其包含:
2.根据权利要求1所述的方法,其中所述细胞培养表面涂覆有细胞外基质。
3.根据权利要求1或2所述的方法,其中所述培养基是化学限定培养基。
4.根据权利要求1至3中任一项所述的方法,其还包含在加入所述分化培养基之前计数干细胞的数量,其中所计数的数量用于确定所述分化的持续时间。
5.根据权利要求1至4中任一项所述的方法,其中所述脱离通过机械工具进行。
6.根据权利要求1至5中任一项所述的方法,还包含去除生长至与所述容器的壁接触的细胞。
7.根据权利要求6所述的方法,其中所述去除包含用机械工具切割所述细胞片的边缘。
8.根据权利要求1至7中任一项所述的方法,其中所述干细胞选自脂肪基质细胞、骨髓干细胞、间充质干细胞和脐带干细胞。
9.根据权利要求1至8中任一项所述的方法,其中由所述干细胞分化的细胞是软骨细胞或成骨细胞。
10.根据权利要求1至9中任一项所述的方法,其中所述分化培养基和所述rock抑制剂在1天内相继加入。
11.根据权利要求1至10中任一项所述的方法,其中在加入所述分化培养基后24小时内加入所述rock抑制剂。
12.根据权利要求1至11中任一项所述的方法,其中所述rock抑制剂选自y-27632、y-33075和h-1152。
13.根据权利要求1至12中任一项所述的方法,其中加入所述rock抑制剂以达到1μm至20μm的浓度。
14.根据权利要求1至13中任一项所述的方法,其中所述细胞片包含5×106至7×106个细胞。
15.根据权利要求1至14中任一项所述的方法,其中所述细胞片是多层细胞片。
16.根据权利要求1至15中任一项所述的方法,其中所述细胞片在脱离后沿任一长度方向收缩不超过20%。
17.一种生产细胞片的方法,其包含:
18.根据权利要求17所述的方法,其中所述去除包含用机械工具切割所述细胞片的边缘。
19.根据权利要求17或18所述的方法,其还包含向所述容器中加入rho激酶(rock)抑制剂,其中所述分化培养基和所述rock抑制剂在2天内相继加入。
20.根据权利要求17至19中任一项所述的方法,其中在加入所述分化培养基后24小时内加入所述rock抑制剂。
21.根据权利要求17至20中任一项所述的方法,其中所述rock抑制剂选自y-27632、y-33075和h-1152。
22.根据权利要求17至21中任一项所述的方法,其中加入所述rock抑制剂以达到1μm至100μm的浓度。
23.根据权利要求17至22中任一项所述的方法,其中所述干细胞选自脂肪基质细胞、骨髓来源细胞、间充质干细胞和脐带来源细胞。
24.根据权利要求17至23中任一项所述的方法,其中由所述干细胞分化的细胞是软骨细胞或成骨细胞。
25.一种修复患者的软骨的方法,所述患者具有受损或不健康软骨,包含将通过根据权利要求1至24中任一项所述的方法制备的细胞片的一部分植入所述患者体内存在受损或不健康软骨的部位。
26.一种治疗患有骨关节炎的患者的骨关节炎或骨软骨缺损的方法,包含将通过根据权利要求1至24中任一项所述的方法制备的细胞片的一部分植入所述患者体内存在与骨关节炎相关的受损或不健康组织或存在骨软骨缺损的部位。
27.根据权利要求25或26所述的方法,还包含在所述植入之前用手术治疗来去除受损或不健康软骨或骨软骨缺损。
28.根据权利要求25至27中任一项所述的方法,其中所述干细胞是自体细胞。
29.根据权利要求25至28中任一项所述的方法,其中所述细胞片包含软骨细胞。
技术总结本发明总体上涉及细胞片的制备和用途。制备可以需要在培养基中在容器的细胞培养表面上培养多个干细胞,向容器中加入分化培养基和Rho激酶(ROCK)抑制剂,其中分化培养基和ROCK抑制剂在2天内相继加入,并且从细胞培养表面脱离由干细胞分化的细胞形成的细胞片。可替代地,可以去除细胞片的边缘,作为使用ROCK抑制剂来去除离心张力的替代或补充。技术研发人员:J·奥利瓦维拉纳,落合纯受保护的技术使用者:埃马尤斯生命科学有限公司技术研发日:技术公布日:2024/8/5本文地址:https://www.jishuxx.com/zhuanli/20240808/272323.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表