一种用于检测绵羊肺腺瘤病毒和梅迪-维斯纳病毒的双重实时荧光RPA引物组合物、试剂盒和检测方法
- 国知局
- 2024-09-05 15:02:45
本发明涉及病毒检测。更具体地,涉及一种用于检测绵羊肺腺瘤病毒和梅迪-维斯纳病毒的双重实时荧光rpa引物组合物、试剂盒和检测方法。
背景技术:
1、绵羊肺腺瘤病(ovine pulmonary adenocarcinoma,opa)是由绵羊肺腺瘤病毒(jaagsiekte sheep retrovirus,jsrv)所引起的进行性、传染性的肺部肿瘤肺病,临床上通常表现为渐进性呼吸困难、咳嗽、消瘦以及抗生素治疗无效的肺炎症状,鼻腔内有大量泡沫性渗出液,肺脏表面出现大小不等的灰白色结节。梅迪-维斯纳病(maedi-visnadisease,mvd)是由梅迪-维斯纳病毒(maedi-visna virus,mvv)引起的绵羊嗜单核/巨噬细胞的慢病毒感染疾病,是绵羊肺部、乳腺、关节以及中枢神经系统的多器官系统炎性疾病,病理组织学上可见肺部组织淋巴滤泡增生、肺泡间质增宽、纵隔淋巴结增大和平滑肌增生。opa和mvd均会引起呼吸困难、咳嗽等呼吸系统问题,临床症状相似,很难区分。二者病程发展缓慢且潜伏期长,期间患病绵羊持续传播病毒,影响羊群健康发展,给养殖业带来重大危害,对社会公共卫生也造成了严重影响。
2、opa和mvd自然发病的混合性感染病例已经在世界许多养羊国家出现,疫病控制传播和根除计划主要依赖于早期诊断并清除感染动物,然而目前未能找到适合的联合诊断方法。opa病羊中无法检测到循环抗体,不能用常规免疫学方法进行诊断,并且尚未成功建立jsrv体外培养体系,不能用病毒学分离法来进行鉴别诊断,同时mvv感染后血清转化耗时长,甚至不会发生血清转化,许多受感染的动物仍然是潜在的传染源,清除标准难以统一。因此,研制快速、敏感且特异的针对mvd和jsrv的同时检测试剂盒十分必要。
3、重组酶聚合酶核酸等温扩增技术(recombinase polymerase amplification,rpa)是近几年发展起来的一种核酸等温扩增技术,而荧光rpa技术是目前较常见的方法。当dna聚合酶延伸链时,使用荧光探针可以观察rpa的扩增过程,荧光信号的产生表明扩增开始,通过荧光信号的变化实现模板扩增的实时监测。相比传统的pcr技术,荧光rpa技术可以在更短的时间内实现对目的核酸的扩增,操作更方便,实验环境要求宽松,更适用于基础设施有限的基层检测。
4、目前用于诊断jsrv和mvv混合感染的双重检测方法,通常依赖于病理组织学以及pcr检测,也有单独针对jsrv的荧光rpa检测的方法,例如中国专利文献cn113373266a公开了一种用于检测绵羊肺腺瘤病毒的荧光rpa引物、试剂盒和检测方法;利用该法,对opa病肺组织cdna的最低检测限为1ng/μl。以及,单独针对mvv的荧光rpa检测的方法,例如:梅迪-维斯纳病毒实时荧光rpa检测方法的建立,《中国动物检疫杂志》2023年第3期,90-96页;该报道中可检测到mvd病肺组织cdna的最低检测限为100pg/μl。但是针对同时进行jsrv和mvd的检测技术尚未有报道涉及实时荧光rpa技术。实时荧光rpa相比于pcr,对引物的设计及反应条件更为严苛,筛选有效的特异性扩增引物、探针和摸索最佳反应条件是实现多重荧光rpa检测的难题。
技术实现思路
1、基于上述问题,本发明的第一个目的在于提供一组用于检测绵羊肺腺瘤病毒和梅迪-维斯纳病毒的双重实时荧光rpa引物组合物,利用该组合物可以基于重组酶聚合酶扩增技术,高效快速地检测样品中是否含有绵羊肺腺瘤病毒和/或梅迪-维斯纳病毒,实现对两种病毒混合感染的诊断,且检测的灵敏度高,特异性强。
2、本发明的第二个目的在于提供一种用于检测绵羊肺腺瘤病毒和梅迪-维斯纳病毒的双重实时荧光rpa试剂盒。
3、本发明的第三个目的在于提供一种利用本发明的双重实时荧光rpa引物组合物检测绵羊肺腺瘤病毒和梅迪-维斯纳病毒的方法。
4、为达到上述目的,本发明采用下述技术方案:
5、本发明提供一种用于检测绵羊肺腺瘤病毒和梅迪-维斯纳病毒的双重实时荧光rpa引物组合物,该双重实时荧光rpa引物组合物包括:
6、用于检测绵羊肺腺瘤病毒的seq id no.1所示的上游引物jsrv-env-f1和seq idno.5所示的下游引物jsrv-env-r1,及与引物配合使用的seq id no.9所示的探针jsrv-env-p;
7、用于检测梅迪-维斯纳病毒的seq id no.11所示的上游引物mvv-ltr-f2和seq idno.15所示的下游引物mvv-ltr-r2,及与引物配合使用的seq id no.18所示的探针mvv-ltr-p。
8、优选地,所述探针jsrv-env-p在距离5’端的第31个碱基“a”用thf替代,在thf位点上游的第一个t碱基标记fam荧光基团,在thf位点下游的第一个t碱基标记bhq1淬灭基团,并在3’末端标记c3 spacer;
9、所述探针mvv-ltr-p在距离5’端的第33个碱基“a”用idsp替代,在idsp位点上游的第一个t碱基标记hex荧光基团,在idsp位点下游的第一个t碱基标记bhq1淬灭基团,并在3’末端标记c3 spacer。
10、本发明还提供一种如上所述的双重实时荧光rpa引物组合物在制备用于检测绵羊肺腺瘤病毒和梅迪-维斯纳病毒的双重实时荧光rpa试剂盒中的应用。
11、根据本发明的第二个目的,本发明还提供了用于检测绵羊肺腺瘤病毒和梅迪-维斯纳病毒的双重实时荧光rpa试剂盒,所述试剂盒包括上面所述的双重实时荧光rpa引物组合物。
12、优选地,所述试剂盒还包括结合单链核酸的重组酶、单链dna结合蛋白、链置换dna聚合酶、反应体系缓冲液和醋酸镁。
13、优选地,所述结合单链核酸的重组酶为uvsx重组酶。
14、根据本发明的第三个目的,本发明还提供一种绵羊肺腺瘤病毒和梅迪-维斯纳病毒的检测方法,所述检测方法包括:
15、提取待测样品的总rna,反转录获得cdna;
16、配制荧光rpa反应体系,所述反应体系包括如权利要求1或2所述的双重实时荧光rpa引物组合物;
17、以反转录获得的cdna为模板,进行荧光rpa扩增反应;
18、结果判定。
19、优选地,所述荧光rpa反应体系,以总体积50μl计,包括10μm的上游引物jsrv-env-f1 1.1μl,10μm的下游引物jsrv-env-r1 1.1μl,10μm的探针jsrv-env-p 0.3μl;10μm的上游引物mvv-ltr-f2 1.1μl,10μm的下游引物mvv-ltr-r2 1.1μl,10μm的探针mvv-ltr-p 0.3μl。
20、优选地,所述荧光rpa扩增反应的反应温度为42℃,反应时间为20min。
21、优选地,所述待测样品为待测羊的肺组织样本。
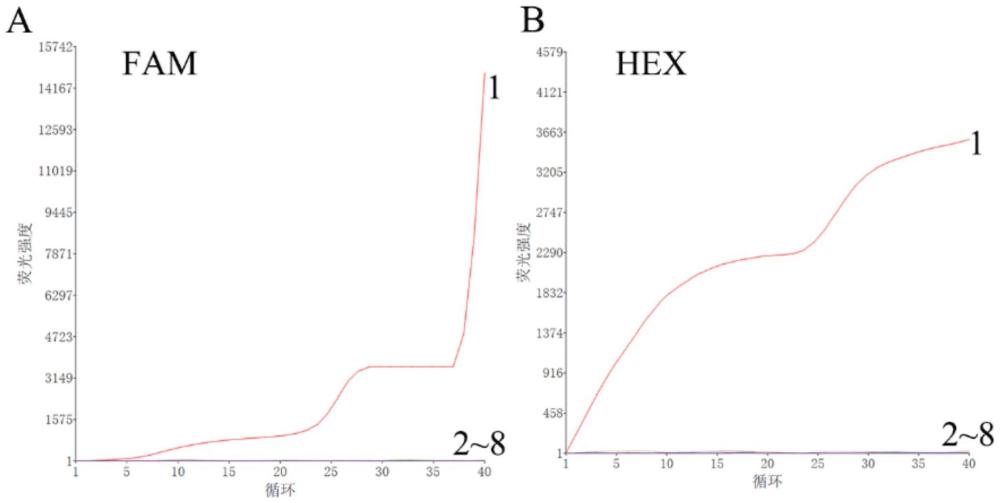
22、优选地,所述结果判定是:在整个扩增过程中仪器fam通道收集jsrv扩增荧光信号,hex通道收集mvv扩增荧光信号,当两个通道均出现明显荧光扩增曲线时,判定为jsrv和mvv混合感染阳性,当仅有fam通道出现明显荧光扩增曲线时,判定为jsrv感染阳性,当仅hex通道出现明显荧光扩增曲线时,判定为mvv感染阳性。
23、本发明的有益效果如下:
24、本发明通过设计和筛选针对绵羊肺腺瘤病毒和梅迪-维斯纳病毒rpa检测引物和探针,实现了对两种病毒的双重实时荧光rpa检测,检测结果通过仪器不同通道收集的荧光信号曲线进行判读,具有检测速度快(20min)、成本低、灵敏度高(对opa病肺组织cdna的最低检测限为1ng/μl,对mvd病肺组织cdna的最低检测限为10pg/μl)、稳定性好以及特异性强的优势,并且对基因扩增设备的要求低,适合在资源受限及突发传染病地区进行现场检测。
本文地址:https://www.jishuxx.com/zhuanli/20240905/289205.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。