一种制备β-氨基酸的方法
- 国知局
- 2024-11-19 09:38:35
本公开属于生物催化,涉及一种制备β-氨基酸的方法,具体涉及一种双酶级联催化合成β-氨基酸的方法。
背景技术:
1、β-氨基酸指氨基结合在羧基β位碳原子上的氨基酸,是α-氨基酸的同分异构体。相比α-氨基酸,β-氨基酸在自然界存在较少,其自身以及由它组成的化合物却显示了良好的药理和生物活性,例如(s)-2-苯基-3-氨基丙酸及其乙酯衍生物具有神经活性,例如(2s,3r)-2-羟基-3-氨基-4-苯基丁酸存在于氨肽酶抑制剂bestatin中。此外,β-氨基酸还是合成具有生物活性或药物活性复杂分子的中间体,例如β-氨基酸是大量具有β-内酰胺结构的抗生素的合成前体。因此,β-氨基酸在药物合成以及蛋白质修饰等方面具有重要的应用价值。
2、非专利文献1中公开了目前β-氨基酸的合成主要方法包括化学拆分、手性色谱柱拆分、arndt-eistert反应、不对称合成和酶催化。在这些方法中,大多数都是用来合成β取代的β-氨基酸,而合成α取代-β-氨基酸的方法是较少的。例如,专利文献1中介绍了一种以氰基乙酸乙酯和醛为原料,通过一步加氢利用化学法合成α-取代基的β-氨基酸的方法。专利文献2中公开了利用具有将α-取代-β氨基酸酯的旋光异构体混合物的酯部位不对称水解能力的酶对所述旋光异构体混合物进行不对称水解制备α-取代-β氨基酸的方法。现有报道的β-氨基酸的合成方法都存在合成步骤繁琐,反应条件苛刻,所需要的原料和试剂价格昂贵等问题。
3、α-氨基酸指氨基结合在羧基α位碳原子上的氨基酸,自然界构成蛋白质等的天然氨基酸均为α-氨基酸,而利用天然易得的α-氨基酸为原料,通过双酶级联催化合成β-氨基酸还未有报道。
4、引用文献:
5、非专利文献1:曾伟川等,β-氨基酸合成研究进展,合成化学,2013.21(5):634-644;
6、专利文献1:cn1435408a;
7、专利文献2:cn103998618a。
技术实现思路
1、发明要解决的问题
2、鉴于现有技术存在的问题,例如,β-氨基酸的合成方法步骤繁琐、反应条件苛刻、生产成本高等问题,发明人利用羧化和脱羧的方式构建c-c键和断裂c-c键,设计了一条以α-氨基酸为底物合成β-氨基酸的新途径,反应步骤及反应条件简单,可用于β-氨基酸及其衍生物、泛酸钙及其衍生物、肌肽及其衍生物的制备。
3、用于解决问题的方案
4、[1].一种制备式iii所示的β-氨基酸的方法,其中,所述方法包括如下步骤:
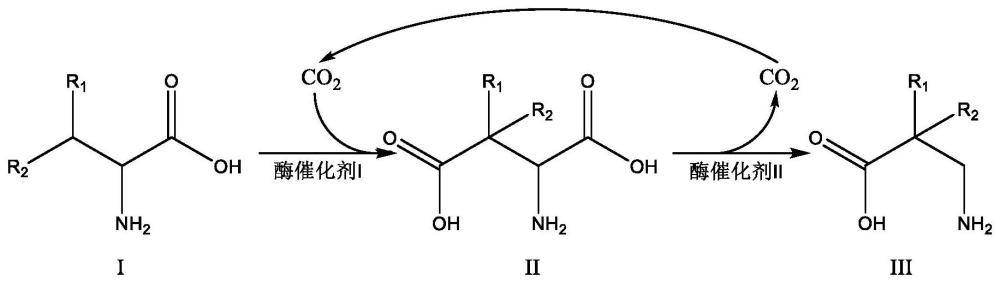
5、第一步反应:式i所示的α-氨基酸和羧基供体在酶催化剂i的作用下得到式ii所示的二羧基化合物;和
6、第二步反应:第一步反应生成的式ii所示的二羧基化合物在酶催化剂ii的作用下得到式iii所示的β-氨基酸并释放co2;
7、
8、其中,式i、式ii和式iii中的r1和r2彼此独立地选自:氢,直链或支链的、任选取代的低级烷基,任选取代的环烷基,单环或多环的、任选取代的芳基,单环或多环的、任选取代的杂芳基,直链或支链的、任选取代的烷氧基,直链或支链的、任选取代的烷硫基,直链或支链的酰基。
9、[2].根据[1]所述的方法,其中,r1和r2彼此独立地选自:氢、低级烷基、低级环烷基、芳基或杂芳基。
10、[3].根据[1]所述的方法,其中,所述酶催化剂i包含天冬氨酸β-脱羧酶,和/或,所述酶催化剂ii包含天冬氨酸α-脱羧酶。
11、[4].根据[3]所述的方法,其中,所述天冬氨酸β-脱羧酶来源于thermohalobaculum xanthum、thermococcus sp、acinetobacter radioresistens、clostridium thermobutyricum或thermoactinospora sp;和/或,
12、所述天冬氨酸α-脱羧酶来源于corynebacterium glutamicum、bacillussubtilis、archaeoglobus fulgidus、pyrococcus furiosus、thermococcuskodakarensis、thermus thermophilus。
13、[5].根据[3]或[4]所述的方法,其中,所述天冬氨酸β-脱羧酶选自如下(a1)~(a4)中的任一项:
14、(a1)包含如seq id no:2,4,6,8,10任一所示的氨基酸序列,且具有将式i所示的α-氨基酸和羧基供体转化为式ii所示的二羧基化合物活性的多肽;
15、(a2)具有如seq id no:2,4,6,8,10任一所示的氨基酸序列经过取代、缺失或添加一个或多个氨基酸的序列,且具有将式i所示的α-氨基酸和羧基供体转化为式ii所示的二羧基化合物活性的多肽;
16、(a3)由编码(a1)或(a2)所示氨基酸序列的多核苷酸编码的多肽;
17、(a4)由与seq id no:1,3,5,7,9任一所示的核苷酸序列具有至少80%、85%、90%、95%、98%或99%以上的同一性的序列编码的,且具有将式i所示的α-氨基酸和羧基供体转化为式ii所示的二羧基化合物活性的多肽;和/或,
18、所述天冬氨酸α-脱羧酶选自如下(b1)~(b4)中的任一项:
19、(b1)包含如seq id no:12,14,16,18,20,22任一所示的氨基酸序列,且具有将式ii所示的二羧基化合物转化为式iii所示的β-氨基酸并释放co2活性的多肽;
20、(b2)具有如seq id no:12,14,16,18,20,22任一所示的氨基酸序列经过取代、缺失或添加一个或多个氨基酸的序列,且具有将式ii所示的二羧基化合物转化为式iii所示的β-氨基酸并释放co2活性的多肽;
21、(b3)由编码(b1)或(b2)所示氨基酸序列的多核苷酸编码的多肽;
22、(b4)由与seq id no:11,13,15,17,19,21任一所示的核苷酸序列具有至少80%、85%、90%、95%、98%或99%以上的同一性的序列编码的,且具有将式ii所示的二羧基化合物转化为式iii所示的β-氨基酸并释放co2活性的多肽。
23、[6].根据[1]~[5]任一项所述的方法,其中,所述羧基供体包括二氧化碳及其溶解在水中形成碳酸盐、碳酸氢盐或其混合物。
24、[7].根据[1]~[6]任一项所述的方法,其中,所述第一步反应和第二步反应在相同或不同的反应器中进行。
25、[8].根据[1]~[7]任一项所述的方法,其中,所述反应器中,式i所示的α-氨基酸的初始浓度不低于10mm,优选为不低于20mm;
26、可选地,所述酶催化剂i和酶催化剂ii可以纯酶、粗酶液、表达其的宿主细胞或含表达其的宿主细胞的发酵液的方式参与反应;
27、可选地,所述反应器中的ph为3.0~8.0,温度为20~70℃;
28、可选地,所述反应器中还包含辅酶,优选为磷酸吡哆醛。
29、[9].一种催化剂组合物,其包括:酶催化剂i和酶催化剂ii,
30、其中,所述酶催化剂i可将式i所示的α-氨基酸和羧基供体催化得到式ii所示的二羧基化合物;所述酶催化剂ii可将式ii所示的二羧基化合物催化得到式iii所示的β-氨基酸并释放co2;
31、
32、其中,式i、式ii和式iii中的r1和r2彼此独立地选自:氢,直链或支链的、任选取代的低级烷基,任选取代的环烷基,单环或多环的、任选取代的芳基,单环或多环的、任选取代的杂芳基,直链或支链的、任选取代的烷氧基,直链或支链的、任选取代的烷硫基,直链或支链的酰基;优选地,r1和r2彼此独立地选自:氢、低级烷基、低级环烷基、或杂芳基或芳基。
33、[10].根据[9]所述的催化剂组合物,其中,所述酶催化剂i包含天冬氨酸β-脱羧酶,和/或,所述酶催化剂ii包含天冬氨酸α-脱羧酶。
34、[11].根据[10]所述的催化剂组合物,其中,
35、所述天冬氨酸β-脱羧酶来源于thermohalobaculum xanthum、thermococcus sp、acinetobacter radioresistens、clostridium thermobutyricum或thermoactinosporasp;和/或,
36、所述天冬氨酸α-脱羧酶来源于corynebacterium glutamicum、bacillussubtilis、archaeoglobus fulgidus、pyrococcus furiosus、thermococcuskodakarensis、thermus thermophilus。
37、[12].根据[10]或[11]所述的催化剂组合物,其中,所述天冬氨酸β-脱羧酶选自如下(a1)~(a4)中的任一项:
38、(a1)包含如seq id no:2,4,6,8,10任一所示的氨基酸序列,且具有将式i所示的α-氨基酸和羧基供体转化为式ii所示的二羧基化合物活性的多肽;
39、(a2)具有如seq id no:2,4,6,8,10任一所示的氨基酸序列经过取代、缺失或添加一个或多个氨基酸的序列,且具有将式i所示的α-氨基酸和羧基供体转化为式ii所示的二羧基化合物活性的多肽;
40、(a3)由编码(a1)或(a2)所示氨基酸序列的多核苷酸编码的多肽;
41、(a4)由与seq id no:1,3,5,7,9任一所示的核苷酸序列具有至少80%、85%、90%、95%、98%或99%以上的同一性的序列编码的,且具有将式i所示的α-氨基酸和羧基供体转化为式ii所示的二羧基化合物活性的多肽;和/或,
42、所述天冬氨酸α-脱羧酶选自如下(b1)~(b4)中的任一项:
43、(b1)包含如seq id no:12,14,16,18,20,22任一所示的氨基酸序列,且具有将式ii所示的二羧基化合物转化为式iii所示的β-氨基酸并释放co2活性的多肽;
44、(b2)具有如seq id no:12,14,16,18,20,22任一所示的氨基酸序列经过取代、缺失或添加一个或多个氨基酸的序列,且具有将式ii所示的二羧基化合物转化为式iii所示的β-氨基酸并释放co2活性的多肽;
45、(b3)由编码(b1)或(b2)所示氨基酸序列的多核苷酸编码的多肽;
46、(b4)由与seq id no:11,13,15,17,19,21任一所示的核苷酸序列具有至少80%、85%、90%、95%、98%或99%以上的同一性的序列编码的,且具有将式ii所示的二羧基化合物转化为式iii所示的β-氨基酸并释放co2活性的多肽。
47、[13].根据[9]~[12]任一项所述的催化剂组合物,其中,所述酶催化剂i和酶催化剂ii为纯酶、粗酶、细胞裂解液或全细胞的形式;任选地,所述纯酶或粗酶为游离或固定化的形式,所述全细胞为游离或固定化的形式。
48、[14].[9]~[13]任一项所述的催化剂组合物在合成β-氨基酸及其衍生物、泛酸钙及其衍生物和/或肌肽及其衍生物中的应用。
49、[15].一种利用重组微生物生产β-氨基丙酸的方法,其包括提供包含碳源的发酵培养基,使所述发酵培养基与表达工程化β-氨基丙酸生物合成途径的重组微生物接触的步骤;
50、所述工程化β-氨基丙酸生物合成途径包含如下步骤(i)和(ii):
51、(i)将α-氨基丙酸转化为天冬氨酸,
52、(ii)将步骤(i)得到的天冬氨酸转化为β-氨基丙酸;
53、可选地,在产生β-氨基丙酸的条件下培养重组微生物。
54、[16].根据[15]所述的方法,其中,所述步骤(i)通过酶催化剂i将α-氨基丙酸转化为天冬氨酸;所述步骤(ii)通过酶催化剂ii将天冬氨酸转化为β-氨基丙酸。
55、[17].根据[16]所述的方法,其中,所述酶催化剂i包含天冬氨酸β-脱羧酶,和/或,所述酶催化剂ii包含天冬氨酸α-脱羧酶。
56、[18].根据[17]所述的方法,其中,
57、所述天冬氨酸β-脱羧酶来源于thermohalobaculum xanthum、thermococcus sp、acinetobacter radioresistens、clostridium thermobutyricum或thermoactinosporasp;和/或,
58、所述天冬氨酸α-脱羧酶来源于corynebacterium glutamicum、bacillussubtilis、archaeoglobus fulgidus、pyrococcus furiosus、thermococcuskodakarensis、thermus thermophilus。
59、[19].根据[17]或[18]所述的方法,其中,所述天冬氨酸β-脱羧酶选自如下(a1)~(a4)中的任一项:
60、(a1)包含如seq id no:2,4,6,8,10任一所示的氨基酸序列,且具有将式i所示的α-氨基酸和羧基供体转化为式ii所示的二羧基化合物活性的多肽;
61、(a2)具有如seq id no:2,4,6,8,10任一所示的氨基酸序列经过取代、缺失或添加一个或多个氨基酸的序列,且具有将式i所示的α-氨基酸和羧基供体转化为式ii所示的二羧基化合物活性的多肽;
62、(a3)由编码(a1)或(a2)所示氨基酸序列的多核苷酸编码的多肽;
63、(a4)由与seq id no:1,3,5,7,9任一所示的核苷酸序列具有至少80%、85%、90%、95%、98%或99%以上的同一性的序列编码的,且具有将式i所示的α-氨基酸和羧基供体转化为式ii所示的二羧基化合物活性的多肽;和/或,
64、所述天冬氨酸α-脱羧酶选自如下(b1)~(b4)中的任一项:
65、(b1)包含如seq id no:12,14,16,18,20,22任一所示的氨基酸序列,且具有将式ii所示的二羧基化合物转化为式iii所示的β-氨基酸并释放co2活性的多肽;
66、(b2)具有如seq id no:12,14,16,18,20,22任一所示的氨基酸序列经过取代、缺失或添加一个或多个氨基酸的序列,且具有将式ii所示的二羧基化合物转化为式iii所示的β-氨基酸并释放co2活性的多肽;
67、(b3)由编码(b1)或(b2)所示氨基酸序列的多核苷酸编码的多肽;
68、(b4)由与seq id no:11,13,15,17,19,21任一所示的核苷酸序列具有至少80%、85%、90%、95%、98%或99%以上的同一性的序列编码的,且具有将式ii所示的二羧基化合物转化为式iii所示的β-氨基酸并释放co2活性的多肽。
69、[20].一种制备β-氨基丙酸盐的方法,其中,所述方法包括如下步骤:
70、第一步反应:以α-氨基丙酸为底物,根据[1]~[8]任一项所述的方法制备得到β-氨基丙酸,或根据[9]~[13]任一项所述的催化剂组合物催化制备得到β-氨基丙酸,或根据[15]~[19]任一项所述的方法制备得到β-氨基丙酸;
71、第二步反应:将第一步反应制备得到的β-氨基丙酸与碱性溶液进行反应,生成β-氨基丙酸盐;
72、优选地,所述β-氨基丙酸盐包含β-氨基丙酸碱金属盐;
73、可选地,所述碱性溶液选自含有碱金属或碱土金属阳离子的碱性溶液。
74、[21].一种制备泛酸盐的方法,其中,所述方法包括如下步骤:
75、第一步反应:包括根据[20]中所述的方法制备得到β-氨基丙酸盐的步骤;
76、第二步反应:将泛解酸内酯或泛解酸与第一步反应制备得到的β-氨基丙酸盐进行反应,生成泛酸盐;
77、可选地,所述泛解酸内酯包括d-泛解酸内酯,所述泛解酸包括d-泛解酸;
78、可选地,所述泛酸盐包括泛酸钙。
79、[22].一种制备肌肽的方法,其中,所述方法包括如下步骤:
80、第一步反应:包括利用根据[1]~[8]任一项所述的方法制备得到β-氨基丙酸,或利用[9]~[13]任一项所述的催化剂组合物催化制备得到β-氨基丙酸,或根据[15]~[19]任一项所述的方法制备得到β-氨基丙酸,或根据[20]所述的方法制备得到β-氨基丙酸盐的步骤;
81、第二步反应:将第一步反应制备得到的β-氨基丙酸或β-氨基丙酸盐,与l-组氨酸或其盐进行反应,生成肌肽;
82、可选地,所述第二步反应在氨肽酶的作用下进行。
83、本公开的有益效果
84、在一些实施方式中,本公开提供的制备β-氨基酸的方法与其他合成方法相比,合成路线简单,原料便宜易得,无需昂贵的特殊试剂,反应条件温和,可采用一锅法反应,操作简单。
85、在一些实施方式中,本公开提供的制备β-氨基酸的途径,能够实现co2的原位自循环,原子的利用率能够达到100%,并且不需提供特殊的辅因子。
86、在一些实施方式中,本公开提供的制备β-氨基酸的方法或催化剂组合物可以利用便宜易得的α-氨基酸为原料,制备在α-取代的一系列β-氨基酸,可以极为方便地扩展β-氨基酸的化学库。
87、在一些实施方式中,本公开提供的制备β-氨基酸的方法或通过催化剂组合物得到的β-氨基酸,还可应用于泛酸钙及其衍生物、肌肽及其衍生物的生产中,具备良好的应用前景。
本文地址:https://www.jishuxx.com/zhuanli/20241118/329598.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表