一种对ACE2进行特定分区的方法及其应用
- 国知局
- 2024-11-19 09:38:42
本发明属于生物医学领域,具体涉及一种对ace2进行特定分区的方法及其应用。
背景技术:
1、2019年新型冠状病毒病(covid-19)已成为国际突发公共卫生事件,对全球人类健康构成最严重的威胁。越来越多的证据表明,新型冠状病毒不仅可以感染人类,还可以感染其他物种,从而导致跨物种感染。为了更加快速、系统和准确地发现具有高度跨物种感染特性的物种需要研究ace2与sars-cov-2结合的关键位点。
2、然而,有关物种ace2分子作为受体与sars-cov-2结合的关键亚结构域对于亲和力的贡献乃至对相关物种是否为新冠病毒潜在传播宿主的重要性方面仍尚未完全解开,需要进行更深入的研究,这对动物模型的建立和靶向药物的研发均有着重要意义。
技术实现思路
1、本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明提出一种对ace2进行特定分区的方法。
2、本发明还提出了上述方法的应用。
3、根据本发明的一个方面,提出了一种对ace2进行特定分区的方法,所述方法包括以下步骤:将ace2蛋白与sars-cov-2rbd的复合物晶体结构利用mutabind2进行蛋白突变计算预测,根据ace2蛋白与新冠病毒界面接触点对ace2进行特定分区。
4、在本发明的一些实施方式中,所述方法还包括将sars-cov-2s蛋白和/或人ace2蛋白所有关键位点氨基酸残基突变为丙氨酸的步骤。
5、在本发明的一些实施方式中,ace2蛋白包括但不限于人、猫、白尾鹿、小鼠和突变的ace2蛋白。
6、在本发明的一些实施方式中,所述突变的ace2蛋白包括以人ace2(ace2为单体ace2(1-615))为骨架替换关键结构域为实验物种相同位置氨基酸残基的hace2突变株。
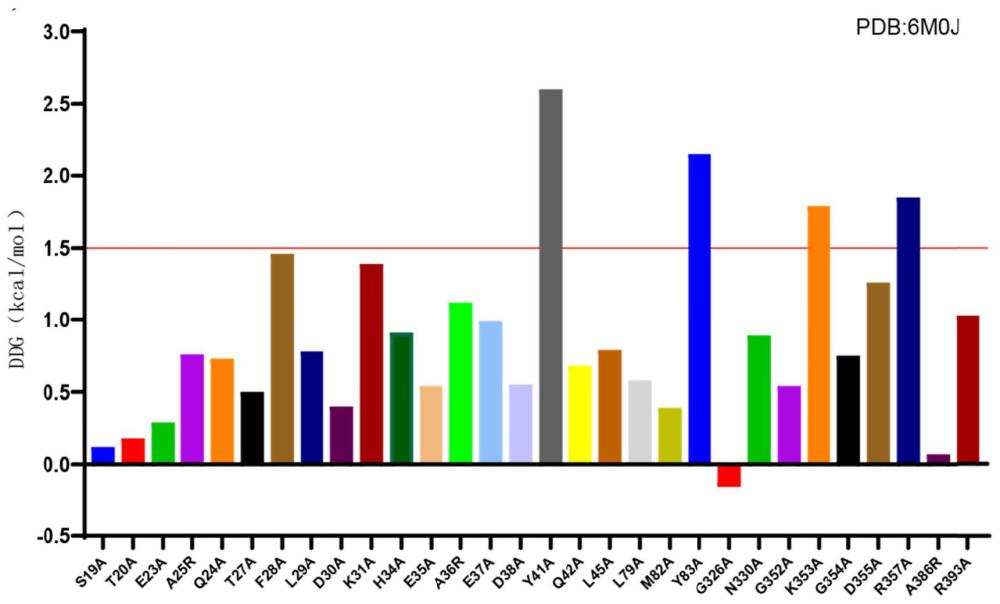
7、在本发明的一些实施方式中,ace2与sars-cov-2rbd的复合物晶体结构的pdb id包括6m0j。
8、在本发明的一些实施方式中,mutabind2的使用通过从蛋白结构数据库(https://ww w.rcsb.org/)中获取关于sars-cov-2s蛋白与人ace2蛋白共晶的三维结构文件(pd b6m0j)后,在mutabind2(https://lilab.jysw.suda.edu.cn/research/mutabind2/method)网站对蛋白复合物中的一些关键氨基酸残基进行突变计算。
9、对于每种蛋白质/突变,mutabind2提供以下结果:
10、δδgbind(kcal/mol)是由突变诱导的结合亲和力的预测变化。正和负信号对应于不稳定和稳定的突变,预计会相应地降低和增加结合亲和力。如果δδg≥1.5kcal/mol则mutabind服务器将突变归类为有害突变,若δδg≤-1.5kcal/mol则认为突变会促进二者结合。
11、在本发明的一些实施方式中,所述特定分区是通过ace2与sars-cov-2rbd的结合界面根据其空间结构和相互作用力划分得到亚区域结构。
12、在本发明的一些实施方式中,所述亚区域结构包括cr1、cr2和cr3。
13、在本发明的一些实施方式中,所述cr1中ace2氨基酸位点包括q24、t27、f28、k31、l79、m82和y83。
14、在本发明的一些实施方式中,所述cr2中ace2氨基酸位点包括t27、d30、k31、h34和e35。
15、在本发明的一些实施方式中,所述cr3中ace2氨基酸位点包括e37、d38、y41、q42、n330、k353、g354、d355、r357和r393。
16、在本发明的一些实施方式中,所述方法还包括采用spr技术进行验证的步骤。
17、在本发明的一些实施方式中,spr技术进行验证的步骤包括:利用spr技术测定不同物种ace2蛋白与sars-cov-2rbd的亲和力和动力学参数。
18、在本发明的一些实施方式中,所述不同物种ace2蛋白和sars-cov-2rbd为通过细胞工程方法进行诱导表达、纯化得到的蛋白。
19、在本发明的一些实施方式中,所述纯化采用akta纯化仪进行。
20、在本发明的一些实施方式中,纯化不同物种ace2蛋白的标签为his tag。
21、在本发明的一些实施方式中,纯化sars-cov-2rbd的标签为fc tag。
22、在本发明的一些实施方式中,akta纯化仪进行纯化ace2蛋白步骤包括:将待纯化的ace2表达蛋白经镍柱采用亲和层析后,再采用分子筛纯化得到纯化后的表达蛋白。
23、在本发明的一些实施方式中,该亲和层析纯化采用的溶液包括镍柱平衡液和镍柱洗脱液。
24、在本发明的一些实施方式中,所述镍柱平衡液包括150~250mm nacl、15~25mmtris和15~25mm imidazole,ph为7.0~8.0。
25、在本发明的一些实施方式中,所述镍柱平衡液包括200mm nacl、20mm tris和20mmimidazole,ph为7.5。
26、在本发明的一些实施方式中,所述镍柱洗脱液包括450~550mm imidazole、15~25mm tris和150~250mm nacl,ph为7.5。
27、在本发明的一些实施方式中,所述镍柱洗脱液包括500mm imidazole、20mm tris和200mm nacl,ph为7.5。
28、在本发明的一些实施方式中,akta纯化仪进行纯化sars-cov-2rbd蛋白步骤包括:用akta纯化仪经protein a柱亲和纯化后在采用分子筛进一步纯化。
29、在本发明的一些实施方式中,亲和层析纯化溶液为ph3.5的柠檬酸和ph3.0的柠檬酸。
30、在本发明的一些实施方式中,分子筛纯化采用分子筛溶液和0.1m naoh溶液,通过双重纯化操作步骤获取高纯度的蛋白。
31、在本发明的一些实施方式中,所述分子筛溶液包括10mm pb和140mm nacl,ph为7.4。
32、在本发明的一些实施方式中,纯化后的蛋白浓度还包括采用bca法进行测定的步骤。
33、在本发明的一些实施方式中,所述spr测定使用protein a芯片进行。
34、在本发明的一些实施方式中,protein a芯片捕获携带有fc标签的sars-cov-2rbd,浓度为1g/ml,不同的ace2流经芯片表面,浓度范围为2000nm~31.25nm,两倍梯度稀释,使用biacore insight评估软件,1:1结合模型分析结合动力学。
35、在本发明的一些实施方式中,spr采用的溶液包括10mm hepes、0.005%tween-20、3mm edta、150mm nacl、配体sars-cov-2rbd和分析物ace2。
36、在本发明的一些实施方式中,配体sars-cov-2rbd的浓度为1g/ml,分析物ace2的浓度为0-2000nm。
37、在本发明的一些实施方式中,分析物ace2的浓度为2000nm、1000nm、500nm、250nm、125nm、62.5nm、31.25nm和0nm。
38、根据本发明的第二方面,提出了上述方法的应用,所述应用为在制备用于防治新冠病毒的药物中的应用。
39、在本发明的一些实施方式中,所述方法在制备解析ace2与新冠病毒接触界面关键位点的产品中的应用。
40、在本发明的一些实施方式中,所述方法在制备解析ace2与新冠病毒棘突蛋白的结合能力的产品中的应用。
41、根据本发明的一些实施方式,至少具有以下有益效果:本发明方案结合蛋白突变计算预测对ace2进行亚结构分区,通过spr实验,将ace2与sars-cov-2rbd分区,研究亚结构突变对结合亲和力的影响,解析ace2与新冠病毒接触界面的关键位点。通过上述方法可探索sars-cov-2rbd与ace2相互作用的关键氨基酸残基,以及新冠病毒感染不同物种过程中,特定物种ace2不同亚结构区域对二者结合亲和力的影响,即病毒跨结构ace2嗜性,为预测新冠病毒的潜在宿主范围,抗体和疫苗的研发提供理论支持。
本文地址:https://www.jishuxx.com/zhuanli/20241118/329607.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表