一种PE-NRGEERmRNA体外转录模板质粒、PE碱基编辑器及其应用
- 国知局
- 2024-06-20 10:45:53
本发明属于遗传修饰和动物基因工程的,具体涉及一种pe-nrgeer mrna体外转录模板质粒、pe碱基编辑器及其应用。
背景技术:
1、对生物体基因组进行有针对性改变的能力继续推动生命科学和医学的发展。双链断裂(double-strand break,dsb)介导的dna编辑策略使用可编程核酸酶,如zfn、talens或crispr-cas核酸酶,可以通过在靶位点诱导插入或缺失(indels)来有效地破坏基因,但dsb通常也会导致不期望的结果,包括编辑结果的不受控制、大规模的dna重排、p53通路激活和染色体断裂重排等。尽管靶向dsb可以通过同源性定向修复刺激精确的基因纠正,但该过程在大多数治疗相关的细胞类型中效率低下。
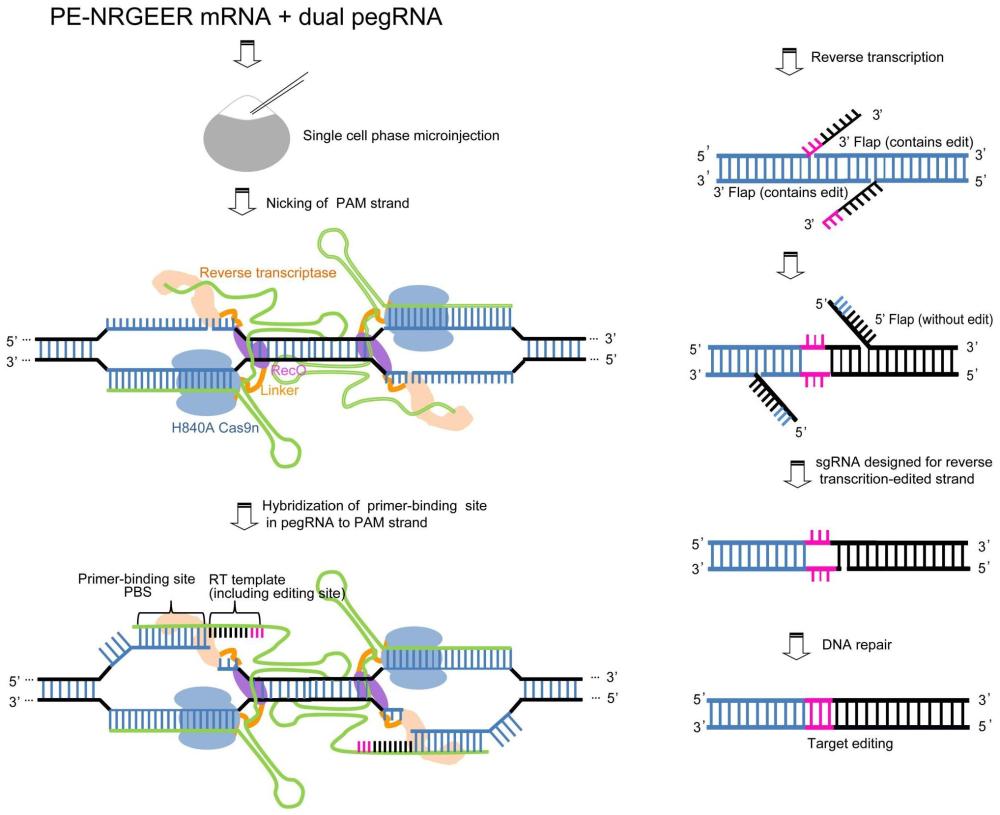
2、现有技术研究发现,碱基编辑器(base edting,be)和prime editing(pe)编辑器可以有效地在相关细胞中实现精准编辑,而不需要dsb。胞嘧啶和腺苷碱基编辑器可分别将c·g转换为t·a和a·t转换为g·c,而pe可实现几乎任何局部突变,包括在目标dna位点替换、插入或删除多达数十个碱基对。pe系统至少由两个组成部分组成:一个含有与工程逆转录酶(rt)融合的可编程dna内切酶的蛋白质,以及引物编辑指南rna或pegrna。pegrna包含指定靶位点的间隔物、sgrna支架和编码所需编辑的3'延伸序列,该延伸序列包含与dna原间隔物的一部分互补的引物结合位点(pbs)和编码所需编辑和下游基因组序列的rt模板。在pe核糖核蛋白(rnp)结合靶位点切割含pam的dna链后,产生的切割dna链碱基对与pegrna中的pbs结合,启动rt模板的逆转录直接进入靶dna位点,然后通过细胞dna修复途径解析新合成的编辑dna的3'端,从而在目标位点安装所需的编辑。然而,目前还没有合适的pe-nrgeer mrna体外转录模板质粒和pe碱基编辑器用于定向改造鱼类基因。
技术实现思路
1、本发明的目的在于提供一种pe-nrgeer mrna体外转录模板质粒、pe碱基编辑器及其应用,以pe-nrgeer mrna体外转录模板质粒结合双peg sgrna制备的pe碱基编辑器具有编辑效率高的特点。
2、为了实现上述目的,本发明提供如下技术方案:
3、本发明提供了一种pe-nrgeer mrna体外转录模板质粒,所述pe-nrgeer mrna体外转录模板质粒的核苷酸序列如seq id no.1所示。
4、本发明提供了一种pe碱基编辑器,所述pe碱基编辑器包括pe-nrgeer mrna、pegsgrna1和peg sgrna2;
5、所述pe-nrgeer mrna由上述技术方案所述pe-nrgeer mrna体外转录模板质粒经体外转录得到;
6、所述peg sgrna1由peg sgrna1体外转录模板经体外转录得到;
7、所述peg sgrna2由peg sgrna2体外转录模板经体外转录得到;
8、所述peg sgrna1体外转录模板和peg sgrna2体外转录模板分别包括:经t7启动子序列、pam靶向识别序列、与靶点序列5’端存在部分互补的带有逆转录酶识别序列pbs和与靶点序列3’端及其后连续的一段基因组序列的反向互补序列顺序连接而得到的序列;
9、所述peg sgrna1位于靶向序列的一条链上;所述peg sgrna2位于与靶向序列互补的另一条链上。
10、优选的,用于合成peg sgrna1体外转录模板的上游引物的核苷酸序列序列如seqid no.4或seq id no.10所示;用于合成peg sgrna1体外转录模板的下游引物的核苷酸序列序列如seq id no.5或seq id no.11所示;
11、用于合成peg sgrna2体外转录模板的上游引物的核苷酸序列如seq id no.6或seq id no.12所示;用于合成peg sgrna2体外转录模板的下游引物的核苷酸序列如seq idno.7或seq id no.13所示。
12、优选的,用于合成所述peg sgrna1体外转录模板和peg sgrna2体外转录模板的核苷酸序列如组合1)或组合2)所示:
13、组合1)中合成peg sgrna1体外转录模板的上游引物、合成peg sgrna1体外转录模板的下游引物、合成peg sgrna2体外转录模板的上游引物、合成peg sgrna2体外转录模板的下游引物的核苷酸序列分别如seq id no.4、seq id no.5、seq id no.6和seq id no.7所示;
14、组合2)中合成peg sgrna1体外转录模板的上游引物、合成peg sgrna1体外转录模板的下游引物、合成peg sgrna2体外转录模板的上游引物、合成peg sgrna2体外转录模板的下游引物的核苷酸序列分别如seq id no.10、seq id no.11、seq id no.12和seq idno.13所示。
15、本发明提供了上述所述pe-nrgeer mrna体外转录模板质粒或所述的pe碱基编辑器在定向改造鱼类中的应用。
16、优选的,所述鱼类包括斑马鱼和/或金鱼。
17、优选的,所述斑马鱼的改造基因包括slc45a2基因;
18、所述金鱼的改造基因包括mitfa基因。
19、本发明提供了一种定向改造鱼类胚胎的方法,包括如下步骤:
20、根据待改造基因的序列分别合成peg sgrna1体外转录模板和peg sgrna2体外转录模板;
21、将所述peg sgrna1体外转录模板、peg sgrna2体外转录模板和pe-nrgeer mrna体外转录模板质粒分别进行体外转录,得到peg sgrna1、peg sgrna2和pe-nrgeer mrna;
22、将所述peg sgrna1、peg sgrna2和pe-nrgeer mrna混合后注入到待改造鱼类的胚胎中培养,得到定向改造后的胚胎。
23、优选的,以水为溶剂混合所述peg sgrna1、peg sgrna2和pe-nrgeer mrna,混合液中peg sgrna1的终浓度为100~300ng/μl;
24、混合液中peg sgrna2的终浓度为100~300ng/μl;
25、混合液中pe-nrgeer mrna的终浓度为50~200ng/μl。
26、有益效果:
27、本发明提供了一种pe-nrgeer mrna体外转录模板质粒,所述pe-nrgeer mrna体外转录模板质粒的序列如seq id no.1所示。该体外转录模板质粒经斑马鱼密码子偏好性优化,毒性小;整合了可特异提高rna模板基因编辑效率的reco蛋白,效率高。
28、基于上述技术优势,本发明还提供了一种pe碱基编辑器,所述pe碱基编辑器包括pe-nrgeer mrna、peg sgrna1和peg sgrna2;所述pe-nrgeer mrna由上述技术方案所述pe-nrgeer mrna体外转录模板质粒经体外转录得到;所述peg sgrna1由peg sgrna1体外转录模板经体外转录得到;所述peg sgrna2由peg sgrna2体外转录模板经体外转录得到;所述peg sgrna1体外转录模板和peg sgrna2体外转录模板分别包括:经t7启动子序列、pam靶向识别序列、与靶点序列5’端存在部分互补的带有逆转录酶识别序列(primer-bindingsite,pbs)和与靶点序列3’端及其后连续的一段基因组序列的反向互补序列顺序连接得到;所述peg sgrna1位于靶向序列的一条链上;所述peg sgrna2位于与靶向序列互补的另一条链上。通过将pe-nrgeer mrna与双pegrna混合,大大提高了基因编辑的效率。
29、本发明还提供了上述技术方案所述pe-nrgeer mrna体外转录模板质粒或所述的pe碱基编辑器在定向改造鱼类中的应用。实验证明,采用本发明提供的技术方案后,显著提升了基因编辑效率达10倍以上,可以高效实现斑马鱼基因组点突变、短片段核酸序列的敲除和敲入。因此,本发明提供的技术方案能够实现对鱼类的定向改造。
本文地址:https://www.jishuxx.com/zhuanli/20240619/290.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。