基于短肽封闭保护CXCL12的设计方法及其在膜蛋白降解中的应用
- 国知局
- 2024-08-05 12:02:51
本发明属于生物医学领域,尤其涉及一种基于短肽封闭保护cxcl12的设计方法及其在膜蛋白降解中的应用。
背景技术:
1、靶向蛋白降解是调节细胞外生物学的重要手段,已经成为一种很有前途的治疗策略,相比于传统的抑制剂具有优势。与抑制剂不同,降解可以持久地敲低蛋白质水平,而且可以靶向耐药突变蛋白以及难以靶向的药物蛋白。大多数降解技术,如蛋白质水解靶向嵌合体(protacs)利用泛素蛋白酶体系统来降解传统上具有挑战性的蛋白质,在靶向60多种蛋白质方面已经取得了成功。然而,由于其胞内作用机制,该方法仅限于降解胞内蛋白质。鉴于大多数药物靶点位于细胞表面或分泌型,越来越多的降解细胞外蛋白的策略被开发出来。溶酶体靶向嵌合体(lytacs)是一种双功能分子通过化学linker相连接,一端是与细胞表面跨膜受体ci-m6pr(cation-independent mannose-6-phosphate receptor)结合的低聚糖肽基团,另一端是一个与靶蛋白结合的抗体或小分子。lytac分子通过与ci-m6pr和靶蛋白同时结合,产生ci-m6pr-lytac-靶蛋白复合物,形成一个运输囊泡。囊泡会将复合物运输到溶酶体中,之后靶蛋白被降解。然而,lytac需要化学合成大聚糖,以有效清除靶标。因此,仍然迫切需要开发更多的完全基因编码的细胞外降解技术。
2、细胞因子受体靶向嵌合体(kinetacs)是新开发的一种完全基因编码的重组双特异性抗体,由两部分组成,一部分是可以结合其同源受体的细胞因子,另一部分是目的蛋白的特异性结合蛋白。利用内源性细胞因子介导同源受体内化,使细胞表面和细胞外蛋白能够广泛而高效的传递到溶酶体中被降解。kinetacs作为一种通用的、模块化的和简单的基因编码策略,用于诱导细胞外和细胞表面靶点递送到溶酶体中发生降解。
3、然而,以上靶向降解蛋白的方法其临床应用可能会受到蛋白质活性位点选择性差和体内脱靶毒性的限制。
技术实现思路
1、本发明要解决的技术问题是克服现有技术中通过靶向降解细胞蛋白而造成的体内脱靶毒性以及蛋白活性位点选择性差等方面的不足,通过设计一种前药的形式来提高靶向降解蛋白的精准性,降低靶向降解蛋白的体内毒性。具体为提供一种基于短肽封闭保护cxcl12的设计方法及其在膜蛋白降解中的应用。该方法通过特异性地封闭药物在体内循环的毒性,在肿瘤细胞高表达蛋白酶存在条件下解除封闭,实现了以一种低毒性、特异性更好的方式靶向降解细胞表面蛋白。
2、为了实现上述目的,本发明提供了一种基于短肽封闭保护cxcl12的设计方法,截取cxcr7中部分与cxcl12相互作用的短肽,通过短肽封闭cxcl12,形成n端封闭的cxcl12纯化蛋白,所述n端封闭的cxcl12蛋白质粒序列如seq id no.1所示。
3、基于一个总的技术构思,本发明还提供了一种所述的设计方法在膜蛋白降解中的应用,所述应用包括:将所述n端封闭的cxcl12蛋白融合spycatcher序列得到蛋白1,将目的蛋白的特异性结合蛋白融合spytag序列得到蛋白2,所述蛋白1和所述蛋白2通过spycatcher-spytag系统共价连接成双特异性蛋白,将所述双特异性蛋白与细胞进行孵育,在肿瘤细胞高表达酶存在的环境下特异性地去除封闭,利用靶向溶酶体降解的方法介导细胞表面的目的蛋白降解。
4、上述的应用,进一步的,所述目的蛋白为her2,所述应用包括以下步骤:
5、s1、将所述n端封闭的cxcl12蛋白融合spycatcher序列得到蛋白1、将her2-specific affibody蛋白融合spytag序列得到蛋白2;
6、s2、所述蛋白1和所述蛋白2通过spycatcher与spytag在体外进行共价连接,得到双特异性蛋白procxcl12-aher2;
7、s3、将所述双特异性蛋白procxcl12-aher2与细胞进行孵育,加入肿瘤细胞高表达酶后细胞膜表面her2蛋白降解。
8、上述的应用,进一步的,所述s1具体包括以下步骤:
9、合成n端封闭的cxcl12融合spycatcher序列的表达质粒1,将所述表达质粒1转化至大肠杆菌bl21(de3)菌株中纯化得到蛋白1;合成her2-specific affibody融合spytag序列的表达质粒2,将所述表达质粒2转化至大肠杆菌bl21(de3)菌株中纯化得到蛋白2。
10、上述的应用,进一步的,所述表达质粒1的dna序列如seq id no.2所示。
11、上述的应用,进一步的,所述表达质粒2的dna序列如seq id no.3所示。
12、上述的应用,进一步的,所述孵育的时间为12h。
13、上述的应用,进一步的,所述细胞为人胚肾细胞系293t。
14、上述的应用,进一步的,所述肿瘤细胞高表达酶为mmp2蛋白酶。
15、上述的应用,进一步的,所述双特异性蛋白procxcl12-aher2浓度为250nm。
16、与现有技术相比,本发明的优点在于:
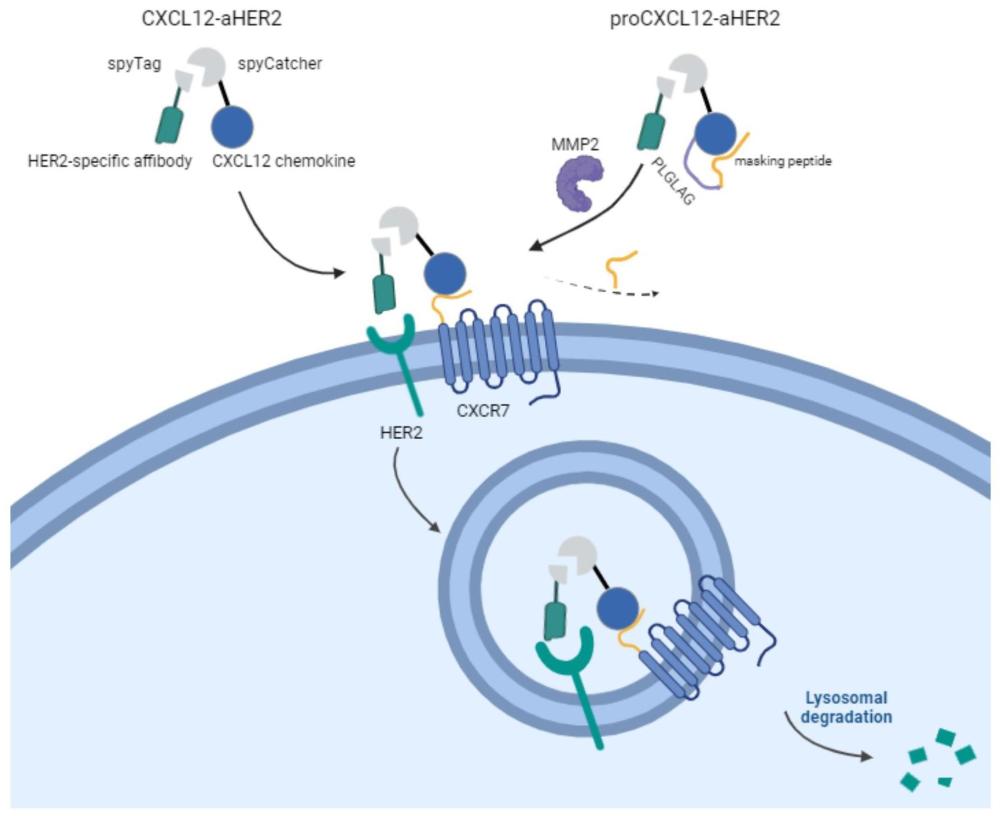
17、(1)本发明提供了一种基于短肽封闭保护cxcl12的设计方法,截取cxcr7中部分与cxcl12相互作用的短肽,通过短肽封闭cxcl12,形成n端封闭的cxcl12纯化蛋白,封闭短肽和cxcl12之间通过肿瘤特异性高表达蛋白酶mmp2底物肽序列相连接,以提高cxcl12介导的溶酶体靶向降解膜蛋白的特异性,达到减少双特异性蛋白cxcl12-aher2的毒性,减少脱靶效应,在肿瘤微环境中解除封闭,提高在肿瘤区域降解的特异性等的目的。
18、(2)本发明提供了一种降解细胞膜蛋白的方法,分别表达纯化受体封闭的趋化因子蛋白和目的蛋白的特异性结合蛋白,通过能够自发形成异肽键的spycatcher-spytag系统共价连接成双特异性蛋白,将双特异性蛋白与细胞进行孵育,在肿瘤细胞高表达酶条件下特异性地去除封闭,利用靶向溶酶体降解的方法介导细胞表面的蛋白降解。通过细胞成像、流式细胞术以及western blot技术评估蛋白降解情况。相较于现有技术中的溶酶体靶向降解蛋白研究,本发明提供了一种双特异性蛋白,是一种靶向降解的前药,降低了药物在体内循环的毒性,在肿瘤细胞高表达蛋白酶存在条件下解除封闭,具有低毒性,特异性更好的优势。
技术特征:1.一种基于短肽封闭保护cxcl12的设计方法,其特征在于,截取cxcr7中部分与cxcl12相互作用的短肽,通过短肽封闭cxcl12,形成n端封闭的cxcl12纯化蛋白,所述n端封闭的cxcl12蛋白的dna序列如seq id no.1所示。
2.一种权利要求1所述的设计方法在膜蛋白降解中的应用,其特征在于,所述应用包括:将所述n端封闭的cxcl12蛋白融合spycatcher序列得到蛋白1,将目的蛋白特异性结合蛋白融合spytag序列得到蛋白2,所述蛋白1和所述蛋白2通过spycatcher-spytag系统共价连接成双特异性蛋白,将所述双特异性蛋白与细胞进行孵育,在肿瘤细胞高表达酶存在的环境下特异性地去除封闭,利用靶向溶酶体降解的方法介导细胞表面的目的蛋白降解。
3.根据权利要求2所述的应用,其特征在于,所述目的蛋白为her2,所述应用包括以下步骤:
4.根据权利要求3所述的应用,其特征在于,所述s1具体包括以下步骤:
5.根据权利要求2至4中任一项所述的应用,其特征在于,所述蛋白1的dna序列如seqid no.2所示;和/或,所述蛋白2的dna序列如seq id no.3所示。
6.根据权利要求4所述的应用,其特征在于,所述大肠杆菌为bl21(de3)菌株。
7.根据权利要求2至4中任一项所述的应用,其特征在于,所述孵育的时间为12h。
8.根据权利要求2至4中任一项所述的应用,其特征在于,所述细胞为人胚肾细胞系293t。
9.根据权利要求2至4中任一项所述的应用,其特征在于,所述肿瘤细胞高表达酶为mmp2蛋白酶。
10.根据权利要求2至4中任一项所述的应用,其特征在于,所述双特异性蛋白procxcl12-aher2浓度为250nm。
技术总结本发明公开了一种基于短肽封闭保护CXCL12的设计方法及其在膜蛋白降解中的应用,基于短肽封闭保护CXCL12的设计方法,通过截取CXCR7中部分与CXCL12相互作用的短肽,通过短肽封闭CXCL12,形成N端封闭的CXCL12纯化蛋白,N端封闭的CXCL12蛋白质粒序列如SEQ ID NO.1所示。本发明的设计方法应用于膜蛋白降解,通过特异性地封闭药物在体内循环的毒性,在肿瘤细胞高表达蛋白酶存在条件下解除封闭,实现了以一种低毒性、特异性更好的方式靶向降解细胞表面蛋白。技术研发人员:蒋健晖,贺建军,赵凌云受保护的技术使用者:湖南大学技术研发日:技术公布日:2024/8/1本文地址:https://www.jishuxx.com/zhuanli/20240802/260795.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。