作为GSK-3β抑制剂的中药组合物及其制备与应用
- 国知局
- 2024-08-08 16:58:36
本发明涉及生物医疗,具体涉及一种作为gsk-3β抑制剂的中药组合物及其制备与应用。
背景技术:
1、
2、阿尔茨海默病目前尚无彻底根治的方法,临床常用药物主要为对症治疗的单靶点药物,如他克林、盐酸多奈哌齐、利斯的明、加兰他敏等,这些药物治疗存在诸多不良反应,局限性较多。而ad的病因尚未明确,发病机制十分复杂,且目前尚无治愈手段,被列为威胁老年人健康的杀手之一。ad往往病程较长,不可逆且致残、致死率高,有多种合并症,需要长期护理,给社会和家庭带来了沉重的经济负担。近年来,国家卫生健康委号召开展全国老年痴呆防治促进行动。对疾病的早发现、早期药物和非药物干预,对危险因素的早期控制,可明显降低阿尔茨海默病的患病风险,改善预后。
3、ad存在多种发病机制的假说,例如胆碱能假说(cholinergic hypothesis)、tau蛋白异常磷酸化假说(tau hypothesis)、淀粉样蛋白假说(amyloid hypothesis)、谷氨酸兴奋毒性假说(glutamate excito-toxicity hypothesis)、维生素b5缺乏(vitamin b5deficiency)、线粒体级联(mitochondrial cascades)。其中,淀粉样蛋白假说和tau蛋白异常磷酸化假说是研究最多的,即主要表现为随人类年龄的增长,不溶性β-淀粉样蛋白(amyloidβ-protein,aβ)聚集形成的淀粉样斑块在脑内沉积,tau蛋白(microtubule-associated protein tau)多位点过度磷酸化导致聚成螺旋丝,最终形成神经元纤维缠结(neurofibrillary tangles,nfts)。nfts发生于内嗅皮质与海马,然后逐步向皮质扩散,是ad病变的重要特征。
4、糖原合酶激酶-3(glycose synthase kinase 3,gsk-3)是一种普遍表达且具有组成型活性的丝氨酸-苏氨酸激酶,参与许多关键细胞生物学通路的调节,其中一些与神经退行性变有关。gsk-3分为gsk-3α和gsk-3β两种亚型。gsk-3β激酶在中枢神经系统中具有较高含量,且随着年龄的增加,其表达水平也随之增加。gsk-3β最早在1993年被koichiishiguro等(ishiguro k,shiratsuchi a,sato s,et al.glycogen synthase kinase3beta is identical to tau protein kinase i generating several epitopes ofpaired helical filaments[j].febs letters,1993,325(3):167-172)证实其具有tau蛋白激酶活性。tau蛋白中有大量能够被gsk-3β催化的磷酸化位点。目前的主流观点认为,aβ会随年龄的增长而逐步积累,gsk-3β活性随aβ的积累逐步增强,最终导致tau蛋白的过度磷酸化。许多研究表明,gsk-3β是ad病理学发生和发展的不同方面及途径的重要的参与者,该激酶的失调会影响tau磷酸化、aβ产生、神经元纤维缠结发生、记忆和突触功能障碍。
5、研究发现,当tau不再能够稳定对神经元细胞骨架产生影响时,就会发生功能丧失,并且类似地可能导致轴突转运缺陷。更高水平的tau磷酸化也被证明可以抑制囊泡和细胞器运输,包括携带淀粉样前体蛋白(amyloid precursor protein,app)的囊泡和细胞器运输,并增加氧化应激水平。tau会通过功能丧失、功能获得或错误定位诱导神经毒性。
6、tau蛋白的磷酸化受多种激酶调控,包括gsk-3β和细胞外aβ激活的周期蛋白依赖激酶5(cdk5)。大脑中激酶-磷酸酶失衡会对tau蛋白磷酸化水平造成影响。蛋白激酶活性的增加或磷酸酶活性的降低是导致过度磷酸化的一个原因,在前期研究中,gsk-3β被确定为可能参与ad病程中tau病理学发展的主要激酶,gsk-3β活性的降低可以减少tau蛋白磷酸化。tobias engel等(engel t,oliver p,lucas j j,et al.chronic lithiumadministration to ftdp-17tau and gsk-3βoverexpressing mice prevents tauhyperphosphorylation and neurofibrillary tangle formation,but pre-formedneurofibrillary tangles do not revert[j].journal of neurochemistry,2006,99(6):1445-55.)人在转基因小鼠中构建gsk-3β过表达模型,探究发现海马神经元中的tau过度磷酸化,并伴有神经原纤维缠结。在对gsk-3β过表达进行抑制后,原先形成的缠结无法消除,但能够防止因过表达造成的异常tau聚集。gsk-3β在通路中的信号异常也是ad诱发因素之一,在轻度认知障碍(mild cognitive impairment,mci)和ad患者脑内,gsk-3β活性较正常人脑显著提升。例如在过表达gsk-3β小鼠中,小鼠脑内tau蛋白磷酸化水平显著提升,同时这些小鼠还表现出呆滞等一系列行为缺陷。hu等(hu s,begum an,jones m r,etal.gsk3 inhibitors show benefits in an alzheimer's disease(ad)model ofneurodegeneration but adverse effects in control animals[j].neurobiol dis,2009,33(2):193-206.)通过脑内注射ad模型小鼠gsk3s特异性抑制剂sb216763(sb)发现,抑制gsk-3β的活性改善了ad小鼠模型的病理表现;hernandez等(hernandez f,lucas j j,avila j.gsk3 and tau:two convergence points in alzheimer's disease[j].journalof alzheimers disease,2013,33(suppl 1).)证实通过锂元素慢性治疗能够通过特异性抑制gsk-3β来改善tau蛋白过度磷酸化从而缓解ad。
7、阿尔茨海默病作为一种慢性疾病,在患病前期仅呈现轻度认知障碍,并无明显症状,但其发病进程可长达15-25年。随着人类平均寿命增长,老年化社会加剧,ad患者呈现迅速增加的趋势,且在65岁人群中占比较高。有研究证实gsk-3β的表达量会随着年龄的增长而增加,进而使tau磷酸化加重,促进ad病理的发生发展。因此随着年龄的增长,如65岁以后,对gsk-3β进行调控可能是预防ad的有效策略,提示将gsk-3β作为抑制靶点以防止tau蛋白过度磷酸化从而防治ad的发生与加剧具有可行性。
8、因此,开发gsk-3β抑制剂可作为阿尔茨海默病防治的一大突破口。
技术实现思路
1、本发明公开了一种作为gsk-3β抑制剂的中药组合物及其制备与应用,采用药食同源的中药——天麻与灵芝的主要成分天麻素(gastrodin,gas)和灵芝三萜(ganodermalucidum triterpenoids,glt)为原料,以特定比例组合可显著抑制gsk-3β的过表达,进而调控tau蛋白的过度磷酸化,可明显改善阿尔茨海默病。
2、为了实现上述目的,本发明提供如下技术方案:
3、本发明的第一个目的在于提供一种作为gsk-3β抑制剂的中药组合物,包括天麻素、灵芝三萜,其中天麻素和灵芝三萜的质量比为(1~4):1。
4、本发明所提供的中药组合物,突破以往单一成分的用法,不仅减少单一成分的使用量,并且通过调配两种中药成分的质量比得到协同效应更优的中药组合物。在该质量比之下,组合物的性能相较于任一单一成分的性能有显著提升。该中药组合物通过对ad相关的关键蛋白gsk-3β的抑制作用,调控对tau蛋白的过度磷酸化,从而实现对阿尔茨海默病的有效改善。因而本发明最重要的发明点在于开发了一种通过抑制gsk-3β蛋白表达来防治阿尔茨海默病的中药组合物。
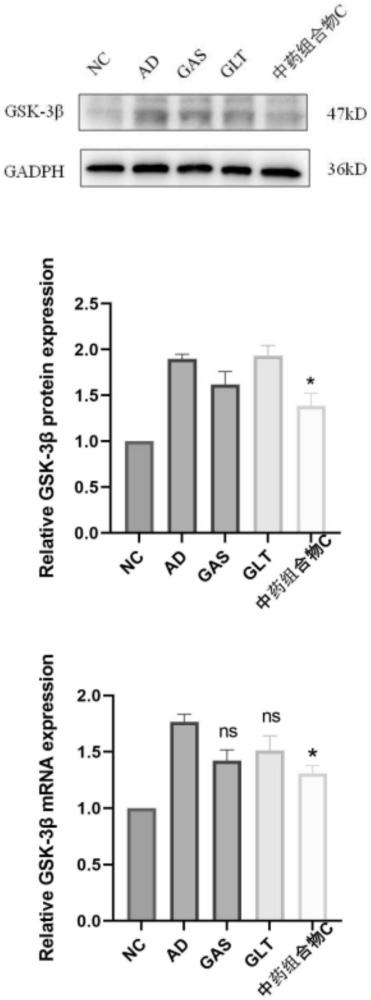
5、为应证上述发明点的实际效果,本技术人设计ad细胞模型和ad小鼠模型,观察ad细胞模型和ad小鼠模型的细胞氧化应激指标(mda、t-aoc、sod)结果、gsk-3β表达水平、tau蛋白磷酸化水平,及ad小鼠模型的动物行为学实验结果可知:本发明制得的中药组合物对细胞氧化应激损伤具有较佳的保护作用,能帮助恢复ad细胞、ad小鼠的氧化应激损伤状态。同时,本中药组合物可明显抑制ad模型中gsk-3β蛋白的表达,明显减少tau(ser396)位点的磷酸化及tau(thr181)位点的磷酸化。更为重要地是,ad细胞模型中,单一天麻素和单一灵芝三萜的使用并未改变的gsk-3β表达水平;而当采用天麻素和灵芝三萜的中药组合物后,gsk-3β在mrna和蛋白水平显著下调。
6、gsk-3β是tau蛋白过度磷酸化的关键酶之一,其活性增强与阿尔茨海默病的发展密切相关,因为它促进了tau蛋白的异常磷酸化,形成神经纤维缠结,这是ad病理特征之一。单独使用天麻素或灵芝三萜时未观察到gsk-3β表达水平的显著变化,说明单一成分可能不足以有效调控这一关键病理途径。然而,当两者结合使用时,能够在mrna和蛋白水平上显著下调gsk-3β,这表明这两者通过不同的作用机制或增强彼此的效应来共同干预gsk-3β信号通路,从而更有效地减轻tau蛋白的过度磷酸化,减缓神经退行性病变的进程。具体而言,天麻素主要通过抑制神经细胞的过度兴奋和提供神经保护来发挥作用;而灵芝三萜则通过其抗炎、抗氧化和免疫调节等特性,以及直接或间接影响gsk-3β活性来产生效应。两者的组合使用,可通过多途径、多靶点的作用机制,共同对抗ad的复杂病理过程。
7、此外,天麻素和灵芝三萜的相互作用增强了各自成分的生物利用度和/或在生物体内的稳定性和活性,使得它们在达到治疗部位时能更有效地发挥其生物学作用。这种协同效应不仅可能减缓疾病的进展,还有可能促进神经元的保护和修复,改善认知功能,为ad的治疗提供了新的策略。因而,本发明所提供的中药组合物可有效改善ad的病症,有望应用于ad的防治中。
8、此外,本发明所选用的天麻素和灵芝三萜分别来自天麻、灵芝。天麻、灵芝均属于药食同源原料成分。
9、因而,此处,本发明隐含的发明点为采用药食同源中药功效成分复合物制备功能性食品,为慢性疾病的预防提供了一种新的健康策略。以药食同源中药功效成分天麻素和灵芝三萜的组合物用于辅助改善记忆的功能性食品的制备,对ad具有预防和减轻症状的作用,对防治阿尔茨海默病高发具有重要的社会意义。
10、综上,本发明提供的中药组合物,具有显著的ad防治效果;且所用中药成分为药食同源中药功效成分,药物安全性高。
11、进一步优选地,所述天麻素和灵芝三萜的质量比为4:1。
12、优选地,所述天麻素的提取方法包括以下步骤:天麻粉超声醇提后过滤、离心、蒸发浓缩,再分离纯化后经乙醇洗脱,浓缩干燥得到天麻素。
13、优选地,所述天麻素的提取方法包括以下步骤:
14、s3.1、按照乙醇溶液和天麻粉液料比30:1ml/g,将过60目筛后的天麻粉用70%乙醇溶液浸泡12h,随后超声提取60min得到天麻素提取液;
15、s3.2、天麻素提取液抽滤、离心后蒸发浓缩得到天麻素粗提液;
16、s3.3、天麻素粗提液上样至大孔吸附树脂,静置吸附后分离纯化,再用70%乙醇溶液洗脱得到洗脱液,将洗脱液旋转蒸发、浓缩、干燥得到天麻素;其中分离条件为流速4bv/h、上样量100ml。
17、优选地,所述灵芝三萜的提取方法包括以下步骤:灵芝粉超声醇提,再抽滤、离心合并滤液后,经蒸发、分离纯化、洗脱、浓缩干燥,得到灵芝三萜。
18、优选地,所述灵芝三萜的提取方法包括以下步骤:
19、s4.1、按照乙醇溶液和灵芝粉液料比25:1ml/g,将过40目筛后的灵芝粉用75%乙醇溶液在80℃下重复两个超声循环后得到灵芝三萜提取液,其中一个超声循环时间为30min;
20、s4.2、灵芝三萜提取液抽滤后保留滤液,再对滤渣进行离心处理保留上清液,合并滤液和上清液得到综合滤液,综合滤液蒸发去除乙醇后用大孔树脂进行分离纯化得到灵芝三萜粗提液,其中分离条件为ph=4、流速2bv/h、上样量30ml;
21、s4.3、依次用15%乙醇溶液、35%乙醇溶液、95%乙醇溶液对灵芝三萜粗提液进行梯度洗脱,并用95%乙醇溶液蒸发、浓缩、干燥得到灵芝三萜。
22、优选地,所述中药组合物加入药学可接受的辅料,制成下列之一的剂型:散剂、片剂、颗粒剂和液体制剂。
23、为了将中药组合物与药学可接受的辅料制成散剂、片剂、颗粒剂和液体制剂,每种剂型的制备过程各有特色,具体如下:
24、散剂:将中药组合物和辅料(如淀粉、乳糖等作为填充剂或助流剂)分别粉碎至所需细度,通过不同目数的筛网进行分级筛选,以保证粒度均匀。随后混合分剂量包装即可得到散剂中药组合物。
25、片剂:将中药组合物与粘合剂(淀粉浆、糖浆等)混合,随后湿法制粒、干法制粒或直接粉末压片,再用压片机压片即可得到片剂中药组合物。
26、颗粒剂:类似于片剂的湿法制粒过程,但颗粒剂的颗粒通常较大,便于冲服。无需压片得到颗粒后干燥即得颗粒剂中药组合物。
27、液体制剂:将提取得到的天麻素溶液、灵芝三萜溶液复配即得液体制剂。
28、除上述剂型外,任一可实现的剂型均在本发明提供的中药组合物的应用范畴内。
29、本发明的第二个目的在于提供一种作为gsk-3β抑制剂的中药组合物的制备方法,将天麻素和灵芝三萜分别溶解于溶剂中,冷藏备用;然后按天麻素与灵芝三萜质量比(1~4):1的比例混合两种溶液,制备得到中药组合物。
30、此处用于溶解天麻素和灵芝三萜的溶剂可为常用于溶解的溶剂,即能达到完全溶解目的且安全无害的试剂,如无菌水、去离子水、蒸馏水、无水乙醇等。
31、优选地,所述作为gsk-3β抑制剂的中药组合物的制备方法包括以下步骤:
32、s6.1、将天麻素与无菌水共混配制得到天麻素溶液,置于4℃冰箱保存备用;
33、s6.2、用食品添加剂乙醇(gb 30610—2014)或dmso溶液将灵芝三萜溶解后再加入无菌水稀释得到灵芝三萜溶液,置于4℃冰箱保存备用;
34、s6.3、混合天麻素溶液、灵芝三萜溶液,使得最终制得的中药组合物中天麻素与灵芝三萜质量比为(1~4):1。
35、本发明的第三个目的在于提供了中药组合物在制备gsk-3β抑制剂上的应用。
36、本发明的第四个目的在于提供了中药组合物在制备tau蛋白抑制剂上的应用。
37、本发明的第五个目的在于提供了中药组合物在制备阿尔茨海默病防治药物或阿尔茨海默病保健品中的应用。
38、本发明人设计ad细胞模型和ad小鼠模型来验证本发明所制得的中药组合物在防治ad上的效果。观察ad细胞模型和ad小鼠模型的细胞氧化应激指标(mda、t-aoc、sod)结果、gsk-3β表达水平、tau蛋白磷酸化水平,及ad小鼠模型的动物行为学实验结果可知:本发明制得的中药组合物对细胞氧化应激损伤具有较佳的保护作用,能帮助恢复ad细胞、ad小鼠的氧化应激损伤状态。而氧化应激是ad发展过程中的一个重要病理机制,涉及到自由基的过度生成和抗氧化防御系统的失衡,导致神经元损伤和死亡。通过调节氧化应激相关的生物标志物(如mda、t-aoc、sod等),本中药组合物可以减轻神经炎症,保护神经元免受损伤,进而可能改善认知功能。同时,本中药组合物可明显抑制gsk-3β蛋白的表达,明显减少tau(ser396)位点的磷酸化及tau(thr181)位点的磷酸化。因而,本发明所提供的包含天麻素和灵芝三萜的中药组合物可有效改善ad的病症,有望应用于ad的防治中。且利用天麻素、灵芝三萜的药食同源特性可制备改善记忆的功能性保健品或是ad的安全防治药物中。
39、因此,本发明具有以下有益效果:
40、(1)本发明提供的中药组合物,能够抑制gsk-3β在ad模型中过度表达,从而抑制tau蛋白的过度磷酸化,发挥对ad的保护作用。
41、(2)本发明提供的中药组合物可作为gsk-3β的抑制剂,具有明显改善阿尔茨海默病的作用。
42、(3)本发明提供的中药组合物包含药食同源中药功效成分天麻素、灵芝三萜,大幅提升了药物安全性,同时为中药组合物作为功能性食品应用提供了思路。
本文地址:https://www.jishuxx.com/zhuanli/20240808/271577.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。