亲脂型SN38前药或其药学上可接受的盐及其合成方法和应用
- 国知局
- 2024-08-22 14:18:59
本发明涉及亲脂型sn38前药或其药学上可接受的盐及其合成方法和应用,具体涉及亲脂型sn38前药及其包含该前药的自组装纳米粒的构建,以及其在制备抗肿瘤药物中的应用,属于药物制剂新辅料和新剂型领域。
背景技术:
1、癌症一直威胁着人类健康,化疗因其广谱的抗肿瘤效果仍然是临床癌症治疗的一线选择。在众多细胞毒性化疗药物中,7-乙基-10-羟基喜树碱(sn38)作为一种半合成喜树碱衍生物,可以通过抑制拓扑异构酶i的活性而造成dna损伤,具有极强的抗肿瘤活性。然而,由于sn38极度疏水,极差的溶解性严重限制了其应用。sn38的羧酸盐形式虽然可以改善溶解度,但会增加系统毒性,降低抗肿瘤效果。此种情况下,sn38的水溶性衍生物伊立替康被开发,并被fda批准用于治疗结直肠癌。伊立替康是通过将sn38与4-哌啶基团通过酯键共价连接得到的,酯键断裂后才能转化为sn38,发挥细胞毒性。然而,酯键在体内水解的效率很低,只有1%到0.1%的伊立替康可以代谢成sn38,且具有极大的个体差异,极大地限制了伊立替康的抗肿瘤活性,导致伊立替康的细胞毒性比sn38的细胞毒性低100至1000倍。
2、纳米药物递送系统是抗肿瘤药物开发的热点领域。精心设计的纳米药物可以保护负载的药物不被提前代谢和清除,并通过增加渗透和滞留(epr)效应改善肿瘤的积累。传统的纳米药物(如脂质体和微球)通常通过分子间的非价相互作用,如载体材料和药物之间的疏水相互作用和静电相互作用来包封药物。然而,sn38的化学结构呈平面状且刚性极强,具有高度的结晶趋势。因此,sn38与载体材料的亲和力很低,容易导致药物装载效率低,稳定性差,药物过早泄漏等问题。此外,过度使用载体材料还可能会导致载体相关毒性和过敏过敏反应。合理设计基于sn38的纳米药物仍是一个挑战。
3、近年来,前药自组装纳米制剂作为一种多功能的抗肿瘤药物递送纳米平台渐渐兴起。通过简单的一步纳米沉淀法,前药分子即可自组装成纳米尺度的粒子,且无需载体材料。前药自组装纳米粒既充当“载体”又充当“货物”,不仅具有超高的载药量(通常>30%),其载体相关不良反应也可忽略不计。此外,前药自组装纳米制剂的制备工艺简单,利于实现工业化生产。此外,根据肿瘤微环境的特点,肿瘤刺激智能响应前药已被大量开发以促进肿瘤特异性药物释放。刺激响应前药自组装纳米制剂结合了前药技术和纳米技术的优点,成为一种有效和安全的抗肿瘤平台。
技术实现思路
1、为了解决现有技术存在的问题,本发明提出了一种亲脂型sn38前药及其应用,具体为sn38与内源性脂质胆固醇(cst)通过二硫键共价结合制备成前药sn38-ss-cst及其自组装纳米粒。采用一步纳米沉淀法,sn38-ss-cst可以在疏水相互作用、π-π堆积和氢键的驱动下自组装成前药自组装纳米制剂(sn38-ss-cst nps)。在结肠癌肿瘤模型上,sn38-ss-cst nps有效地抑制了肿瘤的生长,而不产生全身毒性,展现出良好的临床转化前景。
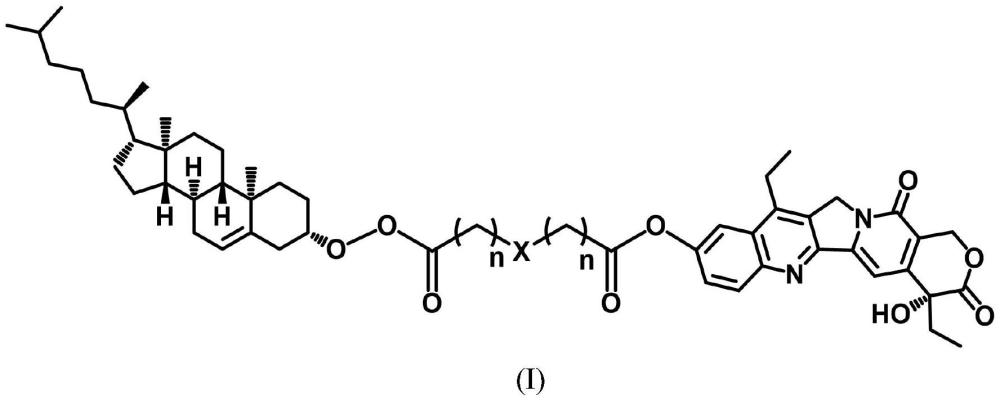
2、亲脂型sn38前药或其药学上可接受的盐,所述的亲脂型sn38前药结构如下述通式(i)所示:
3、
4、其中,n=1~3;x为-s-s-、-s-、-se-se-或-se-。
5、优选地,所述亲脂型sn38前药具有如下化学结构式:
6、
7、本发明的另一目的是提供上述亲脂型sn38前药或其药学上可接受的盐的制备方法,所述的sn38-胆固醇小分子前药的合成反应全程在氮气保护下进行,具体包括如下步骤:
8、步骤1:将二元酸溶解成二元酸酐后,在4-二甲氨基吡啶(dmap)的催化下与胆固醇进行酯化反应,获得胆固醇-二元酸单边酯中间产物;
9、步骤2:胆固醇-二元酸单边酯与sn38发生成酯反应,得到终产物亲脂型sn38前药,
10、其中,所述二元酸为单硫代二乙酸、单硫代二丙酸、单硫代二丁酸、单硒代二乙酸、单硒代二丙酸、单硒代二丁酸、2,2'-二硫代二乙酸、3,3'-二硫代二丙酸、4,4'-二硫代二丁酸、2,2'-二硒代二乙酸、3,3'-二硒代二丙酸或4,4'-二硒代二丁酸。
11、优选地,所述胆固醇与二元酸的摩尔比为(1-10):(5-15);所述胆固醇-二元酸单边酯与sn38的摩尔比为1:(0.5-10)。
12、优选地,所述方法包括如下步骤:
13、步骤1:将二元酸用乙酸酐溶解,室温下搅拌反应,使二元酸转化为二元酸酐,反应完后进行减压蒸馏旋出乙酸酐,确保乙酸酐除尽;用二氯甲烷溶解所得二元酸酐,冰浴搅拌下,逐滴将用二氯甲烷溶解的4-二甲氨基吡啶(dmap)和胆固醇滴入其中,而后在室温条件下搅拌12小时,通过层析柱分离得到胆固醇-二元酸单边酯中间产物;
14、步骤2:将胆固醇-二元酸单边酯中间产物溶解于二氯甲烷中,冰浴搅拌下,依次逐滴加入二氯甲烷溶解的1-(3-二甲氨基丙基)-3-乙基碳化二亚胺盐酸盐(edci)、1-羟基苯并三唑(hobt)和4-二甲氨基吡啶(dmap),冰浴活化2小时,然后加入sn38,室温条件下搅拌24小时,再经制备液相分离纯化得终产物亲脂型sn38前药。
15、优选地,所述二元酸与乙酸酐的比例为1mmol:(1-10)ml;dmap:胆固醇:二元酸的摩尔比为1:(1-10):(2-15);中间产物胆固醇-二元酸单边酯:hobt:edci:dmap:sn38的摩尔比为1:(1-10):(2-6):(0.2-5):(0.5-10)。
16、本发明的又一目的是提供亲脂型sn38前药的自组装纳米粒。
17、一种亲脂型sn38前药的自组装纳米粒,所述的亲脂型sn38前药的自组装纳米粒为非peg化的亲脂型sn38前药自组装纳米粒或peg修饰的亲脂型sn38前药自组装纳米粒。
18、进一步地,非peg化的亲脂型sn38前药自组装纳米粒时,制备方法:用有机溶剂将亲脂型sn38前药溶解并充分混匀,在搅拌下缓缓地滴入去离子水中,亲脂型sn38前药自发形成均匀的纳米粒;
19、进一步地,当为peg修饰的亲脂型sn38前药自组装纳米粒时,制备方法:用有机溶剂将peg修饰剂和亲脂型sn38前药溶解并充分混匀,在搅拌下缓缓地滴入去离子水中,亲脂型sn38前药自发形成均匀的纳米粒;其中,亲脂型sn38前药:peg修饰剂的质量比为1:(0.1-1),peg修饰剂为两亲性聚合物。
20、本发明的又一目的是提供所述亲脂型sn38前药或其药学上可接受的盐或所述亲脂型sn38前药的自组装纳米粒在制备抗肿瘤药物中的应用。
21、本发明的又一目的是提供所述亲脂型sn38前药或其药学上可接受的盐或所述亲脂型sn38前药的自组装纳米粒在制备注射给药、口服给药或局部给药系统中的应用。
22、本发明的有益效果:本发明设计合成了亲脂型sn38前药,合成方法简单易行;并制备了粒径较小、粒度分布均一的亲脂型sn38前药的自组装纳米粒,制备方法简单易行。结果表明:将sn38设计成亲脂型sn38前药自组装纳米粒能有效提高sn38的疗效,降低其毒副作用;这一设计改善了sn38的自身缺陷,为sn38更好地应用于临床提供了可能,有望填补临床上没有高效低毒的喜树碱类化疗药物的空白,对于sn38抗肿瘤药物的开发具有重要意义。本发明为开发高效-低毒化疗制剂提供了新的策略与选择。
本文地址:https://www.jishuxx.com/zhuanli/20240822/278082.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
上一篇
一种梨果酒的制备方法
下一篇
返回列表