Ago蛋白在真核细胞靶向基因编辑中的应用及靶向基因编辑方法
- 国知局
- 2024-10-09 14:39:09
本发明涉及分子生物,具体公开了一种ago蛋白在真核细胞靶向基因编辑中的应用及靶向基因编辑方法。
背景技术:
1、靶向基因编辑技术(也被成为基因组编辑技术)是一类能够对基因组进行高效率、高精准度定点改写技术的总称。靶向基因编辑技术主要包括zfn、talen和crispr技术,这三种技术被誉为基因组编辑三大利器。
2、zfn和talen技术是通过对特定蛋白质结构域进行设计和改造而实现基因组的靶向定位、编辑或修饰,但是这两类技术普遍存在实施操作过程中技术难度较大、操作步骤繁琐和组装时间较长等不足,此外zfn技术还存在被国外行业领头公司垄断的现象。
3、crispr技术利用原核生物针对外来dna入侵的初级免疫系统,使用人工设计的向导rna对基因组特定的靶向区域进行识别并引导cas9蛋白结合、切割dna,造成靶向dna的断裂并引发基于nhej或hdr的基因组修复,从而实现基因编辑。但crispr技术普遍存在以下两个缺陷,其一是cas9、cpf1等crispr相关蛋白的分子量较大,在开展哺乳动物成体细胞的基因编辑时,表达元件的递送存在困难;其二是脱靶现象严重,带来潜在风险,虽然近年开发出一些精准度更高的cas突变体,但仍然缺乏根本性的变革。
4、argonautes蛋白是普遍存在于从原核细菌到高等生物(包括哺乳动物)的一类核酸酶,简称ago蛋白。据报道,一些来自原核微生物的pago蛋白能够与短链寡核苷酸互作并实现对相应互补核酸序列的靶向结合。在高等细胞中一些argonautes蛋白(eago)参与了非编码rna(ncrna)相关的许多重要生理过程。但是现有技术中,多集中于对来自原核微生物的某些pago蛋白在体外具有dna切割活性、某些pago蛋白与向导dna/rna组合共同实现对原核细胞或真核细胞的基因编辑。对于不依赖于外源靶向向导的基于同源重组的基因编辑技术,公告号为cn112481309b的中国专利公开了采用10种来自原核微生物的pago蛋白实现对真核细胞靶向基因编辑的方法,其靶向基因区域位于can1基因,但是是否可通过相近的技术对除can1基因以外的其他靶向基因进行编辑仍然未知。此外,迄今为止对于来自原核生物的其他ago蛋白或来自真核生物的ago蛋白是否可实现对真核生物的多个靶向基因进行编辑也鲜有报道。
技术实现思路
1、鉴于以上所述三大主流基因编辑技术的不足或ago蛋白在真核细胞基因编辑应用的研究现状,本发明旨在挖掘可以用于真核细胞基因编辑的ago蛋白,提供一种既不依赖于蛋白质结构域编程、又不依赖于向导元件编程的基因编辑方法,且该方法可实现在多个靶向基因区域进行基因编辑,达到丰富真核细胞靶向基因编辑的工具箱的目的。
2、为达到上述发明目的,本发明实施例采用了如下的技术方案:
3、第一方面,本发明提供了一种ago蛋白在真核细胞内靶向基因编辑中的应用,其特征在于,所述应用基于同源重组且不依赖于外源靶向向导;
4、所述ago蛋白为来自原核生物的pago蛋白或来自真核生物的eago蛋白中的任意一种。
5、本发明以ncbi等生物信息数据库中,挖掘ago蛋白的氨基酸序列,通过优选的来自原核生物的pago蛋白或来自真核生物的eago蛋白,可以在无需由短链的dna或rna所构成的专用向导的情形下,用于真核细胞基因组中多个靶向区域的编辑,其使用简便、组合方式丰富,为真核细胞的靶向基因编辑提供了更多的工具选择。特别是,本发明首次挖掘和筛选出来自真核生物的eago蛋白可用于真核细胞靶向基因编辑。
6、需要注意的是,本发明中所述的真核细胞具体为活体真核微生物细胞、活体植物细胞或活体动物细胞中的一种。本发明是以活体的酿酒酵母(saccharomyces cerevisiae)这一模式真核细胞为例进行相关试验,以验证可通过本发明提供的方法实现相关靶向基因的编辑。
7、本发明中ago蛋白及其编码基因的简称命名规则的约定如下:
8、默认情况下,对ago蛋白使用其来源的物种的属名的第1个大写字母加种名的第1个小写字母命名,例如来自aliterella atlantica的ago就被命名为aaago;如果该生物物种的命名只由属名、没有种名,则取其属名前3个字母命名,其中第1个字母大写、第2及第3个字母小写,例如来自brevundimonas sp.的breago;如果按照以上命名规则仍然出现重名,则增加其ago基因序列的ncbi登录号作为后缀加以区分,例如来自archaeoglobusfulgidus dsm 4304的ago被命名为afago(o28951.1),以便与来自acidibacillusferrooxidans的afago(kuo96127.1)相区分。本专利中所有的关于ago的表述,皆遵从本命名规则的约定。
9、同样地,对于ago蛋白的编码基因,以ago蛋白名称的小写来表示。例如:来自aliterella atlantica的aaago,其基因命名为aaago;来自archaeoglobus fulgidus dsm4304的afago(o28951.1),其基因命名为afago(o28951.1)。
10、优选地,所述pago蛋白为csago(kuk34412.1)或与csago(kuk34412.1)的氨基酸序列具有至少80%同源性的蛋白,cnago或与cnago的氨基酸序列具有至少80%同源性的蛋白,hrago或与hrago的氨基酸序列具有至少80%同源性的蛋白,psago(wp_013632721.1)或与psago(wp_013632721.1)的氨基酸序列具有至少80%同源性的蛋白,afago(kuo96127.1)或与afago(kuo96127.1)的氨基酸序列具有至少80%同源性的蛋白,asago或与asago的氨基酸序列具有至少80%同源性的蛋白,或者chago或与chago的氨基酸序列具有至少80%同源性的蛋白中的至少一种;
11、所述eago蛋白包括apago或与apago的氨基酸序列具有至少80%同源性的蛋白,mlago或与mlago的氨基酸序列具有至少80%同源性的蛋白,pxago或与pxago的氨基酸序列具有至少80%同源性的蛋白,或者nvago或与nvago的氨基酸序列具有至少80%同源性的蛋白中的至少一种。
12、优选地,所述pago蛋白为csago(kuk34412.1)或与csago(kuk34412.1)的氨基酸序列具有至少80%同源性的蛋白,cnago或与cnago的氨基酸序列具有至少80%同源性的蛋白,hrago或与hrago的氨基酸序列具有至少80%同源性的蛋白,psago(wp_013632721.1)或与psago(wp_013632721.1)的氨基酸序列具有至少80%同源性的蛋白,afago(kuo96127.1)或与afago(kuo96127.1)的氨基酸序列具有至少80%同源性的蛋白,asago或与asago的氨基酸序列具有至少80%同源性的蛋白,或者chago或与chago的氨基酸序列具有至少80%同源性的蛋白中的至少一种;
13、所述eago蛋白包括apago或与apago的氨基酸序列具有至少80%同源性的蛋白,mlago或与mlago的氨基酸序列具有至少80%同源性的蛋白,pxago或与pxago的氨基酸序列具有至少80%同源性的蛋白,或者nvago或与nvago的氨基酸序列具有至少80%同源性的蛋白中的至少一种。
14、优选地,所述csago(kuk34412.1),其氨基酸序列如seq id no.1所示;
15、所述cnago,其氨基酸序列如seq id no.2所示;
16、所述hrago,其氨基酸序列如seq id no.3所示;
17、所述psago(wp_013632721.1),其氨基酸序列如seq id no.4所示;
18、所述afago(kuo96127.1),其氨基酸序列如seq id no.5所示;
19、所述asago,其氨基酸序列如seq id no.6所示;
20、所述chago,其氨基酸序列如seq id no.7所示;
21、所述apago,其氨基酸序列如seq id no.8所示;
22、所述mlago,其氨基酸序列如seq id no.9所示;
23、所述pxago,其氨基酸序列如seq id no.10所示;
24、所述nvago,其氨基酸序列如seq id no.11所示。
25、本发明所述的11个ago蛋白,包括7种原核生物来源的pago蛋白和4种真核生物来源的eago蛋白,可以在无需由短链的dna或rna所构成的专用向导的情形下,用于真核细胞基因组的靶向编辑,其使用简便、组合方式丰富,为真核细胞的靶向基因编辑提供了更多的工具选择。本发明中所述靶向基因包括can1基因、ade2基因、pdc5基因或adh3基因中的任意一种,本发明仅是以这四种与代谢相关的基因为例进行说明在本专利的实施例中,利用上述11种ago蛋白对酿酒酵母其他基因可进行编辑的潜力仍然很大。
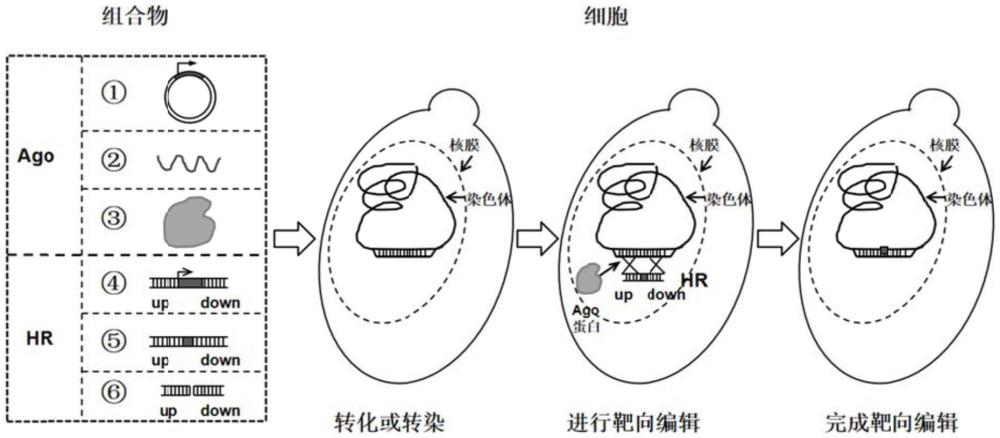
26、第二方面,本发明提供了一种用于真核细胞靶向基因编辑的ago蛋白组合物,所述ago蛋白组合物包括ago蛋白或其表达元件,以及同源重组片段;
27、其中,所述ago蛋白为来自原核生物的pago蛋白或来自真核生物的eago蛋白中的至少一种;
28、所述同源重组片段包括以can1基因、ade2基因、pdc5基因或adh3基因中的任意一种为靶向基因设计所得的同源重组片段;
29、其中,所述所述ago蛋白为上述优选的氨基酸序列如seq id no.1~11所示的任一种ago蛋白,或与上述11个代表性ago蛋白同源性大于等于80%的蛋白,其亦可以是满足序列同源性大于等于80%的众多其它蛋白突变体或嵌合体中的一个。
30、本发明中所述同源重组片段包括89hr0、89hr89、89hrhis、ade2hrhis、pdc5hrhis或adh3hrhis中的任意一种为例进行说明:
31、其中,所述89hr0、89hr89、89hrhis、ade2hrhis、pdc5hrhis或adh3hrhis的基因序列均由上同源臂、外源序列和下同源臂组成;
32、所述上同源臂或下同源臂的长度均不低于200bp。
33、本发明中所记载的同源重组片段仅用于说明内容,并不构成对本发明的限定。根据本领域技术人员的惯常设计及常规操作,同源重组片段的设计和组装可采用搭接pcr、无缝克隆或gibson组装等常规分子生物学方法进行,也可设计其他同源重组片段;优选地,所述同源重组片段的同源臂长度不低于200bp。
34、第三方面,本发明提供了一种真核细胞靶向基因编辑的方法,该方法包括将上述ago蛋白组合物导入真核细胞内,实现对以酿酒酵母为代表的真核细胞的靶向基因编辑,所述靶向基因包括can1基因、ade2基因、pdc5基因或adh3基因中的至少一种。
35、本发明提供的基于同源重组的真核细胞靶向基因编辑的方法,可以通过ago蛋白或其表达元件以及同源重组片段,实现在真核细胞中介导靶向基因编辑、且无需同源重组片段之外的向导元件。其中,ago蛋白为优选的来自原核生物的pago蛋白或来自真核生物的eago蛋白;相关ago蛋白表达元件中包含根据模式真核生物的碱基偏好性设计合成的相关ago蛋白的基因,本发明合成了包括已知不能以5’端磷酸化的单链dna为向导执行靶向基因编辑的ngago在内的一批ago基因。
36、在应用时,同源重组片段应被配置于用于转化或转染的递送体系内,一般情况下,该递送体系的溶剂是水或者te缓冲液等常规缓冲液,溶质是同源重组片段及ago蛋白的表达元件,即:该用于转化或转染的递送体系是由同源重组片段、ago蛋白表达元件、水/缓冲液构成的。按照目前的生物技术通识,所述的由同源重组片段和ago蛋白的表达元件组合而成的组合物,方便于且等同于直接采用体外制备的ago蛋白与同源重组片段的组合物。
37、其中,针对同源重组片段,其应是能够在靶向区域实现基因表达盒插入的同源重组片段,或能够在靶向区域通过替换原有基因片段以实现基因表达盒插入的同源重组片段,或能够在靶向区域实现基因片段插入或替换的同源重组片段,或能够在靶向区域实现基因片段删除的同源重组片段。
38、同源重组片段的设计和组装可采用搭接pcr、无缝克隆或gibson组装等常规分子生物学方法进行,通过对同源重组片段的设计,本发明能够在靶向区域实现外源基因的插入、原有基因的替换(由外源基因替换原有基因)、或者原有基因的删除。
39、其中,所述导入的方式包括化学转化、电转化或基因枪转化中的任一种。
40、优选地,所述基因编辑的形式包括基因片段的靶向敲入或替换、基因片段的靶向删除。
41、敲入或替换的外源基因可以是基因表达盒或基因片段。基因表达盒是指在基因序列两端分别携带宿主可识别的启动子序列和终止子序列、能够独立地转录出mrna进而翻译成蛋白质,其长度一般在数百个碱基对(bp)以上。相对于基因表达盒而言基因片段则是指仅由数十个或更多个碱基对(bp)构成的序列,该序列两端不携带有启动子序列和终止子序列,基因片段只能用于对原有基因序列进行置换但不能够如基因表达盒那样独立地转录出mrna进而翻译成蛋白质。
42、第四方面,本发明还提供了一种真核生物,该真核生物上述真核细胞靶向基因编辑的方法获得。
43、需要说明的是,本发明的靶向基因编辑方法一般在常温下进行,并优选为在酿酒酵母的最适温度下(即30℃)进行。
44、由于采用了上述技术方案,本发明与现有靶向基因编辑技术相比,所取得的技术进步在于:
45、(1)与zfn及talen技术方案相比,本发明提供的真核细胞靶向基因编辑方法,无需编辑改造外源核酸酶,也无需重新编码的ago蛋白,操作更简单、实验周期短;
46、(2)与crispr技术方案相比,本发明提供的真核细胞靶向基因编辑方法不需要向导rna设计和使用,实现了靶向基因编辑的技术方案由“外源核酸酶+向导核酸+同源重组片段”的“三元体系”向“外源核酸酶+同源重组片段”的“二元体系”简化和回归,只需将能够表达ago蛋白的基因元件和同源重组片段导入细胞,即可实现真核细胞靶向基因编辑,从而为真核细胞的靶向基因编辑提供了更便利、更高效、更加多样化的技术方案;
47、(3)与依赖于长度不超过21nt的向导rna的crispr系统相比,本发明提供的真核细胞靶向基因编辑方法,对于靶向区域的精准靶向只依赖于同源重组片段的同源靶向,因而能够大幅度提高靶向精准度、降低基因编辑的脱靶概率;此外,本发明提供的真核细胞靶向基因编辑方法可实现基因删除,效率可达到20%;可实现基因置换,效率可达到15%;可实现基因敲入,效率可达到40%。
48、(4)相对于其他靶向基因编辑方案中所使用的cas9等外源蛋白质,本发明提供ago蛋白普遍小于cas9蛋白,在基因治疗等潜在应用场景中,本发明提供的ago蛋白会因效应蛋白质较小而有明显的优势;
49、(5)本发明提供的真核细胞靶向基因编辑方案,提供了多种可在真核细胞内实现靶向基因编辑的ago蛋白工具,其ago蛋白高达11种,同源重组片段的多样性以及可选靶向基因种类多,在能够完成基因编辑的前提下,不同的ago蛋白、同源重组片段和靶向基因的多种组合可具备各自的独特性,使得本发明方案极大地丰富了靶向基因编辑技术的工具箱。
本文地址:https://www.jishuxx.com/zhuanli/20241009/305971.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 YYfuon@163.com 举报,一经查实,本站将立刻删除。
下一篇
返回列表